Introducción
La fibrilación auricular (FA) es la arritmia más frecuente en el adulto. Según el informe del “Global Burden of Diseases, Injuries, and Risk Factors”, 33,5 millones de individuos en el mundo presentan FA, aproximadamente el 0,5% de la población(1). Además, su incidencia y prevalencia están en aumento. En un seguimiento de 50 años de su cohorte, el estudio Framingham encontró que entre los períodos 1958-1967 y 1998-2007 se cuadriplicó la prevalencia de FA ajustada por edad(2).
La FA aumenta el riesgo de muerte, provoca insuficiencia cardíaca, infarto de miocardio y accidente cerebro vascular (ACV), además de comprometer la calidad de vida de los pacientes. Su prevalencia y riesgos aumentan con la edad3,4. La consecuencia más temida es el ACV. Estudios contemporáneos muestran que entre un 20% y 30% de los pacientes con ictus isquémico tienen un diagnóstico de FA antes, durante o después del evento inicial5. A nivel nacional, un estudio publicado en 20146 reportó la prevalencia de FA analizando el ECG de adultos mayores de 18 años usuarios de una institución de asistencia médica colectiva de Montevideo. Este estudio encontró una prevalencia global de FA de 2%, es infrecuente antes de los 60 años, alcanzando el 5,0% entre los 60 y 79 años y el 12,3% en los mayores de edad.
La FA puede cursar en forma asintomática y su primer registro diagnóstico puede realizarse en el contexto de un ACV7,8. También puede ser intermitente. El riesgo de desarrollo de ACV no está vinculado a la presencia o ausencia de síntomas ni a su curso temporal9-11.
Hacer el cribado de FA es relevante desde los puntos de vista clínico, epidemiológico y sanitario12. Se pueden emplear distintas estrategias de tamizaje: oportunístico, con un registro único (single point screening), o sistemático, con registros repetidos. Se han utilizado múltiples métodos como la toma de pulso, un ECG, el registro de dispositivos implantables (cardiodesfibriladores, marcapasos, registradores de eventos implantables), aplicaciones para teléfonos celulares vinculadas o no a relojes inteligentes usando pletismografía, parches o dispositivos para monitorización a distancia, entre una amplia variedad de opciones tecnológicas disponibles13).
Existe acuerdo en que la FA detectada a través de tamizaje (con cualquiera de los métodos) no es una condición benigna. En estos pacientes es muy común la concomitancia de otros factores de riesgo para ACV, lo cual justifica la planificación de estrategias de cribado14.
Contar con un método de detección que sea rápido, accesible, inocuo, de bajo costo y que pueda superar barreras geográficas es especialmente relevante para la población de riesgo. El propósito de este estudio piloto es valorar la utilidad de un dispositivo móvil de tecnología electrónica (DMTE), disponible comercialmente para uso individual, para el tamizaje de FA en una población de riesgo.
El objetivo primario es evaluar la validez y confiabilidad de un DMTE para identificar FA en un grupo de voluntarios adultos mayores beneficiarios del Plan Ibirapitá.
El objetivo secundario es validar los procesos de recolección, transmisión, almacenamiento, procesamiento e interpretación de los datos obtenidos.
Método
Se utilizó un DMTE cuyo registro se contrastó con el trazado del ECG de 12 derivaciones realizado en forma casi simultánea. El DMTE consiste en un sensor KardiaMobile de AliveCor® vinculado con una aplicación Kardia (Alivecor, Inc.) que se instala en smartphones, aprobado por la Food and Drug Administration de Estados Unidos para uso individual con este propósito. El sistema detecta una única derivada del ECG haciendo registros de 30 segundos de duración. El algoritmo diagnóstico incorporado al sistema se basa en definir la regularidad o irregularidad del ritmo y genera tres posibles diagnósticos automáticos: normal, posible FA o sin clasificar. Se compararon los diagnósticos automáticos con los llevados a cabo por dos cardiólogos expertos de forma independiente, a partir de la lectura del registro realizado con el DMTE y de un ECG de 12 derivaciones (figura 1). En los trazados dudosos, se solicitó la opinión de un tercer revisor especialista en arritmias.
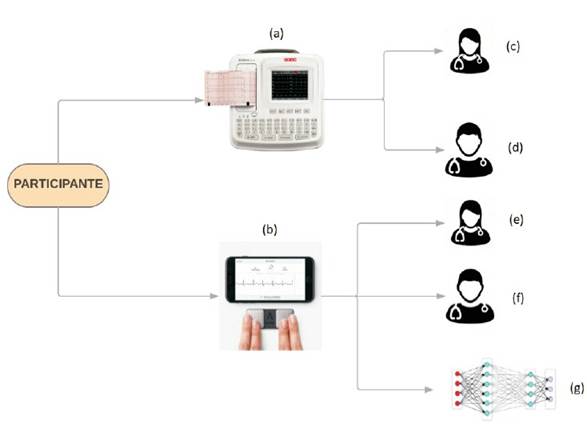
Figura 1: A cada participante se le hacen dos registros: uno con un ECG de 12 derivaciones (a) y otro con el DMTE (b). La definición del diagnóstico electrocardiográfico es llevada a cabo por dos cardiólogos en forma independiente. De esta forma, cada trazado del ECG de 12 derivaciones tiene 2 asignaciones diagnósticas (c y d), en tanto cada registro del DMTE tiene 3 asignaciones diagnósticas que corresponden, una, al diagnóstico automático del DMTE (g) y las otras 2, al diagnóstico realizado por cada uno de los cardiólogos (e y f).
Plan Ibirapitá
Para priorizar la detección en los adultos mayores, la población de mayor riesgo y de menores recursos, se vinculó al Plan Ibirapitá en este trabajo de investigación. Ibirapitá se creó en el año 2015 para promover la inclusión digital de las personas mayores. Realiza talleres de capacitación y pone a disposición de sus usuarios el soporte tecnológico necesario (tabletas). En el contexto de los talleres que organiza el Plan, los participantes fueron invitados a intervenir en el estudio.
Entre el 15 de octubre y el 30 de noviembre de 2018 se llevaron a cabo 5 talleres, con 20 a 25 participantes cada uno, en el local de la Comisión Honoraria para la Salud Cardiovascular. Se elaboró un cuestionario sobre factores de riesgo para desarrollo de FA y conocimiento de presencia de esta arritmia, que quienes accedían debían contestar. Se aseguró la confidencialidad de los datos y los participantes firmaron consentimiento informado.
Se hizo la devolución del diagnóstico a cada uno de los participantes vía correo electrónico, adjuntando una copia del trazado del dispositivo, así como la recomendación de consulta a su médico de cabecera con esta información, en el caso que se considerara necesario.
Análisis estadístico
Se hicieron tablas, medidas de resumen para las variables en estudio y se calcularon valores predictivos positivos y negativos, sensibilidad y especificidad. El análisis de los datos se realizó utilizando el lenguaje de programación y software estadístico R (versión 3.6.2) (R Core Team (2019). R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL https://www.R-project.org/.)
Resultados
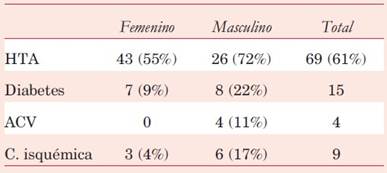
Participaron del estudio 114 beneficiarios del Plan Ibirapitá, 78 del sexo femenino. La edad fue de 72,5 ± 5,36 años (rango: 53-87 años).
Las características de los participantes se describen en la (tabla 1).
Dos cardiólogos realizaron diagnóstico de FA en 4 participantes con el análisis del ECG y del registro del DMTE en forma independiente con una concordancia en el diagnóstico de 100%. De estos 4 participantes, solo 1 conocía que la tenía.
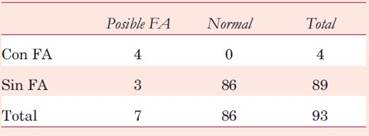
En 7 casos el DMTE diagnosticó posible FA. Este diagnóstico fue confirmado en 4/7 casos con el análisis de los cardiólogos. En los otros 3 casos diagnosticados por el DMTE como posible FA esta no fue confirmada (falsos positivos). No se registraron falsos negativos. En consecuencia, la sensibilidad para el diagnóstico de FA del DMTE es de 100% con una especificidad de 96,6% (VPP = 57,1%, VPN = 100%) y una proporción de diagnóstico correcto de 96,8% (tabla 2).
Tabla 2: Matriz de confusión: Diagnóstico automático del DMTE según diagnóstico de cardiólogos (excluye los trazados con diagnóstico “sin clasificar”).
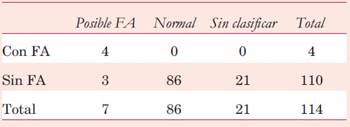
El DMTE catalogó como “sin clasificar” 21 (18,4%) trazados (tabla 3). Considerando esto, la proporción de diagnóstico correcto disminuye a 78,9%. Ninguno de los trazados que el dispositivo clasifica como “sin clasificar” fue FA. Esto fue corroborado por dos cardiólogos independientes y también por un tercer revisor especialista en arritmias cardíacas. Por lo tanto, en este estudio piloto el DMTE utilizado no arrojó resultados falsos negativos, tanto cuando fue capaz de confirmar un diagnóstico automático como cuando definió el trazado como "sin clasificar".
Tabla 3: Diagnóstico automático del DMTE según diagnóstico de cardiólogos (incluye los trazados con diagnóstico “sin clasificar”).
Utilizando un DMTE se logró una correcta adquisición de trazados de corta duración de una sola derivada que se descargan como archivo PDF. Estos archivos PDF se compartieron con los cardiólogos que participaron de este estudio para su interpretación a distancia. Se enviaron estos registros vía mail a los participantes, quienes podían compartirlos con su médico tratante para la toma de decisiones si así lo querían. De esta forma se logran completar los procesos de recolección, almacenamiento, procesamiento e interpretación de los datos obtenidos.
Discusión
En este estudio piloto, utilizando un DMTE para la detección de FA en una población de adultos mayores de bajos recursos, se encontró una sensibilidad y una especificidad comparables a las reportadas en la literatura internacional. Este rendimiento diagnóstico sugiere la validez de los procesos de recolección, transmisión. almacenamiento, procesamiento e interpretación de los datos de un DMTE diseñado para uso individual.
La FA es una arritmia de gran prevalencia, responsable de una importante morbimortalidad y en un alto porcentaje de casos es asintomática y/o intermitente. Una estrategia de detección es necesaria, fundamentalmente en la población de mayor riesgo15. La utilización de DMTE para la detección de FA fue estudiada y validada en múltiples escenarios16 y con distintas tecnologías17.
Una revisión sistemática de la literatura evaluó el valor del tamizaje oportunístico de FA con un registro único en el tiempo (mediante ECG o toma de pulso) para la identificación de pacientes que se podrían beneficiar con el uso de anticoagulantes para la prevención de ACV18. Incluyó 30 estudios (n: 122,571; edad media: 64 años; 9 países) y la prevalencia global de FA encontrada fue de 2,3%, siendo de 4,4% en los mayores de 65 años. La incidencia de FA desconocida fue 1,4% en mayores de 65 años y el 67% de estos pacientes tenían alto riesgo de ACV.
Las guías de práctica clínica recomiendan hacer tamizaje de FA15, pero el significado pronóstico de los individuos en los que se lleva a cabo la detección de FA aún es incierto. Un estudio reciente reporta los resultados del cribado oportunístico, realizado en 7.107 personas mayores de 65 años en las farmacias, utilizando un dispositivo manual que registra una derivada del ECG. En el seguimiento a un año de los individuos en los que se detectó FA no conocida (3,6%) se encontró un exceso de mortalidad comparado con los individuos sin FA19.
El tamizaje sistemático es tan efectivo como el oportunístico para la detección de FA no conocida (1,64% oportunístico vs. 1,62% sistemático). Sin embargo, el tamizaje oportunístico tiene una mejor ecuación costo-efectividad, dado el costo de realizar ECG de 12 derivaciones y las dificultades de enrolamiento, aproximadamente 50% de los pacientes efectivamente concurren a hacerse un ECG20. Estos aspectos deben ser tenidos en cuenta cuando se planifica una estrategia de detección poblacional de FA.
Utilizando la misma tecnología empleada en este estudio, Orchard y colaboradores(12) logran demostrar la factibilidad de la detección de FA a nivel comunitario, comprobando que es de fácil aplicación y aceptado por la población. Durante el período de vacunación antigripal en Sidney, Australia, en 2015, en 5 consultorios de medicina general se registró con el monitor AliveCor el ECG a 2.476 pacientes mayores de 65 años. El registro luego era revisado por dos cardiólogos. La sensibilidad del dispositivo para la detección de FA fue de 95% y la especificidad de 99%. Los trazados catalogados como «sin clasificar» (8,4%) se relacionaban en su mayoría a bradicardia o taquicardia sinusal21. En nuestro estudio reportamos un 18,4% de registros con diagnóstico automático “sin clasificar”. Otro reporte en el que se utilizó el AliveCor, el estudio iREAD reclutó en forma prospectiva 52 pacientes con FA que se hospitalizaban para el inicio de drogas antiarrítmicas, reportando una sensibilidad del 100% y especificidad del 89,2% para el diagnóstico de FA y un 27,6% de registros sin clasificar22. También con el mismo DMTE, otra investigación realizada en Kenia que incluyó 50 pacientes que consultaron en forma consecutiva en un lapso de 2 semanas en el Hospital Kijabe, mostró que la detección de FA en el contexto de un hospital de bajos recursos es factible, tiene un buen rendimiento diagnóstico una vez que los trazados son revisados por cardiólogos y es bien aceptado por los participantes16.
El DMTE que utilizamos en este estudio fue también empleado para validar la exactitud en el diagnóstico de un reloj inteligente, que usa pletismografía y se vincula a la aplicación KardiaMobile en el celular, en una cohorte prospectiva de 672 pacientes hospitalizados. Este estudio encuentra que el diagnóstico de FA por fotopletismografía es factible y seguro, pero una de sus limitaciones es una alta tasa de registros de mala calidad que no permiten definir un diagnóstico23.
El estudio hecho por la Universidad de Stanford y financiado por la empresa Apple Inc. es un estudio icónico en el uso de la tecnología para la detección de FA a distancia24. Al igual que en el estudio previo, se utiliza un reloj inteligente que detecta, a través de fotopletismografía, la presencia de pulso regular o irregular. El reloj (iWatch) está vinculado a un celular inteligente (iPhone) con la aplicación KardiaMobile. Cuando detecta pulso irregular, envía una notificación al participante y se le ofrece una teleconsulta a través de un servicio de telesalud. Una vez que se constata que el participante cumple con los criterios de elegibilidad (mayor de 22 años, no tener FA conocida, no estar usando anticoagulantes), se le envía por correo un parche para registro del ECG que debe usar por al menos 7 días. De los 419.297 participantes el 0,52% (2.161 participantes) recibió notificación de pulso irregular. De estos, 450 devolvieron los parches con registros pasibles de ser analizados. Los autores concluyen que la probabilidad de recibir notificación de pulso irregular fue baja. En los pacientes que recibieron notificación de pulso irregular, 34% tenía FA. Estos hallazgos no sorprenden, dado que los participantes eran personas mayoritariamente jóvenes con una media de 41 ± 13 años, siendo la proporción de participantes mayores de 65 años de 5,9%. La prevalencia de FA detectada en los distintos estudios de tamizaje de FA depende de la población incluida, así como del tiempo de registro (por ejemplo, un solo registro, varios registros puntuales, dispositivos de monitorización continua, etcétera)18,25-27.
Un aspecto relevante del estudio de Perez y Mahaffey y colaboradores24 radica en que logra mostrar las enormes posibilidades que puede ofrecer la tecnología para la atención en salud, destacando que todas las fases del estudio se realizaron a distancia, desde la selección de los participantes, la firma de consentimiento informado, la consulta médica por telemedicina con la derivación a un centro asistencial en el caso de hallazgo de alguna arritmia grave, el envío y la devolución de los parches para el registro electrocardiográfico por correo, etcétera.
Las tecnologías de la información y la comunicación (TICs) han generado una revolución a nivel mundial, también en la medicina y ciencias afines. Su desarrollo ha contribuido a lo que hoy se denomina telemedicina o telesalud28,29. En este contexto de pandemia y quizás de ahora en adelante, disponer de un recurso accesible y sencillo de utilizar que permita hacer a distancia el tamizaje, un eventual diagnóstico y probablemente el inicio de un tratamiento, así como el seguimiento de una patología de trascendencia clínica como la FA, será de enorme utilidad para prevenir complicaciones, evitar traslados innecesarios y optimizar la asistencia.
Asumimos que nuestra experiencia presenta ciertas limitaciones, que son inherentes a su carácter de experiencia piloto. En efecto, se incluyeron pocos participantes y, en particular, un bajo número de sujetos con FA. Además, se trata de una muestra con predominancia del sexo femenino. Se debe ampliar la experiencia para confirmar nuestros resultados preliminares.
Conclusiones
El tamizaje de FA con un DMTE, en una población de adultos mayores de bajos recursos es factible, tuvo buena aceptación y logró identificar FA con una sensibilidad y especificidad comparables a las reportadas en la literatura internacional.
Entre las limitaciones del estudio se encuentra el bajo número de participantes y la presencia de un claro sesgo femenino.
El hallazgo de un 18,4% de trazados con diagnóstico automático «sin clasificar» hace necesario contar con recursos humanos calificados para realizar la confirmación diagnóstica en esos registros.
Un contexto de pandemia jerarquiza la importancia de estos métodos.