Principales aportes
- La mortalidad operatoria y la sobrevida a largo plazo de la población con endocarditis activa que recibió cirugía cardíaca en nuestro medio, son similares a las reportadas internacionalmente.
- Se observó una alta incidencia de agentes intrahospitalarios y procedimientos invasivos como causas probables.
- La presencia de vegetaciones sobre el velo posterior mitral y la infección por Staphylococcus aureus fueron predictores independientes de embolias.
- Los pacientes con complicaciones locales deben ser seguidos estrechamente, incluso a largo plazo, ya que estas resultaron ser el principal predictor de muerte en el seguimiento.
Introducción
La endocarditis infecciosa (EI) es una enfermedad poco frecuente, cuya incidencia anual varía entre 3-7/100.000 personas en estudios contemporáneos1-3. Sigue caracterizándose por una gran morbimortalidad que no ha sido modificada en las últimas cuatro décadas. La mortalidad hospitalaria se encuentra en torno a 25% (pudiendo ser mayor según el microorganismo involucrado), con una mortalidad al año de hasta 40%3,4. En nuestra región, la mortalidad hospitalaria también es elevada, hasta 25,5% en el registro EIRA 3 (Endocarditis Infecciosa en la República Argentina), publicado en 20185. Aunque la incidencia ha permanecido estable 1,2,8, el cuadro clínico y el perfil epidemiológico de la EI han cambiado en los últimos 50 años9,10.
El registro EIRA, que analizó el perfil epidemiológico de la EI en Argentina, constituyó el primer estudio multicéntrico efectuado en nuestra región. Los autores describen características clínicas, terapéuticas y la morbimortalidad de la enfermedad a principios de la década de 19906. Posteriormente, en 2002 y 2017, se realizaron dos nuevos relevamientos (EIRA 2 y 3)5,7 que permitieron comparar las características de la EI a lo largo del tiempo, y mostraron importantes diferencias epidemiológicas en coincidencia con las observadas en países del mundo desarrollado. A pesar de grandes avances en tecnología, conocimiento de la enfermedad, métodos diagnósticos precisos y antibióticos (ATB) más eficaces, la mortalidad permanece incambiada.
En nuestro medio se desconocen las características clínicas y evolutivas de los adultos con EI que requieren intervención quirúrgica. Nuestro objetivo primario fue determinar la mortalidad operatoria (MO) y la sobrevida a largo plazo. Nuestro objetivo secundario fue definir predictores de embolias, complicaciones locales (CL), MO y endocarditis protésica (EP) en la evolución.
Método
Se realizó un trabajo retrospectivo, observacional, aprobado por el Comité de Investigación del Instituto Nacional de Cirugía Cardíaca. Se incluyeron todos los pacientes intervenidos quirúrgicamente por endocarditis activa (EA), definida como aquella bajo tratamiento ATB. La MO fue definida como la muerte ocurrida durante la internación o durante los primeros 30 días de la intervención quirúrgica. Se consideró CL a la presencia (en estudio ecocardiográfico o como hallazgo quirúrgico) de absceso, pseudoaneurisma, fístula o destrucción del aparato valvular11.
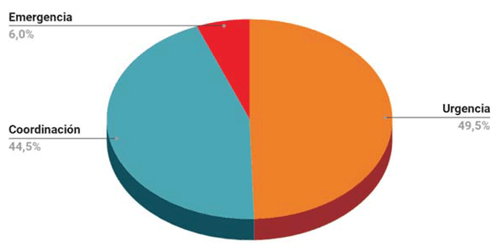
Los pacientes que recibieron cirugía por EA entre enero de 2006 y diciembre de 2017, se identificaron en la base de datos institucional de recolección prospectiva. Se extrajeron variables demográficas, etiológicas, quirúrgicas, ecocardiográficas y evolutivas. Las variables continuas se expresan como media y desvío estándar, las categóricas como porcentaje. Las comparaciones se realizaron mediante test de t o chi cuadrado, según correspondiera. Mediante regresión logística multivariada se identificaron predictores para los objetivos enunciados. Para el análisis multivariado se consideraron variables con p<0,1 en el univariado. La sobrevida a largo plazo se analizó mediante Kaplan-Meier y se comparó mediante log-rank test. Se determinaron predictores de sobrevida mediante regresión de Cox. Se consideró significativa una p<0,05. Se consideraron de emergencia las intervenciones quirúrgicas realizadas dentro de las 24 horas del diagnóstico, de urgencia las realizadas entre las 24 y las 48 horas y de coordinación las realizadas luego de las 48 horas.
Resultados
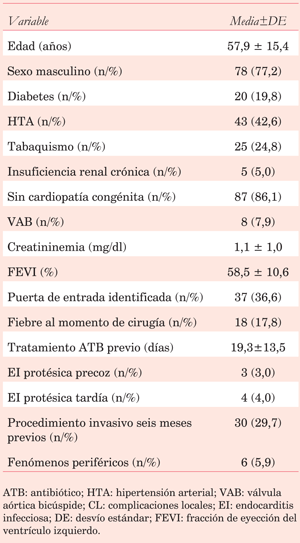
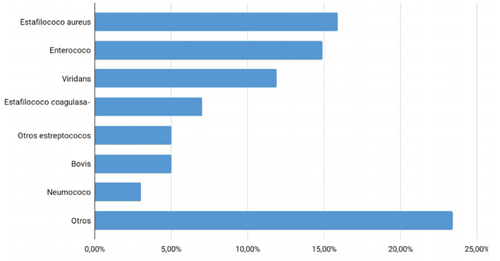
Entre enero de 2006 y diciembre de 2017 se intervinieron quirúrgicamente 101 pacientes con EI definida por criterios de Duke o criterios de Duke modificados, según la fecha de presentación. En la (tabla 1) de describen las características clínicas. El microorganismo más frecuentemente identificado fue Staphylococcus aureus (SA) (15,8%), seguido de enterococo (14,9%); la incidencia de los diferentes microorganimos se encuentra en la (figura 1). La mayoría de los hemocultivos (HC) fueron positivos (72,3%), pero el cultivo valvular fue positivo en una pequeña proporción de casos (16,8%) (figura 2). Se observó EP en 20,8% de los casos, de localización aórtica en 46,5%, mitral 23,8% y mitro-aórtica en 13,9%. La mayoría de las intervenciones se realizaron en condición de urgencia-emergencia (55,4% de los casos) (figura 3).
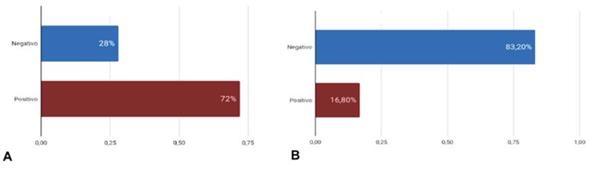
Figura 2: Porcentaje de pacientes con hemocultivos (A) y cultivos valvulares (B), positivos y negativos.
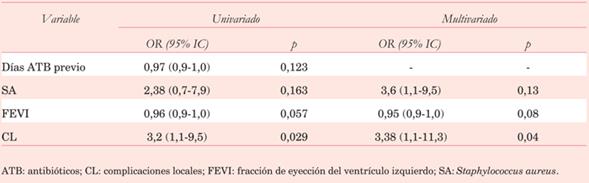
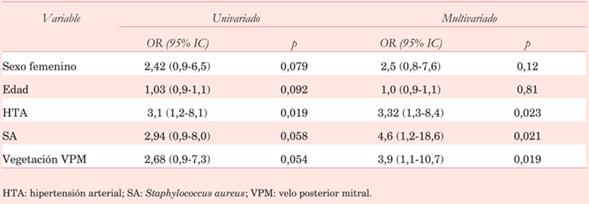
La MO global fue de 19,8%, siendo mayor en pacientes con CL (29,2% vs 11,3% sin CL, p=0,025), única variable asociada a MO luego del análisis multivariado (OR=3,38; IC95%: 1,0-11,3) (tabla 2). La incidencia de CL fue de 47,5%, siendo el absceso la más frecuente (25,7%). La EP (OR=5,8; IC95%: 1,4-24,3), endocarditis sobre válvula aórtica (OR=2,9; IC95%: 1,1-7,8) y sexo masculino (OR=3,5; IC95%: 1,1-11,4) se asociaron a CL tras el análisis multivariado (tabla 3).
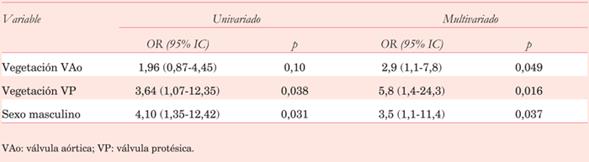
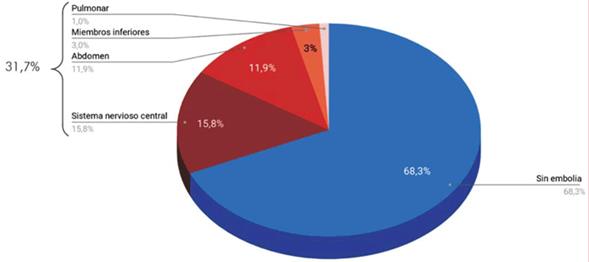
La incidencia de embolias fue 31,7%, localizadas principalmente en el sistema nervioso central (figura 4). Se asociaron a mayor riesgo de embolia: sexo femenino, edad, antecedente de hipertensión arterial (HTA), identificación de SA en HC y presencia de vegetaciones sobre valva posterior de la válvula mitral, pero luego del análisis multivariado resultaron predictores: SA en HC (OR=4,6; IC95%: 1,2-18,6), vegetación en el velo mitral posterior (OR=3,9; IC95%: 1,1-10,7) y antecedente de HTA (OR=3,32; IC95%: 1,3-8,4) (tabla 4). La incidencia de EP precoz fue de 3%, y tardía de 4%. De los siete pacientes con EP en la evolución, seis tuvieron CL en la presentación inicial (p<0,05). Debido a la baja incidencia de EP en la evolución, no se lograron identificar predictores independientes.
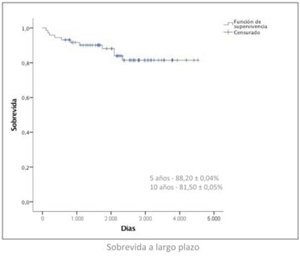
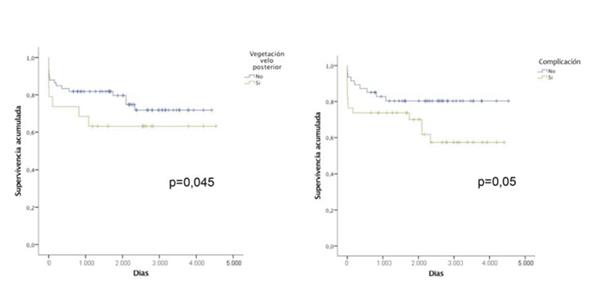
La sobrevida global a cinco y diez años fue de 88,20% y 81,50% respectivamente (figura 5). La sobrevida fue menor en pacientes con CL y vegetación en el velo posterior (figura 6). Luego de la regresión de Cox, la presencia de CL (HR=3,1; IC95%: 1,2-8,1) y vegetación en el velo posterior (HR=2,8; IC95%: 1,0-7,6) resultaron predictores de menor sobrevida. No fueron predictores de eventos adversos, ni la duración del tratamiento ATB previo a la cirugía, ni la presencia de fiebre al momento de la misma.
Discusión
En 1994, Durack y colaboradores12, de la Universidad de Duke, propusieron un esquema de diagnóstico que estratificó a los pacientes con sospecha de EI en tres categorías: definida, posible y rechazada. Estos criterios han sido modificados en base a los avances en los métodos diagnósticos y al mayor conocimiento de la enfermedad13. El diagnóstico de EI debe realizarse precozmente para iniciar tratamiento ATB empírico inmediato e identificar a los pacientes con alto riesgo de complicaciones que pueden requerir un abordaje quirúrgico temprano.
La información respecto a la evolución de los pacientes operados por EI en nuestro medio es limitada. Por este motivo, y debido a la alta mortalidad y al perfil cambiante de la enfermedad, es fundamental conocer su estado actual.
En nuestra población observamos una edad media de 57,9 (±15,4) años, similar a la observada en el registro internacional ICE-PCS4 que incluyó 2.781 pacientes de 25 centros entre 2000 y 2005. Está bien establecido el predominio de sexo masculino en la EI, como se reporta en este trabajo (72,9%). Esto podría explicarse por la protección del endotelio mediada por estrógenos en la mujer en edad reproductiva14 y por el desarrollo más tardío de enfermedad cardiovascular respecto a los hombres, lo que incluye a la enfermedad degenerativa valvular.
La presencia de condiciones predisponentes fue relativamente frecuente, principalmente debido a la presencia de válvula protésica (VP) (20,8%) o cardiopatía congénita (13,9%). A diferencia de estudios realizados hace cinco décadas en los que 50% de los casos eran portadores de enfermedad mitral reumática16, en nuestra población fueron tan solo 2%.
Un grupo emergente en riesgo de EI está formado por pacientes con infecciones asociadas a los cuidados sanitarios4. Casi un tercio de los pacientes adquirieron EI como consecuencia de un procedimiento médico invasivo, al igual que lo observado en el EIRA 3, y otros registros internacionales4; esto evidencia la importancia de la profilaxis en este escenario, ya que es una infección potencialmente prevenible.
La microbiología de la enfermedad también se ha visto modificada. La incidencia de la EI causada por SA ha aumentado, siendo actualmente el agente etiológico más común en la mayor parte del mundo industrializado, incluyendo el registro argentino EIRA 35. La aparición de EI por SA se vincula a los cuidados en salud (contacto hospitalario, procedimientos y dispositivos invasivos) como principal factor de riesgo, además del uso de drogas intravenosas. En contraste con los estreptococos, el SA no requiere la presencia de enfermedad valvular preexistente para determinar la infección17. La importancia de este patógeno potencialmente letal es motivo de preocupación dada la creciente resistencia antimicrobiana18, incluso a la vancomicina19. En nuestro estudio, SA fue también el principal microorganismo causal (15,9%). Siguieron en frecuencia: enterococo y viridans. El enterococo afecta habitualmente a pacientes ancianos con comorbilidades, y es más frecuente la adquisición nosocomial, la cual se asocia a peores resultados. La tasa de mortalidad reportada por este agente es intermedia entre la de estreptococos y la de estafilococos20.
El hecho de que casi un tercio de las EI ocurrieron en pacientes sometidos a un procedimiento invasivo en los seis meses previos y que en igual proporción se identificaron microorganismos asociados a infecciones nosocomiales, tiene implicancias importantes para el diagnóstico y el tratamiento de la EI en nuestro medio. Los pacientes que han recibido un procedimiento invasivo representan un grupo de riesgo que requiere atención diagnóstica cuidadosa en presencia de fiebre o bacteriemia. Este hallazgo pone en tela de juicio la implementación de profilaxis antibiótica en pacientes en riesgo.
Los HC fueron negativos en el 28% de los casos, cifra significativamente más alta que la hallada en registros internacionales (11,1% en ICE-PCS4). Si bien 72% de los casos tuvo HC positivo, solo 16,8% de los cultivos valvulares desarrolló microorganismos. Esto está probablemente vinculado al largo período de tratamiento ATB previo a la cirugía (media 19,3 días). Es importante destacar que ni la duración del tratamiento ATB previo a la cirugía, ni la presencia de fiebre al momento de la misma, resultaron ser predictores independientes de eventos adversos.
Se observó 20,8% de EI sobre VP, similar a lo observado por Hoen B y colaboradores (16%)9, y en el Euro Heart Survey (26%) 21. Dentro de las infecciones sobre válvula nativa, la principal localización fue sobre válvula aórtica (VAo) (46,5%), seguida de la válvula mitral (VM) (23,8%). Nuestros resultados son similares a lo observado en el EIRA 3 (VAo 46% - VM 33% - VP 20,7%). En ICE-PCS se observó EI sobre VP en el 22,2%, seguida por la infección sobre VM (41%) y VAo (38%). Se encontró una elevada incidencia de complicaciones de EI, como embolias o CL. El 31,7% de pacientes sufrió embolias, siendo la principal localización el sistema nervioso central, similar a lo reportado en EIRA 3 y en ICE-PCS (32,1% y 40%, respectivamente).
Diversos parámetros han sido identificados como predictores de eventos embólicos, como ser el tamaño y la movilidad de las vegetaciones30, el aumento del tamaño de la vegetación durante el tratamiento ATB 22, la identificación de SA22, antecedente de embolia previa22 y EI multivalvular. La localización de las vegetaciones sobre la VM ha generado controversias. Varios estudios han sugerido un mayor riesgo embólico en pacientes con endocarditis sobre VM. Pruitt y colaboradores informaron una tasa más alta de embolización cerebral y sistémica en pacientes con EI mitral en un estudio de 218 pacientes con EI23. Cabell y colaboradores encontraron en 145 pacientes con EI que la endocarditis mitral se asoció con un mayor riesgo de ataque cerebrovascular (32,5% vs 11,3%, p = 0,003)24. En el estudio de Rohmann y colaboradores25, a 281 pacientes con sospecha clínica de EI se les practicó ecocardiograma transesofágico y se evaluó el valor pronóstico del sitio de la vegetación: las vegetaciones de la VM asociaron una incidencia significativamente mayor de eventos embólicos que las de la válvula aórtica (25% vs 9,7%). Particularmente la valva anterior mitral ha sido identificada como la localización de mayor potencial embolígeno por algunos autores. Sin embargo, las vegetaciones en la VM fueron significativamente mayores que las de la VAo y se ha puesto en duda si la mayor incidencia de eventos embólicos en la endocarditis mitral podría deberse al mayor tamaño de la vegetación y no a su ubicación. Un estudio europeo multicéntrico no encontró diferencias en eventos embólicos entre EI de la VM y aórtica, que ocurrieron en 70 de 191 pacientes (37%) sobre VM, y 67 de 214 pacientes (31%) sobre VAo26. Un estudio reciente de 847 pacientes con EI encontró seis factores (edad, diabetes mellitus, fibrilación auricular, embolia previa, longitud de la vegetación e infección por SA) asociados a un aumento del riesgo embólico, que se utilizaron para crear una calculadora del riesgo embólico27.
En nuestro estudio los únicos predictores independientes de embolias fueron: identificación de SA en HC, vegetación en el velo mitral posterior y antecedente de HTA (tabla 4). Los efectos mecánicos de la excursión amplia y abrupta de las valvas mitrales, que ocurren dos veces por latido en ritmo sinusal, podrían contribuir a la fragmentación y embolización de las vegetaciones, determinando así mayor incidencia de eventos embólicos.
La incidencia de CL en registros internacionales se encuentra en torno a 37%5 y el absceso perivalvular es la más habitual28. Es más frecuente en la EI aórtica (10%-40%) y en la EP (56%-100%)28. En nuestro grupo de pacientes intervenidos por EI, la incidencia de CL fue de 47,5%, más frecuentemente el absceso (25,7%). Los factores de riesgo de CL más importantes identificados en otros estudios fueron: EP, endocarditis sobre VAo e infección por estafilococo coagulasa negativo28. En nuestra población, encontramos coincidentemente que tanto la EP como la endocarditis aórtica, se vieron asociadas de forma independiente a CL, junto con el sexo masculino (tabla 3).
La MO global registrada en estudios internacionales es alta (12%-22%)5. En nuestra población fue 19,8%, siendo mayor en pacientes con CL (29,5% vs 11,3%, p=0,025). La única variable que vimos asociada a mayor MO, luego del análisis multivariado, fue la presencia de CL (OR=3,38; IC95%: 1,1-11,3). Adicionalmente, encontramos que las CL aumentan el riesgo de EP en la evolución. En las series recientes, las tasas de supervivencia a largo plazo se encuentran en 60%-70% a los cinco años29-31. En diez años de seguimiento la supervivencia fue de 74,8% en el estudio de Pang PY y colaboradores32. En nuestra población, la sobrevida global a cinco y diez años fue mayor que la reportada, 88,20% y 81,50%, respectivamente (figura 5).
Ya fue demostrado que la presencia de CL es un predictor de mal pronóstico a largo plazo33. Otros factores identificados como predictores de sobrevida a largo plazo son: edad, EP, infección por SA y fracción de eyección del ventrículo izquierdo <45%32). La sobrevida a largo plazo en nuestra población fue menor en pacientes con CL y con vegetación en el velo posterior mitral (figura 6). Como se observa en la figura 6, la sobrevida de pacientes con CL es peor que en pacientes sin CL, lo que podría explicarse por la mayor incidencia de EP. Resulta novedoso que los pacientes con localización en el velo posterior mitral hayan tenido peor evolución. En vista de este peor resultado, estos pacientes deberían ser seguidos estrechamente, incluso a largo plazo, a pesar de tener una intervención quirúrgica temprana.
Limitaciones
Se trata de un estudio observacional retrospectivo con sesgos propios de la selección de pacientes candidatos a cirugía. Se realizó en un solo centro quirúrgico, lo que probablemente limite la aplicación de los hallazgos a otros entornos. Una serie prospectiva más amplia y un enfoque multicéntrico nacional, permitirían obtener nuevas conclusiones respecto a los factores pronósticos identificados. El bajo número de EP en la evolución ha limitado el uso del análisis multivariado para evaluar los factores de riesgo.
Conclusiones
La MO de la EA que recibió cirugía cardíaca en nuestro medio es similar a la reportada internacionalmente. Las CL se asocian a EP en la evolución y resultaron ser un predictor independiente de sobrevida a largo plazo. La presencia de vegetaciones sobre el velo posterior mitral, el antecedente de HTA y la infección a SA fueron predictores independientes de embolias. La presencia de CL resultó ser el principal predictor de muerte. La sobrevida a largo plazo de pacientes operados en nuestro medio es muy buena.