1. Introducción
La fibrilación auricular (FA) es la arritmia de importancia clínica más frecuente y su prevalencia aumenta con la edad. Es el trastorno del ritmo que más comúnmente se asocia a la insuficiencia cardíaca (IC) independientemente de la fracción de eyección. Su presencia aumenta el riesgo de complicaciones tromboembólicas, empeora los síntomas y agrava el pronóstico de los pacientes con IC1,2.
Hace ya 20 años que la FA y la IC fueron declaradas “las dos nuevas epidemias de enfermedades cardiovasculares”3.
El envejecimiento de la población, el incremento de algunos factores de riesgo cardiovascular que comparten ambas patologías y la mejoría en los métodos de detección y diagnóstico han hecho que la realidad supere las proyecciones. La prevalencia de obesidad, por ejemplo, factor de riesgo para ambas patologías, se ha duplicado desde 1980 y predomina en los países de ingresos medios y bajos4.
Se estima un crecimiento sostenido de la prevalencia de la IC y de la FA en los próximos años que repercutirá significativamente en la calidad de vida de un número importante de personas a nivel mundial y será un desafío para la sustentabilidad económica de los sistemas sanitarios.
La IC y la FA pueden ser causa o consecuencia una de la otra, y sus efectos deletéreos se potencian mutuamente: el desarrollo de IC en el paciente con FA aumenta la mortalidad de manera comparable a cuando la FA se instala en un paciente con IC5 (Figura 1).
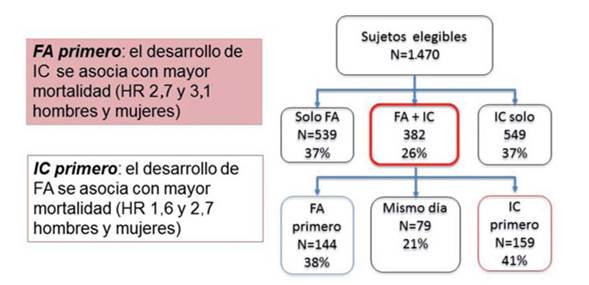
Figura 1: Relaciones temporales entre fibrilación auricular e insuficiencia cardíaca y su influencia en la mortalidad. Del estudio Framingham. Modificado de referencia5.
Ambas patologías comparten no solamente factores de riesgo, también una similar fisiopatología. Entre los mecanismos comunes se destacan el remodelado cardíaco estructural, la activación neurohormonal y la afectación del ventrículo izquierdo. En algunos casos la IC puede ser precipitada por la presencia de FA con frecuencia cardíaca elevada persistente (taquimiocardiopatía), siendo esta de mejor pronóstico que la FA asociada a miocardiopatías primarias. La FA de nueva aparición asociada a IC establecida tiene un peor pronóstico, segura mente vinculado a la presencia de una enfermedad miocárdica más evolucionada.
La IC, por otra parte, es el más fuerte predictor de la aparición de FA, multiplica en seis veces sus probabilidades6.
En resumen, los pacientes con FA e IC tanto con fracción de eyección reducida (ICFEr) (<40%) como preservada (ICFEp) (>50%) tienen peor pronóstico, incluida una mayor mortalidad. La clasificación actual de la guía de IC de la Sociedad Europea de Cardiología introduce una nueva categoría de IC con FEVI descendida de rango intermedio (entre 40%-49%); los datos existentes en este grupo son escasos7. Nos referiremos específicamente a la FA en la ICFEr.
2. Fibrilación auricular e insuficiencia cardíaca con fracción de eyección reducida
La FA y la ICFEr comparten, como se mencionó más arriba, múltiples factores de riesgo: diabetes, hipertensión, obesidad, presencia de cardiopatía (isquémica, valvular, miocardiopatía primaria). La comprensión de los mecanismos de ambas enfermedades y su relación podría generar estrategias para prevenir el desarrollo de las mismas.
La FA puede facilitar la aparición o la agravación de la IC por varios mecanismos (Figura 2).
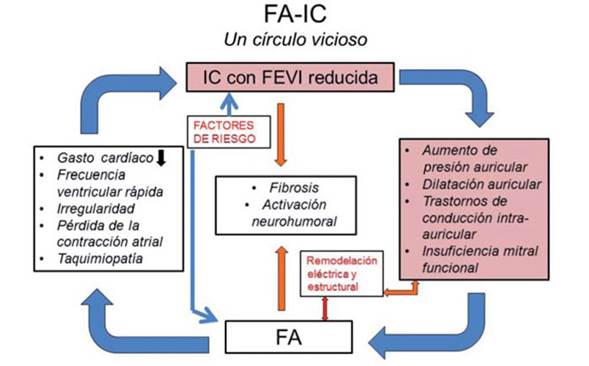
Figura 2: Relación entre los mecanismos de fibrilación auricular e insuficiencia cardíaca. Modificado de referencia10.
La presencia de una frecuencia cardíaca elevada genera un período de llenado diastólico reducido, con la consecuente reducción del gasto cardíaco. Además, el ritmo irregular compromete también el gasto cardíaco en aproximadamente un 25%; los ciclos de llenado largo no logran compensar los ciclos cortos.
Los atrios que están destinados a fibrilar probablemente pierdan su función contráctil antes que se instale la FA.
Existen mecanismos capaces de compensar las alteraciones generadas por la recurrencia o permanencia de la FA, pero estos no se mantienen en el tiempo debido a la progresión paulatina de la fibrosis en las aurículas. El descenso del gasto cardíaco genera aumento de la epinefrina y endotelina incrementando el efecto vasoconstrictor propio de la IC6,8.
Cuando la frecuencia cardíaca está persistentemente elevada se incrementa la regurgitación mitral y se produce el consecuente aumento de la precarga del ventrículo izquierdo favoreciendo aún más la dilatación del anillo. Asimismo, en los pacientes con cardiomiopatía dilatada la FA puede causar por sí sola dilatación del anillo mitral con insuficiencia secundaria. La FA con frecuencia rápida mantenida puede ser, como mencionamos, causa primaria de deterioro de la función ventricular, siendo reversible con el control adecuado y oportuno de la frecuencia cardíaca o, como también ha sido demostrado, con el control del ritmo mediante una ablación exitosa de FA9,10.
La presencia de IC puede facilitar el desarrollo de FA: se generan cambios a nivel estructural, ultraestructural y neuroendócrino. A medida que evoluciona la disfunción ventricular con aumento de las presiones intracavitarias aumenta también el riesgo de desarrollo de FA al generarse cambios importantes a nivel auricular, agrandamiento con incremento de presión auricular e insuficiencia mitral funcional.
El volumen de la aurícula izquierda es uno de los parámetros ecocardiográficos de mayor valor predictivo de desarrollo y recurrencia de FA. Estas alteraciones estructurales se acompañan de cambios eléctricos, cambios a nivel celular, anatómicos y ultraestructurales acumulativos; a nivel del sustrato, estos cambios pueden ser modulados con el uso de inhibidores de la angiotensina, antifibróticos y antiinflamatorios10,11.
La FA no solo es un marcador de IC avanzada, sino también un factor independiente de mortalidad y hospitalizaciones, aunque no todos los ensayos randomizados hayan podido demostrar esta relación. En el estudio V-HeFT la mortalidad de los pacientes con FA no era mayor que la de los pacientes en ritmo sinusal, pero esto podría explicarse porque los pacientes con FA enrolados presentaban una FEVI mayor que los no fibrilados12.
El estudio COMET analizó el valor pronóstico de la presencia de FA en una cohorte de pacientes con ICFEr tratados con betabloqueantes. Los autores encontraron una diferencia significativa con mayor mortalidad e internaciones por IC en los pacientes con FA. En el análisis multivariado observaron que la FA no es un factor de riesgo independiente de mortalidad al considerar el efecto de otros factores pronósticos de IC, si bien encontraron que la instalación de FA en la evolución es un fuerte predictor de muerte en los pacientes con IC13.
El ensayo MADIT II demostró que al ajustar los resultados por edad, clase funcional, función renal y el uso de betabloqueantes, la FA no se asoció a aumento de la mortalidad14.
En un estudio comunitario realizado entre 1986 y 2003, con el objetivo de determinar la mortalidad global en relación con la presencia de FA previa o posterior al desarrollo de IC, se analizaron 1.664 individuos con IC, 553 con historia de FA previa, 384 que desarrollan FA después de IC y 572 sin FA, con un seguimiento medio de cuatro años. El grupo con FA previa tuvo 29% de mayor mortalidad, pero el grupo con FA posterior tuvo el doble de mortalidad, ambos con respecto a los pacientes sin FA15.
Del análisis de estos ensayos surge el concepto de diferenciar a aquellos pacientes con FA establecida de aquellos que en el proceso de la enfermedad agregan FA. Más allá de que en ambos el pronóstico está comprometido, los pacientes con FA incidente (inicio reciente) tienen peor pronóstico, son frecuentemente de mayor edad y tienen una enfer medad cardíaca más avanzada.
La FA tiene un efecto negativo significativo en la mortalidad e internaciones de los pacientes con IC y FEVI reducida.
3. Manejo de la fibrilación auricular en la insuficiencia cardíaca
Llamativamente aún no se dispone de evidencia contundente y particular para el tratamiento de los pacientes con FA e ICFEr. Es conocido que estos suelen tener una respuesta más pobre a la terapéutica, suelen ser más viejos y tener más comorbilidades. Naturalmente, en el paciente con FA se mantienen las pautas terapéuticas determinadas para el manejo de la IC6.
El tratamiento óptimo de la ICFEr mediante el uso de inhibidores de la enzima convertidora de angiotensina o antagonistas de los receptores de angiontensina II, antagonistas de la aldosterona y betabloqueantes, reduce francamente la incidencia de FA en estos pacientes.
Por otra parte, y con respecto a los betabloqueantes (una de las piedras angulares en el tratamiento de la ICFEr), un metaanálisis demostró que no fueron tan útiles en pacientes con FA como lo son en pacientes que mantienen ritmo sinusal en la reducción de las hospitalizaciones por IC y de la mortalidad16.
El manejo de los factores higiénico-dietéticos tiene gran importancia en el desarrollo y progresión de la FA. Se ha demostrado una fuerte relación entre el sobrepeso y la obesidad en el desarrollo de todas las formas de FA. En el estudio Framigham se demostró un 50% de aumento de la incidencia de FA en obesos. Se ha descrito también una relación entre la cantidad de grasa pericárdica y el desarrollo de FA17,18.
El descenso de peso no solo trae aparejado la disminución de la grasa pericárdica, sino también la reducción del tamaño auricular, mejoría en la función mecánica de la aurícula y mejoría del sustrato electrofisiológico. Como consecuencia se reduce el riesgo de desarrollo de FA y se disminuye la carga hemodinámica en los pacientes ya portadores de FA.
Aunque no ha sido aún valorada en un ensayo clínico randomizado, la hipótesis que plantea que la modificación de determinados factores de riesgo cardiovascular pueda disminuir el desarrollo de IC en pacientes con o sin FA, es muy atractiva.
Recientemente se publicaron resultados del Women’s Health Study, que siguió durante más de 20 años a una población de 34.736 mujeres. El desarrollo de una nueva FA aumentaba significativamente el riesgo de desarrollar IC en la evolución (HR 9,03). Se identificaron además otros cuatro factores de riesgo de desarrollo de IC en esta población: hipertensión, obesidad, tabaquismo y diabetes. Su control adecuado podría prevenir el desarrollo de IC19.
Otros factores también se han relacionado fuertemente con la aparición de la arritmia además de la hipertensión arterial y la diabetes: la apnea del sueño y el exceso de ejercicio. El tratamiento con presión positiva continua en pacientes portadores de apnea del sueño posterior a la ablación de la FA disminuye la incidencia de recurrencias20,21.
El tratamiento y control adecuado de los factores de riesgo favorece el mantenimiento en ritmo sinusal.
3.1. Anticoagulación
La anticoagulación oral (ACO) es una parte esencial del tratamiento del paciente con FA para prevenir complicaciones embólicas. Al menos una tercera parte de los accidentes cerebrovasculares (ACV) isquémicos están vinculados a FA; estos ACV son más graves y tienen mayor mortalidad que los no vinculados a FA1,2.
Más allá de las implicancias clínicas en cuanto a morbimortalidad, este hecho tiene una enorme repercusión en los costos sanitarios22.
El tratamiento con ACO puede prevenir la mayoría de los ACV isquémicos en los pacientes con FA y de esa forma mejorar significativamente su pronóstico e impactar positivamente en los costos en salud. El tratamiento con ACO ha demostrado ser superior a la ausencia de tratamiento o al tratamiento con antiagregantes plaquetarios1,2.
Las guías europeas de FA recomiendan, para valorar el riesgo embólico en pacientes con FA y definir el uso de ACO, al score CHA2DS2VASc (Figura 3), siendo hoy el score universalmente utilizado. Recomiendan el tratamiento con ACO a todos los pacientes con CHA2DS2VASc ³1 (excepto cuando este punto se genere por el hecho de ser mujer) (Figura 4). Concretamente, cuando el score es ³ 2 la recomendación del uso de ACO es IA, mientras que cuando el score es 1 el nivel de recomendación es IIaB, es decir, que debe considerarse, pues muchos pacientes podrían tener beneficio clínico de su utilización.

Figura 3: Score CHA2DS2VASc, escala de riesgo de ACV en fibrilación auricular recomendada actualmente por todas las guías. ACV: accidente cerebrovascular; AIT: accidente isquémico transitorio; TE: tromboembolismo.
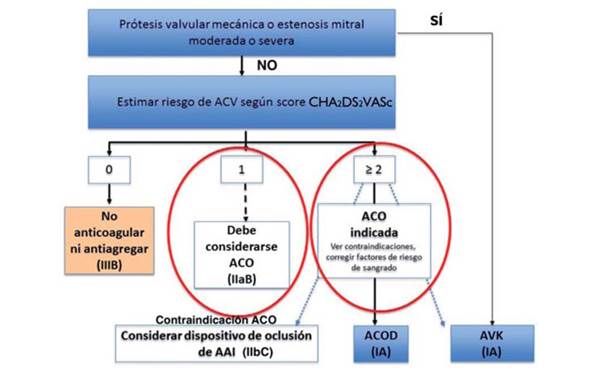
Figura 4: Modificado de referencia 1. ACO: anticoagulación oral; AAI: apéndice auricular izquierdo; ACOD: anticoagulantes orales directos; AVK: anticoagulantes orales antagonistas de la vitamina K; ACV: accidente cerebrovascular.
Por tanto, los pacientes con IC deberán recibir ACO de forma permanente y solo contraindicaciones reales o causas justificadas llevarán a la suspensión de la misma. Sin embargo, las guías norteamericanas publicadas dos años antes no obligan al tratamiento con ACO en pacientes con CHA2DS2VASc de 11,2.
En el estudio ARISTOTELES (apixabán para reducción de ACV y otros fenómenos embólicos en pacientes con FA no valvular) se demostró que la incidencia de eventos embólicos era mayor en pacientes con ICFEr que en pacientes con ICFEp, y a su vez menos frecuentes en pacientes sin IC.
El tratamiento con apixabán redujo el número de eventos embólicos en comparación con la warfarina en los tres grupos23.
En un subanálisis de pacientes con síntomas de IC del estudio RELY (dabigatrán versus warfarina en pacientes con FA no valvular) se mostró que los eventos embólicos eran mayores en pacientes con historia de IC. Se demostró, además, una mayor eficacia en la prevención de embolias de dabigatrán frente a la warfarina para todos los pacientes. Sin embargo, un metaanálisis que comparó pacientes con FA e ICFEr versus ICFEp, si bien encontró que los que tenían compromiso de la FEVI tenían mayor mortalidad, el número de eventos embólicos fue similar24,25.
En todo paciente al cual se le indique ACO, se deberá evaluar el riesgo hemorrágico. La escala HASBLED es la más recomendada actualmente. Debe tenerse en cuenta que ningún valor en el score de riesgo hemorrágico contraindica el uso de ACO, aunque sí incidirá en los controles y precauciones, además de obligar a corregir los factores de riesgo hemorrágico modificables1.
Es útil recordar que el beneficio neto de la ACO para la prevención de embolias en los pacientes con FA es contundente, a pesar de lo cual sigue siendo un tratamiento subutilizado y con una frecuente suspensión prematura del mismo. Las complicaciones hemorrágicas, tanto graves como leves, el alto riesgo percibido de sangrado con la ACO y los esfuerzos necesarios para monitorizar y ajustar la dosis de antagonistas de la vitamina K (AVK) son las razones más comunes para interrumpirlos o no prescribirlos26,27.
Sin embargo, el riesgo de ACV sin ACO normalmente excede el riesgo de sangrado, incluso en pacientes de edad avanzada, pacientes con disfunción cognitiva o con frecuentes caídas o fragilidad28,29.
Debe recordarse que el riesgo de sangrado con ácido acetilsalicílico (AAS) es similar al del tratamiento con AVK o con anticoagulantes orales directos (ACOD) -dabigatrán, rivaroxabán y apixabán-, mientras que estos, pero no el AAS, previenen de manera eficaz los ACV en pacientes con FA30,31).
Los ACOD son los fármacos preferidos para el tratamiento de los pacientes con FA no valvular ya que, comparados con los AVK, parecen ser al menos igual de efectivos y más seguros (menos hemorragias intracraneales) tanto en aquellos pacientes con o sin IC. Sin embargo, persisten dudas sobre su seguridad en pacientes añosos y con función renal reducida, en los cuales se deberá ajustar la dosis.
No están indicados en pacientes en hemodiálisis y con aclaramiento de creatinina por debajo de 15 ml/minuto/m2.
Para pacientes con IC y FA que tienen válvulas cardíacas mecánicas o estenosis mitral moderada o severa, solo se deben emplear AVK para la prevención de las tromboembolias1,2.
Como alternativa a los ACO, en pacientes con contraindicación para esta medicación y riesgo embólico elevado, se puede considerar el uso de un dispositivo de oclusión de la orejuela auricular izquierda32,33) .
La ACO, de preferencia con ACOD, es una parte esencial del tratamiento de todo paciente con FA e IC.
3.2. Control de la frecuencia ventricular
A pesar de ser dos patologías de alta prevalencia existen aspectos de su manejo sobre los cuales no existe una evidencia categórica. Un ejemplo es la mejor estrategia para el control de la frecuencia ventricular; todavía no está definitivamente establecido si el control estricto de la frecuencia cardíaca es mejor que el control más laxo de la misma en los pacientes con FA e ICFEr.
El estudio RACE II randomizó pacientes con FA persistente a control laxo de frecuencia cardíaca versus control estricto de la misma, no habiéndose encontrado diferencias en la mortalidad. El riesgo de hemorragias, hospitalización por IC y la presencia de síntomas fueron similares en ambos grupos. Cabe destacar que dos tercios de los pacientes eran asintomáticos, y la diferencia de la frecuencia cardíaca entre ambos grupos fue de solo 10 pm34).
Un análisis post hoc del RACE II, que se centró en pacientes con IC y FA, definió dos grupos, uno con ICFEr y otro con ICFEp. Aunque los pacientes con ICFEr eran un número pequeño, no existió diferencia entre ambos grupos (control estricto versus control laxo de la frecuencia) en mortalidad u hospitalizaciones, así como tampoco en los síntomas o en la ca lidad de vida.
En contraste, el registro sueco de IC demostró que en los pacientes con FA la mortalidad fue mayor en aquellos que presentaban una frecuencia cardíaca mayor de 100 pm y el uso de betabloqueantes se asoció a mejor pronóstico35,36.
Las guías norteamericanas (Colegio Americano de Cardiología - ACC, Asociación Americana del Corazón - AHA, Sociedad del Ritmo Cardíaco - HRS) de 2014 sobre manejo de la FA recomiendan un control laxo para pacientes asintomáticos y con función del ventrículo izquierdo conservada (recomendación clase IIb, nivel de evidencia B)2.
No existen estudios prospectivos que valoren específicamente el control de la frecuencia en pacientes con FA permanente e IC. En pacientes sintomáticos, el control adecuado de la frecuencia ventricular logra mejoría de la FEVI, que probablemente se deba a un componente taquimiocardiopático.
Por otra parte, la guía de IC 2016 de la Sociedad Europea de Cardiología considera que la frecuencia ventricular óptima en reposo en pacientes con FA e IC podría estar entre 60 y 100 pm, pero no está claramente establecido6.
Los datos del RACE II son tomados también por la guía europea de FA del mismo año, recomendando una frecuencia menor de 110 pm como objetivo de tratamiento para el control de la frecuencia en reposo. Sin embargo, como se mencionó antes, el Grupo de Trabajo de la guía de IC considera que en pacientes con IC es preferible una frecuencia más baja (60-100 pm)1,6.
Las frecuencias ventriculares < 70 pm se han asociado a peores resultados. Esto podría explicar por qué los bloqueadores beta administrados en las dosis máximas recomendadas por las guías no lograron reducir la morbilidad o la mortalidad en pacientes con ICFEr y FA. Podría explicar también la asociación entre digoxina y los resultados adversos con esta droga comunicados en algunos estudios observacionales sobre FA37-39.
Resumiendo, en pacientes sintomáticos con mal control de frecuencia el control laxo parece inapropiado. De no lograrse un control adecuado de la frecuencia y de los síntomas con el tratamiento farmacológico o cuando existen efectos adversos intolerables con este, se deberá considerar la ablación del nodo auriculoventricular (AV) e implante de marca paso definitivo.
Existe un grupo de pacientes con disfunción ventricular izquierda que responderá a la ablación del nodo AV e implante de marcapaso con estimulación unicameral desde el ventrículo derecho mejorando la función; sin embargo, otros pacientes pueden deteriorar su función con la estimulación desde el ápex del ventrículo derecho. El primer grupo, que mejora la función con la ablación y el control de la frecuencia, seguramente tenga asociado un componente taquimiocardiopático. Con la ablación del nodo AV se ha demostrado algún grado de taquimiocardiopatía en 25% a 50% de los pacientes40,41.
Un metaanálisis de Wood y colaboradores acerca de la evolución y sobrevida posterior a la ablación del nodo AV + marcapaso demostró una mejor tolerancia al ejercicio, una mejoría en la calidad de vida y también una mejoría en la FEVI en pacientes con disfunción previa. Sin embargo, no hubo, al año, diferencias signficativas con el tratamiento médico en cuanto a la sobrevida42.
Cabe recordar que la estimulación del ventrículo derecho puede tener consecuencias negativas en la función al generar disincronía ventricular, efectos adversos en el metabolismo y la perfusión con impacto en la remodelación del ventrículo izquierdo. Dado este potencial efecto deletéreo de la estimulación apical derecha, sumado al hecho de que el paciente se transforma en marcapaso dependiente, la estrategia de ablación del nodo AV e implante de marcapaso unicameral ha caído en descrédito, sin una clara justificación por la evidencia.
El advenimiento de la terapia de resincronización cardíaca (TRC) ha aportado otra herramienta útil en pacientes con bloqueo AV e ICFEr. La estimulación biventricular demostró ser mejor en comparación con la estimulación exclusiva del ventrículo derecho. Cuando se considera la TRC en pacientes con FA (pacientes con bloqueo de rama izquierda e ICFEr) se debe tener en cuenta tres factores: la TRC ha demostrado un beneficio en sobrevida, síntomas y parámetros ecocardiográficos comparables al de esta terapia en pacientes con ritmo sinusal; es imprescindible asegurar un porcentaje de estimulación cercano al 100%; se debe considerar la ablación del nodo AV43.
Una revisión sistemática analizó 768 pacientes con FA + IC sometidos a TRC, 339 con ablación del nodo AV y los restantes con control farmacológico de la frecuencia. Se demostró que los pacientes con ablación del nodo AV tenían menor mortalidad global y cardiovascular, y una mejoría en la clase funcional en comparación con aquellos con control farmacológico de la frecuencia ventricular (44.
También ha sido demostrado que la respuesta a la TRC + ablación AV es significativamente mejor en pacientes con miocardiopatia dilatada no isquémica que en la isquémica45.
Finalmente, debe recordarse que la TRC no ha demostrado disminuir la carga de FA en pacientes con ICFEr, aunque algunos pacientes resincronizados pueden recuperar ritmo sinusal43.
3.3. Control del ritmo
3.3.1. Prevención de fibrilación auricular en pacientes con disfunción ventricular
Tanto las guías norteamericanas como las europeas más recientes sugieren el tratamiento con inhibidores de la enzima convertidora de la angiotensina o inhibidores de la angiotensina II y de betabloqueantes en los pacientes con disfunción ventricular para prevención primaria de FA. También el uso de eplerenona ha demostrado su utilidad con este objetivo. No se recomiendan para prevención secundaria1,2,46.
3.3.2. Control farmacológico del ritmo
Las guías europeas 2016 recomiendan el control del ritmo para la mejoría sintomática en los pacientes con FA (recomendación clase I)1.
Muchas veces es difícil valorar clínicamente en forma adecuada la repercusión sintomática de la FA. El paciente se adapta a sus limitaciones y puede no percibir o transmitir adecuadamente las molestias. La reversión a ritmo sinusal con una cardioversión eléctrica y el uso de drogas antiarrítmicas para mantener, aunque sea transitoriamente, el ritmo sinusal, es de gran ayuda en discriminar la real repercusión sintomática de la FA.
En los pacientes con disfunción ventricular izquierda los recursos farmacológicos disponibles para el mantenimiento del ritmo sinusal son limitados. Según la evidencia actual las únicas drogas aceptables para estos pacientes son dofetilide (no disponible en nuestro país) y amiodarona. Son bien conocidas las limitaciones de la amiodarona, sobre todo para su uso en el mediano y largo plazo, por lo cual de elegirse este camino y ser efectiva en mantener el ritmo sinusal, debe usarse la mínima dosis posible10.
No existe evidencia de que el control del ritmo con amiodarona mejore significativamente el pronóstico de estos pacientes. El ensayo clínico más importante que comparó una estrategia de control de la frecuencia versus control del ritmo en pacientes con FA e IC fue el AF-CHF. En este estudio se randomizaron 1.376 pacientes a una estrategia de control del ritmo o de control de la frecuencia. En ambos grupos, 80% de los pacientes recibían betabloqueantes. En la rama de control del ritmo, 80% fueron tratados con amiodarona, y estaba en ritmo sinusal el 73% al final de 47 meses de seguimiento; en la rama de control de la frecuencia solo 35% estaban con ritmo sinusal. Sin embargo, la mortalidad cardiovascular, objetivo primario del estudio, fue similar en ambos grupos. Además, las internaciones fueron mayores en el grupo de control del ritmo47.
El control farmacológico del ritmo no ha demostrado mejorar el pronóstico de los pacientes con FA.
3.3.3. Ablación de la fibrilación auricular
A pesar del tratamiento farmacológico el desarrollo de IC en pacientes con FA no ha descendido en las últimas décadas, confirmando sus limitaciones48.
Más allá del énfasis en el valor del control de sus factores de riesgo, la ablación de la FA ha surgido y se ha posicionado como una alternativa muy atractiva al tratamiento farmacológico, con resultados mejores a este2.
Se han publicado numerosos estudios observacionales de ablación de FA en pacientes con IC que fueron a su vez analizados en conjunto en varios metaanálisis. Estos evidenciaron un éxito del procedimiento variable entre 54% y 82% luego de más de un procedimiento, una tasa de éxito menor a la de otras poblaciones10,49.
Recientemente se publicó un ensayo clínico randomizado, AATAC, comparando en un grupo de pacientes con FA e ICFEr (clase funcional II-III) portadores de un dispositivo (cardiodesfibrilador con o sin resincronización ventricular) el tratamiento con amiodarona (101 pacientes) versus la ablación (102 pacientes). El punto final primario fue la recurrencia de FA, que en este caso pudo ser valorada con gran precisión debido al dispositivo. Luego de un seguimiento de 24 meses, 70% de los pacientes del grupo ablación no tuvieron recurrencias de FA luego de 1,4 ± 0,6 procedimientos versus 34% en el grupo amiodarona (p <0,001). También se demostró una menor tasa de hospitalizaciones y una menor mortalidad, puntos finales secundarios, de menor peso pues el número de eventos fue bajo. La tasa de éxito del primer procedimiento de ablación fue variable en los diferentes centros entre 29% a 61%50.
En el estudio controlado PABA-CHF fue comparada la ablación de FA, en particular el aislamiento eléctrico de las venas pulmonares (41 pacientes), con la ablación del nodo AV + implante de marcapaso o desfibrilador con estimulación biventricular (40 pacientes) en pacientes con FA refractaria al tratamiento farmacológico. Los pacientes del grupo ablación de la FA mejoraron significativamente su calidad de vida, el test de caminata de 6 minutos y mejoraron la FEVI. El seguimiento fue particularmente corto, solo de seis meses51.
El seguimiento a más largo plazo (46 meses) en pacientes con FA y disfunción ventricular izquierda sometidos a ablación mostró una mayor tasa de recurrencias, aunque aquellos que se mantenían en ritmo sinusal demostraban una gran mejoría. Esto genera una gran expectativa en cuanto a que la evolución de las técnicas de ablación y accesorias y la mayor experiencia de los grupos puedan optimizar estos resultados52.
Técnicas de imagen podrían también ayudar a discriminar a priori quiénes son los pacientes que tienen más probabilidades de mejorar con este procedimiento y precisar la indicación. Un estudio con resonancia nuclear magnética evidenció que aquellos pacientes sin realce con gadolinio (ausencia de fibrosis en ventrículo izquierdo) tienen mayor probabilidad de mejoría con la ablación de la FA53) .
La ablación de FA en pacientes con IC es una estrategia a tener en cuenta. Sin embargo, debemos considerar que es más factible que los pacientes requieran más de un procedimiento y que los resultados no son aún comparables a los obtenidos en los pacientes sin cardiopatía.
4. Conclusiones
Prevenir complicaciones y mantener una buena calidad de vida son los objetivos del tratamiento. La estrategia general para el tratamiento de la FA no varía entre los pacientes con IC y otros, pero conviene jerarquizar el control estricto de ciertos factores de riesgo. Debemos recordar que el único tratamiento con un valor pronóstico probado en estos pacientes es el adecuado uso de la anticoagulación para prevención del ACV. El tratamiento inter vencionista es un recurso a considerar en ciertos pacientes.
Resumen conceptual
La IC es el más fuerte predictor de la aparición de FA.
La FA puede facilitar la aparición o la agravación de la IC.
La FA tiene un efecto negativo significativo en la mortalidad e internaciones de los pacientes con ICFEr.
El tratamiento y control adecuado de los factores de riesgo favorece el mantenimiento en ritmo sinusal.
La ACO es una parte esencial del tratamiento de todo paciente con FA e IC.
En pacientes sintomáticos con mal control de frecuencia el control laxo parece inapropiado.
El control farmacológico del ritmo no ha demostrado mejorar el pronóstico de los pacientes con FA.
La ablación de FA en pacientes con IC es una estrategia a tener en cuenta.














