Introducción
Como consecuencia del incremento de la edad poblacional, la estenosis aórtica (EA) es actualmente la valvulopatía que con mayor frecuencia determina un reemplazo valvular. Cuando no se realiza oportunamente el tratamiento quirúrgico adecuado, el pronóstico es malo. La indicación quirúrgica se basa en la presencia de síntomas, en el compromiso de la fracción de eyección de ventrículo izquierdo (FEVI) y en la severidad de la estenosis. El ecocardiograma Doppler (ED) es la técnica de elección para el diagnóstico y la cuantificación de su severidad mediante la utilización de la velocidad máxima (VMáx), el gradiente medio (GM) y el área valvular (AV) medida por la ecuación de continuidad1,2.
Para el diagnóstico preciso es fundamental una calidad óptima del registro de la señal Doppler. Esto se logra con la correcta alineación de las direcciones del chorro transvalvular y el haz de Doppler continuo (DC) y con buena relación señal/ruido. Esta depende de la distancia de la vena contracta (VC) al transductor, del tamaño del chorro en relación con el tamaño del haz de ultrasonido y de la sensibilidad del transductor3. La relación señal/ruido es baja en el adulto porque el chorro de estenosis está ubicado en el campo lejano del transductor, su tamaño es pequeño en relación con el del haz ultrasónico y la VC está próxima a la válvula calcificada, la cual genera ecos de gran amplitud que atenúan la señal del chorro. El transductor Pedof (DC sin imagen de eco 2D), al tener un cabezal más pequeño, permite una mejor penetración en los espacios intercostales, especialmente en la ubicación paraesternal derecha (PED). Por tener frecuencias más bajas que el transductor de eco 2D, mejora además la relación señal/ruido.
La EA debe ser valorada desde diferentes enfoques4-6, pero son muy escasos los trabajos diseñados para cuantificar su impacto7,8. Las Sociedades Europeas de Ecocardiografía y de Imagen Cardiovascular y la Sociedad Americana de Ecocardiografía aconsejan, para la valoración de la estenosis aórtica9,10, la utilización del transductor Pedof cuando se interroga el enfoque PED.
La disminución del tiempo dedicado a cada estudio, la VMáx y GM registrados con el transductor de eco 2D desde el enfoque apical y la utilización excepcional de Pedof desde el enfoque PED en nuestro país, dificultan la correcta valoración de la EA. La mala alineación del haz ultrasónico con el chorro de sangre de la EA subvalora la VMáx y el GM, y sobrevalora el AV.
La finalidad de este trabajo es determinar la magnitud de la reclasificación de la EA con la utilización del enfoque PED con transductor ciego.
Método
Población
Entre marzo de 2012 y diciembre de 2016 se incluyeron en forma prospectiva y consecutiva 100 pacientes con diagnóstico por ED de EA moderada o severa, según los criterios de las guías de la Sociedad Europea de Cardiología (ESC)1) y del Colegio Americano de Cardiología junto a la Asociación Americana del Corazón (ACC/AHA)2. Los criterios de EA moderada fueron: VMáx 3 a 3,9 m/s, GM 20 a 39 mmHg o AV cualquiera de los enfoques: VMáx ³ 4 m/s, GM ³ 40 mmHg o AV ? 1 cm2. Se excluyeron pacientes con FEVI <50%, insuficiencia valvular aórtica o mitral moderada o mayor(11,12), Hb <11g/dl, insuficiencia renal en hemodiálisis o intervención valvular previa.
Protocolo de estudio
A todos se les realizó un ED siguiendo las recomendaciones de la Sociedad Americana de Ecocardiografía9,10,13. El diámetro de la cámara de salida del ventrículo izquierdo (CSVI) se midió con zoom en la mesosístole, de borde interno a borde interno, en paralelo y próximo al plano valvular aórtico. Para medir la velocidad de CSVI se utilizó el Doppler pulsado (DP) en el enfoque apical. Se ubicó la muestra de volumen próxima al lado ventricular de la válvula a una altura que permitiese el registro de un flujo laminar. La VMáx de la válvula aórtica con DC se midió sobre el pico máximo de la curva, densa y bien dibujada, sin considerar ruidos y señales lineales finas. Con el trazado de la integral velocidad-tiempo sobre el borde externo de la señal densa se cuantificó el GM (Figura 1). De forma rutinaria se estudiaron las ventanas apical, PED con Pedof (borde derecho del esternón en diferentes espacios intercostales con el paciente en decúbito lateral derecho) y subxifoidea. Se utilizaron filtros de pared altos y ganancias de DC bajas para definir nítidamente las curvas Doppler que se desplegaron en la pantalla a velocidades de barrido de 100 mm/s. Para la obtención de la curva se tomó en cuenta la nitidez de los bordes, la intensidad de la señal y las características acústicas.
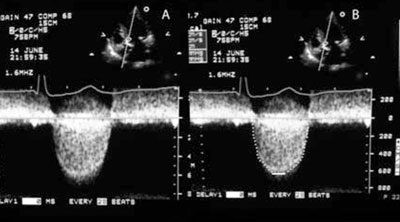
Figura 1 Registro con DC desde el enfoque apical. A: Registro sobre el que se realizan las mediciones. B: La VMáx se mide sobre el pico máximo de la curva, densa y bien dibujada, sin considerar los ruidos y las señales lineales finas. El trazado de la integral velocidad-tiempo se realiza sobre el borde externo de la envolvente, densa y bien definida.
La VMáx y el GM se definieron como el valor más alto obtenido desde cualquiera de los enfoques cuando la diferencia de las mediciones era mayor a 2DS para nuestra variabilidad interobservador: ³0,2 m/s para VMáx y ³4 mmHg para GM14. La FEVI se midió con el método Simpson biplano. Cuando el paciente estaba en ritmo sinusal cada medida se obtuvo promediando las obtenidas en tres latidos y en fibrilación auricular cinco latidos, preferentemente con frecuencias entre 60 y 90 contracciones por minuto. A todos los pacientes se les midió la tensión arterial inmediatamente después de terminado el registro de DC de la válvula aórtica. Si la tensión arterial era superior a 160/100 mmHg se volvía a realizar el estudio una vez normalizada la misma.
Se utilizaron equipos HP7500, HP5500 y GE Vivid I con transductores convencionales y Pedof (pequeños, doble cristal, frecuencia de 1.9 MHz y con alta relación señal/ruido). Los estudios se almacenaron digitalmente para el análisis offline.
Análisis estadístico
Los valores categóricos se expresaron como porcentaje, los continuos como medias ± desvío estándar (DE); las diferencias de las medias se analizaron con el test t de Student y los intervalos de confianza exactos se calcularon mediante el método de Fisher.
ResultadosFigura 3
En forma prospectiva y consecutiva se enrolaron 100 pacientes con una edad media de 74,0 ± 12,0 años, 49% de sexo femenino, 47% asintomáticos y 87% en ritmo sinusal con una FEVI media de 69,1% ± 8,4%, presión arterial sistólica de 133,1 ± 16 mmHg y diastólica de 76 ± 15,6 mmHg (Tabla 1).
Tabla 1 Datos generales de 100 pacientes con estenosis aórtica moderada o severa
| Datos | Resultados |
| Edad | 74,0 ± 12,0 años |
| Sexo femenino | 49/100 (49%) |
| ASC | 1,82 ± 0,2 m2 |
| CSVI | 20,4 ± 3 mm |
| FEVI | 69,1 ± 8,4% |
| Presión arterial sistólica | 133,1 ± 16 mm Hg |
| Presión arterial diastólica | 76 ± 15,6 mm Hg |
| Asintomáticos | 53/100 (53%) |
| Ritmo sinusal | 87/100 (87%) |
| Coronario conocido | 15/100 (15%) |
| HTA | 67/100 (67%) |
| Diabetes | 20/100 (20%) |
| Dislipemia | 36/100 (36%) |
| Tabaquismo | 5/100 (5%) |
ASC: área de superficie corporal; CSVI: diámetro de cámara de salida del ventrículo izquierdo; Coronario conocido: paciente con infarto agudo de miocardio, angioplastia coronaria o puente coronario previos.
No se encontraron diferencias estadísticamente significativas en las VMáx y GM obtenidos desde ÁPEX y PED entre los pacientes en FA y en ritmo sinusal.
La factibilidad del enfoque apical fue de 97% y la de PED 75%. Los valores más altos de VMáx y GM se obtuvieron en el enfoque apical en 33/100 (33%), en PED 48/100 (48%) y en más de un enfoque en 19/100 (19%) (Tabla 2). En el 3% en el enfoque subxifoideo se obtuvieron valores similares al apical o PED.
Tabla 2 Enfoques en que se registran los máximos valores de VMáx y GM
| Enfoques | Resultados |
| Enfoque ÁPEX | 33/100 (33%) |
| Enfoque PED | 48/100 (48%) |
| > de un enfoque | 19/100 (19%) |
Las medias de VMáx y de GM fueron más altas en el enfoque PED que en el apical. La VMáx media en ápex fue 4,09 ± 0,6 m/s y en PED 4,3 ± 0,6 m/s (p < 0,05), en tanto el GM apical fue 40,3 ± 0,7 mmHg y en PED 45,0 ± 0,7 mmHg (p < 0,05) (Tabla 3).
Tabla 3 Promedio de medidas de VMáx, GM y AV
| V Máx en ÁPEX | 4,09 ± 0,6 m/s | p < 0,05 |
| V Máx en PED | 4,3 ± 0,6 m/s | |
| GM en ÁPEX | 40,3 ± 0,7 mmHg | p < 0,05 |
| GM en PED | 45,0 ± 0,7 mmHg | |
| AV por ÁPEX | 0,89 ± 0,27 cm2 | p NS |
| AV por PED | 0,86 ± 0,26 cm2 |
Cuando se catalogó la EA solamente por ÁPEX (Tabla 4), 56 fueron clasificadas como severas y 44 como no severas (33 como moderadas y 11 como leves). La utilización del enfoque PED reclasificó como severas 18/33 (54,6%, IC 95% 36,4-71,9) que eran moderadas por ÁPEX (Figura 1) y 3/11 (27,3% IC 95% 6,0-61,0) leves por ÁPEX (Figura 2) . En total 21/44 (47,7%) de las EA no severas por ÁPEX fueron reclasificadas como severas por PED, es decir uno de cada dos pacientes.
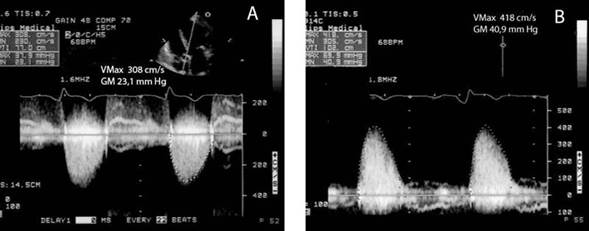
Figura 2 Registros desde ÁPEX y PED en el mismo paciente. A: ÁPEX con valores de VMáx y GM que catalogan la EA como leve. B: PED con Pedof con VMáx y GM correspondientes a EA severa.
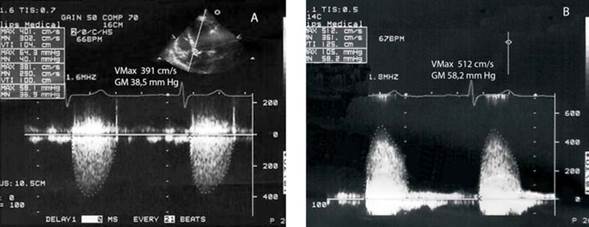
Figura 3 Registros desde ÁPEX y PED en el mismo paciente. A: ÁPEX con valores de VMáx y GM de EA moderada. B: PED con Pedof con VMáx y GM correspondientes a EA muy severa.
Tabla 4 Grados de severidad de la estenosis aórtica desde los diferentes enfoques.
| Severidad de la EA | Resultados |
| EA severa por ÁPEX | 56/100 (56%) |
| EA no severa por ÁPEX | 44/100 (44%) |
| EA moderada por ÁPEX y severa por PED | 18/33 (54,5%) IC 95% 36,4-71,9 |
| EA leve por ÁPEX y severa por PED | 3/11 (27,3 %) IC 95% 6,0-61,0 |
La EA muy severa con VMáx ³5 m/s se registró en 15/100. En ÁPEX se obtuvo en 4/15 (26,7%), PED en 7/15 (46,7%) y en más de un enfoque en 4/15 (26,7%). Entre las EA asintomáticas y severas por ÁPEX, 3/39 (7,7%) fueron reclasificadas por PED como EA muy severas.
Discusión
Este trabajo demuestra que utilizar solo el enfoque apical no diagnostica una de cada dos EA severas, valoradas como leves o moderadas por ÁPEX. Uno de los obstáculos en el manejo clínico de los pacientes con EA es la correcta valoración de la severidad de la valvulopatía. Ella explica la causa de los síntomas y ayuda a establecer el momento óptimo de la sustitución valvular.
Las guías establecen como criterios de severidad de la EA: VMáx ³4 m/s, gradiente medio ³40 mmHg o área valvular ?1 cm2(1,2. Las mediciones de las velocidades, GM y la CSVI tienen variaciones en las medidas que se multiplican en la ecuación de continuidad del AV con el consiguiente arrastre de los errores. En esta población se excluyeron las situaciones que podían aumentar el flujo transvalvular (anemia, regurgitaciones, fístulas arteriovenosas) y las que podían disminuirlo (compromiso de la FEVI). Se tomó el valor más alto entre los enfoques cuando era superior a 2 DS de nuestra variabilidad interobservador14. Como el diámetro y la velocidad de la CSVI no varían si se considera uno u otro enfoque y se minimiza la variación del flujo valvular, la VMáx y el GM dependen directamente de la severidad de la EA. Su valoración requiere especial cuidado en los aspectos técnicos. La causa más frecuente de error es subestimar la VMáx y el GM por no alinear en forma paralela el haz del DC con la dirección del chorro estenótico. Nosotros coincidimos con la reciente recomendación del uso de Pedof desde múltiples enfoques9,10. La disminución del tiempo dedicado a cada estudio en nuestro país, el menor entrenamiento en obtener imágenes desde el PED y la utilización del transductor de eco 2D con DC llevan a que habitualmente la EA solo se valore desde el enfoque apical.
Una de las primeras publicaciones que llama la atención sobre el enfoque PED en la EA4, señala que tiene una factibilidad de solo 49%, pero con mejor correlación con la hemodinamia que el enfoque apical. Otto6, en el trabajo de seguimiento de EA, considera los enfoques PED y supraesternal juntos y obtiene los valores más altos de VMáx y GM en 33% de los casos. De Monchy7 utiliza únicamente el AV como criterio de severidad y describe un error de clasificación entre ápex y PED de 21% (17% de leve a moderada y 4% de moderada a severa). Thaden8, que también utiliza criterios de severidad por AV, describe una factibilidad del PED de 81% con obtención de los valores más altos en el 50%. Si solo se utiliza el enfoque apical hay 23% de error. En nuestra población se considera EA severa cuando, desde cualquier enfoque, está presente uno de los tres criterios: VMáx, GM o AV. En EA no severa por ÁPEX fueron reclasificadas como severas por PED 21/44 (47,7%).
Las guías sobre manejo de la enfermedad valvular de la AHA/ACC2 recomiendan como indicación clase IIA la sustitución valvular aórtica en la EA severa asintomática con FEVI conservada y VMáx ³5 m/s, en tanto la ESC la aconseja con VMáx ³5,5 m/s (1. En un trabajo reciente, Zilberszac15 realiza un seguimiento de 103 pacientes mayores de 70 años con EA severa asintomática. Define la EA muy severa con una VMáx ³5 m/s en base a que es un punto de corte que predice la evolución en forma independiente. La sobrevida libre de eventos de la EA con VMáx entre 4 m/s y 5 m/s comparada con ³5 m/s a un año es de 84% y 57% y a los dos años de 57% y 21%, respec tivamente.
En el presente estudio la EA asintomática y severa por ÁPEX es reclasificada por PED como muy severa en 3/39 (7,7%).
En el informe ecocardiográfico debe consignarse específicamente desde qué enfoque se obtienen las velocidades y gradientes máximos. Estos datos serán fundamentales para el seguimiento clínico del paciente. En los sucesivos ED de control, si no se especifica desde qué enfoque se obtienen las medidas, sus variaciones pueden interpretarse como una rápida progresión de la EA, con la consiguiente indicación errónea de sustitución valvular.
Conclusiones
La utilización rutinaria del enfoque PED es mandatoria en todo estudio de EA. La VMáx y el GM de mayor valor se obtienen en el 48% de los casos desde el PED. Esto lleva a que prácticamente una de cada dos EA no severa por ÁPEX, sea severa por PED. En la EA asintomática severa por ÁPEX, el PED reclasifica como muy severa el 7,7%. En el seguimiento clínico de la EA, el informe ecocardiográfico debe consignar específicamente desde qué enfoque se obtienen VMáx y GM.














