Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Uruguaya de Cardiología
versión impresa ISSN 0797-0048versión On-line ISSN 1688-0420
Rev.Urug.Cardiol. vol.31 no.1 Montevideo abr. 2016
ESPECIAL
FIBRILACIÓN
AURICULAR
Artículo de revisión
Ablación por catéter de fibrilación auricular en Latinoamérica: resultados del primer registro de la Sociedad Latinoamericana de Estimulación Cardíaca y Electrofisiología (SOLAECE)
Catheter ablation of atrial fibrillation in Latin America: results of the first registry of the Latin American Society of Pacing and Electrophysiology Cardiac (SOLAECE)
Dres. Roberto Keegan1, Luis Aguinaga2, Nicolás Valera1, Guilherme Fenelon3,
William Uribe4. En representación de los investigadores del Registro SOLAECE*
1. Servicio de Electrofisiología, Hospital Privado del Sur, Bahía Blanca, Argentina.
2. Centro Privado de Cardiología, Tucumán, Argentina.
3. Escuela Paulista de Medicina, San Pablo, Brasil.
4. Servicio de Electrofisiología, CES Cardiología y Clínica Las Américas, Medellín, Colombia.
* Ver anexo
Resumen
Objetivo: conocer los resultados de la ablación por catéter de fibrilación auricular (FA) en Latinoamérica.
Material y método: se analizaron los resultados (éxito agudo, complicaciones totales y complicaciones mayores) de los procedimientos de ablación de FA paroxística (FA-P), FA-NO paroxística (FA-NP) y FA total (FA-P + FA-NP) incluidos en el Primer Registro Latinoamericano de Ablación por Catéter dirigido y coordinado por la Sociedad Latinoamericana de Estimulación Cardíaca y Electrofisiología (SOLAECE), y su relación con las características de los centros. Las variables categóricas se expresaron como proporciones y se compararon utilizando la prueba de chi cuadrado. Se consideró diferencia estadísticamentemente significativa un valor de P < 0,05.
Resultados: la FA fue el cuarto sustrato más frecuentemente abordado con 1.649 procedimientos (11%). De ellos, 1.161 fueron de FA-P (70,4%) y 488 de FA-NP (29,6%). El número de ablaciones de FA al año fue de 30 o menos en 46 centros (81%); 50 o más en siete centros (12%), y 100 o más en cinco centros (9%). El promedio por centro fue de 26. El éxito agudo de la ablación de FA total fue de 90%. No se observaron diferencias entre FA-P y FA-NP (88,9% versus 90,8%, P=NS). La tasa de complicaciones totales fue de 8,31%, y tampoco se observaron diferencias entre los dos sustratos (FA-P 8,4% versus FA-NP 8,2%, P=NS). Las complicaciones mayores fueron de 4,12%. El resultado de la ablación (éxito agudo y complicaciones) se relacionó principalmente con el volumen de procedimientos de los centros.
Conclusiones: los resultados de la ablación de FA en Latinoamérica son similares a los reportados en el resto del mundo. La experiencia del centro se relacionó directamente con los resultados, en particular con las complicaciones. Aquellos centros con tasas elevadas de complicaciones mayores deberían reanalizar sus programas de ablación de FA a fin de mejorar la seguridad de este tratamiento.
Palabras clave:
FIBRILACIÓN AURICULAR
ABLACIÓN
CATÉTER
REGISTRO
LATINOAMÉRICA
Objective: to evaluate the results of catheter ablation of atrial fibrillation (AF) in
Material and methods: the results (acute success, total complications and major complications) of ablation procedures of paroxysmal-AF (AF-P), Non-paroxysmal (AF-NP), and total FA (AF-P + AF-NP) included in the First Latin American Catheter Ablation Registry coordinated by SOLAECE were analyzed and the relationship of these results with the characteristics of the centers were established. Categorical variables were expressed as proportions and compared using the chi2 test. A P value of <0,05 was considered statistically significant.
Results: AF was the fourth most frequently substrate treated with 1,649 procedures (11%). Of these, 1,161 were AF-P (70.4%) and 488 AF-NP (29.6%). The number of AF ablations per year was 30 or less in 46 centers (81%), 50 or more in 7 (12%) and 100 or more in five (9%). The per center procedures average was 26. The acute ablation success of total AF was 90%. No difference between acute ablation success of AF-P and AF-NP (88.9% vs 90.8%, P=NS) was observed. The total complications rate was 8.31%, and no difference between the two substrates was observed (AF-P 8.4% vs AF-NP 8.2%, P =NS). Major complications rate was 4.12%. The result of ablation (acute success and complications) was related mainly to the number of procedures performed by the center.
Conclusions: the results of AF ablation in
Key words:
ATRIAL FIBRILLATION
ABLATION
REGISTRY
LATIN AMERICA
Introducción
Hasta hace poco más de 15 años la estrategia de control del ritmo de la fibrilación auricular (FA) estaba basada casi exclusivamente en el uso de fármacos antiarrítmicos, la mayoría de ellos de eficacia clínica limitada. Solo muy pocos pacientes eran candidatos a otras alternativas de tratamiento no farmacológico, como la quirúrgica, en particular aquellos pacientes con otras indicaciones para la cirugía cardíaca. Desde que en 1998, Haissaguerre y colaboradores(1) demostraron la utilidad clínica de la ablación por catéter de extrasístoles originadas en las venas pulmonares en el tratamiento de la FA paroxística (FA-P), los resultados alentadores observados en estudios clínicos realizados con posterioridad y en diferentes partes del mundo, empleando diferentes técnicas y estrategias de aislamiento eléctrico de las venas pulmonares(2-12), permitieron que muchos más pacientes comenzaran a beneficiarse de esta nueva terapéutica. Sin embargo, pocos estudios han evaluado los resultados de este tratamiento en Latinoamérica(13-15). En este trabajo se analizan los resultados de los procedimientos de ablación por catéter de FA incluidos en el Primer Registro Latinoamericano de Ablación por Catéter dirigido y coordinado por la Sociedad Latinoamericana de Estimulación Cardíaca y Electrofisiología (SOLAECE)(16).
Material y método
El Primer Registro Latinoamericano de Ablación por Catéter(16) incluyó información relacionada con las características de los centros participantes y con los resultados de la ablación de procedimientos realizados entre el 1º de enero y el 31 de diciembre de 2012. La ablación de la FA-P y la FA no paroxística (FA-NP) fueron dos de los 17 procedimientos analizados.
Entre las características de los centros participantes se evaluó su carácter académico (universitario o no universitario), su relación con el sistema de salud (institución pública o privada), el número de camas de la institución, la disponibilidad de cirugía cardíaca, el tipo de sala para la realización de los procedimientos electrofisiológicos (sala exclusiva de electrofisiología, sala de cateterismos o quirófano), los días de la semana asignados a la realización de procedimientos electrofisiológicos, el tipo de equipamiento para la provisión de fluoroscopía (angiógrafo fijo, arco en C de ánodo rotatorio o arco en C de ánodo fijo), la disponibilidad y tipo de sistema de navegación electroanatómica tridimensional (Carto®, EnSite®, o ambos), la disponibilidad de ecocardiografía intracardíaca y de crioablación, y número de electrofisiólogos en cada centro.
De los procedimientos de ablación se analizó el número total de pacientes y de procedimientos, el éxito agudo, el tipo de catéter utilizado (4 mm, 8 mm o de punta irrigada), el tipo de energía empleada (radiofrecuencia o crioablación), el tipo de fluoroscopía, la utilización de mapeo electroanatómico, el tipo de anestesia (local, sedación consciente o general) y el número de pacientes con al menos una complicación durante la hospitalización.
El éxito agudo se determinó al finalizar el procedimiento y se lo consideró al aislamiento completo (bloqueo de salida y de entrada) de todas las venas pulmonares cuando el paciente tenía FA-P, y al aislamiento de todas las venas pulmonares más lesiones adicionales tales como líneas, electrogramas fraccionados complejos, etcétera, cuando el sustrato ablacionado fue la FA-NP. Las complicaciones incluyeron hematoma, fístula arteriovenosa, trombosis o tromboflebitis, neumotórax, derrame pleural, bloqueo auriculoventricular (AV) que no requirió implante de marcapasos definitivo, bloqueo AV que requirió implante de marcapasos definitivo, pericarditis, derrame pericárdico, taponamiento cardíaco, infarto/isquemia de miocardio, insuficiencia cardíaca/edema agudo de pulmón, accidente cerebrovascular isquémico transitorio (AIT), accidente cerebrovascular (ACV), embolismo sistémico, muerte u otras complicaciones. Se consideraron complicaciones mayores relacionadas a la ablación de FA la fístula arteriovenosa femoral, el derrame pleural, el infarto/isquemia de miocardio, la insuficiencia cardíaca/edema aguado de pulmón, el AIT, el ACV, la embolia periférica, el taponamiento cardíaco y la muerte.
Finalmente se analizó la relación del sustrato (FA total, FA-P y FA-NP) y el resultado del procedimiento (éxito agudo, complicaciones totales y complicaciones mayores) con las características de los centros. Las variables de los centros evaluadas fueron el volumen de procedimientos (cantidad de ablaciones de FA realizadas en el período de inclusión en el registro –un año–), su carácter académico (universitario o no universitario) y su relación con el sistema de salud (público o privado). A fin de realizar análisis comparativos, los centros se agruparon de acuerdo al volumen de procedimientos al año en 0 a 10, 10 a 20, 20 a 30, 30 a 40, 40 a 50, 60 a 70, 70 a 80, 90 a 100, 120 a 130, 130 a 140, 200 a 210 y 290 a 300.
Análisis estadístico
Las variables categóricas analizadas se expresaron como proporciones y se compararon utilizando la prueba de chi cuadrado. Se consideró diferencia estadísticamente significativa un valor de P < 0,05.
Resultados
Se incluyeron datos provenientes de 120 centros de 13 países: Argentina, Bolivia, Brasil, Chile, Colombia, Cuba, El Salvador, Guatemala, México, Perú, República Dominicana, Uruguay y Venezuela.
La ablación de FA fue realizada en 57 de los 120 centros (52%) y en 7 de los 13 países (54%): Argentina, Brasil, Chile, Colombia, México, Uruguay y Venezuela.
Del total de 15.099 procedimientos de ablación incluidos en el registro, la FA total representó el cuarto sustrato más frecuente con 1.649 procedimientos (11%): 1.161 de FA-P (70,4%) y 488 de FA-NP (29,6%).
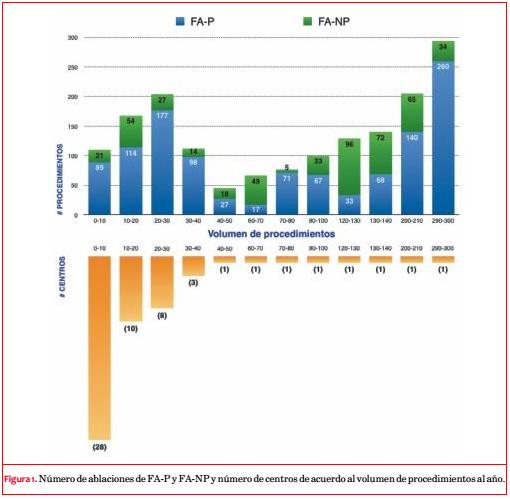
En la figura 1 se observa el número de procedimientos de FA-P y FA-NP y el número de centros en relación con el volumen de procedimientos. El número de ablaciones al año fue de 30 o menos en 46 centros (81%), 50 o más en 7 (12%) y 100 o más en 5 (9%). El promedio de ablaciones por centro fue de 26.
La radiofrecuencia fue la energía utilizada en casi todos los procedimientos. En solo dos se utilizó crioablación con balón (0,12%).
El navegador electroanatómico fue utilizado en el 87% de las ablaciones y la ecocardiografía intracardíaca en 61%.
El 81,3% de los procedimientos fueron realizados con anestesia general.
El éxito agudo de la ablación de FA total fue de 90%. No se observaron diferencias entre el éxito de ablación de FA-P y FA-NP (88,9% versus 90,8%, P=NS). La tasa de complicaciones totales fue de 8,31%, y tampoco se observaron diferencias entre los dos sustratos (FA-P 8,4% versus FA-NP 8,2%, P=NS). Las complicaciones mayores fueron de 4,12%: fístula arteriovenosa 0,73%; derrame pleural 0,36%; infarto/isquemia de miocardio 0,12%; insuficiencia cardíaca/edema agudo de pulmón 0,24%; AIT 0,36%; ACV 0,24%; embolia periférica 0,06%; taponamiento cardíaco 1,94%, y muerte 0,06%. Aunque la única muerte ocurrió fuera del período de hospitalización (alejada) fue incluida igualmente en el análisis. Esta se relacionó a la ablación de FA-P en un centro que realizó menos de diez procedimientos en el año.
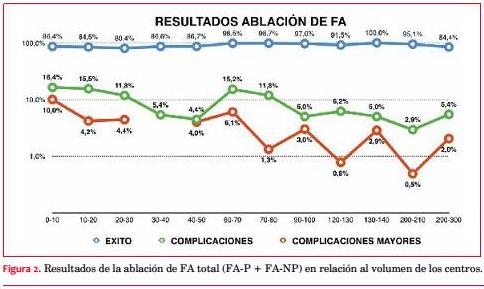
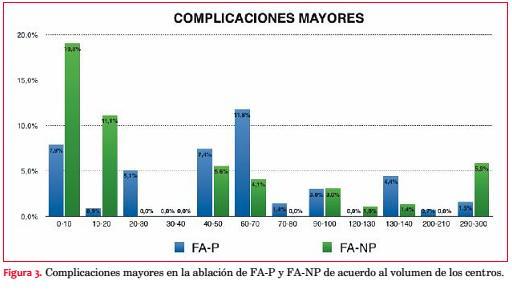
La figura 2 muestra los resultados de la ablación de FA total en relación con el volumen de procedimientos de los centros. Las complicaciones mayores fueron superiores a 4% en los centros con menos de 70 procedimientos al año y de 3% o menos en aquellos con más de 70 ablaciones anuales. Las complicaciones mayores en la ablación de FA-NP superaron el 10% en los centros que realizaron 10 a 20 procedimientos y alcanzaron casi el 20% en aquellos con 0 a 10 (figura 3).
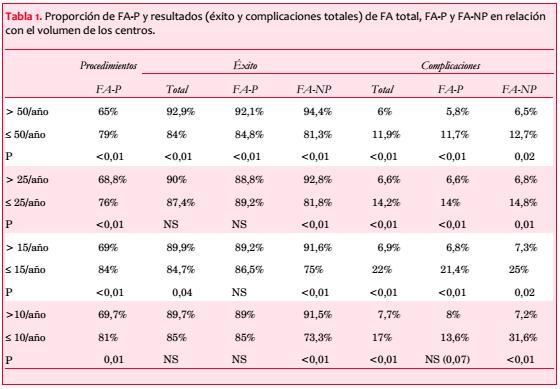
Por último, el volumen de los centros también se relacionó con la tasa de complicaciones totales. Esta fue significativamente más baja para todos los sustratos (FA total, FA-P y FA-NP) en los centros de mayor volumen en casi todos los grupos analizados (>50, >25 o >15 versus £50, £25 o £15, respectivamente). También fue significativamente más baja la tasa de complicaciones de FA total y de FA-NP en los centros con >10 procedimientos al año respecto de aquellos con £10, con una tendencia a presentar menos complicaciones en la ablación de FA-P (tabla 1).
Discusión
La ablación por catéter de la FA sintomática y refractaria al tratamiento médico con al menos un antiarrítmico es una terapia que actualmente se encuentra bien establecida para el control del ritmo, con indicaciones incluidas en diferentes guías de recomendación elaboradas tanto por sociedades científicas de Estados Unidos, Canadá y Europa(17-20) como de Latinoamérica(21-23).
El éxito agudo de la ablación de FA-P al finalizar el procedimiento es determinado por el aislamiento completo de las venas pulmonares. En un estudio reciente que comparó la ablación por catéter con los fármacos antiarrítmicos, el aislamiento completo de las venas pulmonares confirmado por bloqueo de entrada se alcanzó en el 87% de los pacientes(24), resultado similar al observado en el Primer Registro Latinoamericano (90%). En este último solo se analizó el éxito agudo al finalizar el procedimiento, por lo que se desconoce el resultado clínico evaluado por la proporción de pacientes que permanecen libres de arritmia en el seguimiento. Sin embargo, es razonable especular con que sea similar al reportado en otros estudios debido a que la efectividad de este procedimiento no parece haberse modificado significativamente a lo largo del tiempo a pesar de los cambios en las técnicas específicas de ablación utilizadas, de la incorporación de nuevas y mejores tecnologías y la experiencia creciente de los operadores. Entre los primeros 45 pacientes reportados por Haissaguerre y colaboradores en 1998(1), el 62% de ellos estaba libre de arritmia, sin recibir fármacos antiarrítmicos, a los 8±6 meses de seguimiento. Este resultado es similar al observado en una encuesta nacional reciente que analizó 2.137 procedimientos de ablación realizados en 158 instituciones, y en los que el 68,6% de los pacientes con FA-P sometidos a su primer procedimiento y que no recibían fármacos antiarrítmicos estaban libres de recurrencia arrítmica a los 12 meses(12). Tampoco se observó una mejoría significativa en la experiencia de centros únicos de alto volumen a lo largo de los últimos años(25).
Los resultados favorables de esta técnica permitieron que rápidamente se incorporara a la práctica clínica como una alternativa efectiva de tratamiento para pacientes con FA paroxística o persistente, sintomática y en general refractaria a fármacos antiarrítmicos. Por consiguiente, el número de pacientes tratados en el mundo se incrementó notablemente. Sin embargo, la aparición de complicaciones relacionadas al procedimiento, alguna de estas no observada en la ablación de otros sustratos, comenzaron a generar preocupación acerca de la seguridad de esta técnica. En dicho sentido, numerosos factores comenzaron a ser analizados en un intento por establecer estándares que permitieran ofrecer una mayor seguridad a este procedimiento. La seguridad adquiere mayor relevancia aún si se tiene en cuenta que el beneficio clínico de la ablación es la mejoría sintomática y de la calidad de vida, no habiéndose demostrado hasta ahora que este tratamiento reduzca la frecuencia de ACV o la mortalidad.
Existen pocos datos acerca de la ablación de FA en Latinoamérica, todos ellos retrospectivos y provenientes de centros únicos y de registros nacionales. Uribe y colaboradores(26) analizaron los resultados de la ablación realizada en un único centro colombiano en el período comprendido entre diciembre de 2004 y julio de 2008. De los 100 pacientes consecutivos con FA-P refractaria a por lo menos un fármaco antiarrítmico incluidos en el estudio, el aislamiento de las cuatro venas pulmonares fue logrado en el 93% de los casos y las complicaciones mayores alcanzaron el 8% (taponamiento cardíaco 3%; elevación transitoria del segmento ST 1%; atrapamiento del catéter circular 1%; pseudoaneurisma femoral 1%; AIT 1%, y estenosis de venas pulmonares 1%). Labadet y colaboradores(27) presentaron recientemente los resultados de la ablación de FA-P y persistente de 126 procedimientos realizados en Argentina en el período comprendido entre enero de 2010 y agosto de 2013. El aislamiento de todas las venas pulmonares fue logrado en el 92% de los procedimientos y en el 5,5% se presentaron complicaciones mayores (estenosis de venas pulmonares 0,8%; taponamiento cardíaco 0,8%; pseudoaneurisma femoral 1,6%; fístula arterio-venosa 0,8%; relacionada a la anestesia 0,8%, y pericarditis sin derrame 0,8%). En 2007, Fenelon y colaboradores(13) publicaron los resultados del Registro de Ablación de Fibrilación Auricular en Brasil, en el que se analizaron los resultados del procedimiento realizado en 755 pacientes provenientes de 29 centros en cinco estados. La tasa de complicaciones mayores alcanzó el 7,16% (fístula atrio-esofágica 0,1%; estenosis/oclusión de venas pulmonares 0,4%; AIT 1,4%; ACV 1%; taponamiento cardíaco 3,8%; lesión del nervio frénico 0,2%, y mortalidad 0,26%). Otras complicaciones fueron hematoma/hemorragia 2,3%; derrame pericárdico 0,9%; accidentes anestésicos 0,4%, y taquicardia posablación 3,8%. En el Registro Nacional de Ablación por Catéter 2009(14) se analizaron los datos de 1.549 procedimientos realizados en 17 centros de 12 provincias argentinas. La FA fue el cuarto sustrato más frecuentemente abordado (8%, 119 procedimientos) y el de mayor tasa de complicaciones totales (14,3%). La tasa de complicaciones mayores fue similar a la observada en el Registro Brasileño, alcanzando el 6,6% (taponamiento cardíaco 3,4%; ACV 0,8%; embolia periférica 0,8%; sangrado orofaríngeo 0,8%, y fístula arterio-venosa 0,8%). No se observó ninguna muerte relacionada con el procedimiento. En el Registro Nacional de Ablación por Catéter 2010(15), en el que se analizaron los resultados de 1.500 procedimientos realizados en 24 centros de nueve provincias argentinas, la FA permaneció como el cuarto sustrato más frecuentemente abordado. Sin embargo, la proporción de procedimientos de ablación fue mayor que en el registro anterior (16%) y la tasa de complicaciones totales notablemente inferior (5,5%). No se produjo ninguna muerte relacionada con el procedimiento.
Mientras que la mayor efectividad del método sigue siendo un objetivo a mejorar, probablemente los mayores esfuerzos están destinados a brindar mayor seguridad con el fin de reducir las complicaciones, en particular aquellas más serias que pueden poner en riesgo la vida del paciente o que puedan dejar secuelas invalidantes. Sin embargo, aún no se ha establecido con claridad el nivel de experiencia requerido, los niveles mínimos de efectividad y los límites máximos de complicaciones aceptables para la realización de ablación de FA(29). Aunque la guía sobre el manejo de la FA de ACCF/AHA/HRS(19) recomienda que el procedimiento sea realizado en centros experimentados (>50 ablaciones de FA al año), no se hace referencia a ninguna evidencia que avale esta recomendación. La guía de la Sociedad Cardiovascular Canadiense(30) establece niveles de efectividad (60%-75% luego de un procedimiento y 75%-90% luego de dos) y de seguridad (complicaciones totales 2%-3%; del acceso vascular 1%-2%; perforación cardíaca 0,5%- 1%, y tromboembolismo 0,5%-1%) basando la referencia en los datos de la segunda encuesta mundial(10). Sin embargo, llama la atención que la tasa de complicaciones observadas en esta última es superior a la recomendada por la guía. En cuanto al riesgo del procedimiento, es importante también tener presente la posibilidad de subregistro de complicaciones, entre otras causas debido a que la mayoría de los estudios y registros solo incluyen las complicaciones diagnosticadas durante la hospitalización. Datos recientes de una encuesta muestran que las complicaciones mayores durante la internación de 4.156 pacientes sometidos a una primera ablación de FA fueron de 5,1%(31). Sin embargo, 9,4% fueron rehospitalizados dentro de los 30 días. Asumiendo que todos los eventos fueron incluidos, que fueron independientes y que no fueron doblemente contabilizados, las tasas de complicaciones finalmente serían: muerte 0,24%; ACV 0,7%, y taponamiento 2,79%, cifras estas más altas que las observadas en la encuesta mundial(10). Aunque es posible una tasa de complicaciones mayores menor a 2%, este nivel solo ha sido reportado por centros únicos con gran volumen de procedimientos y con la experiencia obtenida a través de largos períodos de práctica(25,28). Por lo tanto, tasas de complicaciones mayores a 4% tal vez deban motivar al centro a reanalizar su programa de ablación de FA con el fin de identificar y modificar los factores relacionados con estas complicaciones a los efectos de mejorar la seguridad del procedimiento.
Limitaciones
Debido al carácter voluntario de la participación en el Primer Registro Latinoamericano, los resultados solo expresan la experiencia de los centros participantes y no la de todos los centros latinoamericanos. Al igual que en otros registros, la información brindada por los investigadores no está sujeta a verificación. Finalmente, la falta de datos de seguimiento no permiten conocer información acerca del resultado clínico de este procedimiento y de las complicaciones alejadas.
Conclusiones
El Primer Registro Latinoamericano de Ablación por Catéter puede considerarse como una muestra de datos representativa de esta técnica en Latinoamérica, en el que los resultados son similares a los reportados en el resto del mundo. La experiencia del centro fue el factor que mayor relación tuvo con los resultados, en particular con las complicaciones. Aquellos centros con tasas elevadas de complicaciones mayores deberían reanalizar sus programas de ablación de FA con el fin de mejorar la seguridad de este tratamiento.
Anexo: investigadores y centros
Argentina: Nicolás Valera, Hospital Privado del Sur, Bahía Blanca; Alejandro Villamil, Hospital El Cruce y Hospital Santojanni, Buenos Aires; Andrés Bochoeyer, Sanatorio Mitre, Buenos Aires y Hospital de Alta Complejidad, Formosa; Carlos Labadet, CEMIC, Buenos Aires; Claudio De Zuloaga, Hospital Nacional Alejandro Posadas, Buenos Aires; Claudio Militello, Sanatorio Sagrado Corazón, Buenos Aires; Claudio Poliserpi, Hospital Policial Bartolomé Churruca, Buenos Aires; Daniel Dasso, Hospital Juan A. Fernández, Buenos Aires; Enrique Retyk, Hospital Castex y Sanatorio Itoiz, Buenos Aires; Fernando Scazzuso, Instituto Cardiovascular de Buenos Aires, Buenos Aires; Néstor Galizio, Fundación Favaloro, Buenos Aires; Gustavo Fabián Maid, Hospital Italiano, Buenos Aires; Hugo Garro, Hospital de Agudos Dr. J. M. Ramos Mejía, Buenos Aires; José Estepo, Hospital Británico, Buenos Aires; José Moltedo, Electrofisiología Pediátrica Clínica y Maternidad Suizo Argentina, Buenos Aires; Karina Alonso, Sanatorio Franchín, Buenos Aires; Leonardo Celano, Hospital Cosme Argerich, Buenos Aires; Mauricio Abello, FLENI, Buenos Aires; Néstor López Cabanillas, Clínica Adventista Belgrano, Buenos Aires; Rodolfo Sansalone, Sanatorio Güemes, Sanatorio San Cayetano, Hospital San Juan de Dios y Clínica Olivos, Buenos Aires y Clínica Pueyrredon y Hospital Privado de Comunidad, Mar del Plata; Sebastián Maldonado, Hospital Nacional J. P. Garrahan, Buenos Aires; Sergio Dubner, Clínica y Maternidad Suizo Argentina, Buenos Aires; Guillermo Mazo, Sanatorio Pasteur, Catamarca; Gustavo Iralde, Cardio Junín, Junín; Mariana Valentino, Clínica La Pequeña Familia, Junín; Andrés Martellotto, Hospital Italiano, Córdoba; Leonardo Atea, Sanatorio del Salvador, Córdoba; Luis Arabia, Instituto Oulton, Córdoba; Miguel Ángel Tibaldi, Sanatorio Allende Cerro, Córdoba; Héctor Manzolillo, Instituto de Cardiología de Corrientes, Corrientes; Roberto Rivero Paz, Sanatorio Quintar, Jujuy; Francisco Bertolotti, Hospital San Juan de Dios y Hospital Español, La Plata; Luis Medesani, Instituto Médico Platense, La Plata; Javier Chaves, Sanatorio Belgrano, Mar del Plata; Francisco Femenia, Instituto Cardiovascular Villa Mercedes, San Luis; Ramón Raña, Clínica Pasteur, Neuquén; Ariel Szyszko, Sanatorio IOT, Posadas; Gerardo Moreno, Instituto de Cardiología y Cirugía Cardiovascular, Posadas; Marisa López, Instituto del Corazón Cordis, Resistencia; Alfredo Del Río, Sanatorio Parque, Rosario; Diego Velasco, Hospital Italiano, Rosario; Horacio Guillén, Sanatorio Adventista del Plata, Rosario; Marcelo Cardona, Hospital Es- pañol, Rosario; Óscar Pellizon, Hospital del Centenario, Rosario; Silvano Diangelo, Instituto Cardiovascular Rosario, Rosario; Jorge Secchi, Hemodinamia Salta, Salta; Miguel Sola, Instituto de Cardiología, Salta; Sebastián Garraza, Sanatorio Mayo, Santa Fe; Alejandro Polti, Sanatorio Alberdi, Santiago del Estero; Juan José Sirena, Instituto de Cardiología, Santiago del Estero; Alejandro Bravo, Hemodinamia y Electrofisiología Parque, Tucumán; Gabriel Salica, Hospital Ángel C. Padilla, Tucumán; Luis Aguinaga, Centro Privado de Cardiología, Tucumán; Sergio González, Instituto de Cardiología, Tucumán.
Bolivia: Luis Mercado, Centro Médico Quirúrgico Boliviano Belga, Cochabamba; Mauricio Arce, Instituto Nacional de Tórax, La Paz.
Brasil: Jose Sobral Neto, Instituto do Coração de Taguatinga, Brasilia; Fernando Cannavan, Ritmocordis, Campinas; Marcio Figueiredo, Universidade Estadual de Campinas, Campinas; Rafael Ronsoni, Instituto de Ritmología Cardíaca, Joinville; Jaime Giovany Arnez Maldonado, Hospital Universitario Francisca Mendes, Manaus; Carlos Kalil, Hospital São Lucas da Pucrs, Porto Alegre; Cidio Halperin, Hospital Ernesto Dornelles, Porto Alegre; Leandro Zimerman, Hospital de Clínicas, Porto Alegre; Eduardo Saad, Hospital Pró Cardíaco, Rio de Janeiro; Fabio Erthal, Instituto Nacional de Cardiología, Rio de Janeiro; Bruno Papelbaum, Clínica de Ritmología Cardíaca, São Paulo; Claudia Da Silva Fragata, Hospital Santa Cruz, São Paulo; Enrique Pachon, Hospital do Coração da Associação do Sanatório Sírio - HCor, São Paulo; Jaber Jefferson, Hospital Santa Marcelina, São Paulo; Mauricio Scanavacca, Instituto do Coração da FMUSP, São Paulo; Petronio Rangel, Universidade Federal de Uberlândia, Uberlândia; Fabricio Sarmento Vassallo, Instituto de Cardiología - Hospital Santa Rita De Cássia, Vitoria.
Colombia: Luis Sáenz, Fundación Cardioinfantil, Bogotá; Alirio Balanta, Clínica Nuestra Señora Remedios, Cali; William Uribe, Clínica Las Américas, Medellín.
Cuba: Michel Cabrera Ortega, Cardiocentro Pediátrico William Soler, La Habana; Roberto Zayas Molina, Instituto de Cardiología, La Habana.
El Salvador: Mauricio Contreras, Instituto Nacional Cardiología y Cirugía Cardiovascular, Hospital de la Mujer, San Salvador.
Guatemala: Sergio Leal, Unicar, Guatemala.
México: Humberto Rodríguez Reyes, Hospital Cardiológica Aguascalientes, Aguascalientes; Vitelio Mareona, Centro Médico de Occidente, IMSS, Guadalajara; Eduardo Ruiz Hernández, Centro Internacional de Medicina, Hermosillo; Susano Lara Vaca, IMSS, León; Enrique Velázquez Rodríguez, Hospital de Cardiología, Centro Médico Nacional Siglo XXI, IMSS, México; Gerardo Rodríguez Diez, Centro Médico Nacional 20 de Noviembre, ISSSTE, México; José Benito Álvarez, Hospital Español SBE, México; Luis Molina, Hospital General de México, UNAM, México; Norma Balderrabano, Hospital Infantil de México Federico Gómez, México; Eric González, Hospital Christus Muguerza Alta Especialidad, Monterrey; Gerardo Pozas, Hospital San José Tec de Monterrey, Monterrey; Ulises Rojel, Instituto del Corazón de Puebla, Puebla; Enrique Asensio, Hospital Médica Tec 100, Querétaro.
Perú: Carolina Guevara, Complejo Hospitalario San Pablo, Lima; Edda Lombardi, Hospital Nacional Edgardo Rebagliati Martins, Lima; Jorge Salinas Arce, Clínica San Felipe, Lima; Ricardo Zegarra Carhuaz, Instituto Nacional Cardiovascular INCOR EsSalud, Lima.
República Dominicana: Fernando Vidal Bett, Hospital Metropolitano Santiago, Santiago de los Caballeros y Plaza de la Salud, Corazones del Cibao, Corazones Unidos e Instituto Dominicano de Cardiología, Santo Domingo.
Uruguay: Alejandro Cuesta, Instituto de Cardiología Infantil, Montevideo; Beatriz Ansin, Asociación Española, Montevideo; Diego Freire, Centro Cardiovascular Universitario, Hospital de Clínicas, Montevideo; Gustavo Tortajada, Centro Cardiovascular de Casa de Galicia, Montevideo.
Venezuela: Armando Pérez Silva, Hospital Miguel Pérez Carreño, Caracas; Manuel Patete, Unidad Especializada de Arritmias, Caracas; Carlos Rodríguez Artuza, Centro Clínico Sagrada Familia, Instituto de Enfermedades Cardiovasculares de la Universidad del Zulia, Maracaibo; Abdel Fuenmayor, Hospital Universitario de Los Andes y Clínica Albarregas, Mérida.
Bibliografía
1. Haissaguerre M, Jais P, Shah DC, Takahashi A, Hocini M, Quiniou G, et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. The
2. Pappone C, Rosanio S, Oreto G, Tocchi M, Gugliotta F, Vicedomini G, et al. Circumferential radiofrequency ablation of pulmonary vein ostia: A new anatomic approach for curing atrial fibrillation. Circulation. 2000;102(21):2619-28.
3. Oral H, Scharf C, Chugh A, Hall B, Cheung P, Good E, et al. Catheter ablation for paroxysmal atrial fibrillation: segmental pulmonary vein ostial ablation versus left atrial ablation. Circulation. 2003;108(19):2355-60.
4. Pappone C, Rosanio S, Augello G, Gallus G, Vicedomini G, Mazzone P, et al. Mortality, morbidity, and quality of life after circumferential pulmonary vein ablation for atrial fibrillation: outcomes from a controlled nonrandomized long-term study. Journal of the
5. Wazni OM, Marrouche NF, Martin DO, Verma A, Bhargava M, Saliba W, et al. Radiofrequency ablation vs antiarrhythmic drugs as first-line treatment of symptomatic atrial fibrillation: a randomized trial. JAMA. 2005;293(21):2634-40.
6. Pappone C, Augello G, Sala S, Gugliotta F, Vicedomini G, Gulletta S, et al. A randomized trial of circumferential pulmonary vein ablation versus antiarrhythmic drug therapy in paroxysmal atrial fibrillation: the APAF Study. Journal of the
7. Stabile G, Bertaglia E, Senatore G, De Simone A, Zoppo F, Donnici G, et al. Catheter ablation treatment in patients with drug-refractory atrial fibrillation: a prospective, multi-centre, randomized, controlled study (Catheter Ablation For The Cure Of Atrial Fibrillation Study). European heart journal. 2006;27(2):216-21.
8. Noheria A, Kumar A, Wylie JV, Jr., Josephson ME. Catheter ablation vs antiarrhythmic drug therapy for atrial fibrillation: a systematic review. Archives of internal medicine. 2008;168(6):581-6.
9. Bertaglia E, Tondo C, De Simone A, Zoppo F, Mantica M, Turco P, et al. Does catheter ablation cure atrial fibrillation? Single-procedure outcome of drug-refractory atrial fibrillation ablation: a 6-year multicentre experience. Europace : European pacing, arrhythmias, and cardiac electrophysiology : journal of the working groups on cardiac pacing, arrhythmias, and cardiac cellular electrophysiology of the European Society of Cardiology. 2010;12(2):181-7.
10. Cappato R, Calkins H, Chen SA, Davies W, Iesaka Y, Kalman J, et al. Updated worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation. Circulation Arrhythmia and electrophysiology. 2010;3(1):32-8.
11. Wilber DJ, Pappone C, Neuzil P, De Paola A, Marchlinski F, Natale A, et al. Comparison of antiarrhythmic drug therapy and radiofrequency catheter ablation in patients with paroxysmal atrial fibrillation: a randomized controlled trial. JAMA. 2010;303(4):333-40.
12. Murakawa Y, Nogami A, Shoda M, Inoue K, Naito S, Kumagai K, et al. Nationwide survey of catheter ablation for atrial fibrillation: the Japanese Catheter Ablation Registry of Atrial Fibrillation (J-CARAF)—report of 1-year follow-up. Circulation journal : official journal of the Japanese Circulation Society. 2014;78(5):1091-6.
13. Fenelon G, Scanavacca M, Atie J, Zimerman L, Pereira de MagalhaÞes L, Lorga Filho A, et al. Atrial Fibrillation Ablation in
14. Keegan R, Aguinaga L, Pozzer D, Femenia F, Valentino M, Del Rio A, et al. Registro Nacional de Ablación por Catéter 2009. Primer reporte oficial de la Federación Argentina de Cardiología 2010. Rev Fed Arg Cardiol. 2011;40(1):65-71.
15. Keegan R, Gant López J. Registro Nacional deAblación por Catéter 2010. Rev Fed Arg Cardiol. 2013; 42(3):200-4.
16. Keegan R, Aguinaga L, Fenelon G, Uribe W, Rodriguez Diez G, Scanavacca M, et al. The first Latin American Catheter Ablation Registry. Europace : European pacing, arrhythmias, and cardiac electrophysiology : journal of the working groups on cardiac pacing, arrhythmias, and cardiac cellular electrophysiology of the European Society of Cardiology. 2015;17(5):794-800.
17. European Heart Rhythm A, European Association for Cardio-Thoracic S, Camm AJ, Kirchhof P, Lip GY, Schotten U, et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). European heart journal. 2010;31(19):2369-429.
18. Mitchell LB, Committee CCSAFG. Canadian Cardiovascular Society atrial fibrillation guidelines 2010: prevention and treatment of atrial fibrillation following cardiac surgery. The Canadian journal of cardiology. 2011;27(1):91-7.
19. Wann LS, Curtis AB, January CT, Ellenbogen KA, Lowe JE, Estes NA, 3rd, et al. 2011 ACCF/AHA/HRS focused update on the management of patients with atrial fibrillation (Updating the 2006 Guideline): a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Journal of the
20. Calkins H, Kuck KH, Cappato R, Brugada J, Camm AJ, Chen SA, et al. 2012 HRS/EHRA/ECAS Expert Consensus Statement on Catheter and Surgical Ablation of Atrial Fibrillation: recommendations for patient selection, procedural techniques, patient management and follow-up, definitions, endpoints, and research trial design. Europace : European pacing, arrhythmias, and cardiac electrophysiology : journal of the working groups on cardiac pacing, arrhythmias, and cardiac cellular electrophysiology of the European Society of Cardiology. 2012;14(4): 528-606.
21. Keegan R, Aguinaga L, Secchi J, Valentino M, Femenia F, Del Rio A, et al. Guía para la ablación por catéter de arritmias cardíacas. Rev Fed Arg Cardiol. 2011;40(4):391-406.
22. Keegan R, Vanegas D. Guías, Recomendaciones y Niveles de Evidencia Relacionados con La Estimulación Cardiaca y la Electrofisiología Cardiovascular (Guías Latinoamericanas). http://www.solaece.org/pdfs/SOLAECE-guiaderecomendaciones.pdf. 2011:23.
23. Keegan R, Aguinaga L, Secchi J, Pozzer D, Valentino M, Femenia F, et al. Guías de ablación de arritmias cardíacas 2011 de la Federación Argentina de Cardiología. Rev Urug Cardiol. 2012;27(1):78-107.
24. Morillo CA, Verma A, Connolly SJ, Kuck KH, Nair GM, Champagne J, et al. Radiofrequency ablation vs antiarrhythmic drugs as first-line treatment of paroxysmal atrial fibrillation (RAAFT-2): a randomized trial. JAMA. 2014;311(7):692-700.
25. Winkle RA, Mead RH, Engel G, Kong MH, Patrawala RA. Trends in atrial fibrillation ablation: have we maximized the current paradigms? Journal of interventional cardiac electrophysiology : an international journal of arrhythmias and pacing. 2012;34(2):115-23.
26. Uribe W, González E, Baranchuk A, Herrera AM, Medina E, Marín J, et al. Ablation of Atrial Fibrillation: First Single-Center Latin-American Consecutive Series. Revista Iberoamericana de Arritmología. 2010.
27. Labadet C, Dubner S, Hadid C, Azocar D, Di Toro D, Valsecchi C, et al. Eficacia y seguridad de la ablación por radiofrecuencia en pacientes con fibrilación auricular. Revista Argentina de Cardiología. 2014;82(4):285-91.
28. Hoyt H, Bhonsale A, Chilukuri K, Alhumaid F, Needleman M, Edwards D, et al. Complications arising from catheter ablation of atrial fibrillation: temporal trends and predictors. Heart Rhythm. 2011;8(12):1869-74.
29.
30. Verma A, Macle L, Cox J, Skanes AC, Committee CCSAFG. Canadian Cardiovascular Society atrial fibrillation guidelines 2010: catheter ablation for atrial fibrillation/atrial flutter. The Canadian journal of cardiology. 2011;27(1):60-6.
31. Shah RU, Freeman JV, Shilane D, Wang PJ, Go AS, Hlatky MA. Procedural complications, rehospitalizations, and repeat procedures after catheter ablation for atrial fibrillation. Journal of the American College of Cardiology. 2012;59(2):143-9.