Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Uruguaya de Cardiología
versión impresa ISSN 0797-0048versión On-line ISSN 1688-0420
Rev.Urug.Cardiol. vol.31 no.1 Montevideo abr. 2016
ESPECIAL
FIBRILACIÓN
AURICULAR
Artículo de revisión
Ablación o drogas en la fibrilación auricular paroxística
Dres. Aldo G. Carrizo1, Juan G. Acosta1, Carlos A. Morillo1,2
1. Servicio de Arritmia y Marcapasos, Hamilton Health Sciences, McMaster University, Ontario, Canada.
2. Population Health Research Institute.
Correspondencia: Dr. Aldo Carrizo,
Correo electrónico: carrizo@HHSC.CA
Resumen
Durante años las drogas antiarrítmicas (DAA) han constituido el tratamiento fundacional para los pacientes con fibrilación auricular paroxística (FAP) en los cuales se desea mantener el ritmo sinusal. Debido a las limitaciones en su eficacia, principalmente a largo plazo, sumado a la gran proporción de pacientes que discontinúan la terapia por efectos adversos, nuevas terapias no farmacológicas han sido desarrolladas con el fin de lograr un adecuado control del ritmo. En la última década la ablación por catéter se ha mostrado como la terapia más efectiva y posiblemente la más segura en aquellos pacientes con falla del tratamiento antiarrítmico. Estudios randomizados y metaanálisis recientemente publicados indican que la ablación podría ser considerada como primera línea de terapia en pacientes seleccionados con FAP en quienes se busca controlar el ritmo. Por lo tanto, en este artículo revisaremos la evidencia actual que avala el uso de DAA o ablación en la FAP.
Palabras clave:
FIBRILACIÓN AURICULAR
ABLACIÓN POR CATÉTER
ANTIARRÍTMICOS
Key words:
ATRIAL FIBRILLATION
CATHETER ABLATION
ANTI-ARRHYTHMIA AGENTS
Introducción
La fibrilación auricular (FA) es la arritmia cardíaca más prevalente en la población. Datos epidemiológicos demuestran que la incidencia y prevalencia de la FA está en aumento debido, en parte, al envejecimiento poblacional, asociándose así a una considerable morbilidad e incremento en la utilización de los recursos y por ende incrementando los costos de salud(1,2). Por lo tanto, una estrategia de tratamiento adecuada es altamente deseada.
- Varios estudios randomizados realizados a principio de la década del 2000 no demostraron beneficios significativos con la estrategia “control del ritmo” comparada con “control de la frecuencia”(3-9). El primer objetivo en el tratamiento de la FA se centra en la prevención de los eventos tromboembólicos a través de la anticoagulación oral según los factores de riesgo de cada paciente. En un segundo plano, pero más relevante para el paciente en el día a día, los esfuerzos se concentran en la reducción de síntomas, mejoría de la calidad de vida y reducción de las hospitalizaciones mediante un adecuado control de la frecuencia ventricular y el control del ritmo(10).
La terapia con DAA para mantener el ritmo sinusal ha constituido el tratamiento fundacional de la FAP. Sin embargo, solo ha demostrado mantener exitosamente el ritmo sinusal en la mitad de los pacientes luego de un año(7). Por lo tanto, la falta de eficacia a largo plazo sumado a la relativa alta proporción de pacientes que discontinúan la terapia por reacciones adversas han favorecido el desarrollo de estrategias no farmacológicas para lograr el control del ritmo.
La ablación por radiofrecuencia con catéter (AC) es actualmente reconocida como una alternativa válida en el tratamiento de la FA. Desde su introducción, hace ya más de 15 años(11), varios estudios han valorado su eficacia en el control del ritmo.
Si bien la AC ha demostrado resultados favorables en la reducción de los síntomas y mejoría en la calidad de vida, no hay estudios que hayan evaluado sistemáticamente su efecto en la mortalidad y el accidente cerebrovascular (ACV). A su vez, las complicaciones relacionadas con la ablación, los costos y la población incluida en los ensayos clínicos son factores que deben tenerse en cuenta al momento de evaluar los riesgos y beneficios del procedimiento.
A pesar de lo anterior, varias guías clínicas recomiendan la AC como estrategia en aquellos pacientes con FAP sintomática en donde la terapia farmacológica con una o más DAA ha fallado en el control del ritmo (clase 1, nivel de evidencia A)(10). Mas aún, la reciente publicación de estudios randomizados (MANTRA-PAF(12) y RAAFT-2(13)) han llevado el debate a un nuevo nivel: ¿Debe la ablación por catéter ser indicada como tratamiento de primera línea?
En la actualidad, la AC de los pacientes con FAP se ha convertido en una práctica habitual en diferentes centros alrededor del mundo, por lo tanto creemos relevante revisar sus ventajas y desventajas así como el papel actual de las DAA. Esta revisión se focalizará en el uso de DAA y de la AC para el control del ritmo en pacientes con FAP. Si bien existen otras modalidades terapéuticas, como la quirúrgica, estas no serán abordadas en el presente artículo. Asimismo, tampoco se abordará la prevención tromboembólica que, con el reciente advenimiento de nuevos anticoagulantes orales y el uso de dispositivos de oclusión para la orejuela, requiere una revisión por separado.
Drogas antiarrítmicas
Las DAA han mostrado una eficacia limitada para el mantenimiento del ritmo sinusal en pacientes con FAP. Los fármacos actualmente indicados para el tratamiento de la FAP incluyen amiodarona, sotalol, dofetilide, dronedarone y fármacos del grupo IC (propafenona, flecainida)(10).
La amiodarona es el fármaco más efectivo con tasas de mantenimiento del ritmo sinusal en torno a 60%-65%(14). En el estudio CTAF(15), el 63% de los pacientes tratados con propafenona y sotalol presentaron recurrencias de FA a 16 meses frente a 35% de los tratados con amiodarona. A pesar de presentar mayor efectividad, el grupo tratado con amiodarona tuvo una tasa de abandono del tratamiento por efectos secundarios ligeramente superior al grupo tratado con sotalol o propafenona (18% vs 11%). Dado su perfil de seguridad actualmente se recomienda reservar su uso como fármaco de segunda línea en caso de fracaso de otros antiarrítmicos, o como primera elección en pacientes con disfunción ventricular o enfermedad coronaria(10).
En el estudio AFFIRM(16), la efectividad de los DAA de clase I para el mantenimiento de ritmo sinusal fue de 23% frente a 34% de sotalol, y 60% en los tratados con amiodarona. Las DAA clase I incluyeron a pacientes tratados con procainamida, disopiramida, moricizina, propafenona y flecainida. El estudio CAST(17), que incluyó a pacientes posinfarto y cuyo objetivo era la reducción de extrasístoles ventriculares, despertó dudas respecto a la seguridad de los fármacos IC debido a un incremento en la mortalidad; sin embargo, con el tiempo se ha probado su seguridad en ausencia de disfunción ventricular o cardiopatía isquémica(18). En estudios frente a placebo se ha reportado una eficacia para el mantenimiento del ritmo sinusal a nueve meses de 65% para DAA de clase IC(19).
En los estudios PAFAC(20) y SAFE-T(21), entre 25% y 33% de los pacientes tratados con sotalol permanecían libres de recurrencias durante el seguimiento, con un potencial efecto pro arrítmico dosis dependiente que se relaciona con la prolongación del QT y desarrollo de taquicardias ventriculares polimórficas.
El dofetilide ha probado ser tan efectivo como el sotalol y la flecainida para el mantenimiento del ritmo sinusal en FAP, siendo relativamente seguro en pacientes con disfunción ventricular o cardiopatía isquémica(22). Una de sus principales limitaciones es que precisa de monitorización durante el inicio del tratamiento debido al riesgo de prolongación del QT(23).
La dronedarona tiene un perfil de seguridad favorable en pacientes con FAP sin disfunción ventricular (DAFNE)(24). En el estudio DYONISIOS(25), la dronedarona fue menos efectiva que la amiodarona para el mantenimiento del ritmo sinusal en pacientes con FAP sin cardiopatía de base (58% vs 46% libres de FA a seis meses), aunque con una menor tasa de efectos adversos. En el estudio ANDROMEDA(26) se evidenció un aumento de la mortalidad en pacientes con disfunción ventricular tratados con dronedarona debido a un empeoramiento de su insuficiencia cardíaca. Asimismo, no se recomienda su utilización en pacientes con FA permanente debido al aumento en la mortalidad evidenciado en el estudio PALLAS(27).
Finalmente, la tasa global de mantenimiento del ritmo sinusal en estudios que comparan estrategias de control del ritmo contra control de frecuencia, y que incluyen diferentes clases de DAA, es de alrededor de 56% a un año (PIAF)(4), 39% a 2,3 años (RACE)(6) y 62% a cinco años (AFFIRM)(3).
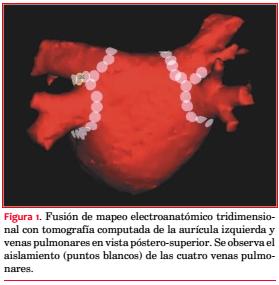
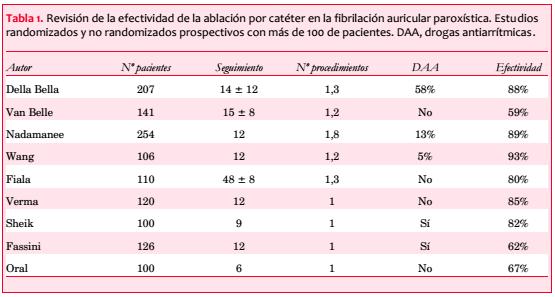
Los desalentadores resultados con las DAA impulsaron la creación de estrategias no farmacológicas para mantener el ritmo sinusal. Es así que la ablación de la FA ha evolucionado rápidamente en los últimos años. A partir del trabajo publicado por Haïssaguerre en 1998, el interés se centró en la ablación de la actividad ectópica originada en las venas pulmonares (VP) con resultados prometedores(11). Actualmente la ablación de la FA tiene como principio fundamental el aislamiento eléctrico de las VP (figura 1). En estudios recientes la ablación muestra una tasa de éxito de hasta el 80% para el control de la FAP a un año de seguimiento, siendo a largo plazo de 54% tras el primer procedimiento y de 80% tras dos o más ablaciones (tabla 1)(28-30). La tasa de complicaciones relacionadas con el procedimiento es de 6%, incluyendo un riesgo de muerte de 1/1.000-2.000 casos, riesgo de taponamiento de 1,2%, 1% de ictus y menos de 2% de estenosis de VP. La incidencia de perforación esofágica, una de las complicaciones más temidas de la ablación de la FA, se estima en 0,01%(31).
No es una tarea fácil comparar los diferentes estudios que evaluaron directamente la ablación con las DAA, ya que hasta hace poco no existía una técnica estandarizada para la ablación (aislamiento de VP, potenciales fragmentados, ablación linear en techo auricular o a nivel mitral, “período de blanqueo”, etcétera). Ni tampoco se había estandarizado la manera en la cual se reportan los eventos. En 2012, el Consenso de Expertos de HRS/EHRA/ECAS (Heart Rhythm Society/ European Heart Rhythm Association/European Cardiac Arrhythmia Society) estandarizó la práctica. Este documento recomienda el aislamiento eléctrico de las VP como estrategia fundamental, y define el éxito del procedimiento como la ausencia de FA, taquicardia auricular o aleteo auricular sintomático o asintomático de duración ³ 30 segundos a 12 meses de seguimiento posablación(32). También se recomienda un “período de blanqueo” de tres meses posablación, en donde cualquier recurrencia arrítmica es esperada y no se considera falla del procedimiento (período de inflamación mio-pericárdica transitoria). Por otro lado, el uso de DAA también varía entre los estudios. Se debe estar consciente de estas limitaciones al analizar los resultados reportados.
Un reciente metaanálisis de estudios randomizados confirman la superioridad de la ablación en pacientes con FAP, con un incremento del riesgo relativo de recurrencia de FA de 2,26 (IC 95%, 1,74-2,94) en pacientes tratados con DAA(41). No solo la ablación ha demostrado ser superior manteniendo el ritmo sinusal, sino también reduciendo los síntomas y aparentemente mejorando la calidad de vida(12,39,40).
Ablación como primera opción terapéutica
Movilizados por los resultados alentadores previamente descritos y también basados en la idea fisiopatológica de brindar la mejor opción terapéutica de manera temprana con el objetivo de modificar los eventos a largo plazo y la progresión de la FA, tres estudios randomizados han sido publicados(12,13,40). Estos han tratado de responder a la siguiente pregunta: ¿Es la ablación por catéter superior a las DAA en pacientes con FAP, vírgenes de tratamiento antiarrítmico? En otras palabras, ¿debería ser la ablación la primera opción terapéutica en pacientes con FAP?
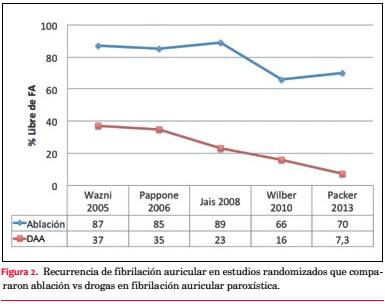
En total, 491 pacientes, predominantemente jóvenes, de sexo masculino, con mínima o nula enfermedad estructural y escasas comorbilidades, fueron enrolados en estos estudios. El estudio RAAFT(40) fue el primero en documentar la superioridad de la AC como primera línea de tratamiento. Este estudio pequeño de 70 pacientes reportó una mayor tasa de pacientes libres de FA en el grupo sometido a ablación (87% vs 37%, RRR 80%; p<0,01) a 12 meses de seguimiento. Posteriormente, MANTRA-PAF(12), con 294 pacientes, fue un estudio negativo al no encontrar diferencias entre AC y DAA con respecto al punto final primario: carga acumulada de FA. Sin embargo, reportó un mayor porcentaje de pacientes libres de FA en el grupo ablación (85% vs 71%, RRR 20%; p=0,004) a dos años de seguimiento. En el RAAFT-2(13), con un total de 127 pacientes y también a dos años de seguimiento, un mayor porcentaje de pacientes se encontraban libres de taquiarritmias auriculares (fibrilación/aleteo/taquicardia auricular) en el grupo sometido a ablación (45% vs 28%, RRR 40%; p=0,02). Es de destacar las diferencias en la tasa de recurrencias entre estos dos últimos estudios. Esto se relaciona con la rigurosidad con la que los eventos fueron monitorizados, habiendo sido más estricto el estudio RAAFT-2.
Luego de la publicación del ensayo clínico RAAFT-2, tres metaanálisis reconfirman la superioridad de la ablación como primera línea terapéutica en esta población(42-44). Khan y colaboradores(42) reportaron una RRR 48% (RR, 0,52; IC95%, 0,30-0,91; p=0,02) en la recurrencia de taquicardias auriculares en pacientes sometidos a ablación. Más recientemente, Hakalahti y colaboradores(43) reportaron resultados similares, obteniendo una menor recurrencia de FA en el grupo ablación RRR 30% (RR 0,70; IC95%, 0,51-0,96; p=0,03). Como el estudio RAAFT-1 presenta riesgo de sesgos debido a que la adjudicación de eventos no fue realizada de forma ciega, un subanálisis excluyendo este estudio muestra que el grupo ablación continúa asociándose a una mayor tasa libre de recurrencias (RR 0,70, IC95%, 0,51-0,96; p=0,03). Por último, Santangeli y colaboradores(44) incluyeron en su metaanálisis tanto estudios randomizados como observacionales y reportaron una tasa libre de FA con la ablación de 67% comparada con 48% en el grupo DAA (OR 0,36, IC95%, 0,24-0,54; p < 0,001).
Complicaciones
El riesgo de la ablación debe ser comparado con los riesgos derivados de una terapia farmacológica mantenida a largo tiempo.
Los estudios randomizados han reportado en general una tasa de complicaciones menor pero de mayor seriedad con respecto al tratamiento farmacológico. Sin embargo, esto podría no reflejar la experiencia de la ablación en el “mundo real”, fuera de centros altamente experimentados. En este sentido, un registro internacional ha reportado una tasa de complicaciones mayores de 6% (taponamiento cardíaco, ACV, estenosis pulmonar, fístula atrio- esofágica o muerte) con la ablación(45). Recientemente se publicó una actualización de dicho registro. En comparación con lo publicado en 2005, la nueva encuesta pone de manifiesto que la ablación se está realizando en pacientes más enfermos (mayor edad, FA persistente y con más comorbilidades), y aun así reporta una tasa de complicaciones más baja (4,5%)(46). Esta mejoría en la seguridad también ha sido documentada en otros estudios(47).
Las complicaciones del procedimiento están muy ligadas a la experiencia del operador y del centro. Un registro nacional de Estados Unidos en centros de alto y bajo volumen reportó las complicaciones intrahospitalarias de más de 90.000 ablaciones de FA realizadas entre los años 2000 y 2010, y muestra cómo las tasas de complicaciones se veían significativamente afectadas por la experiencia del operador y el volumen del centro donde se realiza la ablación(48). Aquellos centros con menos de 50 ablaciones/año tienen una tasa de complicaciones de 7%, mayor que aquellos con mayor número de ablaciones/año (4%). En el mismo sentido, aquellos operadores que realizaban menos de 25 ablaciones/año presentaban mayor tasa de complicaciones (7%) en comparación con los que realizaban mayor número de ablaciones (2%)
Ablación de fibrilación auricular, interrogantes a responder
A diferencia del Wolff-Parkinson-White, en donde la ablación es curativa, la FA no es una enfermedad congénita provocada por una anormalidad anatómica con mecanismos electrofisiológicos únicos y bien entendidos. En la mayoría de los casos su desarrollo está asociado a diversos procesos, anatómicos y funcionales, que promueven un estado pro fibrilatorio en la aurícula izquierda(49). Por lo tanto, resulta simplista pensar que en una enfermedad tan compleja, un procedimiento limitado a las aurículas pueda cambiar a largo tiempo el curso de esta enfermedad.
La ablación de la FA no es un tratamiento curativo, pero sí una de las herramientas a considerar dentro de un tratamiento multidisciplinario (control de la obesidad, hipertensión arterial, apnea del sueño, alcoholismo, etcétera) en una enfermedad multifactorial. Siguiendo esta línea, la ablación no ha demostrado reducir el riesgo de ACV ni la mortalidad. Existen algunos reportes de cohorte que sugieren una reducción en el riesgo tromboembólico en los pacientes sometidos a ablación. Sin embargo, estos estudios no son randomizados y presentan severas limitaciones(50,51). Es así que el tratamiento anticoagulante luego de la ablación debe ser guiado por el riesgo del paciente (CHA2DS2-Vasc score) y no por la ausencia de FA en el seguimiento o el éxito agudo del procedimiento. En la actualidad se están llevando a cabo tres estudios, CABANA (Clinicaltrials. gov: NCT00911508), CASTLE-AF (Clinicaltrials.gov: NCT0064 3188), y el EAST (Clinicaltrials.gov: NCT01288352) con el objetivo de evaluar el impacto de la ablación en el ACV y la sobrevida.
Facilitando el camino: nuevas tecnologías
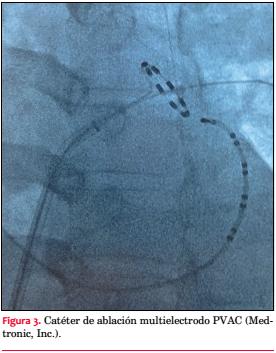
Constantemente nuevas tecnologías se van desarrollando en el campo de la electrofisiología con el objetivo de mejorar la seguridad y eficacia de los procedimientos. En el caso de la ablación de la FAP, donde el objetivo es el aislamiento de las VP, sin la realización de líneas de ablación adicionales, nuevos catéteres de ablación circulares (single shot) se encuentran disponibles. Estos han demostrado reducir el tiempo de procedimiento y de fluoroscopía manteniendo la misma eficacia y seguridad que la ablación convencional “punto por punto”. El Pulmonary Vein Ablation Catheter (PVAC, Medtronic, Inc) es un catéter decapolar que al asentarse alrededor de las venas registra la actividad eléctrica permitiendo simultáneamente liberar radiofrecuencia de forma ciclada bipolar y monopolar, generando lesiones circunferenciales alrededor del ostium (figura 3)(48,52). Siguiendo el mismo concepto, pero usando un sistema de irrigación con la idea de evitar la formación de coágulos en la interface catéter-tejido, el nMARQ (Biosense Webster) es otro catéter multielectrodo circular disponible(49,53).
Una fuente de energía alternativa es la crioablación. A través de un catéter-balón (Medtronic, Inc), que se asienta sobre el ostium de las VP, se logra aislar las venas mediante la congelación del tejido por debajo de -80 °C(36,39). El estudio AF-COR no encontró diferencias en términos de eficacia (tasa libre de FA a 12 meses: 46% vs 34%, p=0,2) entre PVAC y crioablación(50,54). Un nuevo catéter-balón de ablación está siendo evaluado (CardioFocus, Inc). Este tiene la particularidad de utilizar energía láser y además permite, mediante endoscopía, la directa visualización de las VP asegurando un contacto adecuado con el tejido(51,55).
Conclusiones
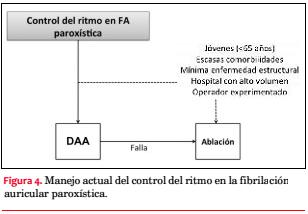
En pacientes con FAP, la evidencia disponible demuestra la superioridad de la AC comparado con el tratamiento farmacológico en el mantenimiento del ritmo sinusal, la reducción de síntomas y la mejoría de la calidad de vida. Esto se ve reflejado en las guías internacionales donde se le asigna una recomendación clase I en aquellos pacientes sintomáticos donde al menos una DAA ha fallado. Aunque las guías clínicas actuales también recomiendan realizar la ablación como primera línea de terapia en pacientes seleccionados (clase IIa, nivel de evidencia B), esta estrategia es todavía infrecuentemente adoptada en nuestro hospital y creemos que diversos elementos se deben tener en cuenta al considerarla (figura 4). Esto resalta la complejidad del procedimiento y las complicaciones potenciales, que si bien son raras, pueden poner en riesgo la vida del paciente. Finalmente, el manejo de la FA demanda un abordaje multidisciplinario con el control adecuado de los factores de riesgo y la prevención de eventos tromboembólicos mediante la anticoagulación oral, siendo el objetivo actual de la ablación el control de los síntomas.
Bibliografía
1. Magnani JW, Rienstra M, Lin H, Sinner MF, Lubitz SA, McManus DD, et al. Atrial fibrillation: current knowledge and future directions in epidemiology and genomics. Circulation. 2011;124(18): 1982-93.
2. Chugh SS, Havmoeller R, Narayanan K, Singh D, Rienstra M, Benjamin EJ, et al. Worldwideepidemiology of atrial fibrillation: a Global Burden of Disease 2010 Study. Circulation. 2014;129(8): 837-47.
3. Carlsson J, Miketic S, Windeler J, Cuneo A, Haun S, Micus S, et al. Randomized trial of rate-control versus rhythm-control in persistent atrial fibrillation: theStrategies of Treatment of Atrial Fibrillation (STAF) study. J Am Coll Cardiol 2003;41(10):1690-6.
4. Hohnloser SH, Kuck KH, Lilienthal J. Rhythmorratecontrol in atrial fibrillation—PharmacologicalIntervention in Atrial Fibrillation (PIAF): a randomised trial. Lancet 2000;356(9244):1789-94.
5. Opolski G, Torbicki A, Kosior DA, Szulc M, Wozakowska-Kaplon B, Kolodziej P, et al. Rate control vs rhythm control in patients with non valvular persistent atrial fibrillation: theresults of the Polish Howto Treat Chronic Atrial Fibrillation (HOT CAFE) Study. Chest 2004;126(2):476-86.
6. Van Gelder IC, Hagens VE, Bosker HA, Kingma JH, Kamp O, Kingma T, et al. A comparison of rate control and rhythm control in patientswithrecurrentpersistent atrial fibrillation. N Engl J Med 2002;347(23):1834-40.
7. Wyse DG, Waldo
8. Roy D, Talajic M, Nattel S, Wyse DG, Dorian P, Lee KL, Bourassa MG, et al. Rhythm control versus rate control for atrial fibrillation and heartfailure. N Engl J Med 2008;358(25):2667-77.
9. Ogawa S, Yamashita T, Yamazaki T, Aizawa Y, Atarashi H, Inoue H, et al. Optimal treatment strategy for patients with paroxysmal atrial fibrillation: J-RHYTHM Study. Circ J 2009;73(2):242-8.
10. January CT, Wann LS, Alpert JS, Calkins H, Cigarroa JE, Cleveland JC, et al. 2014 AHA/ACC/HRS Guideline for the Management of Patients With Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the Heart Rhythm Society. Circulation 2014; 130(23):2071-104.
11. Haïssaguerre M, Jaïs P, Shah DC, Takahashi A, Hocini M, Quiniou G, et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J Med 1998; 339(10): 659-66.
12. Cosedis Nielsen J, Johannessen A, Raatikainen P, Hindricks G, Walfridsson H, Kongstad O, et al. Radiofrequency ablation as initial therapy in paroxysmal atrial fibrillation. N Engl J Med 2012;367(17):1587–95.
13. Morillo CA, Verma A, Connolly SJ, Kuck KH, Nair GM, Champagne J, et al. Radio frequency ablation vs antiarrhythmic drugs as first-line treatment of paroxysmal atrial fibrillation (RAAFT-2): a randomized trial. JAMA 2014;311(7):692–700.
14. Van Erven L, Schalij MJ. Amiodarone: aneffective antiarrhythmic drug with unusual side effects. Heart 2010;96(19): 1593-600.
15. Roy D, Talajic M, Dorian P, Connolly S, Eisenberg MJ, Green M, et al. Canadian Trial of Atrial Fibrillation Investigators. Amiodarone to prevent recurrence of atrial fibrillation. N Engl J Med 2000; 342(13): 913–20.
16. AFFIRM First Antiarrhythmic Drug Substudy Investigators. Maintenance of sinus rhythm in patients with atrial fibrillation: an AFFIRM substudy of the first antiarrhythmic drug. J Am Coll Cardiol 2003;42(1):20-9.
17. Echt DS, Liebson PR, Mitchell LB, Peters RW, Obias-Manno D, Barker AH, et al. CAST: Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med 1991;324(12):781-8.
18. Aliot E, Capucci A, Crijns HJ, Goette A, Tamargo J. Twenty-five years in the making: flecainide is afe and effective for the management of atrial fibrillation. Europace 2011;13(2):161-73.
19. Clementy J, Dulhoste MN, Laiter C, Denjoy I, Dos Santos P. Flecainide acetate in the prevention of paroxysmal atrial fibrillation: a nine-month follow-up of more than 500 patients. Am J Cardiol 1992;70(5):44A-49A.
20. Fetsch T, Bauer P, Engberding R, Koch HP, Lukl J, Meinertz T, et al. Prevention of atrial fibrillation after cardioversion: results of the PAFAC trial. Eur Heart J 2004;25(16):1385-94.
21. Singh BN, Singh SN, Reda DJ, Tang XC, Lopez B, Harris CL, et al. Amiodarone versus sotalolfor atrial fibrillation. N Engl J Med 2005;352(18): 1861-72.
22. Kober L, Bloch Thomsen PE, Moller M, Torp-Pedersen C, Carlsen J, Sandøe E, et al. Effect of dofetilide in patients with recent myocardial infarction and left-ventricular dysfunction: a randomised trial. Lancet 2000;356(9247): 2052-8.
23. Abraham JM, Saliba WI, Vekstein C, Lawrence D, Bhargava M, Bassiouny M, et al. Safety of Oral Dofetilide for Rhythm Control of Atrial Fibrillation and Atrial Flutter. Circ Arrhythm Electrophysiol 2015;8(4):772-6. Publicación electrónica 10 Jun 2015.
24. Touboul P, Brugada J, Capucci A, Crijns HJ, Edvardsson N, Hohnloser SH. Dronedarone for prevention of atrial fibrillation: a dose-rangings tudy. Eur Heart J 2003;24(16):1481-7.
25. Le Heuzey JY, De Ferrari GM, Radzik D, Santini M, Zhu J, Davy JM. A short-term, randomized, double-blind, parallel-group study to evaluate the efficacy and safety of dronedarone versus amiodarone in patients with persistent atrial fibrillation: the DIONYSOS study. J Cardiovasc Electrophysiol 2010; 21( 6):597-605.
26. KoberL, Torp-Pedersen C, McMurray JJ, Gøtzsche O, Lévy S, Crijns H, et al. Increased mortality after dronedarone therapy for severe heart failure. N Engl J Med 2008;358(25): 2678-87.
27. Connolly SJ, Camm AJ, Halperin JL, Joyner C, Alings M, Amerena J, et al. Dronedarone in high-risk permanent atrial fibrillation. N Engl J Med 2011;365(24): 2268-76.
28. Fiala M, Chovancik J, Nevralova R, Neuwirth R, Jiravský O, Nykl I, et al. Pulmonary vein isolation using segmental versus electro anatomical circumferential ablation for paroxysmal atrial fibrillation: over 3-year results of a prospective randomized study. J Interv Card Electrophysiol 2008;22(1): 13-21.
29. Dixit S, Gerstenfeld EP, Ratcliffe SJ, Cooper JM, Russo AM, Kimmel SE, et al. Single procedure efficacy of isolating all versus arrhythmogenic pulmonary veins on long-term control of atrial fibrillation: a prospective randomized study. Heart Rhythm 2008;5(2):174-81.
30. Ganesan AN, Shipp NJ, Brooks AG, Kuklik P, Lau DH, Lim HS, et al. Long-termoutcomes of catheter ablation of atrial fibrillation: a systematicreview and meta-analysis . J Am Heart Assoc 2013;2(2): e004549.
31. Cappato R, Calkins H, Chen SA, Davies W, Iesaka Y, Kalman J, et al. Prevalence and causes of fatal outcome in catheter ablation of atrial fibrillation. J Am Coll Cardiol 2009;53(19):1798-803.
32. Calkins H, Kuck KH, Cappato R, Brugada J, Camm AJ, Chen S-A, et al. 2012 HRS/EHRA/ ECAS expert consensus statement on catheter and surgical ablation of atrial fibrillation: recommendations for patient selection, procedural techniques, patient management and follow-up, definitions, endpoints, and research trial design. Heart Rhythm 2012;9(4):632-96 e21.
33. Krittayaphong R, Raungrattanaamporn O, Bhuripanyo K, Sriratanasathavorn C, Pooranawattanakul S, Punlee K, et al. A randomizedclinical trial of theefficacy of radiofrequency catheter ablation and amiodarone in the treatment of symptomatic atrial fibrillation. J Med Assoc Thai 2003;86 Suppl 1: S8-16.
34. Stabile G, Bertaglia E, Senatore G, De Simone A, Zoppo F, Donnici G, et al. Catheter ablation treatment in patients with drug-refractory atrial fibrillation: a prospective, multi-centre, randomized, controlled study (Catheter Ablation For The Cure Of Atrial Fibrillation Study). Eur Heart J 2006;27(2): 216-21.
35. Pappone C, Augello G, Sala S, Gugliotta F, Vicedomini G, Gulletta S, et al. A randomized trial of circumferential pulmonary vein ablation versus antiarrhythmic drug therapy in paroxysmal atrial fibrillation: the APAF Study. J Am Coll Cardiol 2006;48(11):2340-7.
36. Jaïs P, Cauchemez B, Macle L, Daoud E, Khairy P, Subbiah R, et al. Catheter ablation versus antiarrhythmic drugs for atrial fibrillation: the A4 study. Circulation 2008;118(24):2498-505.
37. Forleo GB, Mantica M, De Luca L, Leo R, Santini L, Panigada S, et al. Catheter ablation of atrial fibrillation in patients with diabetes mellitus type 2: results from a randomized study comparing pulmonary vein isolation versus antiarrhythmic drug therapy. J Cardiovasc Electrophysiol 2009;20(1):22-8.
38. Wilber DJ, Pappone C, Neuzil P, De Paola A, Marchlinski F, Natale A, et al, Thermo Cool AFTI. Comparison of antiarrhythmicdrugtherapy and radiofrequency catheter ablation in patients with paroxysmal atrial fibrillation: a randomized controlled trial. JAMA 2010;303(4):333-40.
39. Packer DL, Kowal RC, Wheelan KR, Irwin JM, Champagne J, Guerra PG, et al. Cryoballoon ablation of pulmonary veins for paroxysmal atrial fibrillation: ?first results of the North American Arctic Front (STOP AF) pivotal trial. J Am Coll Cardiol 2013;61(16):1713-23.
40. Wazni OM, Marrouche NF, Martin DO, Verma A, Bhargava M, Saliba W, et al. Radiofrequency ablation vs antiarrhythmic drugs as first-line treatment of symptomatic atrial fibrillation: a randomized trial. JAMA 2005;293(21):2634-40.
41. Parkash R,
42. Khan AR, Khan S, Sheikh MA, Khuder S, Grubb B, Moukarbel GV. Catheter ablation and antiarrhythmic drug therapy as first- or second-line therapy in the management of atrial fibrillation: systematic review and meta-analysis. Circ Arrhythm Electrophysiol 2014;7(5):853-60.
43. Hakalahti A, Biancari F, Nielsen JC, Raatikainen MJ. Radiofrequency ablation vs. antiarrhythmic drug therapy as first line treatment of symptomatic atrial fibrillation: systematic review and meta-analysis. Europace. 2015;17(3):370-8.
44. Santangeli P, Di Biase L, Natale. Ablation versus drugs: what is the best first-line therapy for paroxysmal atrial fibrillation? Antiarrhythmic drugs are outmoded and catheter ablation should be the first-line option for all patients with paroxysmal atrial fibrillation: pro. Circ Arrhythm Electrophysiol 2014;7(4):739-46.
45. Cappato R, Calkins H, Chen SA, Davies W, Iesaka Y, Kalman J, et al. Worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation. Circulation 2005,111(9): 1100-5.
46. Cappato R, Calkins H, Chen SA, Davies W, Iesaka Y, Kalman J, et al. Updated world wide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation. Circ Arrhythm Electrophysiol 2010;3(1):32-8.
47. Dagres N, Hindricks G, Kottkamp H, Sommer P, Gaspar T, Bode K, et al. Complications of atrial fibrillationablation in a high-volume center in 1,000 procedures: still cause forconcern?. J Cardiovasc Electrophysiol 2009;20(9):1014-9.
48. Deshmukh A, Patel NJ, Pant S, Shah N, Chothani A, Mehta K, et al. In-hospital complications associated with catheter ablation of atrial fibrillation in the United States between 2000 and 2010: analysis of 93801 procedures. Circulation 2013;128(19): 2104–12.
49. Wakili R, Voigt N, Kaab S, Dobrev D, Nattel S. Recentadvances in the molecular pathophysiology of atrial fibrillation. J Clin Invest 2011;121(8):2955-68.
50. Themistoclakis S, Corrado A, Marchlinski FE, Jais P, Zado E, Rossillo A, et al. The risk of thromboembolism and need for oral anticoagulation after successful atrial fibrillation ablation. J Am Coll Cardiol 2010;55(8):735-43
51. Saad EB, d’Avila A, Costa IP, Aryana A, Slater C, Costa RE, et al. Very low risk of thromboembolic events in patients undergoing successful catheter ablation of atrial fibrillation with a CHADS2 score ?3: a long-term outcome study. Circ Arrhythm Electrophysiol 2011;4(5):615-21.
52. McCready J, Chow AW, Lowe MD, Segal OR, Ahsan S, de Bono J, et al. Safety and efficacy of multipolar pulmonary vein ablation catheter vs. irrigated radiofrequency ablation for paroxismal atrial fibrillation: a randomized multicentre trial. Europace 2014;16(8):1145-53.
53. Shin D-I, Kirmanoglou K, Eickholt C, Schmidt J, Clasen L, Butzbach B, et al. Initial results of using a novel irrigated multielectrode mapping and ablation catheter for pulmonary vein isolation. Heart Rhythm 2014;11:375-83
54. Malmborg H, Lönnerholm S, Blomström P, Blomström-Lundqvist C. Ablation of atrial fibrillation with cryoballoon or duty- cycled radiofrequency pulmonary vein ablation catheter: a randomized controlled study comparing the clinical outcome and safety; the AF-COR study. Europace 2013; 15(11):1567-73.
55. Dukkipati SR, Kuck KH, Neuzil P, Woollett I, Kautzner J, McElderry HT, et al. Pulmonary vein isolation using a visually guided laser balloon catheter: the first 200-patient multicenter clinical experience. Circ Arrhythm Electrophysiol 2013;6(3): 467-72.