Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Uruguaya de Cardiología
versión impresa ISSN 0797-0048versión On-line ISSN 1688-0420
Rev.Urug.Cardiol. vol.30 no.3 Montevideo dic. 2015
FIBRILACIÓN AURICULAR
Artículo de revisión
Fibrilación auricular no valvular y anticoagulación
Dr. Ramón Corbalán
División de Enfermedades Cardiovasculares. Pontificia Universidad Católica de Chile.
Palabras clave:
FIBRILACIÓN AURICULAR
FIBRILACIÓN AURICULAR NO VALVULAR
ANTICOAGULACIÓN
Key words:
ATRIAL FIBRILLATION
NON-VALVULAR ATRIAL FIBRILLATION
ANTICOAGULATION
Antecedentes
La fibrilación auricular (FA) es la arritmia sostenida más frecuente en clínica y su prevalencia se ha incrementado con el aumento de las expectativas de sobrevida(1). Por sus consecuencias hemodinámicas, como pérdida de la contracción auricular y aumento de la estasia sanguínea, la FA predispone a un riesgo elevado de tromboembolismo sistémico. Este riesgo era muy conocido en la época en que la FA era parte de la evolución natural de la estenosis mitral reumática. Con el mejor tratamiento de las infecciones estreptocócicas y disminución de la enfermedad reumática esta asociación ha sido cada vez menos frecuente. El conocimiento de que la FA no valvular también conlleva un riesgo elevado de tromboembolismo es de fecha más reciente. En los estudios Framingham(2) y en el Cerebral Embolism Task Force(3) se describe por primera vez que la FA se asocia a un alto riesgo de accidente cerebro vascular (ACV) isquémico, lo que fue corroborado poco tiempo después por el seguimiento en el mismo estudio Framingham(4). Datos de este estudio muestran que el riesgo de ACV ligado a FA aumenta desde 1,5% entre las edades de 50 a 59 años hasta 23,5% en edades entre 80 y 89 años. Se ha demostrado también que los ACV asociados a FA comprometen áreas más extensas del cerebro y dejan secuelas mayores en la etapa de recuperación(5). Más aún, los pacientes que han sufrido un ACV asociado a FA tienen un alto riesgo de recurrencia(6).
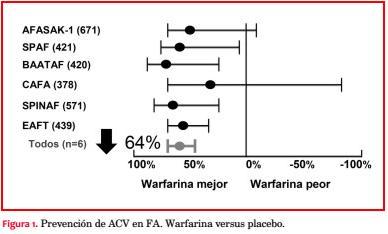
La mayor prevalencia de FA y estos reportes contribuyeron a la implementación de seis grandes estudios multicéntricos durante la década de 1990, en los que se evaluó el efecto de la warfarina, antagonista de la vitamina K (AVK), versus placebo y versus aspirina(7) (figura 1).
A través de estos ensayos clínicos se logró demostrar que el tratamiento anticoagulante oral bien llevado se asociaba a una reducción significativa del riesgo de ACV en 64%. Al mismo tiempo se reportó que la aspirina se asociaba a una reducción de riesgo menor, 19%. En estos ensayos se encontró que el tratamiento anticoagulante en sujetos de alto riesgo se asociaba también a un riesgo importante de hemorragias mayores y menores.
Formas de presentación clínica de fibrilación auricular y riesgo de accidente cerebro vascular
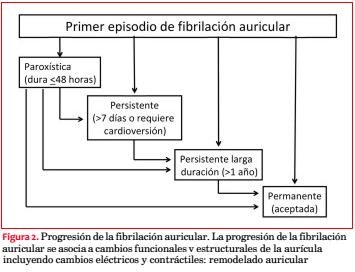
Desde el punto de vista clínico se ha clasificado la FA como paroxística cuando convierte a ritmo sinusal en forma espontánea o por efecto de fármacos dentro de las primeras 48 horas; como FA persistente cuando dura más de siete días y convierte a ritmo sinusal por efecto de fármacos o por cardioversión eléctrica y, por último, la FA permanente cuando la arritmia queda como el ritmo definitivo y su manejo se orienta a controlar la frecuencia cardíaca y a prevenir embolias sistémicas(8) (figura 2).
Cuando aparece o se detecta una nueva FA no se sabe con certeza a cuál de las formas clínicas consideradas en esta clasificación va a evolucionar. Los síntomas de una FA reciente pueden ser muy variados y pueden consistir en palpitaciones irregulares o rápidas, sensación de malestar o fatiga, síncope, dolor en el pecho, o bien puede debutar con insuficiencia cardíaca o embolia cerebral(9). Algunos pacientes con FA, especialmente adultos mayores, pueden ser asintomáticos y la arritmia constituir un hallazgo(10), o bien detectarse por monitorización electrocardiográfica prolongada, como se ha demostrado en pacientes que inicialmente eran clasificados como ACV criptogénicos y en los que se encontró FA paroxística hasta en un 30% en el seguimiento alejado(11).
Independientemente de su forma de presentación clínica la FA puede desencadenar una embolia cerebral y esto depende en gran parte de factores de riesgo preexistentes. La FA se asocia a pérdida de la contracción auricular y a una frecuencia cardíaca rápida, lo que puede precipitar insuficiencia cardíaca(12). Otra complicación, y la más temida, es que por estasia de la circulación sanguínea y activación de la coagulación se puedan formar trombos, especialmente en la orejuela, y dar lugar a embolias sistémicas. Nueve de cada diez embolias sistémicas comprometen la circulación cerebral. Se ha demostrado que la FA es un factor de riesgo independiente de ACV y se encuentra en el 15% de los ACV isquémicos(13).
La FA se asocia a un estado de hipercoagulabilidad, confirmado por la determinación de distintos marcadores sanguíneos como el complejo trombina-antitrombina, p selectina, factor von Willebrand y otros(14,15). Sin embargo, estos marcadores no son factores independientes de riesgo de un ACV, y si bien se encuentran elevados en una FA reciente, tienden a su normalización con el ritmo sinusal.
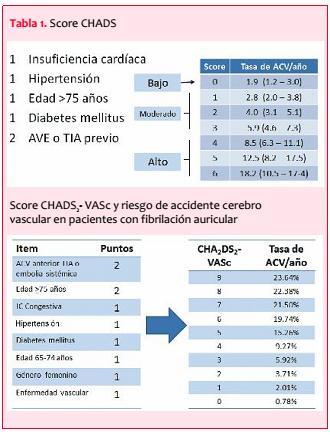
A través de datos obtenidos de dos grandes registros clínicos, como el norteamericano ATRIA, a comienzos del 2000, y el Euro Heart Survey conducido diez años más tarde en Europa, se han construido dos puntajes de riesgo para pacientes con FA y probable ACV, que son actualmente los más utilizados por su simplicidad y valor predictivo(16,17). El primero de ellos es el score de CHADS2, que incluye la historia de ACV previo (2 puntos), hipertensión arterial, insuficiencia cardíaca, diabetes mellitus y edad mayor a 75 años(1 punto cada uno), llegando a un puntaje máximo de 6. El segundo es el CHADS2-Vasc que mantiene los elementos anteriores otorgando 2 puntos a la edad mayor a 75 años y agrega sexo femenino, antecedente de enfermedad vascular asociada y edad mayor a 65 años (1 punto cada uno), llegando de esta manera a un puntaje máximo de 9. Con ambos puntajes de riesgo se observa un aumento progresivo del riesgo de sufrir un ACV y de la necesidad, reconocida en guías americanas y europeas, de administrar anticoagulantes orales con puntajes iguales o mayores a 1 (tabla 1).
La ventaja del CHADS2-Vasc es que permite una mejor discriminación de aquellos pacientes con puntaje de riesgo bajo, aumentando de esta manera el porcentaje de pacientes con indicación de recibir anticoagulantes. Las limitaciones de ambos puntajes de riesgo consisten en que la gran mayoría de los pacientes con FA se agrupan en los puntajes de riesgo intermedio y sus curvas ROC apenas sobrepasan el 60%(18). Aun con sus limitaciones estos puntajes de riesgo son los más utilizados en clínica para la indicación de anticoagulación oral. La información obtenida de grandes registros de pacientes con FA, como fueron el Euro Heart Survey y el más reciente GARFIELD FA, ha confirmado que solo 50% a 60% de los pacientes con indicación de anticoagulación oral reciben esta terapia(19,20). Esto se debe en gran parte al temor de los médicos tratantes de que los pacientes presenten complicaciones hemorrágicas o a las dificultades inherentes al tratamiento anticoagulante oral por parte de los mismos pacientes. Por estas mismas razones se han desarrollado también puntajes de riesgo para sangrado, cuyos componentes son muy similares a los de indicación de anticoagulación oral. El más utilizado de estos puntajes es el llamado score HAS BLED(21), el que incluye edad avanzada (> 65 años), hipertensión, falla renal o hepática, INR de difícil control, consumo de alcohol o drogas, historia de sangrado o de ACV previo, con un puntaje total de 9 (figura 3).
Es prudente evaluar por un lado el puntaje de riesgo para ACV como también el de sangrado para la toma de decisión respecto a la anticoagulación oral, especialmente en pacientes mayores.
Antagonistas de la vitamina K
Los AVK, como warfarina y acenocumarol, han constituido por muchos años el principal recurso utilizado para el tratamiento anticoagulante oral en pacientes con FA. La dosificación de los AVK se evalúa determinando el tiempo de protrombina y a través de este calculando el INR (international normalized ratio). Así se ha demostrado que la anticoagulación oral óptima se obtiene alcanzando un INR entre 2 y 3. Estudios multicéntricos efectuados en la década de 1990 confirmaron que los AVK, comparados con placebo y después con aspirina en pacientes con FA, podían reducir el riesgo de ACV en más del 60% de los casos(7) (figura 1). Desde entonces y hasta ahora han constituido el tratamiento estándar para la prevención de ACV. A través de estudios multicéntricos en que más adelante se comparó la combinación de aspirina con otro antiagregante plaquetario, clopidogrel versus warfarina en pacientes con FA, se demostró que además de la superioridad de la warfarina era necesario que el nivel óptimo de INR (entre 2 y 3) debía alcanzarse en promedio por sobre el 60% de las determinaciones para lograr una protección efectiva de embolias sistémicas (TRT) y con ello superar el efecto de los antiplaquetarios(22). Este concepto se había ya planteado en grandes registros de pacientes con FA, en los que se demostró que cuando el INR alcanzado era inferior a 2 persistía un riesgo elevado de ACV y cuando el INR sobrepasaba el valor de 3 aumentaban los riesgos de hemorragias(23). Por estos motivos en la gran mayoría de los centros hospitalarios en el mundo se organizaron policlínicos especiales para el control de la anticoagulación oral y asegurar de esta forma una protección efectiva y disminuir los riesgos de sangrado.
Los AVK tienen limitaciones importantes derivadas de su interacción con la dieta y con diversos medicamentos que se administran a los pacientes con FA. Estos quedan expuestos a pérdida de eficacia o a riesgos de sangrado menor o mayor y requieren constantes ajustes de dosificación y con ello de controles más frecuentes de INR. Al mismo tiempo las comorbilidades asociadas que tienen los pacientes con FA también conspiran para mantener un TRT óptimo. Entre estas destacan la insuficiencia cardíaca y la diabetes como factores que contribuyen a un TRT subóptimo y fluctuante(24). Las ventajas y desventajas de los AVK se muestran en la tabla 2.
Nuevamente, a través de diversos registros nacionales e internacionales de pacientes con FA, se ha demostrado que aproximadamente la mitad de los pacientes que debieran ser tratados con anticoagulación oral reciben este tipo de terapia y que en ellos el tiempo promedio óptimo de INR no sobrepasa el 40% en la mayoría de los casos. Los riesgos del tratamiento con AVK se corroboran también con un reporte sobre causas de hospitalización por reacciones adversas a medicamentos en servicios de urgencia norteamericanos en los cuales los AVK constituyen la principal causa(25). En el registro GARFIELD FA se ha comprobado que los pacientes con TRT óptimo tienen menor incidencia de ACV y de sangrado comparado con aquellos en los cuales el TRT bordea el 40%(26). Por estas razones es que existe la necesidad de contar con anticoagulantes orales más seguros y eficaces que puedan disminuir los riesgos inherentes a este tipo de tratamiento y que hagan posible que se trate con éxito a un mayor porcentaje de pacientes con FA.
Anticoagulantes orales directos
Los nuevos anticoagulantes directos (NOAC) ofrecen ventajas comparativas respecto a los AVK: se pueden administrar en una dosis fija, no requieren monitoría del INR, tienen menos interacción con la dieta y medicamentos, y alcanzan un efecto terapéutico muy rápido, entre dos a cuatro horas después de su ingesta. Al mismo tiempo tienen un mejor perfil de seguridad en cuanto a riesgo de hemorragia intracraneana (HIC). Su mayor limitación estaba dada por la ausencia de un antídoto conocido, pero se acaba de aprobar por la Food and Drug Administration (FDA) un antídoto para dabigatrán de acción muy rápida por vía endovenosa, el iderocizumab, y se encuentra en fase 3 un antídoto para los inhibidores del factor Xa, el andexanet. La incorporación de estos nuevos fármacos permitirá ofrecer un mejor margen de seguridad en la práctica clínica.
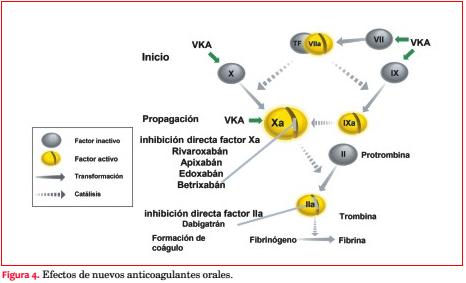
Por su sitio de acción se distinguen dos tipos de NOAC, los que inhiben directamente la trombina o factor II, como dabigatrán, y los que inhiben el factor Xa, como rivaroxabán, apixabán y edoxabán (figura 4).
Estos fármacos han sido evaluados en grandes estudios multicéntricos en los que se han comparado con los AVK y en total suman más de 71 mil pacientes(27-30). Las características farmacológicas se muestran en la tabla 3.
En breve, los NAOC alcanzan una concentración plasmática máxima entre las dos y cuatro horas, se transportan unidos a glicoproteínas, y tienen una vida media de doce a catorce horas. La mayor diferencia entre ellos es su vía de eliminación, ya que dabigatrán se elimina en un 80% por el riñón, en tanto que los otros tienen una eliminación mixta por el hígado y en menor proporción por el riñón. La unión a proteínas plasmáticas varía entre ellos. Para los efectos de prevención de tromboembolismo sistémico, dabigatrán ha sido ensayado en dosis de 110 y 150 mg cada doce horas, rivaroxabán y edoxabán en dosis únicas de 15 a 20 y 30 a 60 mg, respectivamente; por último, apixabán en dosis de 2,5 y 5 mg cada doce horas. Los estudios efectuados con estas drogas difieren entre sí en cuanto al perfil de riesgo de los pacientes y en cuanto a metodología de investigación (abierto o doble ciego), pero coinciden en cuanto a que han demostrado superioridad o no inferioridad respecto a los AVK.
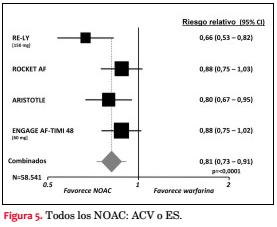
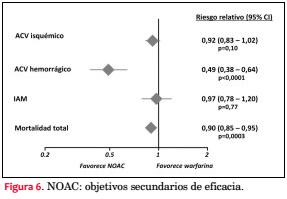
La utilización de NOAC en pacientes con FA ha ido en progresivo aumento desde su introducción clínica hace seis años, especialmente en países de mejores ingresos y con mayor cobertura de sus servicios de salud(31). En un metaanálisis reciente se ha confirmado que los NOAC disminuyen el ACV en 19%, a expensas de una disminución de HIC de 51% y disminuyen la mortalidad global en 10%. Por otra parte, estos fármacos aumentan el riesgo de sangrado gastrointestinal en 21% en comparación con warfarina(32) (figuras 5 y 6).
En los pacientes de alto riesgo de embolias o sangrado, como es el caso de adultos mayores, falla renal, antecedentes de ACV previo o reciente, también se ha demostrado que los NOAC ofrecen un perfil de seguridad igual o superior al tratamiento óptimo con warfarina(33).
La prescripción de NOAC se ha incrementado en el mundo y en la medida en que bajen su precio y la disponibilidad de nuevos antídotos continuará aumentando. Ambas medidas permitirán que el cuerpo médico se sienta más seguro y confiado en su prescripción. Por ahora, en aquellos pacientes que mantienen un TRT adecuado y estable no se requiere un cambio en su terapéutica. Por el contrario, en pacientes en que existen dificultades para controlar el INR en forma adecuada por su constante fluctuación o dificultades de acceso, el cambio a NOAC puede constituir la mejor opción y el cambio es sencillo de efectuar(34).
Bibliografía
1. Schnabel RB, Yin X, Gona P, Larson MG,
2. Wolf PA, Dawber TR, Thomas HE Jr, Kannel WB. Epidemiologic assessment of chronic atrial fibrillation and risk of stroke: the
3. Cardiogenic brain embolism. The second report of the Cerebral Embolism Task Force. Arch Neurol 1989 Jul;46(7):727-43. Fe de erratas en: Arch Neurol 1989;46(10):1079.
4. Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation as an independent risk factor for stroke: the Framingham Study. Stroke 1991;22(8):983-8.
5. Marini C, De Santis F, Sacco S, Russo T, Olivieri L, Totaro R, et al. Contribution of atrial fibrillation to incidence and outcome of ischemic stroke: results from a population-based study. Stroke 2005 ;36(6):1115-9.
6. Singer DE, Albers GW, Dalen JE, Go AS, Halperin JL, Manning WJ. Antithrombotic therapy in atrial fibrillation: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest 2004;126 Suppl 3:S429-56.
7. Hart RG, Benavente O, McBride R,
8. European Heart Rhythm Association; European Association for Cardio-Thoracic Surgery; Camm AJ, Kirchhof P, Lip GY, Schotten U, Savelieva I, Ernst S, et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010;31(19):2369-429. Fe de erratas en: Eur Heart J 2011;32(9):1172.
9. Corbalán R, Arriagada D, Braun S, Tapia J, Huete I, Kramer A, et al. Risk factors for systemic embolism in patients with paroxysmal atrial fibrillation. Am Heart J 1992;124(1):149-53
10. Potter BJ, Le Lorier J. Taking the pulse of atrial fibrillation. Lancet 2015 ;386(9989):113-5
11. Sanna T, Diener HC, Passman RS, Di Lazzaro V, Bernstein RA, Morillo CA, et al. Cryptogenic stroke and underlying atrial fibrillation. N Engl J Med 2014;370(26):2478-86.
12. Schnabel RB, Rienstra M, Sullivan LM, Sun JX, Moser CB, Levy D, et al. Risk assessment for incident heart failure in individuals with atrial fibrillation. Eur J Heart Fail 2013;15(8):843-9.
13. Benjamin EJ, Levy D, Vaziri SM, D’Agostino RB, Belanger AJ, Wolf PA. Independent risk factors for atrial fibrillation in a population-based cohort. The
14. Feng D, D’Agostino RB, Silbershatz H, Lipinska I, Massaro J, Levy D, et al. Hemostatic state and atrial fibrillation (the Framingham Offspring Study). Am J Cardiol 2001;87(2):168-71.
15. Alonso A, Tang W, Agarwal SK, Soliman EZ, Chamberlain AM, Folsom AR. Hemostatic markers are associated with the risk and prognosis of atrial fibrillation: the ARIC study. Int J Cardiol 2012;155(2):217-22.
16. Gage BF, Waterman AD,
17. Lip GY, Nieuwlaat R, Pisters R, Lane DA, Crijns HJ. Refining clinical risk stratification for predicting stroke and thromboembolism in atrial fibrillation using a novel risk factor-based approach: the euro heart survey on atrial fibrillation. Chest; 137(2):263-72.
18. Lip GY, Frison L, Halperin JL, Lane DA. Identifying patients at high risk for stroke despite anticoagulation: a comparison of contemporary stroke risk stratification schemes in an anticoagulated atrial fibrillation cohort. Stroke 2010;41(12):2731-8.
19. Nieuwlaat R, Capucci A, Camm AJ, Olsson SB, Andresen D, Davies DW, et al. Atrial fibrillation management: a prospective survey in ESC member countries: the Euro Heart Survey on Atrial Fibrillation. Eur Heart J 2005; 26(22):2422-34.
20. Kakkar AK, Mueller I, Bassand JP, Fitzmaurice DA, Goldhaber SZ, Goto S, et al. Risk profiles and antithrombotic treatment of patients newly diagnosed with atrial fibrillation at risk of stroke: perspectives from the international, observational, prospective
21. Pisters R, Lane DA, Nieuwlaat R, de Vos CB, Crijns HJ, Lip GY. A novel user-friendly score (HAS-BLED) to assess 1-year risk of major bleeding in patients with atrial fibrillation: the Euro Heart Survey. Chest 2010; 138(5):1093-100.
22. ACTIVE Writing Group of the ACTIVE Investigators; Connolly S, Pogue J, Hart R, Pfeffer M, Hohnloser S, Chrolavicius S, et al. Clopidogrel plus aspirin versus oral anticoagulation for atrial fibrillation in the Atrial fibrillation Clopidogrel Trial with Irbesartan for prevention of Vascular Events (ACTIVE W): a randomised controlled trial. Lancet 2006;367(9526):1903-12.
23. Hylek EM, Go AS, Chang Y, Jensvold NG, Henault LE, Selby JV, et al. Effect of intensity of oral anticoagulation on stroke severity and mortality in atrial fibrillation. N Engl J Med 2003;349(11):1019- 26.
24. Nelson WW, Choi JC, Vanderpoel J, Damaraju CV, Wildgoose P, Fields LE, et al. Impact of co-morbidities and patient characteristics on international normalized ratio control over time in patients with nonvalvular atrial fibrillation. Am J Cardiol 2013;112(4):509-12.
25. Budnitz DS, Lovegrove MC, Shehab N, Richards CL. Emergency hospitalizations for adverse drug events in older Americans. N Engl J Med 2011;365(21):2002-12
26. Haas S, Goto S, Fitzmaurice D, Eikelboom J, Ten Cate H, Koretsune Y, et al. International normalized ratio control and 1year outcomes in patients with newly diagnosed atrial fibrillation: the GARFIELD Registry [Abstract]. European Heart Journal 2014;35:1110.
27. Connolly SJ, Ezekowitz MD, Yusuf S, Eikelboom J, Oldgren J, Parekh A, et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009;361(12):1139-51.
28. Patel MR, Mahaffey KW, Garg J, Pan G, Singer DE, Hacke W, et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med 2011;365(10):883-91.
29. Granger CB, Alexander JH, McMurray JJ, Lopes RD, Hylek EM, Hanna M, et al. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2011;365(11):981-92.
30. Giugliano RP, Ruff CT, Braunwald E, Murphy SA, Wiviott SD, Halperin JL, et al. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2013;369(22):2093-104.
31. Olesen JB, Sørensen R, Hansen ML, Lamberts M, Weeke P, Mikkelsen AP, et al. Non-vitamin K antagonist oral anticoagulation agents in anticoagulant naïve atrial fibrillation patients: Danish nationwide descriptive data 2011-2013. Europace 2015; 17(2):187-93.
32. Ruff CT, Giugliano RP, Braunwald E, Hoffman EB, Deenadayalu N, Ezekowitz MD, et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of randomised trials. Lancet 2014;383(9921):955-62.
33. Potpara TS, Lip GY. Oral Anticoagulant Therapy in Atrial Fibrillation Patients at High Stroke and Bleeding Risk. Prog Cardiovasc Dis 2015; 58(2): 177-94.
34. Beyer-Westendorf J, Gelbricht V, Förster K, Ebertz F, Röllig D, Schreier T, et al. Safety of switching from vitamin K antagonists to dabigatran or rivaroxaban in daily care—results from the Dresden NOAC registry. Br J Clin Pharmacol 2014;78(4): 908-17.