Services on Demand
Journal
Article
Related links
Share
Revista Uruguaya de Cardiología
On-line version ISSN 1688-0420
Rev.Urug.Cardiol. vol.30 no.2 Montevideo Aug. 2015
Artículo original
Cambios reversibles de alteraciones basales de la contractilidad parietal del ventrículo izquierdo con drogas antiisquémicas.Estudio ecocardiográfico
Dres. Juan Bautista González Moreno, Álvaro Beltrán, Lics. Adriana De Lilla,
Nenúfar Di-Paola, Laura Firpi, Rossana Frattini, Miriam Saviotti,
Gustavo Strata, Dr. Jorge Pouso
Servicio de Ecografía Cardíaca (SEC). Montevideo, Uruguay.
Departamento de Cardiología. Centro Cardiovascular Casa de Galicia. Montevideo, Uruguay.
Correspondencia: Dr. Juan Bautista González Moreno. Aquiles Lanza 1348 Ap. 302. Montevideo, Uruguay.
Correo electrónico: gonzalezmorenojuan@yahoo.com.ar
Recibido junio 15, 2015; aceptado julio 7, 2015.
Resumen
Objetivos: determinar la utilidad clínica de la detección ecocardiográfica de alteraciones parietales basales de la contractilidad (ABC) reversibles con drogas antiisquémicas en pacientes con cardiopatía isquémica (CI) estable sospechada o conocida.
Antecedentes: no hay referencias en la literatura al respecto.
Población y método: estudio prospectivo observacional de la práctica clínica corriente en 93 pacientes ambulatorios, consecutivos (52,7% hombres, mediana 69,7 años), con indicación de ecoestrés mostrando ABC no cicatrizales. En su lugar se aplicó un protocolo con nitritos y metoprolol. Se consignaron los cambios del score segmentario (SS), del ángor y del electrocardiograma (ECG). Los pacientes fueron derivados directamente a cateterismo (n=9), internación (n=34) o domicilio (n=50). Se realizó un seguimiento a largo plazo (3,25 años-personas).
Resultados: los cambios del SS, ángor y ECG fueron significativos (p < 0,001). La mortalidad global fue 6,34 p-mes-1 x 1000, con tratamiento médico versus invasivo: 8,59 vs 3,8 p-mes-1 x 1000, cateterismo directo vs internados con cateterismo diferido: 3,93 vs 7,22 p-mes-1 x 1000, internados sin cateterismo: 18,62 p-mes-1 x 1000 y domiciliarios con y sin cateterismo: 4,03 vs 4,05 p-mes-1 x 1000, respectivamente. Los pacientes con cateterismo presentaron lesiones severas mayormente de múltiples vasos.
Conclusiones: la detección ecocardiográfica de ABC reversibles con drogas antiisquémicas en pacientes con CI evoca la presencia de isquemia miocárdica de reposo en una población de alto riesgo y tiene un importante valor pronóstico.
Palabras clave:
ECOCARDIOGRAFíA
ALTERACIONES DE LA CONTRACTILIDAD
NITROGLICERINA
METOPROLOL
Summary
Objectives: to determine the clinical usefulness in detecting reversible resting echocardiographic segmental wall motion contractile abnormalities (ABC) in patients with stable coronary artery disease (CI).
Background: There are no references in the literature.
Population and method: This is a current clinical practice prospective observational study on 93 consecutive patients (58% men, median 69,7 years) with stress echocardiograms requested and showing non scarring ABC who were submitted to echocardiograms with nitrates and metoprolol instead. Left ventricular segmental wall motion score index (SS), electrocardiographic abnormalities (ECG) and chest pain changes were determined. Patients were referred either to direct catheterization (n=9), hospitalization (n=34) or to their residences (n=50). A 3,25-years-persons follow-up was performed.
Results: SS, ECG abnormalities and chest pain changed significantly (p<0,001). The higher SS, the higher mortality. Global mortality was 6,34 p-mes-1 x 1000; patients with medical vs. invasive treatment: 8,59 vs 3,8 p-mes-1 x 1000, with direct catheterization vs. those hospitalized with deferred catheterization: 3,93 vs 7,22 p-mes-1 x 1000, patients hospitalized without catheterization: 18,62 p-mes-1 x 1000, and domiciliary patients with and without catheterization: 4,03 vs 4,05 p-mes-1 x 1000. Patients with catheterization showed severe multi-vessel disease mainly.
Conclusions: Reversible echocardiographic ABC with anti-ischemic drugs evokes resting myocardial ischemia, a high risk CI population and has important prognostic value.
Key words:
ECHOCARDIOGRAPHY
WALL MOTION CONTRACTILE ABNORMALITIES
NITRATES
METOPROLOL
Introducción
La cardiopatía isquémica (CI) es una de las mayores causas de muerte en el mundo y es altamente variable en su presentación clínica(1).
En la coronariopatía suelen coexistir lesiones con distinto nivel de progresión lesional(2-4), de tal manera que los pacientes pueden iniciarse clínicamente con una angina de pecho estable, una angina inestable, un síndrome coronario agudo o síndromes clínicos intrincados a veces de difícil definición.
Al evaluar a un paciente con una CI estable sospechada o conocida, la presencia de una angina de pecho típica acompañada de nuevas alteraciones del electrocardiograma (ECG) o del ecocardiograma bajo la forma de nuevas alteraciones basales de la contractilidad del ventrículo izquierdo (ABC)(5,6) son suficientes para decidir la realización de una coronariografía sin más trámite y el potencial intervencionismo hemodinámico(7).
Sin embargo, también es posible observar estas alteraciones en un ecocardiograma rutinario o en un ecocardiograma previo a la realización de un ecoestrés, tanto en pacientes que no refieren síntomas o con síntomas atípicos.
En la primera situación el ecocardiografista se limita a destacarlo en el informe y el paciente usualmente continúa ambulatorio hasta que consulte a su médico responsable, y, en la segunda situación, tendrá que decidir la suspensión o la realización de la prueba sin desconocer las potenciales complicaciones que conlleva, a veces muy importantes cuando se trata de pruebas de provocación de isquemia miocárdica(8-12).
Desde hace ya mucho tiempo, Helfant(13), Lawrie(14), Chesebro(15) y Rahimtoola(16) demostraron con ventriculografía de contraste que la reversibilidad de las ABC utilizando nitroglicerina, un potente vasodilatador coronario y que normalizaron después de la revascularización quirúrgica, correspondía a miocardio isquémico en reposo recuperable y por lo tanto viable.
Este trabajo pretende determinar si el ecocardiograma tiene utilidad clínica en detectar ABC reversibles utilizando drogas antiisquémicas, como nitritos y metoprolol, en pacientes con CI tanto para confirmar el diagnóstico presuntivo como para valorar el pronóstico en pacientes con CI. No hay referencias en la literatura al respecto.
Pacientes y métodos
De 6.900 pacientes consecutivos recibidos en nuestros laboratorios de ecocardiografía (Servicio de Ecografía Cardíaca y Departamento de Cardiología de Casa de Galicia, Montevideo, Uruguay), desde enero del 2004 a marzo del 2011 para la realización de ecoestrés en diversas modalidades (4.204 ecoestrés con dobutamina, 2.550 ecoestrés con ejercicio y 146 ecoestrés con dipiridamol) surgieron 107 pacientes (1,55%) con ABC pero sin criterios de isquemia cicatrizal, es decir segmentos parietales del ventrículo izquierdo (VI) sin disminución del espesor diastólico menores de 6 mm y sin aumento de la ecogenicidad.
También se consignaron los cambios en quienes presentaran síntomas (ángor) y alteraciones del electrocardiograma (ECG).
Ciento seis pacientes respondieron a la mejoría con el ECDAI y uno no. Catorce pacientes fueron perdidos en el seguimiento.
Finalmente, 93 pacientes constituyeron la cohorte, con una mediana de 69,77 años (DE 9,551). Cuarenta y nueve pacientes (52,7%) fueron de sexo masculino con una mediana de 68,83 años (DE 8,611), el sexo femenino con una mediana de 71,05 años (DE 10,452).
Este es un estudio prospectivo observacional de la práctica clínica corriente que tomó en cuenta las recomendaciones de los cardiólogos ecocardiografistas luego de los resultados de las pruebas (cateterismo directamente, internación o domicilio) en común acuerdo con los médicos tratantes, quienes tomaron las decisiones clínicas subsecuentes.
Se realizó un seguimiento a largo plazo (87 meses de evolución total con una mediana de 3,25 años-personas) determinando la mortalidad de causa cardiovascular.
De la historia clínica realizada por los cardiólogos ecocardiografistas (JBGM y AB) antes de las pruebas surgió que el 85% de los pacientes tenían dos o más factores de riesgo coronario: 58 eran hipertensos (62%), 27 dislipémicos (29%), 16 diabéticos (17%) y 13 fumadores (14%).
Setenta pacientes (75,3%) tenían una historia de angina de pecho típica y el resto (24,7%) estaban asintomáticos o presentaban dolor torácico atípico.
Cuarenta pacientes (43%) tenían una historia de CI conocida, 30 de ellos (32%) con angioplastia coronaria o revascularización quirúrgica previas. Contamos con los cateterismos correspondientes consignando las lesiones coronarias previas y los vasos tratados tanto de las cirugías como de las angioplastias realizadas.
Diecinueve pacientes (20,4%) se presentaron con ángor al momento de la prueba (Clase IV de la Sociedad Canadiense de Cardiología)(17,18) y 68 (73,1%) mostraban alteraciones de la repolarización en el ECG.
La base de datos contempló: 1) Ficha patronímica. 2) Factores de riesgo coronario. 3) Antecedentes de CI previa. 4) Alteraciones del ECG. 5) Fecha del ecocardiograma basal consignando: a) las ABC en el ecocardiograma basal, b) la presencia o no de ángor y c) el SS basal. 6) El ECDAI consignando los cambios de: a) ABC, b) ángor (si estuvo presente), c) SS y d) ECG. 7) La conducta tomada luego del ECDAI en cuanto a la derivación del paciente: a) cateterismo directo, b) internación y c) al domicilio. 8) Datos del cateterismo: a) fecha de realización, b) lesiones coronarias encontradas. 9) Tratamiento: a) invasivo (angioplastia o cirugía) y b) médico.
Todos los pacientes dieron su consentimiento a la realización de las pruebas. El Comité de Ética de nuestro hospital aprobó el estudio.
Protocolo del ECDAI
Se utilizaron los mismos equipos de las pruebas para ecoestrés: a) ecocardiógrafos Phillips 7500 (Andover, Massachusetts, USA) equipados con software de estrés para análisis lado a lado de las imágenes; b) electrocardiógrafos de 12 derivaciones; c) esfigmomanómetros de presión arterial, y d) monitorización del ECG con cardiodesfibriladores externos en posición de espera.
Dos ecocardiografistas experimentados (JBGM, AB) en ecoestrés realizaron y analizaron los estudios randomizados. Con el paciente en decúbito lateral izquierdo obtuvieron las imágenes de los planos paraesternales izquierdos y apicales antes y después de la aplicación del protocolo.
Enfermeras realizaron los controles vitales y aplicaron las drogas. Asimismo, técnicas neumocardiólogas realizaron los trazados electrocardiográficos.
El protocolo (figura 1) comienza aplicando una dosis de 5 mg de nitritos vía sublingual si la presión arterial fuera igual o mayor a 100 mmHg. Si la frecuencia cardíaca es mayor a 90 cpm comienza con metoprolol en dosis de 1,25 mg i/v hasta que la frecuencia cardíaca descienda a 60 cpm y a un máximo total de 5 mg. Las etapas son sucesivas, de 3 minutos de duración, y se completan de acuerdo a la secuencia de inicio con nitritos o metoprolol respectivamente. Es criterio de suspensión: 1) la reversibilidad de las ABC y 2) la aparición de hipotensión arterial (PAS <100 mmHg) sintomática.
Para el ECG se consideraron alteraciones leves un desnivel del segmento ST de 0,5 mm a 0,08 segundos del punto J y cambios de la onda T, lteraciones moderadas de 0,5 a 1,0 mm y severas más de 1 mm (ganancia 1 cm/mV).
Para las ABC: uno o dos segmentos se consideraron alteraciones leves, tres o cuatro alteraciones moderadas y más de cuatro segmentos alteraciones severas
Para el SS y su cambio después del ECDAI se utilizó el modelo de 16 segmentos de las guías de la Sociedad Americana de Ecocardiografía(19), adjudicando el puntaje de 1 (normal), 2 (hipoquinesia), 3 (aquinesia) y 4 (disquinesia) a cada segmento y dividiendo la suma por 16. La severa hipoquinesia (porcentaje de acortamiento sistólico menor de 10%) también se consideró puntaje 3. Un SS de 1,0 se consideró normal; hasta 2,0 moderadamente anormal, y mayor de 2,0 severamente anormal.
La variabilidad interobservador de ambos ecocardiografistas (JBGM y AB) determinada para la contractilidad segmentaria(20) es de 9,2% (kappa 0,78). En los casos dudosos se realizó una estimación en consenso.
Análisis estadístico
La tendencia central de la distribución de variables numéricas continuas se reportaron como media ± 1 DE, en tanto los datos nominales y categóricos se representaron a través de proporciones porcentuales con su intervalo de confianza de 95% (IC95%), según la cuadrática de Fleiss y las comparaciones entre ellos se efectuaron por medio de chi cuadrado o probabilidad exacta de Fisher, según correspondiera.
Para la comparación entre los valores medios de SS (reposo vs ECDAI) se utilizó la prueba no paramétrica de Wilcoxon.
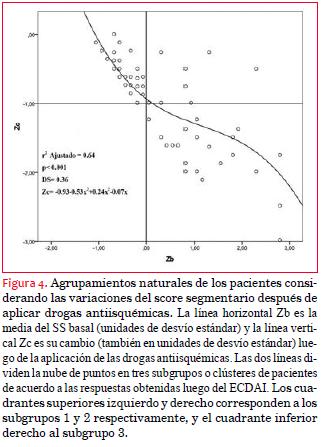
Se calculó media ± 1 DE del SS antes (reposo) y luego de ECDAI. Ambas distribuciones fueron estandarizadas en unidades Z (Zb y Za, respectivamente) y se determinó su diferencia Zc=Za–Zb como representativa del cambio. Los cambios negativos implican mejoría, tanto mayor cuanto menor Zc (mayor valor absoluto de Zc). Con el propósito de explorar los agrupamientos naturales de los datos de los pacientes se construyó un gráfico cartesiano entre Zb (eje de x) y Zc (eje de y), dividiéndose el área resultante en cuatro cuadrantes de acuerdo con dos líneas rectas que se intersectan: una vertical que se origina cuando Zb=0 y otra horizontal cuando Zc=–1 DE. De acuerdo con esto, el modelo se ajusta por los mínimos cuadrados y el procedimiento se repite a sí mismo en cada cuadrante. Se calculó el coeficiente de correlación por rangos de Spearman para determinar la correlación entre el cambio en SS (unidades Z) y existencia de nuevas lesiones en los pacientes.
Una p=0,05 a dos colas se consideró significativa. Todos los cálculos estadísticos se realizaron en SPSS V.17 /SPSS Inc. Chicago, IL, USA.
Resultados
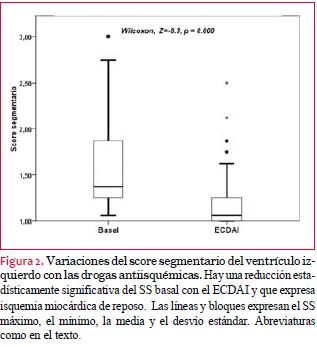
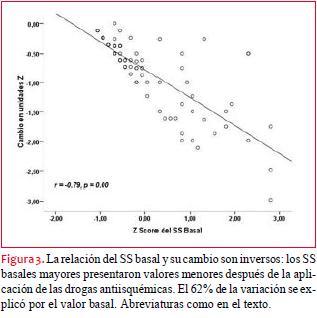
El SS cambió significativamente con el ECDAI con una p < 0,001 (figura 2). Hay una relación inversa entre el SS basal y su cambio (disminución) con las drogas antiisquémicas, lo que supone que los pacientes con peor SS fueron los que presentaron las mayores mejorías de la contractilidad. El 62% de la variación se explicó por su valor basal (figura 3).
También se registró una disminución significativa del ángor y de las alteraciones de la repolarización del ECG presentes en el momento de la prueba (tabla 1).
La mortalidad acumulada fue mayor en los pacientes con mayores SS basales: el subgrupo 2 (44% de mortalidad en 53 meses de seguimiento con cuatro decesos en nueve pacientes) y el subgrupo 3 (25% en 82 meses de seguimiento con cinco decesos en 20 pacientes) respecto al subgrupo 1 (19% en 87 meses de seguimiento con 12 decesos en 64 pacientes). La probabilidad de sobrevida acumulada de los tres subgrupos a uno y cinco años se muestra en la tabla 2.
Ya se trate de anormalidades leves o moderadas en el ecocardiograma basal, las diferencias entre los SS basal y ECDAI fueron significativas, con un SS siempre significativamente menor en el ECDAI (tabla 3).
Los pacientes fueron derivados a cateterismo directo (n=9), internación (n=34) o domicilio (n=50) después del ECDAI (tabla 4).
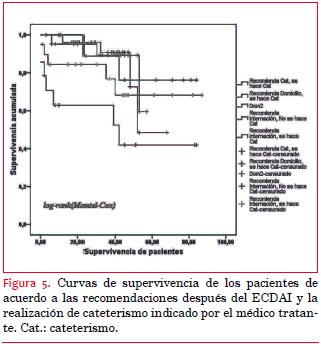
En 58 pacientes (62%) se solicitó la realización de cateterismo. En 52 de ellos (89,7%) se encontraron nuevas y severas lesiones tanto de arterias coronarias como de puentes coronarios (venosos o arteriales) de pacientes revascularizados previamente, con una incidencia de 2,28 nuevas lesiones severas de vasos por paciente.
Para aquellos con o sin antecedentes de reperfusión coronaria previa, la incidencia de lesiones fue de 1,87 y 2,47, respectivamente. Esta tendencia no fue correspondida con una significación estadística, y tampoco respecto al SS basal y su cambio después del ECDAI (tabla 5).
La tabla 6 muestra las lesiones encontradas independientemente que se hubieran registrado normalizaciones parciales o totales en el ECDAI. Predominaron las lesiones de tres vasos, siendo la arteria descendente anterior la más frecuentemente afectada.
La figura 6 muestra uno de los casos cllìnicos
Comentarios
Es sugestivo que hayan llegado estos pacientes con CI a realizarse un ecoestrés (situación poco frecuente en nuestra experiencia, ya que solamente surgió en 1,55% de 6.900 pacientes), aunque no estuviera indicado, pues presentaban ABC sugestivamente de isquemia de reposo, por lo cual, en contrapartida, debían haber sido referidos a un cateterismo cardíaco.
Pudo suceder que no se les hubiera solicitado un ecocardiograma, o que si contaban con uno previo, esas alteraciones no hubieran sido ponderadas debidamente o que las mismas hubieran surgido en el interín entre la fecha de solicitud del ecoestrés y la fecha de su realización.
En este sentido, realizar una prueba alternativa “antiestrés” con drogas como nitritos o betabloqueantes permitía ponerla en evidencia rápidamente al mejorar la contractilidad, pero sin riesgos para el paciente.
Faltaba conocer el devenir de los pacientes en términos de mortalidad de acuerdo a la conducta clínica tomada una vez conocidas las respuestas a las pruebas y justificar o no su utilización en la práctica clínica corriente.
No obstante, había otros (24,7%) que referían una historia con síntomas atípicos o estaban asintomáticos. Ellos seguramente fueron quienes más se beneficiaron con la aplicación del ECDAI, en especial los que tenían ECG normales, al haber permitido exponer el único signo de sospecha de isquemia miocárdica de reposo: las ABC.
Nuestros resultados confirman precisamente que la mejoría de la contractilidad total o parcial de uno o varios segmentos de las paredes del VI por medio de drogas antiisquémicas, como nitritos y betabloqueantes, se corresponda con una mejoría de la perfusión miocárdica críticamente alterada, ya en condiciones de reposo como era de esperar y sustentada por la mejoría de las alteraciones del ECG y de los síntomas de algunos pacientes que las presentaban al momento de la realización de la prueba.
Una serie de elementos deben considerarse con nuestros resultados:
1. El método muestra alta factibilidad. Una vez que se detecta el cambio del SS, lo hace en una relación inversa: a mayor SS basal, mayor cambio pos-ECDAI.
2. A mayor SS, mayor mortalidad. Los pacientes con mayores SS y más alteraciones del ECG expresan un quantum mayor de miocardio en riesgo y en consecuencia tienen mayor mortalidad acumulada. Pero su sobrevida depende de la mayor cantidad de miocardio viable expresado en una mayor respuesta de cambio del SS en el ECDAI y por ende pasibles de mejorar con revascularización, como se vio en el subgrupo 3 respecto al subgrupo 2, que tenía un SS basal alto pero poca (< 1 DE) respuesta a las drogas antiisquémicas.
Ya se ha demostrado que hay asociación entre la magnitud del SS con la extensión y la severidad de la depresión del ST en la mortalidad a 30 días de pacientes con IAM sin elevación del segmento ST(21). Las determinaciones del SS se han manifestado como un marcador poderoso de mortalidad frente a otros parámetros como las troponinas o la CK-MB y el propio diámetro telesistólico, o la fracción de eyección del VI(22). Su mayor poder discriminatorio, especialmente en las disfunciones no severas del VI, puede explicarse por su independencia del efecto compensador generado por la hiperquinesia de los segmentos remanentes no afectados por la isquemia, a diferencia de la fracción de eyección. Esta se constituye en una medida más precisa de daño miocárdico.
4. La mortalidad global de nuestros pacientes es alta (6,3% p-mes-1x 1000) y constituyen una población de alto riesgo que incluye, como observamos, a pacientes asintomáticos o con síntomas atípicos.
5. La mortalidad disminuye dramáticamente con la celeridad de la revascularización miocárdica. La derivación directa a cateterismo permite descender mucho la mortalidad. Asimismo es evidente el beneficio en quienes se aplica un tratamiento invasivo (angioplastia o cirugía) respecto a quienes se decide un tratamiento médico.
6. Una multiplicidad de lesiones (2,28 vasos/paciente) severas (nuevas lesiones para los pacientes con antecedentes de revascularización) y frecuentemente combinadas (uno, dos y tres vasos con o sin puentes coronarios incluidos) o lesión del tronco de la coronaria izquierda, son la expresión de una enfermedad aterosclerótica avanzada. Estos elementos se aplican a todos los pacientes con o sin antecedentes de CI, con o sin antecedentes de reperfusión previa e independientemente de la cuantía de la respuesta lograda con el ECDAI.
7. Desconocemos los criterios clínicos utilizados por los médicos tratantes para mantener a algo más de la mitad de los pacientes en tratamiento médico indicando o no la coronariografía. Pudo haber influido en sus decisiones que este grupo estaba constituido por pacientes más añosos (mediana de 74 años), la mitad de ellos con antecedentes de revascularización miocárdica previa, por lo que no hubieran admitido nuevas revascularizaciones, o por comorbilidades agregadas. También estaban los seis pacientes con pruebas falso positivas que no mostraban lesiones coronarias significativas.
Si bien no es frecuente encontrar ABC en pacientes enviados a ecoestrés, seguramente sería muy diferente si se consideran los distintos escenarios clínicos donde interviene la ecocardiografía en la valoración de pacientes con CI: consultorios de ecocardiografía, unidades de dolor torácico, servicios de puerta hospitalarios, etcétera.
También el ECDAI es una técnica alternativa útil a las pruebas funcionales de provocación de isquemia miocárdica, hasta hoy no referida en la literatura y no contemplada en las guías de práctica clínica, al permitir la identificación de una población de alto riesgo no sospechada a priori, especialmente si es clínicamente estable aun cuando la clínica y el ECG no sean concluyentes.
Puede ser aplicada fácilmente en todo lugar que cuente con un ecocardiógrafo y un técnico capacitado y no requiere equipo sofisticado de apoyo para reanimación cardiovascular al aliviarse y no provocar isquemia miocárdica.
Limitaciones
Por tratarse de una población con una alta probabilidad pretest de CI tiene un sesgo natural, pero que también ubica a estas alteraciones como de etiología prioritariamente isquémica.
Los pocos pacientes falsos positivos (n=6), al no haberse comprobado lesiones coronarias significativas, correspondieron a pacientes con hipocontractilidad global y remodelación difusa del VI. Ello implica tener cautela al interpretar una mejoría global de la función sistólica y no segmentaria, en especial si el paciente tiene una clínica predominantemente de insuficiencia cardíaca y una probable miocardiopatía. Al aumentar el flujo coronario también puede aumentar la contractilidad miocárdica creando una falsa interpretación de isquemia de reposo.
Reconocemos que puede ser difícil visualizar ABC en pacientes con mala ventana ultrasónica o malinterpretarlas por anclaje de la pared posterior al anillo mitral, o en los casos de disquinesias generadas por alteraciones de la conducción intraventricular (como el bloqueo de rama izquierda del haz de Hiss o estímulo de marcapasos). Por lo tanto, el criterio del engrosamiento sistólico de la pared y no del desplazamiento debe primar al momento de decidir o no realizar el ECDAI.
Desconocemos si fueron realizadas pruebas de laboratorio para descartar un síndrome coronario agudo después de la realización del ECDAI, probabilidad muy baja de ocurrir desde que las alteraciones segmentarias eran reversibles y no fijas en la gran mayoría de los pacientes (solamente en un paciente no revirtieron).
No contamos con tecnología reciente como strain o strain-rate con rastreador de muestras (speckle-tracking), una herramienta interesante a usarse en este grupo especial de pacientes al permitir valorar selectivamente la función endocárdica, ya que puede estar reducida en pacientes con síndromes coronarios agudos sin elevación del segmento ST acompañados de lesiones coronarias severas(23).
Conclusiones
La detección ecocardiográfica de ABC reversibles con drogas antiisquémicas en pacientes con CI evoca la presencia de isquemia miocárdica de reposo en una población de alto riesgo y tiene importante valor pronóstico.
Nota: este trabajo no hubiese sido posible realizarlo sin el aporte fundamental del Dr. Jorge Pouso (†), tanto en la preparación del proyecto como del celo del análisis estadístico.
Además, los autores desean agradecer la colaboración incondicional de las secretarias Raquel Brasil Suárez y Milka Colombo Gómez en el seguimiento de los pacientes.
Bibliografía
1. Fuster V, Voute J, Hann M, Smith S. Low –priority of cardiovascular and chronic diseases on the global health agenda: a cause of concern. Circulation 2007: 1176: 1966-70.
2. Hansson GK. Mechanisms of disease: inflammation, atherosclerosis, and coronary disease. N Engl J Med 2005; 352 (16): 1685-95.
3. Prati F, Uemura S, Souteyrand G, Virmani R, Mostreff P, Di Vito Luca, et al. OCT- based diagnosis and management of STEMI associated with intact fibrous cap. J Am Coll Cardiol Img 2013;6:283-
4. Pandian NG, Kieso RA, Kerber RE. Two-dimensional echocardiography in experimental coronary stenosis. II. Relationship between systolic wall thinning and regional myocardial perfusion. Circulation 1982;66;603-11.
6. Montalescot G, Sechtem U, Achenbach S , Andreotti F, Arden Ch, Budaj A, et al. 2013 ESC guidelines on the management of stable coronary artery disease. The Task Force on the management of stable coronary artery disease of the European Society of Cardiology European Heart Journal 2013 34, 2949-3003.
7. Fihn SD, Gardin J et al. 2012 ACCF/AHA/ ACP/AATS/PCNA/SCAI/STS Guideline for the diagnosis and management of patients with stable ischemic heart disease. JACC 2012:60:e44-e164 .
8. Vignolo G, Durán A, González Rama A, Lluberas R. Ecocardiograma con dobutamina. Un caso poco frecuente pero grave. Rev Urug Card 2004; 19:88.
9. Geleinjse ML, Fioretti PN, Roelandt J. Methodology, feasibility, safety, and diagnostic accuracy of dobutamine stress echocardiography. J Am Coll Cardiol 1997; 30: 595-606.
10. Rodríguez García MA, Iglesias-Garriz I, Corral Fernández F, Garrote Coloma C, Alonso-Orcajo N, Branco L, et al. Evaluation of safety of stress echocardiography in
11. Mathias W Jr, Arruda A, Santos FC, Arruda AL, Mattos E, Osorio A, et al. Safety of dobutamine-atropine stress echocardiography: A prospective experience of 4,033 consecutive studies. JASE 1999; 12(10):785-91.
12. Varga A, Kraft G, Lakatos F, Bigi R, Paya R, Picano E. Case report. Complications during pharmacological stress echocardiography: a video-case series .Cardiovascular Ultrasound 2005; 3:25.
13. Helfant RH, Pine R, Meister SG, Feldman MS, Trout RG,
14. Lawrie GM, Morris GC Jr, Chapman DW, Winters WL, Lie JT. Patterns of patency of 596 vein grafts up to 7 years after aorta-coronary bypass. J Thorac Cardiovasc Surg 1977, 73: 433.
15. Chesebro JH, Ritman EL, Frye RL, Smith HC, Rutherford BD, Fulton RE, et al. Regional myocardial wall thickening response to nitroglycerine. Predictors of myocardial response to aortocoronary bypass surgery. Circulation. 1978; 57:952-7.
16. Rahimtoola SH. Coronary bypass surgery for chronic angina—1981- A perspective. Circulation 1982: 65:225-61.
17. Campeau L. Canadian Cardiovascular Society Functional classification of angina pectoris. Letter: Grading of angina pectoris. Circulation 1976: 522-3.
18. Campeau L. Canadian Cardiovascular Society Functional classification of angina pectoris. Letter: Grading Mertes H, Sawada SG, Ryan T, Segar DS, Kovacs R, Foltz J et al. Symptoms, adverse effects, and complications, associated with dobutamine stress echocardiography. Experience in 118 patients . Circulation 1993,88:15-9.
19. Schiller NB, Sha PM, Crawford M. Recommendations for quantitation of the left ventricle by two-dimensional echocardiography. J Am Soc Echocardiogr 1989:2: 358-67.
20. González Moreno JB, Beltrán A, Pouso J, Ortiz A, Lado M, Galain G, et al. Clinical utility of low dose dobutamine echocardiography in regional myocardial viability detection before and after surgical revascularization. Echocardiography 2002, 19: 537-47.
21. Figueras J, Barrabés J, Evangelista A, Lidón RM, Gutiérrez L, García del Blanco B, et al. Admission wall motion score and quantitative ST-segment depression in the assessment of 30-day mortality in patients with first non–ST-segment elevation acute coronary syndromes. J Am Soc Echocardiogr 2013;26:885-92.
22. Galasko GIW, Basu S, Lahiri A, Senior RA. Prospective comparison of echocardiographic wall motion score index and radionuclide ejection fraction in predicting outcome following acute myocardial infarction. Heart 2001; 86:271-6.
23. Sarvari S, Haugga K, Zahid W, Bendz B, Aakhus S, Aaberge L, et al. Layer-specific quantification of myocardial deformation by strain echocardiography may reveal significant CAD in patients with non-ST segment elevation acute coronary syndrome. J Am Coll Cardiol Img 2013;6:535-44.