Services on Demand
Journal
Article
Related links
Share
Revista Uruguaya de Cardiología
On-line version ISSN 1688-0420
Rev.Urug.Cardiol. vol.29 no.2 Montevideo Aug. 2014
Artículo original
Ateromatosis carotídea y características del tratamiento en pacientes con disfunción sistólica de origen isquémico y no isquémico: comparación con población control
Dres. Juan Albistur1, Yanina Zócalo2, Pablo Álvarez3, Ignacio Farro4,
Lucía Florio5, Br. Victoria García6, Lic. Marcelo Bermúdez7, Dr. Daniel Bia8
5. Médica. Prof. Adjunto, Depto. Cardiología, Hospital de Clínicas, Udelar.
6. Br. Estudiante de Medicina, Becaria (Espacio Interdisciplinario, Udelar), CUiiDARTE.
7. Licenciado en Neumocardiología. Becario (Espacio Interdisciplinario, Udelar; ANII), CUiiDARTE.
Instituciones responsables: (1) Depto. Cardiología, Facultad de Medicina, Hospital de Clínicas, Udelar; (2) Depto. Fisiología, Facultad de Medicina, Centro Universitario de Investigación, Innovación y Diagnóstico Arterial (CUIIDARTE), Udelar, Hospital de Clínicas, Udelar; (3) Unidad Multidisciplinaria de Insuficiencia Cardíaca (UMIC).
Correspondencia: Dr. Juan Sebastián Albistur, Rambla República de Chile 4573 apto. 706, Montevideo, Uruguay.
Correo electrónico: jsalbistur@gmail.com
Recibido mayo 2, 2014; aceptado julio 22, 2014
Resumen
Fundamento: la insuficiencia cardíaca sistólica (ICS) genera un aumento del estrés oxidativo que podría explicar un riesgo aumentado de aterosclerosis. Sin embargo, se desconoce si la prevalencia de ateromatosis carotídea es mayor en pacientes con disfunción sistólica del ventrículo izquierdo de etiología no isquémica respecto de la población general. El tratamiento con estatinas en la insuficiencia cardíaca (IC) es discutido, si bien existe evidencia de que algunos grupos podrían beneficiarse de estas. Conocer si pacientes con ICS de etiología no isquémica presentan mayor ateromatosis permitiría reconocer un subgrupo de pacientes que podrían beneficiarse de estrategias de tratamiento específicas
Objetivo: determinar si la prevalencia de placas de ateroma carotídea en pacientes con ICS isquémica, no isquémica y en sujetos asintomáticos sin ICS y similar exposición a factores de riesgo tradicionales presenta diferencias.
Método: se incluyeron (1) pacientes con ICS isquémica (grupo 1, G1; n=39; edad: 65±8 años; 67% hombres), (2) ICS no isquémica (grupo 2, G2; n=23; edad: 62±12, 78% hombres) y (3) un grupo control (grupo 3, G3; n=199; edad 58±9, 75% hombres) de sujetos con características similares a las del G2 (edad, sexo, factores de riesgo CV), pero sin IC. Se determinó presencia de placa de ateroma carotídea por ultrasonido. Se analizó prevalencia de placa en relación con el antecedente de dislipemia, tratamiento con estatinas y nivel objetivo de lipoproteínas de baja densidad (LDL) en sangre.
Resultado: la prevalencia de placa de ateroma carotídea en G1 fue de 87% (intervalo de confianza del 95% [IC95%]: 76%-98%), en G2 de 61% (IC95%: 41%-81%) y en G3 37% (IC95%: 30%-44%) (p<0,05). La indicación de estatinas en el G2 se limitó a pacientes con dislipemia (65%). El 22% de los pacientes del G2 con placa no recibía estatinas. El 26% de los pacientes del G1 alcanza LDL objetivo (LDL<70mg/dL). En el G2 se logró LDL objetivo en el 40% (LDL < 100 mg/dL). Si el LDL objetivo es < 70 mg/dL, en pacientes con IC y ateromatosis el objetivo se cumple en el 25%.
Conclusión: la prevalencia de ateromatosis carotídea en pacientes con ICS es elevada, incluso en pacientes con ICS de etiología no isquémica, habiendo en esta una prevalencia mayor que en la de sujetos sin IC, con similar prevalencia de factores de riesgo tradicionales. En la mayoría de los pacientes con IC no se alcanzan niveles de LDL objetivo.
Palabras clave:
INSUFICIENCIA CARDÍACA
INSUFICIENCIA CARDÍACA SISTÓLICA
PLACA ATEROESCLERÓTICA
ENFERMEDADES DE LAS ARTERIAS CARÓTIDAS
DISLIPEMIAS
ESTATINAS HMG-COA
Summary
Background: systolic heart failure (SHF) is associated with an increased oxidative stress which may be related with an increased risk of atherosclerosis; but it is unknown if carotid atherosclerosis is more frequent in patients with SHF of non-ischemic etiology than general population. Statins treatment in heart failure is discussed, although some groups may benefit from them. Identification of patients with SHF with non-ischemic etiology and atherosclerosis, would recognize a sub group of patients who can benefit from specific treatment strategies.
Objective: to compare the prevalence of carotid plaques in patients with ischemic SHF, non-ischemic SHF and patients without HF or systolic dysfunction and similar cardiovascular risk factors.
Method: thirty nine patients with ischemic SHF (Group 1, G1, age: 65±8 years; 67% men), 23 with non-ischemic SHF (Group 2, G2, age: 62±12, 78% men) were included. A control group with 199 patients (Group 3, G3; age 58±9 years, 75% men) with similar characteristics to G2 (age, sex, CV risk factors) was selected. Ultrasound was used to determine the presence of atherosclerotic carotid plaque. We defined prevalence of plaque in relation to the history of dyslipidemia, treatment with statins and low density lipoproteins (LDL) target level.
Results: the prevalence of carotid plaque was: G1:87% (95% confidence interval (CI95%): 76-98%); G2:61% (CI95%:41–81%) and G3:37% (CI95%:30–44%) (p<0,05). Statins indication in G2 was limited to patients with dyslipidemia (65%). Twenty two % of patients in G2 with plaque were not receiving statins. Twenty six % of patients in G1 reached target LDL (LDL 70mg/dL); 40% in G2 reached LDL target level (LDL 100mg/dL). If LDL target level were 70 mg/dL in patients with heart failure and atherosclerosis, the objective was met in 25%.
Conclusion: the prevalence of atherosclerotic carotid plaque is high in patients with SHF regardless etiology and it is higher than subjects with similar CV risk factors without SHF. Target LDL levels for treatment are not reached in most patients with SHF.
Key words:
HEART FAILURE
HEART FAILURE, SYSTOLIC
PLAQUE, ATHEROSCLEROTIC
CAROTID ARTERY DISEASES
DYSLIPIDEMIAS
HYDROXYMETHYL-GLUTARYL-COA REDUCTASE INHIBITORS
Introducción
En pacientes con insuficiencia cardíaca (IC) sistólica (ICS), en particular aquellos con disfunción sistólica del ventrículo izquierdo, se producen alteraciones neuroendócrinas que a largo plazo resultan perjudiciales y explican en parte el carácter progresivo de la IC. Dentro de las alteraciones se ha evidenciado un aumento de especies reactivas del oxígeno y disminución del óxido nítrico, lo que lleva como consecuencia a un aumento del estrés oxidativo. El estrés oxidativo se ve en etapas tempranas de la aterosclerosis. Ambas patologías tienen, entonces, procesos fisiopatológicos en común(1-6).
Esta situación podría determinar que pacientes con ICS presentasen una mayor prevalencia de aterosclerosis que sujetos sin ICS. Si bien en teoría esto es claro para pacientes con ICS de etiología isquémica, donde la ateromatosis podría ser causa y a la vez producto de la ICS, no resulta tan claro para pacientes con ICS de etiología no isquémica. En nuestro conocimiento, no se ha reportado si la prevalencia de ateromatosis en pacientes con ICS de etiología no isquémica es mayor que la existente en la población general.
Los resultados del uso de estatinas en IC son controversiales y su indicación es discutida en las guías actuales, incluso en pacientes con ICS isquémica(7,8). Si la ausencia de administración resulta en el incumplimiento de objetivos terapéuticos, y en qué grado, resta por ser establecido.
En este contexto, el presente trabajo tiene como objetivo primario determinar si la prevalencia de ateromatosis carotídea en pacientes con ICS isquémica, ICS no isquémica y un grupo control sin ICS es diferente. Como objetivo secundario se plantea determinar el porcentaje de pacientes con ICS que logran los niveles de LDL objetivos.
Como hipótesis de trabajo planteamos que los pacientes con ICS de etiología isquémica tendrán un alto porcentaje de ateromatosis carotídea, que será mayor al del grupo de pacientes con ICS de etiología no isquémica. A su vez, el grupo de ICS no isquémica, basados en la etiopatotogenia de la alteración (por ejemplo, elevado estrés oxidativo) tendría mayor prevalencia de ateromatosis que el grupo control sin ICS.
Material y método
Población
Se incluyeron pacientes portadores de ICS pertenecientes a la cohorte de la Unidad Multidisciplinaria de Insuficiencia Cardíaca del Hospital de Clínicas (UMIC). Los criterios de inclusión para dicha cohorte fueron: tener una fracción de eyección del ventrículo izquierdo (FEVI) menor de 40% en el momento del ingreso y ser mayor de 18 años. Para nuestro trabajo se incluyeron aquellos pacientes con etiología definida como isquémica o no isquémica, separándolos en función de esta característica, como pertenecientes al grupo 1 (G1, n=39) o grupo 2 (G2, n=23). La ateromatosis clínicamente evidente (stroke, artropatía obstructiva de miembros inferiores, etcétera) fue criterio de exclusión del grupo G2. La mejora de la FEVI a más de 40% en la evolución no fue criterio de exclusión para nuestro trabajo.
Para definir la etiología de la disfunción sistólica como isquémica (Grupo 1) se utilizó la definición de cardiopatía isquémica utilizada por Felker y colaboradores(9). Se definió cardiopatía isquémica como: al menos dos vasos epicárdicos con estenosis mayor a 75%, o estenosis de la arteria descendente anterior proximal o de tronco coronario izquierdo mayor al 75%; o historia de infarto agudo de miocardio o revascularización previa. La estenosis mayor a 75% de un solo vaso epicárdico, cineangiocoronariografía sin estenosis mayor a 75%, ausencia de antecedentes de infarto agudo de miocardio o revascularización se consideró cardiopatía no isquémica.
Todo paciente con disfunción sistólica (G1 y G2) contó con un ecocardiograma transtorácico realizado en los últimos 12 meses. Este estudio se realizó a los efectos de contar con una FEVI actualizada, para poder evaluar si ambos grupos al momento del estudio presentaban similitud en esta variable. Para los ecocardiogramas transtorácicos se utilizó una sonda 3/4MHz, ecógrafo Siemens Cypress, Erlangen, Alemania. La FEVI se estimó por método de Simpson (ventana apical de cuatro cámaras y dos cámaras). Todos los ecocardiogramas fueron realizados por personal altamente entrenado del servicio de imagen cardiovascular del Centro Cardiovascular Universitario.
El grupo 3 (G3, n=199), o grupo control, surgió de seleccionar estudios incluidos en la base de datos del Centro Universitario de Investigación, Innovación y Diagnóstico Arterial (CUiiDARTE, Universidad de la República). Para conformar el G3 se seleccionaron estudios realizados en personas asintomáticas, sin enfermedad cardiovascular conocida y residentes en Uruguay. La selección aleatoria de los pacientes del G3 se realizó de manera de equiparar la prevalencia de personas de similar sexo y edad, y exposición a factores de riesgo cardiovascular tradicionales, que aquellos de los grupos con ICS.
En todos los casos se aceptó como válido un perfil lipídico con menos de seis meses de realizado, al igual que el resto de la paraclínica sanguínea registrada. Se definió dislipemia si contaba con el antecedente en la historia clínica o en el perfil lipídico actual el colesterol total era mayor a 240 mg/dL, el LDL colesterol mayor a 159 mg/dL o los triglicéridos mayores a 199 mg/dL.
Protocolo de estudio
Estudio analítico observacional de una serie de individuos de dos cohortes, en un corte transversal. El protocolo de estudio fue aprobado por el Comité de Ética de la Facultad de Medicina y del Hospital de Clínicas. Para su inclusión, todos los participantes consintieron participar del estudio, brindando para ello consentimiento informado por escrito.
Recolección de datos clínicos
La selección del G1 y del G2 fue por agenda de consulta en UMIC y posterior consentimiento de ingreso al estudio. Se realizó una entrevista clínica en donde se registraron: edad, sexo, presencia de factores de riesgo cardiovascular (FRCV); hipertensión arterial, diabetes, tabaquismo, dislipemia, alcoholismo, antecedentes patológicos a destacar y clase funcional de la IC, entre otros. Se realizaron medidas antropométricas (talla, peso y cálculo del índice de masa corporal [IMC]). De la revisión de la historia clínica y de la entrevista clínica se extrajo información del tratamiento recibido por el paciente. Se cuantificó la dosis de estatinas recibida, en miligramos, como el promedio de la dosis recibida en los últimos 12 meses.
Estudio vascular
Para realizar el estudio se solicitó que el paciente evitara en las cuatro horas previas al mismo la ingesta de cafeína u otros estimulantes del sistema nervioso, y el consumo de tabaco. El día del estudio arterial, y tras 10-15 minutos de reposo en ambiente tranquilo y con temperatura controlada en 21 a 23 ºC, se realizó medición de frecuencia cardíaca y presión arterial en ambos brazos mediante empleo de esfigmomanómetros aneroides (Omron HEM- 433INT Oscillometric System; Omron Healthcare Inc., Ill, USA). Estas mediciones fueron repetidas tres veces durante la realización del estudio carotídeo.
Utilizando ultrasonido en modo B y Doppler color (SonoSite, MicroMaxx, SonoSite Inc.,21919 30th Drive SE, Bothell,WA98021, USA; sonda:L38e), se estudió en ambos hemicuerpos la presencia de placas ateroscleróticas a nivel de carótida común, carótida interna y externa. Para este fin se visualizaron las arterias en el plano transversal y longitudinal. La presencia de placa se definió como la existencia en pared anterior y/o posterior de: (a) espesor íntima-media mayor a 1,5 mm, (b) presencia de un sector parietal con un nivel de espesor íntima-media mayor a 50% de la pared vecina, y/o (c) sitio con espesor parietal que invade focalmente la luz arterial al menos 0,5 mm.
Análisis de datos
Para la base de datos y el posterior análisis de los datos se utilizó el software SPSS Statistics 20® (IBM) y Microsoft Excel 2010® (Microsoft Office). Para comparar las variables continuas se utilizó el test de t de Student y Anova+Bonferroni, y para las variables discretas el test de chi cuadrado (X2). El nivel de significancia estadística alpha se estableció en 0,05 (p=0,05).
Resultados
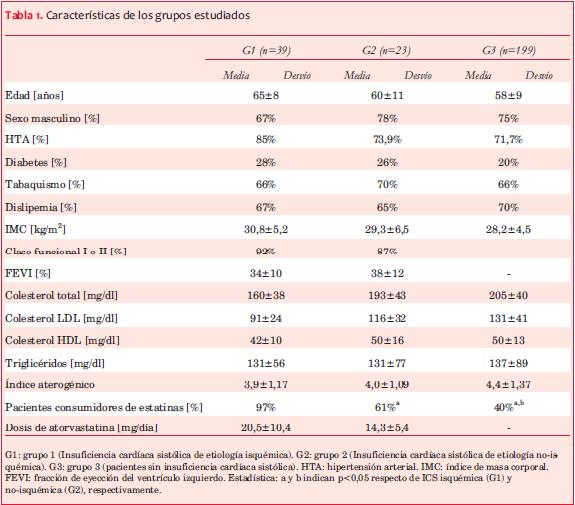
Las características de los grupos estudiados se muestran en la tabla 1. La información se presenta en porcentaje de la población en las variables discretas y como media (M) con ± desvíos estándar en las continuas. No hubo diferencias estadísticamente significativas en las características generales de los grupos analizados. El 92% del G1 y el 91% del G2 se encuentran en clase funcional I o II de la New York Heart Association (NYHA). El 98% de los pacientes con ICS reciben betabloqueantes (solo un paciente del G1 no recibe por intolerancia) y 100% IECA o ARAII. La FEVI media es de 34%±10% en G1 y 38%±12% en G2.
El 97% y 61% del G1 y del G2, respectivamente, reciben tratamiento con estatinas. Del grupo 3, 40% se medicaba con estatinas (p<0,05%).
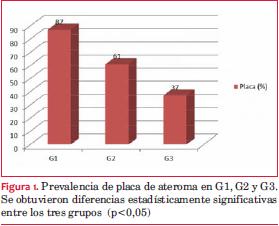
La prevalencia de placa de ateroma carotídea en G1 fue de 87% (intervalo de confianza del 95% [IC95%]:76%-98%), en G2 de 61% (IC95%:41%- 81%) y en G3 37% (IC95%:30%-44%) (p<0,05) (figura 1). Las diferencias estadísticamente significativas fueron encontradas para la comparación global (p=0,000) y las tres comparaciones realizadas entre grupos (G1 vs G2: p=0,000; G1 vs G3: p=0,018; G2 vs G3: p=0,024).
El 95% de la población dislipémica del G2 recibe tratamiento con estatinas (65% del G2). La indicación de estatinas en el G2 se limitó a pacientes con dislipemia. Un paciente dislipémico de este grupo no recibe estatinas por efectos adversos. En G1, 97,4% recibía estatinas (solo un paciente no la recibe).
Se detectaron placas de ateroma en pacientes del G2 que no recibían tratamiento con estatinas (no dislipémicos), representando 21,7% del G2.
La identificación o no de ateromatosis en relación con el diagnóstico previo de dislipemia en el G2 se muestra en la figura 2.
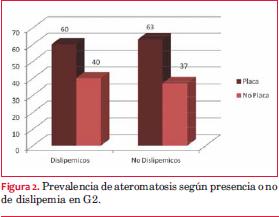
En cuanto al objetivo de LDL, 26% de los dislipémicos del G1 alcanza LDL objetivo (LDL < 70 mg/dL). En el G2 se logró LDL objetivo en 40% (LDL< 100 mg/dL). Si el LDL objetivo en pacientes con ateromatosis es <70 mg/dL, el objetivo se cumple en el 25%.
En el G1 la dosis media de atorvastatina fue de 20,5±10,4 mg y en el G2 de 14,3±5,4 mg.
Discusión
En nuestro conocimiento este es el primer trabajo en que se describe la prevalencia de ateromatosis en una población de pacientes con disfunción sistólica de etiología no isquémica y se la compara con la de una población de personas de similar riesgo aterosclerótico pero sin IC. Los principales hallazgos fueron:
1. Observamos una alta prevalencia de ateromatosis carotídea en pacientes con ICS de etiología isquémica (G1), siendo la misma mayor que la observada en pacientes con ICS de etiología no isquémica (G2).
2. La prevalencia de ateromatosis en pacientes con ICS de etiología no isquémica fue mayor que la población sin ICS, con similar exposición a factores de riesgo cardiovascular tradicionales.
3. El 63% de pacientes con IC de etiología no isquémica no dislipémicos (sin tratamiento con estatinas) presentan ateromatosis carotídea.
4. En pacientes con ICS (isquémica y no isquémica) los objetivos de LDL colesterol se cumplen en un porcentaje bajo (~25%).
Prevalencia de ateromatosis e insuficiencia cardíaca
Respecto de los primeros resultados, la alta prevalencia de ateromatosis en la población con IC podría explicarse, al menos en parte, por los mecanismos fisiopatológicos en común entre la IC y la aterosclerosis. Sabemos que en la IC existe un aumento de vasoconstrictores como noradrenalina, angiotensina II, endotelina, urotensina, troboxano A2 que provocan, entre otros efectos, un aumento de las especies reactivas del oxígeno (aumento de estrés oxidativo), aumento de mediadores inflamatorios como factor de necrosis tumoral alfa, interleucina 1 y 6 y disminución de interleuquinas antiinflamatorias y óxido nítrico (vasodilatador y antiinflamatorio)(1,3-6). El estado pro inflamatorio, la activación de metaloproteinasas y el estrés oxidativo se observan también en la aterosclerosis, por lo que ambas entidades comparten mecanismos comunes(1,3-6).
En nuestro trabajo hemos demostrado una mayor prevalencia de ateromatosis en la población con ICS, independiente de ser de origen isquémico (G1) o no isquémico (G2), en comparación con la población general con similar riesgo aterosclerótico (G3). Por lo tanto, el hecho de presentar IC incluso podría aumentar el riesgo de aterosclerosis.
Ateromatosis, dislipemia, estatinas e insuficiencia cardíaca
Según las pautas europeas(10), el objetivo de colesterol total y LDL colesterol en pacientes con riesgo bajo o moderado es menor a 190 mg/dL y 115 mg/dL, respectivamente. En pacientes de riesgo alto, el objetivo de LDL colesterol se ha establecido como menor a 100 mg/dL y en pacientes de riesgo muy alto (por ejemplo, aquellos con enfermedad aterosclerótica establecida) se ha determinado como menor a 70 mg/dL. Por otra parte, las pautas estadounidenses(11) establecen niveles de reducción de LDL colesterol. Al respecto, para pacientes de moderado riesgo el objetivo es una reducción de 30%-50% del LDL basal y en pacientes de alto riesgo una reducción mayor a 50%. Para dicho objetivo se plantea utilizar dosis moderadas de estatinas (20 a 40 mg de atorvastatina) en los pacientes de riesgo moderado y dosis altas (40-80 mg de atorvastatina) en los pacientes de alto riesgo.
En este contexto, nuestros resultados muestran que un 62,5% de los individuos no dislipémicos del G2 (21,7% del total de G2), presentaban ateromatosis, y no estaban recibiendo tratamiento con estatinas. Este subgrupo, no estaba recibiendo tratamiento a pesar de que claramente podría beneficiarse del tratamiento a dosis altas de estatinas según las pautas actuales. Por otra parte, 39% de G2 (que recibían estatinas por ser dislipémicos) se beneficiarían de aumentar la intensidad del tratamiento al detectarse enfermedad ateroesclerótica a nivel carotideo (objetivo de LDL se reduce de 100 mg/dL a 70 mg/dL). Asimismo, con el uso ecografía bidimensional reclasificamos a un 61% de la población de G2 en un escalón de mayor riesgo, y tal vez podrían beneficiarse de un cambio en la estrategia de tratamiento, en particular con estatinas.
A su vez destacamos que los pacientes del G1 reciben dosis por debajo de las recomendadas (20,5 mg de media). Este resultado puede estar reflejando la dificultad en nuestro medio de acceder a dosis altas de estatinas. Además, la falta de consenso sobre la utilidad de las mismas en pacientes con disfunción sistólica puede colaborar en la subutilización (al menos en dosis) de estos fármacos.
Como mencionamos previamente, las guías de práctica clínica actuales de prevención cardiovascular plantean objetivos de LDL colesterol para pacientes con alto riesgo cardiovascular <100 mg/dL o en pacientes con riesgo muy alto o con aterosclerosis demostrada, LDL colesterol <70 mg/dL o reducción mayor a 50%(12-14).
Dosis altas de estatinas tienen mayor efecto sobre los niveles de colesterol y efectos favorables a nivel de prevención secundaria, aunque podría observarse una mayor incidencia de efectos adversos no graves(15,16).
Además, el tratamiento intenso con estatinas ha demostrado en varios estudios (en aterosclerosis sintomática y asintomática) lograr disminuir la progresión, e incluso regresión, del espesor íntima-media a nivel carotídeo (un marcador de aterosclerosis). La estatina más estudiada es la pravastatina a dosis de 40 mg y atorvastatina 80 mg, entre otras(17-23). La combinación de betabloqueantes y estatinas demostró, además de disminuir la progresión del espesor íntima-media, cambiar la ecogenicidad de la placa haciéndola ecogénicamente más estable (menos vulnerable)(24,25).
En ambas poblaciones de pacientes con ICS (isquémica y no isquémica) encontramos que los objetivos de LDL colesterol se cumplen en un porcentaje muy bajo. Además la dosis media de estatinas utilizada es baja (media de 20,5 mg y 14,3 mg para G1 y G2, respectivamente). La utilización de dosis bajas de estatinas es crítica frecuente de los diversos estudios que intentan demostrar los beneficios del tratamiento con estatinas.
La evidencia de la eficacia del tratamiento con estatinas en IC es discutida, e incluso las guías actuales de IC concluyen que no hay evidencia suficiente para recomendar el tratamiento con estatinas. Se basan en los dos estudios con mayor número de casos (GISSI-HF y CORONA), los cuales incluyeron a más de 9.000 pacientes. El primero incluyó tanto a pacientes con IC de etiología isquémica como no isquémica. El segundo solo etiología isquémica. Ambos estudiaron el impacto del tratamiento con rosuvastatina 10 mg. Ninguno de los dos logró demostrar beneficio con dicho tratamiento (resultados neutros)(7,8).
Un metaanálisis publicado en 2011, que incluye los dos estudios anteriormente mencionados, no evidencia beneficios con el tratamiento con estatinas (por el gran n, los estudios GISSI-HF y CORONA tienen alto peso en la conclusión). Sin embargo, un subanálisis del mismo evidencia reducción de mortalidad e internación por IC en menores de 65 años(26). Contrariamente, un reciente metaanálisis evidencia beneficios con el tratamiento con estatinas tanto en mortalidad como en internaciones(27). En este contexto es claro que la evidencia actual es controversial, siendo no concluyente a la hora de establecer qué pacientes con ICS se benefician con el tratamiento con estatinas. Por este motivo, y a la luz de nuestros resultados, podría plantearse que tal vez la identificación de ateromatosis (o más ampliamente, enfermedad aterosclerótica) podría ser una herramienta útil para identificar a una población que se beneficie de dicho tratamiento.
La alta reproducibilidad, el bajo costo y el carácter no invasivo hacen de la ultrasonografía modo B una excelente técnica –a nuestro juicio– para identificar a pacientes con mayor riesgo que puedan beneficiarse de una estrategia terapéutica en particular.
Limitaciones
Es un trabajo unicéntrico, descriptivo, transversal, con un número de pacientes que podría considerarse pequeño y que no está diseñado para extraer conclusiones de causa - efecto, ni para definir la eficacia de un tratamiento. Dicha limitación podría subsanarse ampliando el estudio a otros centros (multicéntrico) para incrementar el número de pacientes y disminuir los riesgos de selección de los mismos.
El grupo sin insuficiencia cardíaca (G3) fue seleccionado para obtener un perfil de riesgo cardiovascular similar al grupo con ICS no isquémica (G2). Si bien ambos grupos no presentan diferencias estadísticamente significativas en su exposición a factores de riesgo, se aprecia una tendencia en el G3 a ser más jóvenes y tener menor prevalencia de sexo masculino, hipertensión arterial, diabetes e IMC, pero mayor prevalencia de dislipemia y cifras de colesterol. La elección de cualquier grupo control conlleva limitaciones, y en este caso estas pequeñas diferencias, si bien no significativas, podrían estar determinando pequeñas diferencias en los niveles de ateromatosis encontrados en ambos grupos.
En cuanto a las cifras de colesterol mayor en el G3 y un menor uso de estatinas en este grupo puede estar relacionado al menor control médico de dicha población.
El hecho de no haber realizado ecocardiograma transtorácico a la población control (G3), si bien podría considerarse una limitación, no lo consideramos así, ya que en la peor de las situaciones (pacientes con ICS en grupo control), los resultados tenderían a no ser estadísticamente diferentes entre G2 y G3, y no lo contrario (lo hallado).
Puede considerarse que los datos obtenidos en este estudio favorecen la hipótesis planteada y que por su implicancia terapéutica sería conveniente que fuera seguida por estudios con mayor potencia para marcar evidencias clínicas de importancia.
Conclusiones
La prevalencia de placas de ateroma en pacientes con IC de etiología isquémica es mayor que en los pacientes con IC de etiología no isquémica.
La prevalencia de aterosclerosis asintomática en pacientes con IC no isquémica es mayor que la de sujetos sin IC, con similares características de exposición a factores de riesgo.
En la mayoría de los pacientes con IC no se alcanzan niveles de LDL objetivo.
Bibliografía
1. Grieve DJ, Shah AM. Oxidative stress in heart failure. More than just damage. Eur Heart J 2003;24(24):2161-3.
2. Libby P, Aikawa M, Jain MK. Vascular endothelium and atherosclerosis. Handbook of experimental pharmacology. Berlin:Springer;2006:285-306.
3. Spinale FG. Matrix metalloproteinases: regulation and dysregulation in the failing heart. Circ Res 2002; 90:520-30.
4. Kameda K, Matsunaga T, Abe N, Hanada H, Ishizaka H, Ono H, et al. Correlation of oxidative stress with activity of matrix metalloproteinase in patients with coronary artery disease. Possible role for left ventricular remodelling. Eur Heart J 2003; 24:2180-5.
5. Byrne JA, Grieve DJ, Cave AC, Shah AM. Oxidative stress and heart failure. Arch Mal coeur vaiss 2003;96(3):214-21.
6. Chen K, Keaney JF. Evolving concepts of oxidative stress and reactive oxygen species in cardiovascular disease. Curr atheroscler rep 2012;14:476-83.
7. Tavazzi L, Maggioni AP, Marchioli R, Barlera S, Franzosi MG, Latini R, et al. Effect of rosuvastatin in patients with chronic heart failure (the gissi-hf trial): a randomised, double-blind, placebo-controlled trial. Lancet. 2008;372(9645):1231-1239.
8. Kjekshus J, Apetrei E, Barrios V, Bohm M, Cleland JG, Cornel JH, et al. Rosuvastatin in older patients with systolic heart failure. N Engl J Med 2007;357(22):2248-61.
9. Perk J, De Backer G, Gohlke H, Graham I, Reiner Z, Verschuren M, et al. European guidelines on cardiovascular disease prevention in clinical practice (version 2012). The fifth joint task force of the european society of cardiology and other societies on cardiovascular disease prevention in clinical practice (constituted by representatives of nine societies and by invited experts). Eur Heart J 2012;33(13): 1635-701.
10. Stone NJ, Robinson J, Lichtenstein AH, Merz CN, Blum CB, Eckel RH, et al. 2013 acc/aha guideline on the treatment of blood cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the american college of cardiology/american heart association task force on practice guidelines. Circulation 2013. Publicación electrónica 12 Nov 2013.
11. Baigent C, Blackwell L, Emberson J, Holland LE, Reith C, Bhala N, et al. Efficacy and safety of more intensive lowering of ldl cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010;376(9753):1670-81.
12. Brugts JJ, Yetgin T, Hoeks SE, Gotto AM, Shepherd J, Westendorp RG, et al. The benefits of statins in people without established cardiovascular disease but with cardiovascular risk factors: Meta-analysis of randomised controlled trials. BMJ 2009;338:b2376.doi: 10.1136/bmj.b2376.
13. Mills EJ, Rachlis B, Wu P, Devereaux PJ, Arora P, Perri D. Primary prevention of cardiovascular mortality and events with statin treatments: A network meta-analysis involving more than 65,000 patients. J Am Coll Cardiol 2008;52(22):1769-81.
14. Pedersen TR, Faergeman O, Kastelein JJ, Olsson AG, Tikkanen MJ, Holme I, et al. High-dose atorvastatin vs usual-dose simvastatin for secondary prevention after myocardial infarction: The ideal study: A randomized controlled trial. JAMA 2005;294(19):2437-45.
15. LaRosa JC, Grundy SM, Waters DD, Shear C, Barter P, Fruchart JC, et al. Intensive lipid lowering with atorvastatin in patients with stable coronary disease. N Engl Med 2005;352(14):1425-35.
16. Furberg CD, Adams HP, Applegate WB, Byington RP, Espeland MA, Hartwell T, et al. Effect of lovastatin on early carotid atherosclerosis and cardiovascular events. Asymptomatic carotid artery progression study (acaps) research group. Circulation 1994;90(4):1679-87.
17. Byington RP, Furberg CD, Crouse JR, Espeland MA, Bond MG. Pravastatin, lipids, and atherosclerosis in the carotid arteries (plac-ii). Am J Cardiol 1995;76(9):54C-59C.
18. Salonen R, Nyyssonen K, Porkkala E, Rummukainen J, Belder R, Park JS, et al. Kuopio atherosclerosis prevention study (kaps). A population-based primary preventive trial of the effect of ldl lowering on atherosclerotic progression in carotid and femoral arteries. Circulation 1995;92(7):1758-64.
19. Mercuri M, Bond MG, Sirtori CR, Veglia F, Crepaldi G, Feruglio FS, et al. Pravastatin reduces carotid intima-media thickness progression in an asymptomatic hypercholesterolemic mediterranean population: The carotid atherosclerosis italian ultrasound study. Am J Med 1996;101(6):627-34.
20. de Groot E, Jukema JW, van Boven AJ, Reiber JH, Zwinderman AH, et al. Effect of pravastatin on progression and regression of coronary atherosclerosis and vessel wall changes in carotid and femoral arteries: A report from the regression growth evaluation statin study. Am J Cardiol 1995;76(9): 40C-46C.
21. Taylor AJ, Kent SM, Flaherty PJ, Coyle LC, Markwood TT, Vernalis MN. Arbiter: Arterial biology for the investigation of the treatment effects of reducing cholesterol: A randomized trial comparing the effects of atorvastatin and pravastatin on carotid intima medial thickness. Circulation 2002; 106(16):2055-60.
22. Noyes AM, Thompson PD. A systematic review of the time course of atherosclerotic plaque regression. Atherosclerosis 2014;234(1):75-84.
23. Hedblad B, Wikstrand J, Janzon L, Wedel H, Berglund G. Low-dose metoprolol cr/xl and fluvastatin slow progression of carotid intima-media thickness: main results from the beta-blocker cholesterol-lowering asymptomatic plaque study (BCAPS).Circulation 2001;103(13):1721-6.
24. Ostling G, Goncalves I, Wikstrand J, Berglund G, Nilsson J, Hedblad B. Long-term treatment with low-dose metoprolol cr/xl is associated with increased plaque echogenicity: the beta-blocker cholesterol-lowering asymptomatic plaque study (BCAPS). Atherosclerosis 2011;215(2):440-5.
25. Zhang S, Zhang L, Sun A, Jiang H, Qian J, Ge J. Efficacy of statin therapy in chronic systolic cardiac insufficiency: a meta-analysis. Eur J Intern Med 2011;22( 5):478-4.
26. Wang JQ, Wu GR, Wang Z, Dai XP, Li XR. Long-term clinical outcomes of statin use for chronic heart failure: a meta-analysis of 15 prospective studies. Heart Lung Circ 2014;23(2):105-13.