Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Uruguaya de Cardiología
versión On-line ISSN 1688-0420
Rev.Urug.Cardiol. vol.29 no.2 Montevideo ago. 2014
Artículo original
calo, Gonzalo Varela y colaboradores
Terapia de resincronización cardíaca: experiencia a diez años y análisis de la evolución clínica de los pacientes en un centro de nuestro país
Dres. Agustina Bonino1, Yanina Zócalo2, Gonzalo Varela3, Fernando Calleriza4, LNC Graciela Do Mato5, Dr. Walter Reyes Caorsi6, FACC, FHRS.
1. Ex-Residente, Centro Cardiovascular Casa de Galicia.
2. Médica, Servicio de Electrofisiología, Centro Cardiovascular Casa de Galicia, Prof. Adj. Depto. Fisiología, UDELAR.
3. Médico Asistente, Servicio de Electrofisiología, Centro Cardiovascular Casa de Galicia; Ex-Asistente de Depto. de Cardiología, UDELAR.
4. Médico Asistente, Servicio de Electrofisiología, Centro Cardiovascular Casa de Galicia.
5. Licenciada Neumocardióloga, Servicio de Electrofisiología, Centro Cardiovascular Casa de Galicia; Directora, Escuela de Tecnología Médica, UDELAR.
6. Médico Jefe, Servicio de Electrofisiología, Centro Cardiovascular Casa de Galicia
Servicio de Electrofisiología. Centro Cardiovascular de Casa de Galicia.
Avda. Millán 4480. Montevideo, Uruguay.
Correo electrónico: seef@adinet.com.uy
Recibido marzo 6, 2014; aceptado julio 9, 2014
Resumen
Introducción: la terapia de resincronización cardíaca (TRC) mediante estimulación biventricular (BiV) es un tratamiento establecido que ha demostrado disminuir la mortalidad y mejorar la capacidad funcional y la calidad de vida en un subgrupo de pacientes con insuficiencia cardíaca avanzada. En nuestro país existen escasos reportes acerca del número de implantes, de la evolución clínica de los pacientes y de datos de seguimiento prolongado.
Material y método: cohorte prospectiva de 85 pacientes consecutivos con implante de TRC reclutada en el período junio de 2000 a mayo de 2011, que se cerró el 31 de julio de 2011. Edad media: 62 años, 65% hombres, 35% cardiopatía isquémica. Veintidós pacientes recibieron TRC con desfibrilador (TRC-D), 63 TRC solo marcapaso (TRC-P), 71 primo implante y 9 upgrade. Se valoró la evolución clínica de acuerdo a la modificación en la clase funcional (CF). La probabilidad acumulada de supervivencia se estimó a través de un modelo de Kaplan-Meier, utilizando el SPSS V20.0.
Resultado: de los 80 pacientes resincronizados, 2 (3%) que se encontraban en CFII evolucionaron a CFI. El 68% (54) del total de pacientes se encontraban en CFIII antes del implante: 30 pacientes (55,5%) pasaron a CFI y 7 pacientes (13%) a CFII. De los 24 (30%) que se encontraban en CFIV, 7 (29%) pasaron a CFII y 8 (33%) a CFI. Supervivencia de pacientes: luego de una mediana de seguimiento de 21 meses, la probabilidad acumulada de supervivencia a los dos años fue de 75,5% y a los cinco años de 67%. La media de supervivencia fue de 83,5 meses (IC95% 68,1-98,8).
Conclusión: la TRC en nuestro medio se asoció a mejora de CF y menor mortalidad que la esperada en la población estudiada. El tratamiento médico de la población referida para TRC es subóptimo. Las tasas de implante exitoso por vía venosa e incidencia de complicaciones son semejantes a los reportes internacionales.
Palabras clave:
TERAPIA DE RESINCRONIZACIÓN CARDÍACA
EVOLUCIÓN CLÍNICA
TASA DE SUPERVIVENCIA
Summary
Introduction: Cardiac resynchronization therapy (CRT) by biventricular pacing (BiV) is an established treatment that has been shown to reduce mortality and improve functional capacity and quality of life in a subgroup of patients with advanced heart failure. In Uruguay, reports about the number of implants, the clinical course of patients and follow-up data are scarce.
Methods: A prospective cohort of 85 consecutive patients with CRT implantation was enrolled between June/2000 and May/2011. The follow up period was closed on 31/07/2011. Clinical characteristics: average age 62 y.o., 65% were men, 35% had coronary artery disease. Twenty-two patients received a CRT with defibrillator (CRT-D) device and 63 patients a CRT pacemaker only (CRT-P) device; 71 patients received de novo CRT implantations and in 9 patients were upgrades. Clinical outcome according to the change in NYHA functional class (FC) was assessed. Survival curves were calculated by the Kaplan-Meier method (KM), using the SPSS V20.0.
Results: At the time of implant, 2 (3%) patients who were in FC II progressed to FCI. 68% (54) of the patients were in FC III before implantation: 30 patients (55.5%) improve to FC I and 7 patients (13 %) a FCII. Of the 24 patients (30%) who were in class IV, 7 patients (29%) improve to FCII and 8 patients (33%) to FCI. Survival of patients: After a median follow up of 21 months, the cumulative probability of survival at 2 years was 75.5% and at 5 years of 67%. The median survival was 83.5 months [CI95% 68.1 to 98.8]).
Conclusion: The CRT in our centre was associated with improvement in FC and lower mortality than expected in the population studied. Medical treatment of that population for CRT is suboptimal. The implant success rates and incidence of venous complications are similar to international reports.
Key words:
CARDIAC RESYNCHRONIZATION THERAPY
CLINICAL OUTCOME
SURVIVAL RATE
Introducción
La terapia de resincronización cardíaca (TRC) mediante estimulación biventricular (BiV) es un tratamiento establecido que ha demostrado disminuir la mortalidad y mejorar la capacidad funcional y la calidad de vida en un subgrupo de pacientes con insuficiencia cardíaca avanzada(1). Adicionalmente, en los últimos 20 años, varios estudios multicéntricos, controlados, prospectivos y con distribución aleatoria, han demostrado que el beneficio de la TRC no se limitaría a pacientes con insuficiencia cardíaca (IC) en estadios avanzados y han contribuido a establecer y ampliar las indicaciones de la TRC(2-12).
En Uruguay, la TRC se indica desde el año 2000; a pesar de ello contamos con escasos reportes acerca del número de implantes, de la evolución clínica de los pacientes y de datos de seguimiento prolongado.
En este contexto, el objetivo del presente trabajo fue: a) analizar las características y evolución clínica, y b) estimar la función de supervivencia de los pacientes sometidos a TRC en un centro de nuestro país, considerando los primeros diez años de experiencia.
Material y método
El presente es un estudio retrospectivo de una cohorte prospectiva y consecutiva.
En el período comprendido entre el 1º de junio de 2000 al 31 de mayo de 2011 fueron derivados al Servicio de Electrofisiología de Casa de Galicia (Montevideo, Uruguay) 85 pacientes para TRC con indicación clase I o IIa, nivel de evidencia A de acuerdo a las guías clínicas actuales(13-15).
El evento referente fue el implante del dispositivo de estimulación BiV cuya fecha abre el período de observación para cada paciente que finaliza con la fecha de muerte o de cierre del estudio, el 31 de julio de 2011. Se realizó la evaluación de todas las historias clínicas obteniéndose los datos patronímicos y demográficos, los antecedentes patológicos, la etiología de la IC, el estado funcional, la fracción de eyección del ventrículo izquierdo (FEVI) y el tratamiento recibido. Se evaluó la evolución clínica de los pacientes de acuerdo al cambio en la clase funcional (CF) según la clasificación de la New York Heart Association (NYHA) luego del implante del dispositivo y la supervivencia de pacientes fue definida como la diferencia entre la fecha del implante y la fecha de cierre del estudio o de muerte. Se confeccionó una base de datos utilizando el programa Excel donde se ingresó toda la información, tarea realizada por un mismo operador.
Características de la población
En la tabla 1 se muestra las características de los 85 pacientes referidos para TRC.
Implante
Del total de 85 pacientes derivados se logró la estimulación BiV en 80 (94%). En los cinco pacientes restantes no se logró el implante del electrodo del ventrículo izquierdo por vía endovascular y no se realizó el implante quirúrgico.
En la mayoría de los pacientes (74/85, 87%) fue posible el implante del electrodo del ventrículo izquierdo por vía transvenosa. En seis pacientes se debió realizar un segundo procedimiento, implante epicárdico a través de una minitoractomía izquierda.
En cuanto al dispositivo implantado, 22 pacientes (26%) recibieron TRC asociado a desfibrilador automático implantable (TRC-D) y 63 (74%) TRC exclusiva (TRC-P).
Once pacientes (13%) eran portadores de fibrilación auricular (FA), requiriendo seis de ellos ablación del nodo auriculoventricular.
El umbral de estimulación del ventrículo izquierdo al momento del implante tuvo una media de 1,2 V a 0,5 ms de ancho de pulso.
En cinco pacientes (6%) hubo complicaciones vinculadas al implante: dos disecciones del seno coronario al realizar venografía ocluyendo el seno coronario con catéter de Swan Ganz, sin otras consecuencias; un taponamiento cardíaco que se drenó, logrando completarse el implante en el mismo acto; dos pacientes presentaron edema pulmonar que requirió soporte ventilatorio, uno de ellos fallece posteriormente en terapia intensiva.
Seguimiento
En los 85 pacientes se realizaron controles clínicos y del dispositivo, el primero a los 15 días y luego cada cuatro meses. Se obtuvo un seguimiento completo de 82 pacientes, con tres perdidos de vista (PDV). Se calculó una mediana de seguimiento de 21 meses hasta el cierre del estudio, el 31 de julio de 2011.
Métodos estadísticos
Las variables continuas se presentan como media desviación típica (mínimo-máximo). Las variables categóricas se analizaron usando la frecuencia y el porcentaje. Utilizando SPSS V20.0 se estimó la función de supervivencia de toda la cohorte con un modelo de Kaplan-Meier.
Resultados
Evolución clínica
Clase funcional – resincronizados (tabla 2)
La mayoría de los 80 pacientes efectivamente resincronizados (54 pacientes, 68%) se encontraban en CF III, de los cuales 30 (55,5%) pasaron a CF I, siete (13%) a CF II y un paciente se mantuvo en CF III. Quince pacientes fallecen en el seguimiento y un paciente fue perdido de vista.
De los 24 pacientes que se encontraban en CF IV (30%), 8 evolucionaron a CF I y 7 a CF II. Dos pacientes no mejoraron persistiendo en CF IV, de los cuales uno fue trasplantado. Siete pacientes fallecen.
Dos pacientes (3%) se encontraban en CF II y pasaron a CF I con la TRC.
De estos 80 pacientes realmente resincronizados, 54 (68%) mejoraron con la TRC, evolucionando a CF I 40 de ellos (50%). Tres pacientes no respondieron clínicamente a la TRC (4%).
Clase funcional – no resincronizados
De los cinco pacientes que no se pudieron resincronizar, cuatro estaban en CF III y uno en CF II. Este último paciente se mantuvo en CF II en el seguimiento, dos pacientes fallecieron y dos fueron perdidos de vista.
Globalmente, considerando los 85 pacientes referidos para TRC, de los cuales el 96% estaban en CF III-IV, el 64% mejoró su clase funcional.
Mortalidad
Del total de 85 pacientes referidos para TRC, 24 (28%) fallecieron durante el seguimiento. La mayoría eran hombres (83%) y portadores de miocardiopatía no isquémica (62,5%); la FEVI media era de 20% (10%-26%) y tenían un diámetro diastólico final del ventrículo izquierdo medio de 72 mm (60-90 mm).
No hubo diferencia en la mortalidad entre los pacientes en CF III (28%) y CF IV (g9%).
Once de los individuos derivados para TRC (13%) eran portadores de una fibrilación auricular permanente. Mayoritariamente eran hombres (91%) con una edad media de 68 años (51-79) y portadores de cardiopatía no isquémica (55%). Este grupo reducido de pacientes tuvo una mortalidad del 55% (seis pacientes) en el seguimiento.
Otros 9 pacientes (11%) eran portadores de un dispositivo previo y fueron referidos para cambio de modo de estimulación a estimulación BiV. Cuatro pacientes tenían un marcapaso VVI y 5 pacientes un cardiodesfibrilador (prevención secundaria) con un bloqueo de rama izquierda funcional por estimulación permanente del ventrículo derecho. Cuatro de estos 9 pacientes (44%) fallecieron en el seguimiento.
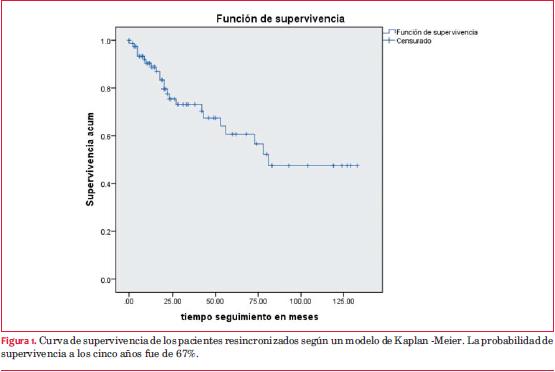
Supervivencia de los pacientes
La probabilidad acumulada de supervivencia de los pacientes a 2 años fue de 75,5%, siendo a los 5 años de 67% (figura 1). La media de supervivencia fue de 83.5 meses (IC95% 68,1-98,8).
Discusión
En la tabla 3 se muestra nuestra cohorte de individuos resincronizados con sus características demográficas, mediana de seguimiento y porcentaje de mortalidad en comparación con los estudios clínicos de referencia en el tema(7,8,10-12,16,17).
Comparando con la evidencia actual vemos que nuestra población presenta características distintas a la de dichos estudios. Por un lado es más joven (en promedio seis años menos) y presenta un menor porcentaje de etiología isquémica (35% versus > 50% en dichos estudios); ambos hechos podrían tener influencia en los resultados.
Por otro lado, al igual que el registro europeo, nuestra población contiene a un grupo de pacientes que habitualmente no han sido incluidos en los ensayos clínicos aleatorizados, como los portadores de FA (13%) y de dispositivos previamente implantados (11%)(12,16).
Se logró la estimulación BiV en 80 (94%) de los 85 pacientes derivados a TRC. En esos cinco pacientes en los que no se logró el implante del electrodo del ventrículo izquierdo por vía endovascular, tampoco se pudo coordinar por abordaje quirúrgico. Cuatro fueron mujeres y en cuatro de ellos la etiología de su cardiopatía fue no isquémica (dos pacientes con miocardiopatía idiopática, una paciente con miocardiopatía puerperal y otra con miocardiopatía valvular). Varios trabajos demuestran que alcanzar una localización óptima de la posición del electrodo ventricular izquierdo durante el implante puede ser una tarea difícil y esto puede ser debido a peculiaridades de la anatomía venosa coronaria, a la imposibilidad de avanzar el catéter guía en el seno coronario (SC), a la presencia de estimulación frénica y/o inestabilidad del electrodo en la posición seleccionada y, excepcionalmente, a la incapacidad de canular el ostium del seno coronario(19-22).
Tanto la tasa de implante exitoso por vía venosa (74/85 pacientes: 87%) como la incidencia de complicaciones (6%) se asemejan a las cifras internacionales(7,8,16).
Existen diferencias entre nuestro trabajo y los estudios internacionales respecto al dispositivo implantado. En comparación con los países europeos, por ejemplo, se destaca la diferencia en cuanto al número de implantes de TRC-D, 26% en nuestra población versus 73% en el registro Europeo(17). Del mismo modo, en comparación con los países europeos, en el registro GUERNICA se observó un porcentaje menor de pacientes ambulatorios con DAI (1,75% de la población vs 13,27%, OR 0,12 [IC95% 0,04-0,31]); que significa 86,8% menos que en Europa) y TRC-D: 0,88% vs 8,81%, (OR 0,09, [IC95% 0,02-0,37]). El porcentaje de resincronizadores sin capacidad para desfibrilación (TRC-P) fue más alto en la fase uruguaya en comparación con la europea (2,63% versus 1,02%, OR 2,61 [IC 95% 1,09- 6,30])(18).
Nuestros datos están en concordancia con los antecedentes aportados por el Fondo Nacional de Recursos (FNR), institución paraestatal que financia el implante de dispositivos intracardíacos en nuestro país. El FNR cuenta con una base de datos informatizada a partir del año 2003 en la que están ingresados los procedimientos de primoimplantes y segundos procedimientos de marcapasos y cardiodesfibriladores (DAI) cubiertos por dicha institución.
Desde esa fecha y hasta la fecha de cierre del presente trabajo se registraron 186 implantes de resincronizadores: 148 dispositivos de TRC-P (80%) y 38 TRC-D (20%) en un total de 15 centros registrados para realizar implantes de TRC-P y 10 centros para implante de TRC-D. De los 148 TRC-P, 131 fueron primoimplantes (89%) y 17 upgrade de marcapaso a TRC-P (11%). De los 38 pacientes con TRC-D, 31 fueron primoimplantes (82%) y 7 upgrade de cardiodesfibrilador a TRC-D (18%).
La concordancia de nuestros datos con los aportados por el FNR (SEEF: 74% TRC-P/26% TRC-D vs FNR: 80% TRC-P/20% TRC-D) probablemente esté vinculado al hecho de que este organismo financia el implante de DAI solamente en prevención secundaria, autorizando la TRC-D en prevención primaria solamente en casos especiales, requiriendo muchas veces la financiación del dispositivo por el propio paciente.
En cuanto a los upgrades, en nuestra población se registraron nueve (correspondiendo al 11%), mientras que en el registro europeo se reportó 29% de mejoría del sistema a TRC(23).
Analizando la evolución clínica de los 85 pacientes, previo al implante el 96% se encontraba en CFIII-IV, mejorando sus síntomas luego del implante el 64% de la población: CFII 14 pacientes (16%) y CFI 40 pacientes (48%).
El registro Europeo reportó una evolución de la CF similar a la nuestra. (17) Al momento del implante, el 78% de los pacientes se encontraban en CFIII-IV. Se registró un aumento del 50% en la proporción de pacientes en CFI-II durante el seguimiento(16,17).
La mortalidad en nuestra serie fue de 28%, distribuyéndose por igual entre aquellos que se encontraban en CFIII (28%) y IV (29%), resultados comparables al del grupo de pacientes resincronizados del estudio CARE-HF(8) (cuya población tiene características similares a la nuestra en cuanto a mediana de seguimiento, etiología y CF) con 24,7% de mortalidad. La tasa de mortalidad al año fue de 4,09% y a los dos años de 3,4% mientras que en el CARE-HF(8) fue de 9,7% y 18,0%, respectivamente. Quizá estas diferencias estén vinculadas a los factores mencionados previamente.
Limitaciones
La principal limitación del trabajo es inherente a su diseño observacional y no aleatorizado, realizado en un único centro y con un número de pacientes limitado. Los pacientes son referidos para TRC, pero el manejo médico y farmacológico de los mismos no depende del centro y no se realiza en unidades especializadas de IC.
Conclusiones
En diez años de experiencia en pacientes con implante de TRC se demuestra una mejora de la CF y menor mortalidad que la esperada en la población estudiada. El tratamiento médico de la población referida para TRC es subóptimo. Las tasas de implante exitoso por vía venosa e incidencia de complicaciones son semejantes a los reportes internacionales. Los datos presentados resultan importantes considerando los escasos reportes acerca de la TRC en nuestro país.
A la Dra. Irene Lombide, de la Dirección Técnica del FNR, que muy amablemente contestó todas nuestras interrogantes y nos aportó los datos de esa institución.
Bibliografía
1. Díaz-Infante E, Hernández-Madrid A, Brugada-Terradellas J, Fernández-Lozano I, García-Bolao I, Leal del Ojo J, et.al. Consenso sobre la terapia de Resincronización Cardíaca Rev Esp Cardiol Supl. 2005;5 SuplB:B3-11.
2. Acena M, Regoli F, Auricchio A. Terapia de resincronizacion cardiaca. Indicaciones y contraindicaciones. Rev Esp Cardiol 2012;65(9):843-9.
3. Abraham WT, Fisher WG, Smith AL, Delurgio DB, Leon AR, Loh E; MIRACLE Study Group, Multicenter InSync Randomized Clinical Evaluation, et al. Cardiac resynchronization in chronic heart failure. N Engl J Med 2002; 346: 1845-53.
4. Auricchio A, Stellbrink C, Sack S, Block M, Vogt J, Bakker P, et al. The Pacing Therapies for Congestive Heart Failure (PATH-CHF) study: rationale, design, and endpoints of a prospective randomized multicenter study. Am J Cardiol 1999;83(5B): 130D-135D.
5. Cazeau S, Leclercq C, Lavergne T, Walker S, Varma C, Lind C, et al. Effects of multisite biventricular pacing in patients with heart failure and intraventricular conduction delay. N Engl J Med 2001; 344(12): 873-80.
6. Linde C, Leclercq C, Rex S, Garige S, Lavergne T, Cazeau S, et al. Long term benefits of biventricular pacing in congestive heart failure: Results from the Multisite Stimulation in Cardiomyopathy (MUSTIC) Study. J Am Coll Cardiol 2002; 40(1): 111-8.
7. Bristow MR, Saxon LA, Boehmer J, Krueger S, Kass DA, De Marco T, et al. Cardiac resynchronization therapy with of without an implantable defibrillator in advanced chronic heart failure. N Engl J Med 2004; 350(21):2140-50. .
8. Cleland JGF, Daubert JC, Erdmann E, Freemantle N, Gras D, Kappenberger L; The Cardiac Resynchronization Heart Failure (CAREHF) Study Investigators, et al. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med 2005; 352(15): 1539-49.
9. Young JB, Abraham WT, Smith AL, Leon AR, Lieberman R, Wilkoff B; Multicenter Insync ICD Randomized Clinical Evaluation (MIRACLE-ICD) Trial Investigators; et al. Combined Cardiac Resynchonization and Cardioversion Defibrillation in Advanced Chronic Heart Failure. The MIRACLE-ICD Trial. JAMA 2003; 289(20): 2685-94.
10. Linde C, Abraham W, Gold M, St John Sutton M, Ghio S, Daubert C. Randomized trial of cardiac resynchronization in mildly symptomatic heart failure patients and in asymptomatic patients with left ventricular dysfunction and previous heart failure symptoms. J Am Coll Cardiol 2008; 52(23): 1834-43.
11. Moss A, Hall W, Cannom D, Moss AJ, Hall WJ, Cannom DS, et al. Cardiac resynchronization therapy for the prevention of heart-failure events. N Engl J Med 2009; 361(14): 1329-38.
12. Tang AS, Wells GA, Talajic M, Arnold MO, Sheldon R, Connolly S, et al. Cardiac-resynchronization therapy for mild-to-moderate heart failure. N Engl J Med 2010; 363:2385-95.
13. Dickstein K, Vardas PE, Auricchio A, Daubert JC, Linde C, McMurray J, et al. Actualización detallada 2010 de la guía de práctica clínica de la ESC sobre la terapia con dispositivos para la insuficiencia cardiaca. Rev Esp Cardiol 2010; 63(12):e1-e13.
14. Bonow RO, Ganiats TG, Beam CT, Blake K, Casey DE, Goodlin SJ, et al. ACCF/AHA/AMA-PCPI 2011 Performance Measures for Adults With Heart Failure. A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Performance Measures and the American Medical Association-Physician Consortium for Performance Improvement. Circulation 2012;125(19): 2382-401.
15. McMurray JJ, Adamopoulos S, Anker SD, Auricchio A, Böhm M, Dickstein K, et al.ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC. Eur Heart J 2012;33(14):1787-847. Fe de erratas en:Eur Heart J 2013 Jan;34(2):158.
16. Dickstein K, Bogale N, Priori S, Auricchio A, Cleland J, Gitt A, et al. The European cardiac resynchronization therapy survey. Eur Heart J 2009; 30(20):2450-60.
17. Bogale N, Priori S, Cleland J, Brugada J, LindeC, Auricchio A, et al. The European CRT Survey: 1 year (9-15months) follow-up results. Eur J Heart Fail 2012;14(1):61-73.
18. Layerle B, Chafes D, Estragó V, Alvarez P, Pereda M, Spera E, et al. Heart Failure Pilot Survey by the Uruguayan-European Survey Group (GUERNICA) Rev Urug Cardiol 2012; 27(3): 286-303.
19. Auricchio A, Klein H, Tockman B, Sack S, Stellbrink C, Neuzner J, et al. Transvenous biventricular pacing for heart failure: can the obstacles be overcome? Am J Cardiol 1999;83(5 Suppl2):S136-42.
20. Worley SJ, Leon A, Wilkoff B. Anatomy and Implantation Techniques for Biventricular Devices. En: Ellenbogen KA, Kay GN, Wilkoff B, editors. Device Therapy for Congestive Heart Failure. Philadelphia, Pensylvannia: Elsevier; 2004:118-231.
21. Arbelo Lainez E, Medina Fernández-Aceytuno A, García Quintana A, Caballero Dorta E, Melián Nuez F, Delgado A, et al. Prevalencia de válvulas de Vieussens y válvulas venosas restrictivas en la desembocadura de la vena coronaria diana: observaciones anatómicas y angiográficas. Rev Esp Cardiol 2005; 58 Supl 1:S11.
22. Arbelo Lainez E, Medina Fernández-Aceytuno A, Bolaños J, García Quintana A, Caballero Dorta E, Suárez de Lezo Herreros de Tejada J, et al. La válvula de Tebesio como determinante de la dificultad de acceso al seno coronario: observaciones anatómicas y angiográficas. Rev Esp Cardiol 2004; 57 Supl 2:145.
23. Nigussie Bogale, Witte K, Priori S, Cleland J, Auricchio A, Gadler F, et al. The European Cardiac Resynchronization Therapy Survey: comparison of outcomes between de novo cardiac resynchronization therapy implantations and upgrades. Eur J Heart Fail 2011;13(9):974-83.