Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Uruguaya de Cardiología
versión On-line ISSN 1688-0420
Rev.Urug.Cardiol. vol.28 no.3 Montevideo dic. 2013
Artículo de revisión
Tercera definición universal de infarto de miocardio.
Implicancias en la práctica clínica
Dr. Óscar Bazzino
“El progreso de la medicina nos depara el fin de aquella época liberal en la que el hombre aún podía morirse de lo que quería”.
Stanislaw Jerzy Lec
INFARTO DEL MIOCARDIO
BIOMARCADORES FARMACOLóGICOS
Key words:
MIOCARDIAL INFARCTION
BIOMARKERS, PHARMACOLOGICAL
Introducción
El desarrollo de biomarcadores con mayor sensibilidad y especificidad, así como de nuevas técnicas de imagen, permiten la detección de áreas pequeñas de injuria y/o necrosis miocárdica. Al mismo tiempo, hemos sido testigos del progreso en el manejo de los pacientes que padecen un infarto agudo de miocardio (IAM), con la consiguiente reducción en la morbimortalidad. La complejidad en la atención de la principal causa de muerte en el mundo occidental obliga a distinguir entre las múltiples condiciones que pueden provocar un IAM, sea espontáneo o relacionado a procedimientos terapéuticos. Todo ello ha generado la necesidad de homogeneizar la terminología en torno a esta patología a través de un consenso internacional que culmina en la tercera definición universal de infarto de miocardio (IM).
Breve reseña histórica
A comienzos del año 2013, un hombre de mediana edad, con factores de riesgo cardiovascular, consulta por ángor prolongado, con electrocardiograma (ECG) y curva de CK MB normales, y con una elevación de troponina por encima del percentil 99 respecto al valor de referencia. El equipo actuante realizó diagnóstico de IAM tipo I, iniciando el tratamiento específico de prevención secundaria. A partir de ese momento, el individuo en cuestión pasó a engrosar las estadísticas sobre la prevalencia de IM en la población a la cual pertenece.
¿Cuál hubiese sido la historia si este mismo escenario ocurría antes de finalizar el siglo pasado? El resumen de egreso se habría cerrado con el diagnóstico de angina inestable, y entre los antecedentes patológicos del paciente no figuraría el de IM.
La diferencia entre estos dos enfoques históricos no es meramente semántica. Cuando en el año 2000 se presentó el documento que redefinía el IM (1), se preveía, bajo este nuevo abordaje, un incremento del orden de 30% en la incidencia de IAM, así como un descenso en la mortalidad por este concepto (2). Por esos días, se analizaron las implicancias de este cambio de paradigma desde el punto de vista patológico, electrocardiográfico, bioquímico, de los ensayos clínicos, epidemiológico, de los exámenes imagenológicos y de las políticas públicas. Se llegó al acuerdo general de que el término IM no debía utilizarse sin algunos atributos, tales como el monto de la pérdida de miocitos (tamaño del infarto), las circunstancias en las que se presenta (espontáneo o en el contexto de una intervención coronaria) y el tiempo de evolución de la necrosis en relación con el momento de la observación.
En 2007 se presenta la definición universal de IM (3), que destaca dos aspectos fundamentales: por un lado pone énfasis en la importancia de la troponina en el diagnóstico, y, por otro, define cinco tipos de infarto, a saber: 1) IAM espontáneo relacionado a un evento coronario primario (complicación de placa aterosclerótica); 2) IAM secundario a un aumento de la demanda de oxígeno por el miocardio, o a un déficit de oferta, no relacionados a un accidente de placa; 3) muerte súbita vinculada a isquemia miocárdica (síntomas, alteraciones electrocardiográficas o demostración de trombo intracoronario); 4) IAM en el contexto de una intervención coronaria percutánea, y 5) IAM en el escenario de una cirugía de revascularización miocárdica.
Desde el punto de vista patológico, el IM se define como la necrosis de miocitos secundaria a isquemia prolongada. Durante esta situación se detecta un aumento y/o descenso de biomarcadores cardíacos, preferentemente troponinas, con al menos un valor que supera el percentil 99 del límite mayor de referencia, junto a la evidencia de isquemia miocárdica, reconocida a través de alguna de las siguientes condiciones: síntomas de isquemia, alteraciones electrocardiográficas compatibles con isquemia, desarrollo de ondas Q patológicas, evidencias imagenológicas de pérdida reciente de miocardio viable, o la presencia de nuevas alteraciones regionales de la contractilidad parietal. En resumen, la definición universal con cinco tipos de infarto se basa en la elevación de troponinas asociada a síntomas isquémicos, alteraciones electrocardiográficas típicas, o evidencia de pérdida de miocardio viable(3, 4).
En 2012, Moscoso y colaboradores (5) publicaron un elegante trabajo que examinó el impacto en la mortalidad a diez años del IM diagnosticado en base a troponina cardíaca específica, de acuerdo a la definición universalmente aceptada en el año 2007. Para ello, compararon la mortalidad en 676 pacientes ingresados con diagnóstico de síndrome coronario agudo en relación con la presencia o ausencia de IM según tres definiciones: 1) síntomas típicos y elevación persistente del segmento ST o bloqueo de rama izquierda (diagnóstico por ST); 2) síntomas típicos más elevación y/o descenso de CK MB (definición antigua), y 3) síntomas típicos más ascenso y/o descenso de troponina I por encima del percentil 99 (definición universal). La mortalidad total a diez años fue de 23,8%. La proporción de pacientes con IAM fue de 33,6% para el grupo definido por ST; 55,8% para el grupo de acuerdo a la definición antigua, y 70,1% para el grupo de definición universal. La razón de riesgo ajustada (HR) de muerte a diez años entre presencia y ausencia de IAM fue 0,71 (intervalo de confianza [IC] 95%: 0,46-1,08; p=0,11) para el grupo definido por ST; 0,84 (IC 95% 0,55-1,27; p=0,40) para la definición antigua, y 1,58 (IC 95% 1,07-2,40; p=0,03) para la definición universal. Los autores concluyeron, en primer lugar, que la definición universal, con su enfoque bioquímico, identifica un mayor número de infartos, y en segundo término, que este grupo tiene un perfil de riesgo mayor que es un predictor independiente de muerte a diez años.
La necesidad de actualizar la definición universal de IM publicada en el año 2007 surgió como consecuencia de la evolución de las herramientas diagnósticas y el mejor entendimiento del valor y las limitaciones de la definición previa. Es así que en el año 2012 se llega a la tercera definición universal de IM (6).
Tercera definición universal de infarto de miocardio
Los aspectos centrales de esta tercera versión 2012 de la definición de IM son los síntomas clínicos, los biomarcadores cardíacos y las alteraciones electrocardiográficas compatibles con isquemia miocárdica. Es así que la tercera definición universal pone énfasis en la importancia de una historia clínica de síntomas isquémicos de por lo menos 20 minutos de duración, no necesariamente constituidos por dolor torácico típico. También analiza los escenarios clínicos en los que ocurre el IM (por ejemplo, pacientes críticos). En este consenso, los biomarcadores siguen teniendo un protagonismo central en el diagnóstico y las pruebas con imágenes han sido mejor ponderadas (7).
La tabla 1 sintetiza los criterios para el diagnóstico de IAM e IM previo.
Evaluación clínica de isquemia miocárdica e infarto
La isquemia miocárdica resultante de la alteración del equilibrio entre oferta y demanda del aporte de oxígeno al miocardio es el paso inicial en el desarrollo de un IAM. Esta isquemia miocárdica se reconoce a través de una minuciosa historia clínica y mediante la realización de ECG seriados. El principal síntoma consiste en dolor torácico de los miembros superiores, a nivel mandibular o epigástrico; en reposo o desencadenado por un esfuerzo físico. Existen otros síntomas equivalentes isquémicos como disnea y fatiga. El dolor torácico provocado por un IAM es típicamente prolongado (superior a 20 minutos) y suele estar acompañado de diaforesis, náuseas o síncope. No obstante, estos síntomas no son específicos de isquemia miocárdica y pueden confundir a quienes los interpretan, conduciendo a errores diagnósticos y terapéuticos. A su vez, existe una gran variedad de presentaciones clínicas atípicas, en particular en mujeres, ancianos, diabéticos durante el posoperatorio y en las unidades de medicina crítica. Hay que tener especial cuidado al interpretar una alteración en los valores de biomarcadores cardíacos en estos escenarios.
El electrocardiograma en el infarto de miocardio
El ECG debe ser realizado e interpretado en los 10 primeros minutos luego del contacto médico con un paciente que padece un posible síndrome coronario agudo (8, 9). El carácter dinámico de las alteraciones electrocardiográficas exige la realización de múltiples trazados en forma seriada (cada 15-20 minutos), particularmente cuando el primero no es diagnóstico, cuando existen síntomas recurrentes luego de un período asintomático, o antes del alta de pacientes que presentaron cambios evolutivos, como referencia basal para comparaciones futuras. Las alteraciones agudas o evolutivas del ST-T y de ondas Q permiten conocer el tiempo de evolución del evento, identificar la arteria culpable, estimar el monto de miocardio en riesgo, definir una estrategia terapéutica y establecer el pronóstico(6). Las manifestaciones electrocardiográficas de isquemia miocárdica están condicionadas por diferentes variables: la distribución de la arteria culpable, la existencia de vasos colaterales, la localización, extensión y severidad de la obstrucción coronaria, y la existencia de infarto previo (10). El ECG suele ser insuficiente para el diagnóstico de isquemia miocárdica o infarto en virtud de que las alteraciones del ST pueden observarse en otras patologías, como pericarditis, hipertrofia ventricular izquierda, bloqueo de rama izquierda, síndrome de Brugada, miocardiopatía por estrés y repolarización precoz (11). Una elevación nueva y prolongada (20 minutos) del ST, asociada a un descenso recíproco, refleja una oclusión coronaria aguda que desencadena una injuria miocárdica con necrosis. Las ondas Q pueden aparecer vinculadas a fibrosis miocárdica en miocardiopatías sin enfermedad coronaria. A su vez, pueden observarse ondas Q transitorias durante episodios de isquemia aguda o en pacientes con un IAM con reperfusión exitosa.
En la tabla 2 se establecen las manifestaciones electrocardiográficas de isquemia miocárdica aguda en ausencia de hipertrofia ventricular izquierda y de bloqueo de rama izquierda.
La tabla 3 refiere los cambios electrocardiográficos asociados a IM previo.
Detección de injuria miocárdica mediante biomarcadores cardíacos
La injuria miocárdica se detecta mediante la elevación de los niveles de un biomarcador sensible y específico, como las troponinas o la fracción MB de la creatinfosfoquinasa (CK). Las troponinas T e I son componentes del aparato contráctil de los miocitos y tienen expresión exclusiva a nivel del corazón. A pesar de que la elevación de estos biomarcadores refleja una injuria que conduce a necrosis miocárdica, no revela el mecanismo subyacente (12). Se han propuesto varias explicaciones para la liberación de estas proteínas estructurales desde los miocitos: recambio normal de los miocitos, apoptosis, liberación celular de los productos de degradación de troponina, aumento de la permeabilidad de la pared celular, formación y liberación de vesículas membranosas y necrosis de los miocitos (13). Nos referiremos a IM solo ante la existencia de necrosis miocárdica secundaria a isquemia. En contraposición a esto, pueden detectarse pequeñas áreas de necrosis en condiciones clínicas no asociadas a injuria isquémica, como en la insuficiencia cardíaca, insuficiencia renal, miocarditis, arritmias, embolia pulmonar, o procedimientos cardíacos percutáneos o quirúrgicos libres de eventos. Estas circunstancias no deben ser catalogadas como IM ni como complicaciones de los procedimientos terapéuticos involucrados. En estas circunstancias es importante distinguir entre las causas agudas de elevación de troponinas, que se caracterizan por un ascenso y/o descenso de sus valores, de las alteraciones crónicas que no tienden a sufrir cambios agudos.
La tabla 4 ilustra las condiciones clínicas que pueden cursar con elevación de troponinas.
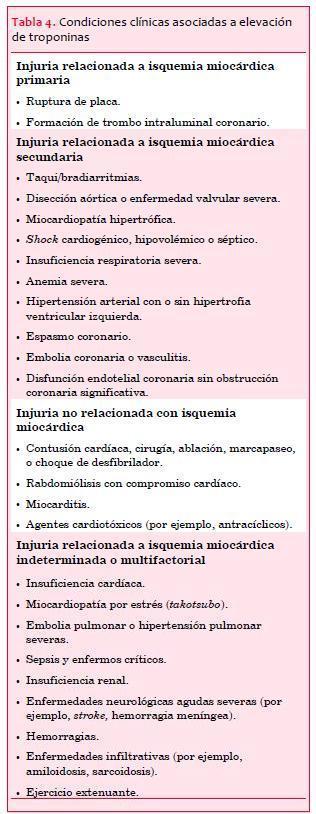
Los biomarcadores preferidos son las troponinas (T o I) debido a su alta especificidad por el tejido miocárdico, así como por su alta sensibilidad clínica. La detección de un ascenso y/o descenso de sus niveles séricos resulta imprescindible para el diagnóstico de IAM (14).
Las muestras de sangre para la medición de troponina deben tomarse al tiempo de la primera evaluación y repetirse a las 3-6 horas. Se requieren muestras adicionales si ocurren nuevos episodios isquémicos, o en casos en que el síntoma inicial sea de evolución incierta (15). Si bien se sugiere identificar un ascenso y/o descenso de los valores de troponinas para el diagnóstico de infarto agudo, esta condición no es absolutamente necesaria para el caso de pacientes con una probabilidad pretest muy elevada de IAM que se presentan en forma tardía luego del inicio de los síntomas (durante la meseta de la curva o en la fase de descenso lento), tiempo en el que resulta difícil identificar variaciones. Debemos de tener presente que estos valores pueden persistir elevados durante dos o más semanas luego de iniciado el proceso de necrosis (16).
La troponina de alta sensibilidad tiene un valor predictivo negativo de 95% en una sola prueba realizada al ingreso en individuos que consultan por dolor torácico, y casi 100% en una repetición de la muestra después de tres horas(9).
Si no se dispone de troponina, la mejor alternativa es la CK MB medida a través de un test de masa. Al igual que la troponina, se define un valor anormal como aquel que supera el percentil 99 de un rango normal de referencia (17).
Clasificación clínica del infarto agudo de miocardio
En la práctica clínica habitual, y en favor de una correcta toma de decisiones terapéuticas, en particular de la reperfusión, designamos como IAM con elevación del ST a aquellos que se presentan con dolor torácico prolongado, u otro síntoma isquémico, acompañado de una elevación del ST en, por lo menos, dos derivaciones contiguas. Por el contrario, a los casos que se presentan sin elevación del segmento ST los definimos como IAM sin elevación del ST. Muchos pacientes que padecen un IM desarrollan ondas Q (infartos Q); en contraste, otros no las desarrollan (infartos no Q). En aquellos individuos que cursan un síndrome coronario agudo sin alteración de los niveles plasmáticos de biomarcadores realizamos diagnóstico de angina inestable.
Más allá de estas apreciaciones de índole práctica, la definición universal propone una clasificación en cinco tipos de infarto, basada en diferencias patológicas, clínicas y pronósticas, en el contexto de diferentes estrategias terapéuticas. La tabla 5 resume estas cinco variantes.
Rol de las técnicas de imagen en el diagnóstico y caracterización del infarto de miocardio
La hipoperfusión e isquemia miocárdicas conducen a una cascada de eventos fisiopatológicos que incluyen: disfunción miocárdica, muerte celular y cicatrización mediante fibrosis. Los estudios de imagen aportan información acerca de la perfusión, viabilidad, espesor miocárdico, engrosamiento y motilidad, así como de la presencia y distribución de fibrosis evaluadas por resonancia nuclear magnética (RNM) o agentes de contraste radioopacos.
Las técnicas de imagen no invasivas utilizadas para la evaluación del IM agudo o crónico son la ecocardiografía, la ventriculografía radioisotópica, la centellografía de perfusión miocárdica y la RNM. La tomografía por emisión de positrones (en inglés, PET) y la tomografía computada son menos utilizadas en estos escenarios (18).
Todas ellas superponen su capacidad para evaluar perfusión, función y viabilidad miocárdicas. La única técnica que provee información directa acerca de la viabilidad miocárdica es aquella que utiliza radionúclidos como consecuencia de las propiedades inherentes de estos radiotrazadores. Otras brindan datos indirectos, como la respuesta contráctil a la dobutamina evaluada por ecocardiografía, o la distribución de fibrosis miocárdica mediante RNM.
En el contexto de IAM, las técnicas de imagen resultan útiles para su diagnóstico en función de su capacidad para detectar anormalidades en la motilidad parietal o la pérdida de miocardio viable en presencia de valores elevados de biomarcadores cardíacos. Si por alguna razón no se han realizado mediciones de biomarcadores, la demostración de una pérdida nueva de miocardio viable, en ausencia de causas no isquémicas, alcanza para realizar diagnóstico de IAM. La función contráctil y viabilidad conservadas presentan un valor predictivo negativo muy elevado, y prácticamente excluyen el diagnóstico de IAM (19). No obstante, la obtención de mediciones normales de biomarcadores durante la ventana de tiempo adecuada excluye el diagnóstico de IAM y se antepone al criterio por imagen(6). Si bien estas técnicas poseen un elevadísimo valor predictivo negativo, no sucede lo mismo con su valor predictivo positivo debido a las múltiples condiciones que afectan la contractilidad parietal, a saber: IM previo, isquemia aguda, atontamiento, hibernación, y afecciones no isquémicas como miocardiopatías o enfermedades inflamatorias e infiltrativas.
La ecocardiografía brinda información sobre muchas de las causas no isquémicas de dolor torácico, tales como miopericarditis, valvulopatías, miocardiopatías, embolia pulmonar o disección aórtica (20). Asimismo, es la técnica de elección para la detección de complicaciones del IAM, incluyendo rotura de pared libre, comunicación interventricular, insuficiencia mitral secundaria a isquemia o rotura del músculo papilar.
Las imágenes con radionúclidos pueden utilizarse para cuantificar el monto de miocardio salvado luego de una revascularización aguda (21).
La evidencia en favor del diagnóstico de IM que se presenta en forma tardía se obtiene comprobando una anormalidad regional de la motilidad parietal, afinamiento o escara, en ausencia de causas no isquémicas. La especificidad y resolución elevadas de la RNM, con realce tardío de gadolinio, determinan que esta técnica sea la preferida para la detección, localización y distribución de la fibrosis miocárdica, diferenciando los patrones de etiologías diversas.
Por último, las técnicas de imagen contribuyen, más allá del diagnóstico, a evaluar el pronóstico de individuos que padecen un IM mediante la detección de isquemia residual, viabilidad y/o disfunción sistólica.
Infarto de miocardio ante intervenciones quirúrgicas no cardíacas y en el escenario de las unidades de medicina crítica
Si bien los pacientes que presentan un IM perioperatorio no suelen sufrir síntomas isquémicos, esta condición está asociada a un incremento de la mortalidad a los 30 días (22). Por esta razón, se recomienda un control sistemático de los biomarcadores cardíacos en pacientes de alto riesgo, tanto antes como 48-72 horas después de la cirugía mayor. Existe amplia evidencia en favor de que la mayoría de los infartos diagnosticados en este contexto se deben a un desequilibrio prolongado entre el suministro y la demanda de oxígeno por el miocardio (IM tipo 2) (23,24). No obstante, también existe información que demuestra la rotura de placa y agregación plaquetaria, con la consiguiente formación de trombo, en aproximadamente la mitad de los pacientes con IM perioperatorio fatal (IM tipo 1) (25). Las diferencias en el abordaje terapéutico de ambas situaciones exige un análisis exhaustivo, caso a caso, guiado por el juicio clínico.
La elevación de troponinas es un hallazgo frecuente en los pacientes que ingresan en unidades de cuidados intensivos y se asocian a un pronóstico adverso, independientemente del estado de la enfermedad subyacente (26,27). Durante la atención del paciente crítico con enfermedad grave de uno o varios órganos, resulta un verdadero desafío la elección de un plan de acción frente a valores de troponina elevados. Luego de que el paciente se recupere de la enfermedad crítica, se recomienda definir la estrategia para evaluar la enfermedad coronaria subyacente en base al criterio clínico (28). Una vez más, estos pacientes pueden presentar IM tipo 2 en el contexto de mayor demanda de oxígeno y enfermedad coronaria subyacente, IM tipo 1 por accidente de placa, o lesión miocárdica con necrosis inducida por catecolamina y/o efecto tóxico directo de las toxinas circulantes (29).
Implicancias de la nueva definición
En investigaciones realizadas durante los últimos años se han empleado distintas definiciones de IM, lo que afecta la comparación, y, por lo tanto, las conclusiones generales de las mismas. Los investigadores deberían brindar datos que permitan analizar los distintos tipos de IM con los criterios diagnósticos aquí presentados, para así permitir tanto la adecuada comparación de los ensayos clínicos como de los metaanálisis(6).
La nueva definición de IM también tiene consecuencias para los pacientes y sus familias en cuanto al estado psicológico, seguro de vida, carrera profesional, permiso de conducir y licencia de piloto. El diagnóstico también conlleva repercusiones sociales respecto a la codificación del diagnóstico, reembolsos hospitalarios, estadísticas de salud pública, bajas por enfermedad y certificados de discapacidad(6).
En el sistema sanitario, la definición de IM afecta las decisiones terapéuticas del equipo asistencial. En epidemiología, los datos suelen ser retrospectivos, por lo que resulta esencial una definición homogénea para los análisis de tendencias. Para evaluar estas tendencias evolutivas es importante contar con definiciones concordantes y cuantificar los ajustes reactivos a los cambios que surjan en los criterios diagnósticos (30), siendo la viñeta clínica del inicio un ejemplo de estos cambios (31).
Conclusiones
En general, el significado conceptual del término IM no ha cambiado, aunque se han desarrollado nuevos métodos de diagnóstico sensibles. De este modo, el diagnóstico de IAM es clínico y basado en los síntomas del paciente, los cambios del ECG y de marcadores bioquímicos muy sensibles, así como de la información obtenida a través de varias técnicas de imagen.
Para finalizar, y a modo de síntesis, enumeramos diez puntos para recordar:
1. Para el diagnóstico de IAM se requiere una curva típica de biomarcadores asociada a la evidencia de isquemia mediante síntomas, ECG y/o hallazgos imagenológicos (troponina y su contexto).
2. El clínico debe conocer el arsenal de pruebas imagenológicas disponible para un manejo eficiente (costo-efectivo) de esta enfermedad.
3. No es suficiente el diagnóstico de IAM. Debe presentarse información adicional como las circunstancias en las que se presenta, el tamaño del mismo y el tiempo de evolución de la necrosis en relación con el momento de la observación.
4. Es importante caracterizar el tipo de IM, la función del ventrículo izquierdo residual y la extensión y gravedad de la enfermedad coronaria subyacente.
5. El IM ocurre en individuos con diferente carga de comorbilidades que debemos identificar debido a la influencia directa que ejercen sobre la decisión de la estrategia terapéutica.
6. El juicio clínico es fundamental para la toma de decisiones en escenarios como el perioperatorio o las unidades de medicina crítica.
7. Es fundamental inferir las consecuencias pronósticas frente al diagnóstico de IM.
8. Es necesario conocer y anticipar las implicancias sobre el estado psicológico y social de los pacientes en quienes se realiza diagnóstico de IM, así como de sus familias.
9. Para interpretar y comparar ensayos clínicos se debe atender el momento histórico en que se realizaron y los criterios diagnósticos que imperaban por esas fechas.
10. La modificación de los criterios diagnósticos de IM afecta no solo a los clínicos y a sus pacientes, sino también a investigadores, administradores y epidemiólogos, quienes deben conocer estos criterios universalmente aceptados así como sus consecuencias.
Bibliografía
1. Alpert JS, Thygesen K, Antman E, Bassand JP. Myocardial infarction redefined-a consensus document of The Joint European Society of Cardiology/American College of Cardiology Committee for the redefinition of myocardial infarction. J Am Coll Cardiol 2000;36(3):959-69. Fe de erratas en: J Am Coll Cardiol 2001 Mar 1;37(3):973.
2. Galvani M, Panteghini M, Ottani F, Cappelletti P, Chiarella F, Chiariello M, et al. The new definition of myocardial infarction: analysis of the ESC/ACC Consensus Document and reflections on its applicability to the Italian Health System. Ital Heart J 2002;3(9):543-57.
3. Thygesen K, Alpert JS, White HD. Universal definition of myocardial infarction. Eur Heart J 2007;28(20):2525-38.
4. Thygesen K, Alpert JS, Jaffe AS, White HD. Diagnostic application of the universal definition of myocardial infarction in the intensive care unit. Curr Opin Crit Care 2008;14(5):543-8. doi: 10.1097/MCC. 0b013e32830d34b9
5. Moscoso Costa F, Ferreira J, Aguiar C, Dores H, Figueira J, Mendes M. Impact of ESC/ACCF/ AHA/WHF universal definition of myocardial infarction on mortality at 10 years. Eur Heart J 2012;33(20):2544–50. doi: 10.1093/eurheartj/ ehs311
6. Thygesen K, Alpert JS, Jaffe AS, Simoons ML, Chaitman BR, White HD. Third universal definition of myocardial infarction. Eur Heart J 2012; 33(20):2551–67.
7. White HD, Thygesen K, Alpert JS, Jaffe AS. Clinical implications of the third universal definition of myocardial infarction. Heart. Publicación electrónica 27 Abr 2013 doi:10.1136/heartjnl-2012-302976.
8. Steg G, James SK, Atar D, Badano LP, Blömstrom-Lundqvist C, Borger MA, et al. ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur Heart J. doi:10.1093/eurheartj/ ehs215.
9. Hamm CW, Bassand JP, Agewall S, Bax J, Boersma E, Bueno H, et al. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: The Task Force for the management of acute coronary syndromes (ACS) in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2011;32(23):2999–3054.
10. Zimetbaum PJ, Josephson ME. Use of the electrocardiogram in acute myocardial infarction. N Engl J Med 2003;348(10):933–40.
11. Wang K, Asinger RW, Marriott HJ. ST-segment elevation in conditions other than acute myocardial infarction. N Engl J Med 2003;349(22):2128–35.
12. Jaffe AS, Babuin L, Apple FS. Biomarkers in acute cardiac disease: the present and the future. J Am Coll Cardiol2006;48(1):1–11.
13. White HD. Pathobiology of troponin elevations: do elevations occur with myocardial ischemia as well as necrosis?. J Am CollCardiol 2011;57(24):2406–8. Fe de erratas en: J Am Coll Cardiol 2011;58(22):2356
14. Jaffe AS. Chasing troponin: how low can you go if you can see the rise? J Am Coll Cardiol 2006; 48(9):1763–4.
15. MacRae AR, Kavsak PA, Lustig V, Bhargava R, Vandersluis R, Palomaki GE, et al. Assessing the requirement for the six-hour interval between specimens in the American Heart Association classification of myocardial infarction in epidemiology and clinical research studies. Clin Chem 2006;52(5):812–8.
16. Thygesen K, Mair J, Katus H, Plebani M, Venge P, Collinson P, et al. Recommendations for the use of cardiac troponin measurement in acute cardiac care. Eur Heart J 2010;31(18):2197–204.
17. Apple FS, Quist HE, Doyle PJ, Otto AP, Murakami MM. Plasma 99th percentile reference limits for cardiac troponin and creatine kinase MB mass for use with European Society of Cardiology/American College of Cardiology consensus recommendations. Clin Chem 2003;49(8):1331-6.
18. Stillman AE, Oudkerk M, Bluemke D, Bremerich J, Esteves FP, Garcia EV, et al. Assessment of acute myocardial infarction: current status and recommendations from the North American society for Cardiovascular Imaging and the European Society of Cardiac Radiology. Int J Cardiovasc Imaging 2011; 27(1):7-24.
19. Amsterdam EA, Kirk JD, Bluemke DA, Diercks D, Farkouh ME, Garvey JL, et al. Testing of low-risk patients presenting to the emergencydepartment with chest pain. Circulation 2010; 122(17):1756-76.
20. Flachskampf FA, Schmid M, Rost C, Achenbach S, de Maria AN, Daniel WG. Cardiac imaging after myocardial infarction. Eur Heart J 2011;32(3):272–83.
21. Gibbons RJ, Valeti US, Araoz PA, Jaffe AS. The quantification of infarct size. J Am Coll Cardiol 2004;44(8):1533-42.
22. Devereaux PJ, Xavier D, Pogue J, Guyatt G, Sigamani A, Garutti I, et al. Characteristics andshort-term prognosis of perioperative myocardial infarction in patients undergoing noncardiac surgery: a cohort study. Ann Intern Med 2011;154(8):523–8.
23. Fleisher LA, Nelson AH, Rosenbaum SH. Postoperative myocardial ischemia: etiology of cardiac morbidity or manifestation of underlying disease? J Clin Anesth 1995;7(2):97-102.
24. Landesberg G, Mosseri M, Shatz V, Akopnik I, Bocher M, Mayer M, et al. Cardiac troponin after major vascular surgery: The role of perioperative ischemia, preoperative thallium scanning, and coronary revascularization. J Am Coll Cardiol 2004; 44(3):569-75.
25. Cohen MC, Aretz TH. Histological analysis of coronary artery lesions in fatal postoperative myocardial infarction. Cardiovasc Pathol 1999;8(3):133-9.
26. Guest TM, Ramanathan AV, Tuteur PG, Schechtman KB, Ladenson JH, Jaffe AS. Myocardial injury in critically ill medical patients. A surprisingly frequent complication. JAMA 1995; 273(24):1945-9.
27. Babuin L, Vasile VC, Rio Perez JA, Alegria JR, Chai HS, Afessa B, et al. Elevated cardiac troponin is an independent risk factor for short- and long-term mortality in medical intensive care unit patients. Crit Care Med 2008;36(3):759-65.
28. Thygesen K, Alpert JS, Jaffe AS, White HD. Diagnostic application of the universal definition of myocardial infarction in the intensive care unit. Curr Opin Crit Care 2008;14(5):543-8.
29. Landesberg G, Vesselov Y, Einav S, Goodman S, Sprung CL, Weissman C. Myocardial ischemia, cardiac troponin, and long-term survival of high-cardiac risk critically ill intensive care unit patients. Crit Care Med 2005;33(6):1281–7.
30. Rosamond W, Chambless L, Heiss G, Mosley T, Coresh J, Whitsel E, et al. Twenty-two year trends in incidence of myocardial infarction,CHD mortality, and case-fatality in four US communities, 1987 to 2008.Circulation 2012;125(15):1848–57.
31. Luepker RV, Duval S, Jacobs DR, Smith LG, Berger AK. The effect of changing diagnostic algorithms on acute myocardial infarction rates. Ann Epidemiol 2011;21(11): 824-9














