Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Uruguaya de Cardiología
versión On-line ISSN 1688-0420
Rev.Urug.Cardiol. vol.28 no.3 Montevideo dic. 2013
Artículo original
Minitoracotomía anterior derecha para abordajes valvulares en cirugía cardíaca
Dres. Juan C. Reinoso 1, Leonardo González 1, Alejandro Heuer 1,
Favio Gutiérrez 1,2, Daniel Bigalli 3
1. Cirujano cardíaco del Centro de Investigación Cardiovascular Uruguayo.
2. Codirector del Centro de Investigación Cardiovascular Uruguayo. Centro Cardiovascular de Casa de Galicia. Montevideo, Uruguay
3. Director del Centro de Investigación Cardiovascular Uruguayo. Centro Cardiovascular de Casa de Galicia. Montevideo, Uruguay
Correspondencia: Dr. Juan Carlos Reinoso. Correo electrónico: jcreinoso@gmail.com
Recibido junio 16, 2013; aceptado setiembre 19, 2013.
Resumen
La cirugía mínimamente invasiva de la válvula mitral ha tenido un gran impulso en la última década. El abordaje de la misma a través del tercer o cuarto espacio intercostal se ha podido efectuar gracias al desarrollo de nuevos materiales e instrumental específico, permitiendo una exposición quirúrgica y resultados comparables con las técnicas clásicas de esternotomía. Ha permitido acortar estadías hospitalarias con menores molestias posoperatorias y un mejor resultado cosmético para los pacientes.
Resultados: entre mayo de 2007 y julio de 2009 se realizaron 13 abordajes por minitoracotomía derecha para cirugía de sustitución valvular mitral (diez pacientes), cierre de comunicación interauricular (dos pacientes); además, en un paciente con anomalía de Ebstein, se realizó cierre de comunicación interauricular aislada con plastia tricuspídea. Los resultados fueron en todo similares a los pacientes operados a través de una esternotomía convencional y se mantuvieron igual luego de un seguimiento medio de cinco años.
Conclusiones: nuestra experiencia en este abordaje ha demostrado que es reproducible y que puede ser practicado con seguridad y resultados comparables con la técnica convencional.
Palabras clave:
PROCEDIMIENTOS QUIRúRGICOS MíNIMAMENTE INVASIVOS
VáLVULA MITRAL-cirugía
Summary
The minimal invasive surgery of the mitral valve has had a great impulse in the last decade. The surgical approach of this valve through the third or fourth intercostal space was possible to perform thanks to the development of new materials and specific devices, permitting a surgical exposition and results comparable to classic techniques of sternotomy. Therefore hospitals stays have been shortened, with less postoperative discomfort and better cosmetic outcomes for patients.
Results: between may 2007 and july 2009, 13 patients (p) were approached for right mini-thoracotomy for mitral valve substitution surgery (10 p), closing an interatrial communication in 2 p, and closing the isolated interatrial communication with tricuspid repair in one patient with Ebstein anomaly. The results were similar to the patients operated through a sternotomy, and after a median follow-up of 5 year they were maintained. Conclusion: our experience in this approach has demonstrated that it is reproducible and can be practiced safely with comparable results using the conventional technique.
Key words:
SURGICAL PROCEDURES, MINIMALLY INVASIVE
MITRAL VALVE-surgery
Introducción
La buena exposición de la válvula mitral (VM) es uno de los factores más importantes para lograr una reparación o sustitución con óptimos resultados. Lillehei fue el primero en emplear el bypass cardiopulmonar para la reparación de una lesión valvular mitral(1).
Los avances en cirugía mitral han dependido del desarrollo de diferentes biomateriales e innovadoras técnicas de reparación desde la temprana década de 1960, pero el abordaje a través de la esternotomía media convencional no había cambiado hasta hace poco tiempo(2).
Los trabajos pioneros de Cohn(3 ) , Cosgrove(4) y Navia(5) le dieron verdadero impulso a la cirugía miniinvasiva de la VM. En febrero de 1996 la primera cirugía mitral compleja a través de una minitoracotomía fue realizada por Carpentier y su grupo(6).
Varios reportes de cirugía mínimamente invasiva de la VM han sido publicados en la última década(6 -9). Describen la técnica quirúrgica a través del tercer o cuarto espacio intercostal y la aplicación de nuevo instrumental desarrollado para la misma, brindando una excelente exposición y un buen campo quirúrgico. Este abordaje permite tratar a estos pacientes con mejores resultados cosméticos, menor dolor posoperatorio y una corta estadía hospitalaria.
Como resultado de la cirugía video-asistida y endovascular se han desarrollado nuevas técnicas que se agrupan bajo el nombre de cirugía mínimamente invasiva, que comprenden modificaciones de las incisiones clásicas, limitando su longitud, para el abordaje de la VM, el aparato subvalvular y la cirugía de congénitos (10-12 ).
La reparación o la sustitución valvular mitral vía minitoracotomía es todavía una técnica en desarrollo, pero ya adoptada como de elección, con varios detalles técnicos propios en constante actualización, como la canulación femoral que se ha transformado en una canulación aórtica directa y la venosa percutánea. El balón intraaórtico de oclusión fue dejado de lado a favor de la oclusión (clampeo) aórtica a través de una incisión accesoria. Los cirujanos tienen hoy día la posibilidad de seleccionar dispositivos e instrumentos y la técnica quirúrgica acorde a sus preferencias y adaptada a las necesidades del paciente. Este abordaje se ha vuelto muy reproducible y adaptable a las aptitudes de cada cirujano cardíaco en particular.
Estudios prospectivos aleatorizados han mostrado que las ventajas de estas incisiones incluyen disminuir la agresión, el dolor posoperatorio, reducir el sangrado perioperatorio, un mejor resultado cosmético y una recuperación funcional más temprana, acortando la estancia posoperatoria y disminuyendo los costos (13,14) .
Procedimiento
El paciente es colocado en posición decúbito supino elevando la escápula derecha a 30º, para mejorar la posición de este hemitórax y la visión del cirujano. Se colocan parches adhesivos de desfibrilación externa a cada lado del tórax.
Se realiza anestesia general de acuerdo con el protocolo habitual para una plastia o sustitución mitral convencional. Se utiliza intubación endotraqueal selectiva, permitiendo colapsar el pulmón derecho, según sea necesario, para mejorar la visualización. Disponemos de fibrobroncoscopía de control durante la cirugía para posicionar y asegurar la ubicación de la sonda endotraqueal al movilizar al paciente; se realiza fibrobroncoaspiración al finalizar la intervención para disminuir el riesgo de atelectasias residuales.
Con ecocardiografía transesofágica se monitorea el resultado funcional valvular o protésico así como la función ventricular posoperatoria.
El bypass cardiopulmonar para la circulación extracorpórea (CEC) se realiza por canulación periférica, se diseca el pedículo femoral y, luego de la heparinización sistémica, se introduce una cánula simple de 17-21F a través de la vena femoral y una cánula de similar calibre para la arteria femoral.
La incisión es de 6 a 7 cm a nivel del cuarto espacio intercostal, sobre la línea axilar anterior. Inicialmente realizábamos incisiones mayores y más anteriores; con mayor experiencia, la incisión se vuelve más pequeña y más lateral, submamaria, lo que permite una buena exposición valvular.
Se moviliza el músculo pectoral mayor y a través del sector anterior del cuarto espacio intercostal derecho, seccionando los intercostales y utilizando un retractor costal ThoraGate Geister®. Para mejorar la exposición, el anestesista colapsa el pulmón derecho y se abre el pericardio por delante del pedículo frénico.
La vena cava superior se aborda a través de la incisión y se introduce una cánula acodada de 24-28F. Una vez canuladas ambas cavas se ocluyen (clampean) en su desembocadura a la aurícula derecha (AD) con torniquetes de cinta. En los pacientes que se realiza canulación de aorta ascendente se dispone de una cánula aórtica acodada flexible de 18-20F, colocada por el mismo abordaje.
La oclusión aórtica es realizada por contraabertura a través del tercer espacio intercostal con un clamp de Chitwood DeBakey Scanlan®.
La cardioplejia usada es una solución cristaloide (Custodiol®) a 4ºC de temperatura, infundida en forma anterógrada a través de una cánula colocada en la aorta ascendente, se utiliza una única dosis de 2 litros.
El abordaje de la VM fue transeptal a través de la AD; se incide el septum interauricular a nivel de la fosa oval e introduciendo un retractor manual de aurícula Geister®, la VM es expuesta. Explorada la misma se decide su reparación o sustitución siguiendo técnicas estándar, pero con instrumental específico para cirugía miniinvasiva (ValveGate Geister®).
Material y método
Entre mayo de 2007 y julio de 2009 fueron operados 13 pacientes, no consecutivos, de coordinación. Se les informó de los riesgos y beneficios tanto de la técnica quirúrgica como del abordaje a utilizar, y se obtuvo el consentimiento por escrito.
Las contraindicaciones para la inclusión en el trabajo fueron: toracotomía derecha previa, fracción de eyección del ventrículo izquierdo(FEVI) menor a 45%, presencia de anillo mitral severamente calcificado, dificultades en la canulación femoral y cirugía de urgencia.
La edad media fue de 47±17 años, nueve pacientes eran mujeres (69%).
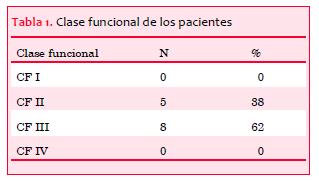
La clase funcional se muestra en la tabla 1.
En todos los pacientes la miniincisión fue en el cuarto espacio intercostal anterior, con una media (± 1 ds) de 7 cm ± 2cm.
La canulación arterial fue femoral en 11 pacientes (85%) y en aorta ascendente en dos (15%). La canulación venosa por acceso femoral a la cava inferior y directamente en la cava superior. La oclusión aórtica se hizo por contraabertura a través del tercer espacio intercostal como fue descrito anteriormente.
La cirugía de SVM se realizó con conservación de la valva posterior y el aparato subvalvular correspondiente. En ninguno de los casos la incisión tuvo que ser ampliada, ni aun en aquellos que requirieron desfibrilación al término de la CEC, ya que se utilizaron parches externos con buen resultado.
El tiempo de CEC (± 1 ds) fue de 120±25 minutos y un tiempo de oclusión (clampeo) aórtico, isquemia (± 1 DE) de 93±22 minutos.
La estancia en CTI/CI (± 1 DE) fue de 3,5±3,8 días y la internación posterior en sala (± 1 DE) de 6,9±4,9 días; el rango de horas de intubación orotraqueal fue de 6-36 horas, con un tiempo medio (± 1 DE) de 15±13 horas (mediana 13). El 100% recibió infusión de fármacos inotrópicos, con un rango de 2-168 horas y un tiempo medio (± 1 DE) de 34±50 horas (mediana 20).
No hubo reintervenciones por sangrado. Ningún paciente tuvo un registro electrocardiográfico de infarto perioperatorio ni síndrome de bajo gasto que requiriera el uso de dosis elevadas de inotrópicos, ni la colocación de balón de contrapulsación intraaórtico.
Solo un paciente (7,5%) mantuvo atelectasias en el posoperatorio que no se resolvieron con maniobras de reclutamiento alveolar y requirió fibrobroncoaspiración.
Tres pacientes tenían antecedentes de fibrilación auricular (FA) paroxística (23%) y los mismos (23%) tuvieron episodios de FA en el posoperatorio inmediato. Solo un paciente (8%) mantuvo FA al alta.
En el control con ecocardiograma a los seis meses, en dos pacientes (15%) se constató una fuga paravalvular leve que no se agravó en el seguimiento.
Con un seguimiento medio de cinco años, los pacientes no han presentado complicaciones en relación al procedimiento realizado, sin mortalidad vinculada a la técnica ni por otras causas.
Discusión
La intención de este trabajo ha sido demostrar la factibilidad y reproducibilidad de la técnica miniinvasiva para abordajes sobre la VM y el septum interauricular.
Siguiendo este camino, en nuestro centro se han intervenido 13 pacientes, no consecutivos, en cirugías de coordinación, investigando los aspectos técnicos y demostrando resultados de este abordaje para la cirugía valvular mitral al menos no inferiores a las técnicas convencionales.
No hay estudios prospectivos aleatorizados que comparen el abordaje miniinvasivo con la esternotomía convencional en cirugía mitral a la fecha de este estudio(21) . Holzhey hace hincapié en la experiencia previa en cirugía mitral convencional que deberían tener los cirujanos encargados de realizar esta técnica, y que sea desarrollada por un grupo pequeño en cada centro, permitiendo así concentrar la experiencia y disminuir la tasa de eventos adversos durante su curva de aprendizaje(21).
Muchos años después de su introducción en la cirugía ginecológica, abdominal y torácica, las técnicas mínimamente invasivas se aplicaron a la cirugía valvular (16,17). Diferentes grupos han reportado resultados alentadores, con baja mortalidad (1%-3%) y escasa morbilidad utilizando este abordaje (3,4-19 ).
En 1994, cirujanos de la Universidad de Stanford (Estados Unidos) ocluyeron por primera vez la aorta en forma endoluminal mediante un balón en una cirugía mitral con CEC(20). Reportes posteriores sugirieron mayores complicaciones con el uso de este dispositivo intravascular, a la vez costoso y complejo. Actualmente se prefiere la oclusión aórtica transtorácica más sencilla, segura y económica a través de una incisión accesoria en el tercer espacio intercostal en la línea axilar media. Comparado con el abordaje tradicional la oclusión aórtica transtorácica minimiza la distorsión cardíaca y aórtica y mantiene la competencia valvular(8).
Fueron incluidos diez pacientes a quienes se les realizaría sustitución valvular mitral por insuficiencia valvular severa en los que se había descartado la reparación valvular por ecocardiograma previo; tres pacientes para corrección de CIA, incluyendo uno con anomalía de Ebstein también para reparación de válvula tricúspide. Los tiempos de isquemia y bypass cardiopulmonar están dentro de los rangos considerados adecuados y exentos de riesgo para el paciente.
El uso de intubación endotraqueal selectiva, con ayuda de fibrobroncoscopio y el manejo del mismo durante la intervención así como la broncoaspiración al finalizar la cirugía, permitió minimizar las atelectasias residuales del pulmón derecho, disminuyendo las complicaciones respiratorias posoperatorias. Las atelectasias constituyen la complicación pulmonar más frecuente en cirugía cardíaca, aparecen en 50% a 70% de los pacientes(15) ; en nuestra serie solo un paciente presentó atelectasias y requirió fibroncoaspiración en CTI para su tratamiento. No se reportaron otras complicaciones respiratorias.
La canulación aórtica se realizó en tan solo dos pacientes de la serie, siendo estos los últimos intervenidos dada la mayor experiencia obtenida. Se hizo sin complicaciones utilizando la vía descrita anteriormente. Tampoco hubo complicaciones en la canulación venosa.
Las estadías tanto en CTI como en sala común son similares a aquellas en las que se realizó el abordaje tradicional. Los tiempos de asistencia respiratoria y requerimiento de inotrópicos tampoco fueron mayores a los habituales en estas cirugías.
Con un seguimiento medio de cinco años, los pacientes no han presentado complicaciones en relación al procedimiento realizado, sin mortalidad en el seguimiento vinculada a la técnica ni por otras causas.
La presencia de fuga paravalvular se describió en dos pacientes (15%) a los seis meses, siendo leve, y se mantuvo de igual manera en el seguimiento.
Conclusiones
En nuestro servicio actualmente hemos desarrollado este abordaje tanto para procedimientos mitrales aislados como combinados con procedimientos sobre la válvula tricúspide, más tratamiento de la FA concomitante.
Nuestra experiencia con la reparación o sustitución valvular mitral vía minitoracotomía derecha ha demostrado que es un abordaje reproducible y que puede ser practicado con seguridad y resultados al menos no inferiores en cuanto a morbimortalidad en relación con la técnica convencional.
Bibliografía
1. Lillehei CW, Gott VL, DeWall RA, Varco RL. The surgical treatment of stenotic or regurgitant lesions of the mitral and aortic valves by direct vision utilizing a pump-oxygenator. J Thorac Surg 1958; 35(2): 154-91.
2. Ikonomidis JS. Minimal access cardiothoracic surgery. Port access cardiothoracic surgery. En: Yim A, Hazelrigg SR, Izzat MB, Landreneau RJ, Mack MJ, Naunheim KS, et.al. Minimal access heart valve surgery. New Jersey: W.B Saunders; 2000: 576-83.
3. Cohn LH, Adams DH, Couper GS, Bichell DP, Rosborough DM, Sears SP, et al. Minimally invasive cardiac valve surgery improves patient satisfaction while reducing costs of cardiac valve replacement and repair. Ann Surg 1997;226(4):421-6.
4. Cosgrove DM, Sabik JF, Navia JL. Minimally invasive valve operations. Ann Thorac Surg 1998; 65(6):1535-8.
5. Navia JL, Cosgrove DM. Minimally invasive mitral valve operations. Ann Thorac Surg 1996; 62(5):1542-4.
6. Loulmet D, Carpentier A, Cho PW, Berrevi A, d’Attellis N, Austin CB, et al. Less invasive techniques for mitral valve surgery. J Thorac Cardiovasc Surg 1998;115(4):772-9.
7. Burke RP, Wernovsky G, van der Velde M, Hansen D, Castaneda AR. Video-assisted thoracoscopic surgery for congenital heart disease. J Thorac Cardiovasc Surg 1995;109(3):499-508.
8. Chitwood WR, Elbeery JR, Chapman WH, Moran JM, Lust RL, Wooden WA, et al. Video-assisted minimally invasive mitral valve surgery: The micro-mitral operation. J Thorac Cardiovasc Surg. 1997;113(2):413-4.
9. Walther T, Falk V, Mohr FW. Minimally invasive surgery for valve disease. Curr Probl Cardiol 2006;31(6):399-437.
10. Cooley DA. Minimally invasive valve surgery versus the conventional approach. Ann Thorac Surg 1998;66(3):1101-5.
11. Schwartz DS, Ribakove GH, Grossi EA, Stevens JH, Siegel LC, St Goar FG, et al. Minimally invasive cardiopulmonary bypass with cardioplegic arrest: a closed chest technique with equivalent myocardial protection. J Thorac Cardiovasc Surg 1996;111(3):556-66.
12. Glauber M, Karimov JH, Farneti PA, Cerillo AG, Santarelli F, Ferrarini M, et al. Minimally invasive mitral valve surgery via right minithoracotomy. Multimedia Manual Cardiothoracic Surgery 2009. doi: 10.1510/mmcts. 2008.003350.
13. Goldstein DJ, Oz MC. Minimally invasive cardiac surgery. En: Goldstein DJ, Oz MC, editors. Minimally invasive cardiac surgery. 2°ed. New Jersey: Humana Press; 2004: 255-72.
14. Arom KV, Emery RW. Minimallly invasive mitral operations. Ann Thorac Surg 1997;63(4):1219-20.
15. Peláez Romero R, Hortal FJ, Riesgo M. Tratamiento del dolor postoperatorio en cirugía cardíaca. Rev Esp Anestesiol Reanim. 2002;49:474-84.
16. Bruhat MA, Manhes H. Essai de traitement per coelioscopique de la grossesse extra-uterine. Presse Med 1977; 6:2606.
17. Soper NJ, Brunt LM, Kerbl K. Laparoscopic general surgery. N Engl J Med 1994;330(6):409-19.
18. Pompili MF, Stevens JH, Burdon TA, Siegel LC, Peters WS, Ribakove GH, et al. Port-access mitral valve replacement in dogs. J Thorac Cardiovasc Surg 1996;112(5):1268-74.
19. Schwartz DS, Ribakove GH, Grossi EA, Buttenheim PM, Schwartz JD, Applebaum RM, et al. Minimally invasive mitral valve replacement: Port-access technique, feasibility, and myocardial functional preservation. J Thorac Cardiovasc Surg. 1997;113(6):1022-31.
20. Mohr FW, Falk V, Diegeler A, Walther T, Van Son JA, Autschbach R. Minimally invasive port-access mitral valve surgery. J Thorac Cardiovasc Surg 1998;115(3):567-71.
21. Holzhey DM, Seeburger J, Misfeld M, Borger MA, Mohr FW. Learning Minimally-Invasive Mitral Valve Surgery: A cumulative Sum Sequential Probability Analysis of 3895 Operations from a Single High Volume Center. Circulation 2013;128(5):483-91.