Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Uruguaya de Cardiología
versión On-line ISSN 1688-0420
Rev.Urug.Cardiol. vol.27 no.2 Montevideo ago. 2012
Caso clínico
Asociación cianosis central grave y dilatación de aorta ascendente
Pablo Díaz, José Pérez Arrarte, Alicia Salvarrey y colaboradores
Un enigma fisiopatológico.
Asociación cianosis central grave y dilatación de aorta ascendente
Dres. Pablo Díaz 1, José Pérez Arrarte 2, Alicia Salvarrey 3, Roberto Canessa 4
1. Cardiólogo intervencionista. Servicio de Ecocardiografía del Hospital Italiano.
2. Cardiólogo. Unidad Cardiológica de Asociación Española 1ª de Socorros Mutuos.
3. Jefe de Unidad Cardiológica Asociación Española 1ª de Socorros Mutuos.
4. Cardiólogo. Servicio de Ecocardiografía del Hospital Italiano.
Correspondencia: Dr. Pablo Díaz. Correo electrónico: pdcardio@adinet.com.uy
Recibido junio 7, 2012; aceptado julio 26, 2012
Palabras clave:
CIANOSIS
DILATACIÓN AORTA
FORAMEN OVAL PERMEABLE
Key words:
CIANOSIS
AORTIC DILATATION
PATENT FORAMEN OVALE
La asociación cianosis central con dilatación y/o elongación de aorta torácica ha sido descripta en escasos reportes aislados desde 1996 (1). Cada una de las publicaciones ha dado lugar a diversas explicaciones y a interesantes discusiones fisiopatológicas. Es que en realidad, además de ser esporádicos, estos casos desafían nuestra comprensión del sistema circulatorio. Se destaca en ellos habitualmente una prolongada historia de dudas diagnósticas, paraclínica no concluyente, tratamientos inefectivos y frustración profesional médica, con las negativas consecuencias para el paciente.
Presentamos dos casos de cianosis central grave con presencia concomitante de aorta ascendente dilatada, finalmente diagnosticados en forma correcta por ecocardiografía, luego de algunas vacilaciones diagnósticas.
Caso 1
Paciente de 61 años, ex fumadora leve, hipertensa moderada, en tratamiento con enalapril, con una historia de cinco años de disnea y cianosis, fue ingresada en octubre del 2008 en un centro de asistencia mutual para nueva evaluación diagnóstica y eventual tratamiento. La historia clínica se había iniciado cinco años atrás, con disnea de esfuerzo, progresiva, hasta hacerse de mínimos esfuerzos. En el examen físico se describía entonces la presencia de cianosis de lecho subungueal, labios y lóbulo de orejas, sin otros hallazgos significativos a nivel de la esfera cardiovascular (CV) central y periférica. El electrocardiograma (ECG) mostraba ritmo sinusal de 75 min, bloqueo aurículoventricular (BAV) de primer grado y alteraciones inespecíficas leves de la repolarización ventricular de carácter difuso. Radiografía (Rx) de tórax fue informada como leve dilatación de mediastino, silueta cardíaca normal, sin otras alteraciones significativas. Fue estudiada con ecocardiograma transtorácico (ETT), el cual informaba cavidades cardíacas de dimensiones normales, buena contractilidad de ambos ventrículos, ausencia de alteraciones sectoriales, hipertrofia ventricular izquierda concéntrica leve, mixomatosis leve y prolapso de valva anterior mitral, dilatación leve de raíz de aorta y moderada de aorta ascendente, insuficiencia mitral leve e insuficiencia aórtica leve. Valorada en varias oportunidades mediante funcional respiratorio, los resultados coincidían en mostrar hipoxia muy severa, pero diferían en su corrección con tratamiento con oxígeno al 100%. Se realizó centellografía de ventilación perfusión, el cual fue informado como normal. La sintomatología progresó lentamente. La cianosis y la disnea fueron adquiriendo la particular característica de exacerbarse con la posición ortostática, al punto de que la paciente llegó a guardar reposo en cama horizontal en forma permanente. Dejó de levantarse siquiera para ir al baño. Pasó a recibir visitas médicas a domicilio. Se repitió el ecocardiograma en varias oportunidades, sin verificarse cambios en el resultado. Se inició entonces tratamiento con oxígeno a permanencia en forma empírica. Se realizó trámite ante el Banco de Previsión Social y se le otorgó una pensión definitiva por discapacidad severa. A inicios del 2006 fue estudiada con cateterismo cardíaco izquierdo y derecho con angiografía pulmonar, demostrándose la ausencia de lesiones coronarias, presiones pulmonares normales y la presencia de un trombo endoluminal en arteria pulmonar izquierda basal. Se realizó además ecocardiograma transesofágico (ETE), el cual confirmó los hallazgos de los estudios transtorácicos y describió la presencia de foramen oval permeable (FOP), con cortocircuito o shunt de derecha a izquierda que no se dimensionó, pero que se describió como más acentuado en “situaciones de descompensación clínica”. Con el diagnóstico de tromboembolismo pulmonar se inició tratamiento con warfarina y se mantuvo con oxígeno a permanencia. A los seis meses, con sintomatología incambiada, se repitió la angiografía pulmonar en diferente centro, siendo informada como normal. Durante los dos años siguientes mantuvo reposo en cama, con cianosis permanente, con severa disnea y sensación de muerte inminente durante la posición ortostática. Valorada por psiquiatra por depresión y posible simulación de síntomas, se inició tratamiento crónico con antidepresivos y ansiolíticos. La anticoagulación fue suspendida tres meses previo al ingreso. Por cambio de mutualista fue enviada a cardiólogo para valoración de necesidad de oxigenoterapia a domicilio, quien, debido a su severa cianosis, decidió ingresarla a sanatorio para valoración adicional.
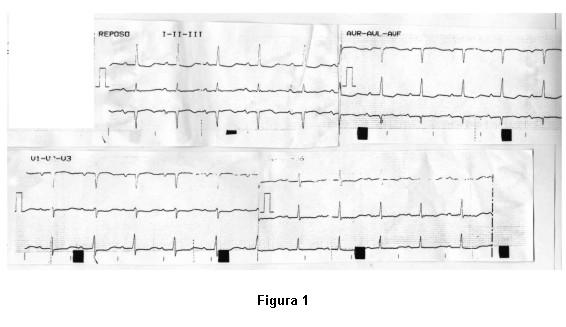
Del examen físico al ingreso se destacaba paciente en decúbito dorsal, lúcida, eupneica, con máscara de flujo libre y cianosis universal. Saturación del 85% por oximetría de pulso. En lo CV, ritmo regular de 75 latidos/min, ruidos bien golpeados, sin soplos, auscultación pleuropulmonar libre de estertores, abdomen sin particularidades a destacar, ausencia de edema sacro o de miembros inferiores con pulsos presentes y simétricos. ECG se informó como RS de 75 lpm, BAV de primer grado, y alteraciones inespecíficas de la repolarización (figura 1). Hemograma normal. Se repitió ETT, el cual fue informado como ventrículo izquierdo (VI) no dilatado, con hipertrofia moderada, concéntrica, con buena contractilidad global y sectorial, ventrículo derecho (VD) normal, aurícula izquierda (AI) en límite superior de dimensiones normales, aurícula derecha (AD) de dificultosa valoración por yuxtaposición de aorta sinusal dilatada, válvula aórtica con esclerosis leve, regurgitación moderada a severa, válvula mitral mixomatosa con insuficiencia leve, válvula tricuspídea de dificultosa visualización. No se observaron cortocircuitos. Dilatación de aorta sinusal y proximal ascendente con los caracteres de anulectasia aórtica. Vena cava inferior no dilatada. Se decide realizar consulta con servicio de hemodinamia para eventual estudio hemodinámico con el fin de “valorar ‘shunt’ de derecha a izquierda en paciente con presiones pulmonares normales e HTA”.
En el servicio de hemodinamia se realizó una revisión de la historia clínica de la institución y de todos los estudios aportados por la paciente y familia. Se realizó una búsqueda bibliográfica a través de la web. Llamaron nuestra atención publicaciones de casos aislados de similares características, con dilatación de aorta proximal y concomitante presencia de FOP, con importante cortocircuito de derecha a izquierda a su través. Los pacientes reportados en la literatura se han caracterizado, en su enorme mayoría, por presentar el síndrome de platipnea ortodesoxia: desaturación y disnea con la posición ortostática.
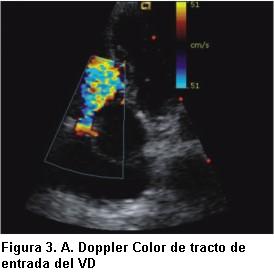
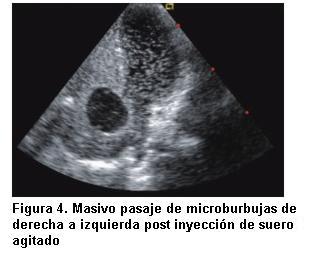
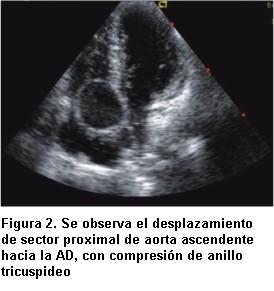
Una reevaluación clínica de nuestra paciente mostró una caída de la saturación por oximetría de pulso bajo máscara de flujo libre en posición horizontal de 85% a 75% al sentarse al borde de la cama, sin llegar a estabilizarse completamente en su descenso dada la incapacidad de la paciente de mantener esta posición. Gasometría en decúbito dorsal reveló pH normal, pCO2 normal y pO2 de 50 mm de Hg con máscara de flujo libre. Con el diagnóstico de platipnea-ortodesoxia, se realizó un nuevo ETT dirigido a la búsqueda de los caracteres descriptos en los pacientes reportados en la literatura. Un laborioso estudio permitió visualizar una clara compresión del anillo tricuspídeo por la raíz de aorta dilatada (figura 2), que generaba en decúbito lateral izquierdo un gradiente pico de onda A de 15 mm de Hg, con una onda E cuyo PHT de 224 mseg permitió estimar un área de 1.25 cm2 para una constante de 180 para la válvula tricúspide (figuras 3 A y B). Se apreció un septum interauricular (SIA) levemente aneurismático, protruyendo hacia AI. Se realizó entonces infusión de suero agitado por vía venosa periférica proximal y se comprobó importante pasaje de microburbujas hacia cavidades izquierdas (figura 4). Esta misma maniobra se repitió con paciente semisentada y el “shunt” se exacerbó marcadamente. Se solicitó ETE. El estudio confirmó hallazgos del ETT. Reveló, además, que el SIA se caracterizaba por presentar un FOP, con franca apertura durante sístole auricular y cambios con la ventilación, con marcado cortocircuito de derecha a izquierda visualizado por color e inyección de suero agitado.
Con el diagnóstico de anulectasia aórtica, insuficiencia aórtica moderada a severa, compresión de anillo tricuspídeo y FOP se realizó consulta con servicio de cirugía cardíaca. Se completó valoración de aorta con tomografía de tórax y abdomen, la cual no aportó nueva información. Se revisó la coronariografía realizada dos años antes. Dada la ausencia de lesiones se decidió no repetirla.
Fue intervenida quirúrgicamente en noviembre de 2008. Se comprobó en la cirugía la presencia de una aorta dilatada que ocupaba la mayor parte de la AD, comprimiendo el anillo tricuspídeo. Se realizó sustitución de válvula aórtica y de aorta ascendente por tubo valvulado y cierre de foramen oval por puntos. La hipoxemia se corrigió inmediatamente. La paciente cursó su postoperatorio sin incidentes mayores. ETT de control mostró la desaparición de la obstrucción de anillo tricuspídeo y la ausencia de shunt residual. Luego de cuatro semanas de fisioterapia y apoyo psicológico fue dada de alta a domicilio. Ha tenido una buena evolución en estos años.
Caso 2
Paciente de 69 años, sexo femenino, con antecedentes de hipertensión arterial de larga data tratada con ARA-2 y alfametildopa, consultó en febrero de 2012 por historia de dos meses de evolución caracterizada por disnea de esfuerzo progresiva, hasta hacerse de esfuerzos leves. Negaba síntomas de reposo ni variaciones en sus síntomas con los cambios de posición. No había sufrido reposo prolongado, ni traumatismos. Negaba edema de miembros inferiores. En valoración médica se constató normotensión arterial, cianosis de labios y lecho subungueal, ritmo regular de 75 lpm, punta no desplazada, soplo diastólico en mesocardio 1/6, campos pulmonares libres a la auscultación y pulsos normales en los cuatro miembros. Se realizó ECG que mostró ritmo sinusal de 75 lpm y leves alteraciones de la repolarización ventricular en cara anterolateral. Oximetría de pulso de 78% ventilando al aire se decidió su ingreso inmediato a centro de tratamiento interno para valoración y tratamiento. Con paciente asintomática se inició oxigenoterapia con máscara de flujo libre, alcanzando saturaciones de 80%. Rx de tórax reveló silueta cardíaca normal, no infiltrados pleuropulmonares, con disminución de trama vascular pulmonar. Gasometría con pH normal, PaO2 de 45 mm Hg ventilando con FiO2 de 1. Hemoglobina de 15 g/dL. Se utilizó temporariamente ventilación mecánica no invasiva, sin efecto ostensible en las cifras de saturación. Se solicitó ecocardiograma transtorácico urgente, el cual fue informado como cavidades cardíacas de dimensiones normales, con buena contractilidad global y sectorial de ambos ventrículos. Dilatación leve de aorta ascendente. No se observaron cortocircuitos.
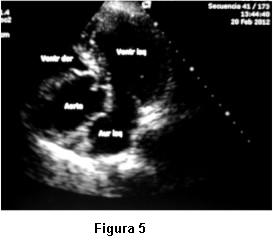
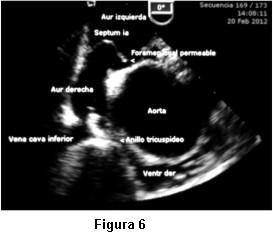
Dada la persistente sospecha clínica de un shunt de derecha a izquierda no detectado por el ETT, se nos solicitó la realización de ETE. Las imágenes transtorácicas pre ETE fueron claras en mostrar una raíz de aorta dilatada, ocupando gran parte de la AD y comprimiendo el anillo tricuspídeo (figura 5). Insuficiencia aórtica moderada. VD colapsado. Flujo a través de válvula tricúspide de difícil detección, no valorable por Doppler. Arteria pulmonar no dilatada. Se realizó inyección de suero agitado y se comprobó masivo pasaje de microburbujas hacia cavidades izquierdas. El ETE mostró adicionalmente un septum interauricular deformado, con un foramen oval persistentemente abierto, hacia el cual se observaba flujo direccionado desde vena cava inferior, lo cual producía un muy severo y constante cortocircuito de derecha a izquierda. Raíz de aorta y aorta ascendente dilatada (44 y 47 mm) con elongación de aórtica torácica. Severa compresión de anillo tricuspídeo por aorta ya descripta (figura 6).
Se realizó consulta con cirujano cardíaco. Se realizó una resonancia magnética que confirmó los hallazgos de los estudios ecocardiográficos. Cateterismo cardíaco reveló ausencia de lesiones coronarias. No se realizó cateterismo derecho. Fue intervenida quirúrgicamente en marzo de 2012. En la exploración se comprobó la presencia de aorta ascendente horizontalizada, moderadamente dilatada, con desplazamiento del anillo y sector más proximal hacia la AD, con distorsión del SIA y compresión de tracto de entrada del VD. Se realizó sustitución de válvula aórtica y aorta ascendente por tubo valvulado. No se realizó cierre de FOP. Tuvo un postoperatorio sin complicaciones mayores. La saturación se normalizó. ETT de control mostró ausencia de obstrucción en tracto de entrada del VD y ausencia de “shunt” residual.
Discusión
La hipoxemia severa es una situación grave, con importante morbilidad, que puede conducir a la muerte por shock hipoxémico. Existen múltiples causas de hipoxemia severa. Para que ella se traduzca en cianosis debe existir una concentración capilar de hemoglobina reducida mayor a 4 g/dL. La cianosis se puede subdividir en dos grandes tipos: central y periférica.
La cianosis periférica se debe a un enlentecimiento circulatorio y a una mayor extracción tisular de oxígeno desde sangre arterial con saturación central normal. Tal es el caso de pacientes con gasto cardíaco severamente disminuido.
La cianosis central se debe muy raramente a la presencia de hemoglobinas anormales, como la metahemoglobina, y generalmente a una disminución de la saturación central de oxígeno. Dentro de estas últimas se destacan el descenso de la FiO2 (cianosis de alta montaña), la patología pulmonar crónica o aguda y los cortocircuitos o shunts de sangre venosa hacia el circuito arterial por una comunicación anatómica anormal. Estas últimas se caracterizan porque la saturación no se corrige en forma significativa con la administración de oxígeno. Dado que la sangre fluye siempre de la región de mayor presión a la de menor presión, para que este shunt efectivamente se produzca es necesaria la presencia adicional de un aumento de las resistencias vasculares pulmonares o de una obstrucción anatómica distal al defecto.
Durante la vida fetal la sangre oxigenada proveniente de la placenta a través de la vena umbilical y la vena cava inferior es derivada hacia la AI a través del foramen oval, gracias a la dirección de la válvula de Eustaquio y a la presencia de alta resistencia y mayor presión en cavidades derechas y en el circuito pulmonar. Con la expansión pulmonar y la caída de las resistencias y presiones pulmonares inmediatamente luego del nacimiento, la sangre venosa de la AD pasa preferencialmente hacia el VD. El aumento de la presión en la AI lleva al cierre del septum secundum por aposición de ambas membranas del septum interauricular. En 25% de los adultos estas láminas no se fusionan totalmente y persiste una comunicación muy escasa y hasta virtual, muchas veces anfractuosa, el FOP, que en condiciones basales permite un mínimo shunt de izquierda a derecha. En situaciones donde aumenta la presión en la AD, puede aparecer un cortocircuito de derecha a izquierda, transitorio o fijo, con consecuencias variadas para los pacientes. Las embolias paradójicas son una de las eventualidades más estudiadas. Su análisis escapa a los objetivos de este artículo. La caída de saturación central de oxígeno es otra de las posibles consecuencias de la apertura de un FOP por aumento de la presión en la AD. La embolia pulmonar, la disfunción sistólica severa del VD por infarto, traumatismo o herida cardíaca penetrante, el derrame pericárdico severo y el aumento de la presión intratorácica durante ventilación asistida son algunaos de las causas de aumento de la presión en la AD que pueden llevar a la aparición de cianosis central si existe suficiente “shunt” de derecha a izquierda a través de un FOP.
El enigma que plantean los pacientes con cianosis central con concomitante hallazgo de dilatación aórtica es por demás fascinante. Las explicaciones que se han manejado varían con cada caso (2-10). Se habla de una deformación del septum interauricular debido al crecimiento y elongación de la aorta ascendente, con la consecuente apertura del foramen oval. Se ha puesto especial énfasis en la persistencia de la válvula de Eustaquio prominente, la cual dirige el flujo de la vena cava inferior hacia el septum, tal cual lo hacía en la circulación fetal. Algunos autores hablan de la compresión del anillo tricuspídeo por la aorta dilatada, creando una suerte de estenosis tricuspídea. También se menciona la presencia de una AD pequeña, ocupada mayoritariamente por la raíz de aorta, como causa de aumento de presión en esta cavidad.
La vivencia de estos dos casos ciertamente dramáticos nos ha llevado a interesarnos en la fisiopatología de esta asociación cianosis/dilatación de aorta ascendente. En estudios ecocardiográficos y angiográficos frecuentemente se observa la horizontalización del corazón, consecuencia de la fuerza o tracción sobre él aplicada por aortas elongadas o dilatadas. En los casos en que existe un FOP con las características anatómicas adecuadas creemos que el crecimiento de la aorta vence la resistencia del corazón, como órgano en su conjunto, por el sector más débil, el septum interauricular. Este se deforma y se distorsiona permitiendo una apertura más amplia del FOP. Si no existe una alteración de las presiones auriculares habituales, no debería existir shunt importante de derecha a izquierda. En todo caso, por el contrario, estaríamos frente a un mayor cortocircuito de izquierda a derecha, similar a una comunicación interauricular. ¿Cuál es entonces el mecanismo responsable de la aparición del “shunt” en estos pacientes?
Planteamos como explicación unificada a este fenómeno que la debilidad y deformación de un septum interauricular con las características anatómicas predisponentes contribuye a que frente a un progresivo aumento de la dilatación o elongación de la aorta, este vaso protruya cada vez más hacia la AD, no solo ocupando su luz interior sino lentamente comprimiendo el anillo tricuspídeo. Ya que a nivel auricular se manejan presiones bajas, es suficiente con que exista un leve aumento del gradiente en el tracto de entrada del VD (dado por la estrechez del canal entre borde inferior y lateral del anillo tricuspídeo y la raíz de aorta protruyente) para que la presión en la AD se eleve por encima de la presión en la AI. Esto lleva a que la sangre tome preferencialmente por un camino amplio, de menor resistencia, hacia una AI con menor presión: el FOP. Se crea de esta manera un “shunt” amplio de derecha a izquierda, silencioso, sin soplos ni grandes hallazgos semiológicos excepto la cianosis. De alguna forma podemos decir que se vuelve a la circulación fetal, con la diferencia de que la sangre venosa que cruza el foramen oval no tiene oxígeno para compartir con los tejidos.
La mayor parte de los casos reportados en la literatura se caracterizan por presentar una exacerbación de la disnea y desaturación durante la posición ortostática, platipnea y ortodesoxia.Una de nuestras pacientes tenía tan marcada manifestación de esta característica que durante cinco años se mantuvo en cama. La explicación para este peculiar hallazgo parece estar en una mayor compresión del tracto de entrada del VD y/o una mayor apertura del FOP por los cambios de posición de los órganos torácicos durante la postura erecta. El resultado de los estudios puede en estos casos variar de acuerdo a la posición en la que se realizan y esto lleva a confusión en su interpretación (11). Nuestro segundo caso no tenía tal presentación. La severa “obstrucción tricuspídea” y la apertura fija del FOP en este último caso era tal que no se afectaba por los cambios posicionales. Su relativamente corta historia podría ser explicada por una muy rápida dilatación aórtica o un reciente cambio importante en la morfología del FOP.
En cuanto al tratamiento, ambos casos se solucionaron reemplazando la aorta ascendente y la válvula aórtica incompetente por tubo valvulado. Existen reportes en la literatura de cierre con éxito del FOP por dispositivo percutáneo (12). Si bien este método menos cruento puede resultar atractivo, en estos casos en particular, dada la patología de aorta y el escaso borde aórtico del FOP, creemos que se tomó la decisión correcta. Un dispositivo de cierre percutáneo quedaría apoyado sobre la pared aórtica patológica y seguramente mal orientado. Esto contribuiría a un mayor número de complicaciones intraprocedimiento y a posibles erosiones vasculares alejadas. Estamos convencidos, sin embargo, de que cada caso debe ser analizado individualmente para definir la mejor opción de tratamiento.
Conclusiones
La asociación de dilatación de raíz de aorta, apertura de foramen oval y compresión de anillo tricuspídeo por la propia raíz de aorta invadiendo el espacio de la AD es una causa muy poco frecuente de cianosis central, de difícil diagnóstico si no reconocemos sus características clínicas y ecocardiográficas. Nuestros casos son un claro ejemplo de ello. Dado que se presenta predominantemente en pacientes hipertensos de edad avanzada, es de esperar una incidencia cada vez mayor a medida que la población envejezca.
Destacamos el rol de la ecocardiografía en sus modos transtorácicos y transesofágicos como métodos de diagnóstico definitivo. Los técnicos deben familiarizarse con la característica imagen en el ETT de ocupación de la AD y compresión de anillo tricuspídeo por parte de una aorta ascendente dilatada o una aorta torácica desenrollada. El ETE es fundamental para definir con mayor claridad la anatomía del septum interauricular y de la aorta torácica. Es necesario además jerarquizar la importancia de la inyección de suero agitado en vía venosa periférica para detectar “shunts” a través del septum interauricular. Aquí los flujos son de baja velocidad y como consecuencia muchas veces no se identifican con Doppler color. Se recomienda en caso de duda la utilización de vías en miembros inferiores, ya que es el flujo de la vena cava inferior el que drena mayormente hacia la AI a través del FOP.
A nuestro entender es la primera vez que se plantea la teoría de la “herniación interna” en la AD de la aorta como mecanismo simultáneo de deformación de un SIA debilitado por FOP previo y de la consecuente y concomitante compresión del anillo tricuspídeo. Refutamos la teoría de flujo direccional preferencial como la explicación más probable de este fenómeno y planteamos la solución a este enigma fisiopatológico por un simple juego de presiones. A mayor resistencia en el tracto de entrada del VD, mayor cortocircuito a través del FOP.
Bibliografía
1. Savage EB, Benckart DH, Donahue BC, Casaday FM, Cho YD. Intermittent hypoxia due to right atrial compression by an ascending aortic aneurysm. Ann Thorac Surg 1996; 62: 582-3.
2. Al Khouzaie T, Busser JR. A rare cause of dyspnea and arterial hypoxemia. Chest 1997; 112: 1681-2.
3. Popp G, Melek H, Garnett AR. Platypnea-orthodeoxia related to aortic elongation. Chest 1997; 112: 1682-4.
4. Laybourn KA, Martin ET, Cooper RA, Holman WL. Platypnea and orthodeoxia: shunting associated with an aortic aneurysm. J Thorac Cardiovasc Surg1997; 113: 955-6.
5. Cheng TO. Platypnea-orthodeoxia syndrome: etiology, differential diagnosis, and management. Cathet Cardiovasc Interv. 1999; 47: 64-6.
6. Medina A, Suarez de Lezo J, Caballero E, Ortega JR. Platypnea-orthodeoxia due to aortic elongation (Abstract). Circulation 2001; 104: 741.
7. Cheng TO. Mechanisms of Platypnea-Orthodeoxia: What Causes Water to Flow Uphill? (Abstract).Circulation 2002, 105: e47
8. Eicher JC, Bonniaud P, Baudouin N, Petit A, Bertaux G, Donal E, et-al. Hypoxaemia associated with an enlarged aortic root: a new syndrome?. Heart. 2005; 91: 1030-5.
9. Pemberton J, Irvine T, Stewart MJ, Antunes G, Gibson GJ. Platypnoea orthodeoxia in a patient with aortic root dilatation and a patent foramen ovale. Eur Heart J Cardiovasc Imaging 2007; 8: 151-4
10. Baptista R, Marinho Da Silva A, Castro G, Monteiro P. Aneurisma da aorta ascendente e foramen ovale patente: uma causa rara de platipneia-ortodeóxia Rev Port Cardiol 2011; 30 : 445-50.
11. Nakahira A, Matsumura Y, Tatsumi H, Sasaki Y, Hirai H, Hanatani A, et al. Platypnea-Orthodeoxia Diagnosed by Sitting Transesophageal Echocardiography. Ann Thorac Surg 2010; 89: 1284-6.
12. Cheng TO. Transcatheter closure of patent foramen ovale: a definitive treatment for platypnea-orthodeoxia (letter). Cathet Cardiovasc Interv. 2000; 51: 120.