Services on Demand
Journal
Article
Related links
Share
Revista Uruguaya de Cardiología
On-line version ISSN 1688-0420
Rev.Urug.Cardiol. vol.26 no.3 Montevideo Dec. 2011
ARTÍCULO DE REVISIÓN
Valoración del riesgo operatorio en cirugía no cardíaca
DR. GUSTAVO JUNKER 1
1. Médico cardiólogo de Asociación Española 1ra de Scocorros Mutuos, CASMU, IMPASA, ASSE.
Recibido mayo 9, 2011; aprobado octubre 11, 2011.
PALABRAS CLAVE:
REVISIÓN
FACTORES DE RIESGO
CIRUGÍA
KEY WORDS:
REVIEW
RISK FACTORS
SURGERY
La valoración preoperatoria de pacientes que van a ser sometidos a cirugía no cardíaca constituye un motivo de consulta frecuente en la práctica cotidiana del cardiólogo. Dada la importancia del tema y el aporte que realizan dos nuevas guías internacionales referidas al tema, se realiza la presente revisión (1,2).
ESTRÉS QUIRÚRGICO
El estrés quirúrgico está determinado por el tipo de cirugía, envergadura, su duración, así como por los cambios de temperatura y recambio de fluidos producidos durante la misma, elementos estos que predisponen a los eventos cardíacos mayores (ECM). En base a ello se han establecido tres categorías de riesgo de infarto agudo de miocardio (IAM) y de muerte cardíaca a los 30 días luego de la cirugía (1,2):
1. Bajo riesgo (<1% de ECM): cirugías de piel, mama, ocular, dental, ginecológica, reconstructiva, ortopédica menor (rodilla), urológica menor.
2. Riesgo intermedio (1%-5% de ECM): cirugías con apertura de tórax o abdomen, de carótida, de cabeza y cuello, neurológica, ortopédica mayor (cadera/columna), renal, pulmonar, trasplante de hígado, urológica mayor.
3. Alto riesgo (>5% de ECM): aorta abdominal y vascular periférica.
Estas últimas intervenciones son de alto riesgo, lo que se asocia a su mayor potencial de variación hemodinámica y de recambio de fluidos, a lo que se agrega, en el caso de la cirugía vascular periférica, el riesgo incrementado debido a la mayor comorbilidad de estos pacientes.
Una vez establecido el riesgo que implica la cirugía a realizar, se debe definir la situación cardiovascular del paciente.
CONDICIONES CARDíACAS ACTIVAS
Mediante el interrogatorio y el examen físico se deben descartar situaciones que podrían obligar a diferir la cirugía, excepto que sea de emergencia, dado el alto riesgo vital. La presencia de una condición cardíaca activa, tal como coronariopatía inestable, insuficiencia cardíaca descompensada, trastorno severo de la conducción, arritmia significativa y valvulopatía severa (tabla 1), obliga a un manejo cuidadoso del paciente.
Si bien no existen ensayos clínicos randomizados al respecto, parece razonable esperar de cuatro a seis semanas luego de un IAM para realizar una cirugía electiva.
Los defectos severos de la conducción pueden ser una amenaza para la vida del paciente y requieren la colocación de marcapaso.
Las extrasístoles ventriculares asintomáticas y la taquicardia ventricular no sostenida se asocian a un incremento de ECM en el perioperatorio.
La estenosis aórtica severa es la valvulopatía con mayor riesgo en cirugía no cardíaca; si es sintomática y se realizará una cirugía electiva, esta debe ser pospuesta debiendo realizarse previamente el reemplazo aórtico. En pacientes con estenosis aórtica severa que rechazan la cirugía o no son candidatos a la misma, existen técnicas alternativas como la valvuloplastia con balón o la implantación valvular percutánea. De realizarse la cirugía sin corrección de la estenosis aórtica, la misma tiene una mortalidad de 10%.
En pacientes con estenosis mitral significativa, asintomáticos, y con presión sistólica pulmonar mayor de 50 mmHg, así como en pacientes sintomáticos (disnea progresiva, presíncope de esfuerzo, falla cardíaca), debe considerarse la corrección de la valvulopatía antes de la cirugía no cardíaca, especialmente en la de alto riesgo.
CAPACIDAD FUNCIONAL
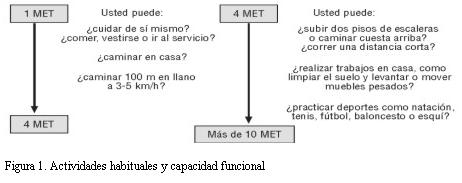
Es necesario establecer cuál es la capacidad funcional del paciente, dado que si en su actividad diaria éste realiza un esfuerzo ³ 4 MET, tolerará adecuadamente el estrés quirúrgico, siendo innecesarios estudios adicionales. En la figura 1 se presenta la equivalencia en MET de diferentes actividades de la vida diaria.
Los pacientes que desarrollan 4 MET en su vida diaria, aunque tengan cardiopatía, presentan baja probabilidad de desarrollar complicaciones con la cirugía, por lo que la misma puede ser realizada. Por el contrario, los individuos sedentarios o con mala capacidad funcional, más aun si tienen factores de riesgo para la cirugía, deben ser evaluados detalladamente.
En pacientes con cardiopatía isquémica la capacidad funcional permite definir el umbral isquémico, el que junto a la carga isquémica y a la función ventricular izquierda son los principales predictores de ECM vinculados a la cirugía.
Debe tenerse presente que solo se solicitarán aquellos estudios que puedan cambiar la conducta y que se indicarían independientemente de la cirugía, siendo conscientes de que la realización de los mismos puede retardar la cirugía durante semanas.
ÍNDICES Y PREDICTORES DE RIESGOS
Existen múltiples índices predictores de riesgo y morbilidad perioperatoria. El empleado en las guías norteamericanas es el Índice de Riesgo Cardíaco Revisado, considerado el que mejor predice el riesgo cardíaco en cirugía no cardíaca (3).
Este índice considera seis puntos:
1. Cirugía de alto riesgo (intratorácica, abdominal, vascular).
2. Cardiopatía isquémica (IAM, isquemia en estrés, angor, uso de nitratos, ondas Q en el electrocardiograma [ECG]).
3. IC congestiva (disnea, R3, estertores bilaterales, hipertensión venocapilar pulmonar en la radiografía de tórax).
4. Enfermedad cerebrovascular.
5. Uso de insulina en la diabetes.
6. Creatininemia > 2 mg/dl.
El riesgo de eventos es 0,4% con 0 punto; 0,9% con 1 punto; 6,6% con 2 puntos, y 11% con 3 o más puntos. En este índice se consideraron los IAM, edema pulmonar, fibrilación ventricular, paro cardíaco o bloqueo aurículo-ventricular (BAV) completo.
ESTUDIOS DE VALORACIóN CARDIOLóGICA
ELECTROCARDIOGRAMA
Si la cirugía es de bajo riesgo y se trata de pacientes asintomáticos, sin factores de riesgo clínicos, el ECG no aporta información adicional, por lo que no debe realizarse (clase III B). Su realización está indicada en cirugía de alto riesgo o de riesgo intermedio en pacientes con FRC (clase I B).
ECOCARDIOGRAMA
El valor predictivo del ecocardiograma es limitado, por lo que se recomienda solo en las cirugías de alto riesgo (clase IIA).
ESTUDIOS FUNCIONALES
Una investigación evaluó el impacto de los estudios funcionales en pacientes sometidos a cirugía electiva de aorta abdominal o vascular infrainguinal. En la misma, la incidencia de ECM varió de acuerdo a la presencia de FRC (edad > 70 años, angina, IAM previo, IC compensada, diabetes mellitus tratada, creatininemia > 1 mg/dl) (4,5). Al cabo de tres años los ECM fueron 15% en el grupo con ³ 3 FRC), 4% en el grupo con 1-2 y 0% en el grupo sin FRC. La realización de estudios funcionales a los pacientes de riesgo intermedio no modificó su pronóstico si se realizaba tratamiento b-bloqueante (6). Por ello no deben realizarse estudios funcionales a los pacientes que serán sometidos a cirugía de bajo riesgo o que no tienen FRC; por el contrario, los mismos estarían indicados en pacientes con cirugía de riesgo alto o intermedio con mala clase funcional y/o ³ 3 FRC.
REVASCULARIZACIóN PROFILáCTICA
El estudio CARP incluyó a 510 pacientes coronarios estables que iban a ser sometidos a cirugía electiva de aorta abdominal o periférica de alto riesgo (6). Antes de la cirugía vascular, los pacientes fueron distribuidos al azar a revascularización coronaria o tratamiento médico, existiendo la misma incidencia de complicaciones perioperatorias de la cirugía vascular entre ambos grupos. En el estudio DECREASE V, 101 pacientes con isquemia extensa que iban a ser sometidos a cirugía de aorta abdominal o a reconstrucción vascular infrainguinal, fueron randomizados a revascularización previa o no, recibiendo todos b-bloqueantes tratando de mantener la frecuencia cardíaca (FC) entre 60 y 65 latidos/min durante la cirugía (7). Al cabo de 30 días no existió diferencia en muerte o IAM entre los pacientes revascularizados y los no revascularizados antes de la cirugía vascular. De acuerdo a estos estudios, la angiografía coronaria con eventual revascularización no debe ser realizada de forma profiláctica en pacientes coronarios estables o con isquemia extensa tratados con b-bloqueantes.
Se ha observado que manteniendo la FC <60 cpm existe menor mortalidad, y que ella aumenta de forma exponencial al incrementarse la FC, lo que obedecería a menor isquemia y liberación de troponina (8).
El estudio DECREASE I, realizado en cirugía de alto riesgo en pacientes con compromiso isquémico que involucraba ³ 3 segmentos en el ecocardiograma de estrés, los distribuyó al azar a bisoprolol o placebo, observándose reducción de muerte o IAM con el b-bloqueante. En este estudio los b-bloqueantes se suministraron como mínimo una semana antes (media 37 días), a diferencia de otros estudios donde se administraron horas antes de la cirugía.
Un metaanálisis de b-bloqueantes en cirugía no cardíaca no mostró beneficio de su empleo, observándose beneficio solamente en el estudio en que se hizo titulación progresiva de la dosis hasta alcanzar la meta preestablecida de FC y presión arterial.
Un estudio observacional en pacientes de alto riesgo y de riesgo intermedio sometidos a cirugía vascular mostró que el uso de ß-betabloqueantes desde antes de una semana de la cirugía se asoció a menor mortalidad que cuando se los inició después (10).
De acuerdo a la evidencia disponible parece adecuado emplear estos fármacos en pacientes con isquemia documentada, los que van a ser sometidos a cirugía de alto riesgo o aquellos que los estuvieran tomando previamente. También podría considerarse su empleo en pacientes con cirugía de riesgo intermedio y varios FRC (11).
ANTIPLAQUETARIOS Y ANTICOAGULANTES
ASPIRINA
Un metaanálisis de 41 estudios que incluyeron 49.590 pacientes, comparó la interrupción versus la continuación de aspirina, existiendo un aumento de 1,5% de las complicaciones hemorrágicas, pero sin aumento de las hemorragias graves. En los pacientes con riesgo elevado o con cardiopatía isquémica la interrupción de la aspirina se asocia a un riesgo de eventos cardíacos graves tres veces mayor. Por lo tanto solo se debería suspender si el riesgo de hemorragia supera los beneficios cardíacos conocidos. Tampoco debe suspenderse el AAS previo a las cirugías menores o procedimientos endoscópicos. Frente a los sangrados se recomienda reponer con plaquetas u otros agentes hemostáticos.
ANTICOAGULANTES
La administración de anticoagulantes depende del riesgo trombótico del paciente, el que puede ser bajo, moderado o alto. Tienen bajo riesgo trombótico cuando hubo tromboembolismo pulmonar (TEP) >12 meses atrás, sin factores de riesgo (FR) adicionales; con fibrilación auricular escore CHADS 2 de 0 a 2, sin AIT ni ACV previo; y prótesis valvular aórtica bidisco sin fibrilación auricular ni otros FR para ACV (12).
Son pacientes de riesgo intermedio para tromboembolia quienes han tenido un TEP en los últimos 3 a 12 meses, TEP recurrente, condiciones trombofílicas no severas, cáncer activo, fibrilación auricular con escore CHADS 3 o 4, y válvula aórtica protésica con fibrilación auricular, AIT previo, ACV, hipertensión, diabetes, falla congestiva y edad mayor de 75 años.
Son pacientes de alto riesgo tromboembólico quienes han padecido un TEP reciente, trombofilia severa, fibrilación auricular con escore CHADS 2 de 5 o 6, o con AIT, ACV o cardiopatía reumática.
Los pacientes con válvulas mecánicas en posición mitral son de alto riesgo, así como los pacientes con válvulas aórticas antiguas de bola o monodisco.
En los pacientes de alto riesgo se recomienda la denominada terapia puente con dosis terapéuticas de heparina de bajo peso molecular (HBPM) o heparina no fraccionada (HNF), mientras que en los casos de riesgo moderado se puede optar, dependiendo del tipo de cirugía, por una dosis profiláctica (en caso de cirugía de alto riesgo de sangrado) o terapéutica (en bajo riesgo de sangrado).
La terapia puente implica, de acuerdo con Seventh American College of Chest Physicians Conference on Antithrombotic and Thrombolytic Therapy provides guidelines for outpatient management of anticoagulation therapy, la suspensión del AAS siete días antes y la warfarina cinco días antes del procedimiento; tres días antes iniciar la HBPM en una o dos dosis diarias según el riesgo tromboembólico establecido.
La última dosis de HBPM se debe dar 12 o 24 horas antes de la coordinación del procedimiento.
El día del procedimiento no se da ninguna medicación.
Al día siguiente se inicia warfarina en dosis habituales en forma simultánea con HBPM, hasta lograr INR en rangos, momento en que se suspende la HBPM.
Con respecto a dabigatran, no hay una guía establecida; solo la opinión de expertos.
En los pacientes de bajo riesgo puede no realizarse anticoagulantes o prescribir dosis profilácticas.
En los casos de utilización de terapia puente con HBPM, no debería darse la noche anterior a la cirugía, y en el caso de HNF debería suspenderse cuatro a seis horas antes del procedimiento. Se recomienda reiniciar la HBPM a las 24 horas del procedimiento y resolver con el cirujano actuante el eventual reinicio de la warfarina a las dosis habituales al otro día de la cirugía, realizando INR diario hasta llegar al valor deseado, discontinuando entonces la HBPM.
INTERVENCIÓN CORONARIA PERCUTÁNEA Y CIRUGÍA
Los pacientes con angioplastia tienen mayor riesgo de eventos cardíacos perioperatorios, existiendo hasta 20% de trombosis intrastent en el perioperatorio con la suspensión de los antiplaquetarios. Por esto se prefiere posponer la cirugía electiva un mínimo de seis semanas y hasta tres meses en los implantes de stents no liberadores de drogas manteniendo la aspirina. Con los stents liberadores de drogas se sugiere un tiempo de espera de al menos 12 meses, luego del cual se realiza la cirugía bajo aspirina.
En cuanto al clopidogrel se debe mantener, en lo posible, un mínimo de 12 meses de acuerdo a las guías vigentes, aunque se debe destacar que en el reciente congreso de la Sociedad Europea se presentó el estudio PRODIGY que comparó la prolongación del tratamiento dual antiplaquetario por 24 meses versus 6 meses y no se observaron diferencias netas, dado que no hubo diferencias en el punto final compuesto de eficacia: muerte, IAM, ACV o trombosis intrastent y sí hubo resultados favorables al plazo de seis meses en cuanto a menor riesgo por menos sangrados y reposición de sangre. Por lo que seguramente en el futuro se revisarán estos plazos.
Algunos autores recomiendan la utilización de HBPM o de inhibidores de las glicoproteínas IIb/IIIa como terapia alternativa frente a la suspensión de los antiplaquetarios en las cirugías que deban efectuarse antes de los plazos mencionados.
Si llega a ser necesaria la suspensión se recomienda cinco días para el caso del clopidogrel y siete días para el caso del AAS previo a la cirugía.
Como conclusiones, se pueden resumir los nuevos conceptos en estos puntos:
1. Valorando el tipo de cirugía asociado a un adecuado interrogatorio y examen físico con ECG se puede establecer con buen grado de aproximación el riesgo quirúrgico.
2. Sólo se justifican estudios funcionales en pacientes que van a cirugía de alto riesgo y que tienen mala clase funcional con múltiples factores de riesgo.
3. El uso de b-bloqueantes iniciados una semana antes de la cirugía en pacientes con isquemia miocárdica moderada a severa que van a cirugía de alto riesgo disminuye significativamente los ECM en el entorno de la cirugía.
4. Los pacientes anticoagulados que van a cirugía deberían recibir terapia puente con heparinas, según el riesgo tromboembólico preestablecido.
5. En pacientes con stents metálicos se debería mantener, siempre que sea posible y en acuerdo con el cirujano, el clopidogrel por un espacio de tiempo mínimo de tres meses de su implante y de 12 meses en el caso de stents con drogas, manteniéndose el AAS.
BIBLIOGRAFíA
1. Fleisher LA, Beckman JA, Brown KA, Calkins H, Chaikof E, Fleischmann KE, et al. American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines on Perioperative Cardiovascular Evaluation for Noncardiac Surgery); American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Rhythm Society; Society of Cardiovascular Anesthesiologists; Society for Cardiovascular Angiography and Interventions; Society for Vascular Medicine and Biology; Society for Vascular Surgery. ACC/AHA 2007 guidelines on perioperative cardiovascular evaluation and care for noncardiac surgery. Circulation 2007; 116(17): e418–e499, pmid:17901357
2. Poldermans D, Bax J, Boersma E, De Hert S, Eeckhout E, Fowkes G, et al. Guía de práctica clínica para la valoración del riesgo cardiaco preoperatorio y el manejo cardiaco perioperatorio en la cirugía no cardiaca. Rev Esp Cardiol 2009; 62: 1467. e1-e56
3. Lee TH, Marcantonio ER, Mangione CM, Thomas EJ, Polanczyk CA, Cook EF, et al. Derivation and Prospective Validation of a Simple Index for Prediction of Cardiac Risk of Major Noncardiac Surgery. Circulation 1999; 100: 1043-9.
4. Poldermans D, Bax JJ, Schouten O, Neskovic AN, Paelinck B, Rocci M, et al. Should Major Vascular Surgery Be Delayed Because of Preoperative Cardiac Testing in Intermediate-Risk Patients Receiving Beta-Blocker Therapy With Tight Heart Rate Control? J Am Coll Cardiol 2006; 48: 964–9.
5. Poldermans D, Schouten O, Bax JJ, Winkell T. Reducing cardiac risk in non-cardiac surgery: evidence from the DECREASE studies. Eur Heart J Supplements (2009) 11 (Supplement A), A9–A14.
6. McFalls EO, Ward HB, Moritz TE, Goldman S, Krupski WC, Littooy F, et al. Coronary-Artery Revascularization before Elective Major Vascular Surgery. N Engl J Med 2004; 351: 2795-804.
7. Poldermans D, Schouten O, Vidakovic R, Bax JJ, Thomson IR, Hoeks SE, et al. A Clinical Randomized Trial to Evaluate the Safety of a Noninvasive Approach in High-Risk Patients Undergoing Major Vascular Surgery. The DECREASE-V Pilot Study. J Am Coll Cardiol 2007; 49: 1763-9.
8. Feringa HH, Bax JJ, Boersma E, Kertai MD, Meij SH, Galal W, et al. High-dose beta-blockers and tight heart rate control reduce myocardial ischemia and troponin T release in vascular surgery patients. Circulation 2006; 114: I344-9.
10. Poldermans D, Boersma E, Bax JJ, Thomson IR, Paelinck B, Ven LL, et al. Bisoprolol reduces cardiac death and myocardial infarction in high-risk patients as long as 2 years after successful major vascular surgery. Eur Heart J 2001; 22: 1353-8.
11. Flu WJ, van Kuijk JP, Chonchol M, Winkel TA, Verhagen HJ, Bax JJ, et al. Timing of pre-operative beta-blocker treatment in vascular surgery patient. J Am Coll Cardiol 2010; 56: 1922-9.
12. Lindenauer PK, Pekow P, Wang K, Mamidi DK, Gutierrez B, Benjamin EM. Perioperative beta-blocker therapy and mortality after major noncardiac surgery. N Engl J Med 2005; 353: 349-61.
13. Douketis JD, Berger PB, Dunn AS, Jaffer AK, Spyropoulos AC, Becker RC, et al. The Perioperative Management of Antithrombotic Therapy: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th edition). Chest 2008; 133: 299S-399S.