Services on Demand
Journal
Article
Related links
Share
Revista Uruguaya de Cardiología
On-line version ISSN 1688-0420
Rev.Urug.Cardiol. vol.23 no.2 Montevideo Sept. 2008
Trabajo original
Amiodarona como profilaxis de la fibrilación auricular en el postoperatorio de cirugía cardíaca
DRES. JAVIER IRIGOIN 1, YANINA ZÓCALO 2, JORGE POUSO 3, GONZALO VARELA 4,
DANIEL BIGALLI 5, NICOLÁS RUSSO 6, OMAR MONTES DE OCA 7, WALTER REYES CAORSI 8
1. Postgrado de Cardiología, becario del Centro Cardiovascular Casa de Galicia.
2. Asistente del Departamento de Fisiología, Facultad de Medicina, Universidad de la República. Postgrado de Cardiología, becario del Centro Cardiovascular Casa de Galicia.
3. Jefe de Estadística del Departamento de Cardiología de Casa de Galicia.
4. Ex asistente del Departamento de Cardiología del Hospital de Clínicas.
5. Cirujano Cardíaco, jefe de Cirugía Cardíaca de CICU.
6. Coordinador de Insuficiencia Cardíaca y Transplante de CICU.
7. Coordinador de la Unidad de Cuidados Intensivos de CICU.
8. Ex Profesor Adjunto de Cardiología, jefe del Servicio de Electrofisiología de Casa de Galicia.
Servicio de Electrofisiología de Casa de Galicia, Centro de Investigación Cardiovascular del Uruguay (CICU).
Correspondencia: Dr. Javier Irigoin. General Espartero 1489. Montevideo. Correo electrónico:javoirigoin@adinet.com.uy
RESUMEN
La fibrilación auricular (FA) es la arritmia más común del postoperatorio de cirugía cardíaca. Genera morbilidad y aumenta los tiempos de internación y costos hospitalarios. Múltiples estudios randomizados han demostrado la eficacia de la amiodarona en su profilaxis. En nuestro servicio se comenzó a utilizar un protocolo de profilaxis de FA postoperatoria con amiodarona intravenosa.
Objetivo: analizar la factibilidad de este protocolo en la práctica clínica habitual, luego de un año de iniciado.
Material y método: se consideraron todos los pacientes intervenidos desde octubre de 2006 a setiembre de 2007. De los pacientes elegibles para recibir la profilaxis (n=272), ésta se comenzó en 67% (n=183). Se administró amiodarona intravenosa comenzando en las primeras 24 horas de postoperatorio con una dosis mínima de 1 gramo. Se determinó la incidencia acumulada de FA para los pacientes con y sin profilaxis, y la estadía hospitalaria para los mismos pacientes, y para aquellos con y sin FA.
Resultados: la mediana de seguimiento fue de 32 días. De los pacientes que iniciaron el protocolo, 27% (49/183) debieron suspenderlo. La incidencia acumulada de FA fue de 28% (77/272) para los pacientes elegibles. La incidencia acumulada de FA fue menor para los pacientes tratados con amiodarona. El tiempo de internación fue significativamente menor en los pacientes que recibieron amiodarona y en los que no presentaron FA.
Conclusiones: el protocolo fue factible en dos terceras partes de los pacientes intervenidos, si bien se completó en la mitad. La incidencia de FA continúa siendo elevada en la población elegible. Los pacientes que recibieron amiodarona tuvieron menor incidencia de FA y menores tiempos de internación.
PALABRAS CLAVE:
AMIODARONA
FIBRILACIÓN AURICULAR
CIRUGíA CARDíACA
SUMMARY
Atrial fibrillation (AF) is the most frequent arrhythmia in the post-operative period of cardiac surgery. It generates morbidity and increases hospital length of stay and costs. Multiple randomized trials have shown the efficacy of amiodarone in the prophylaxis of AF. In our institution, a postoperative AF prophylaxis protocol with intravenous amiodarone is taking place.
Aims: to analyze the feasibility of this protocol in the regular clinical practice, one year after it started.
Methods: from October 2006 to September 2007, all patients who underwent open heart surgery were considered. Prophylaxis was started in 67% (183/272) of eligible patients. Intravenous amiodarone was started in the first 24 hours with a target dose of at least 1 g. Cumulative incidence of AF was calculated for patients with and without prophylaxis. Length of stay was calculated for the same groups of patients and for those with and without AF.
Results: median of follow-up was 32 days; the protocol had to be interrupted in 27% (49/183) of patients. Cumulative incidence of AF was 28% (77/272) in the eligible population. Cumulative incidence of AF was lower in patients who received amiodarone. Length of stay was significantly shorter in patients treated with amiodarone and in those without AF.
Conclusions: prophylaxis protocol was feasible in two thirds of patients undergoing open heart surgery, but it was completed in half of them. The incidence of AF persists high in eligible patients. Patients who received amiodarone had fewer incidence of AF and shorter length of stay.
KEY WORDS:
AMIODARONE
ATRIAL FIBRILLATION
CARDIAC SURGERY
INTRODUCCIóN
La fibrilación auricular (FA) es la arritmia más frecuente del postoperatorio de cirugía cardíaca (POCC) (1). La incidencia reportada varía de 20% a más de 50% (2), debido en parte a las diferencias metodológicas de los trabajos que la han estudiado. Esta incidencia elevada se ha mantenido a pesar de la evolución en las técnicas quirúrgicas (1,3). Ocurre con mayor frecuencia durante el segundo y tercer día del postoperatorio y suele ser transitoria y autolimitada (1,3).
La importancia de la FA en el POCC radica fundamentalmente en que se asocia a mayor morbilidad (4,5), y a que aumenta el tiempo de internación y los costos hospitalarios (4,6-10).
No se conoce la etiopatogenia de la FA en el POCC, si bien se han identificado factores de riesgo para su desarrollo. Entre ellos se destacan: la edad avanzada, el sexo masculino, el antecedente de FA, la cirugía valvular, patologías asociadas como la enfermedad pulmonar crónica y la enfermedad vascular periférica (6-13). El contexto en que ocurre hace que su profilaxis y manejo sean complejos y a menudo de diseño individual. Múltiples estudios han sido llevados a cabo con el fin de disminuir su incidencia. Estos estudios incluyen el uso de sotalol y otros agentes â-bloqueantes, antiarrítmicos como propafenona y amiodarona, suplemento de magnesio, la estimulación auricular y más recientemente el uso de estatinas (14-17).
Respecto a la amiodarona existen estudios que han la han utilizado en forma oral o intravenosa, pre y postoperatoria, y que han demostrado reducir en forma significativa la incidencia de FA cuando se la compara con placebo (18-22).
Teniendo en cuenta esto último, el Servicio de Cirugía Cardíaca de Casa de Galicia (Centro de Investigación Cardiovascular Uruguayo, CICU) conjuntamente con el Servicio de Electrofisiología, desarrollaron un protocolo de profilaxis de FA en el POCC, utilizando amiodarona intravenosa. El objetivo de este trabajo es determinar la factibilidad y los efectos de dicho protocolo en la práctica clínica habitual, luego de un año de haberse comenzado a utilizar.
MATERIAL Y MéTODO
PACIENTES
Se consideraron todos los pacientes intervenidos consecutivamente en el Servicio de Cirugía Cardíaca de Casa de Galicia (CICU), entre los meses de octubre de 2006 y setiembre de 2007 (n= 295).
Se definieron criterios de exclusión preoperatorios para la aplicación del protocolo de profilaxis con amiodarona (tabla 1). Las causas de exclusión preoperatorias fueron las siguientes: FA permanente (n=9), cirugía de FA (n=1), tratamiento con amiodarona (n=1). Los pacientes sin criterios de exclusión preoperatorios se consideraron elegibles para iniciar el protocolo de profilaxis. Los criterios de exclusión postoperatorios (tabla 1) se aplicaron al ingresar el paciente a la unidad de cuidados intensivos postoperatorios (UCIPo) y durante las primeras 24 horas.
TABLA 1. CRITERIOS DE EXCLUSIóN Y SUSPENSIóN PARA RECIBIR PROFILAXIS CON AMIODARONA INTRAVENOSA
Para el análisis de los resultados se excluyeron los pacientes con criterios de exclusión preoperatorios (n=11), los pacientes fallecidos en las primeras 24 horas del postoperatorio (n=8) y los pacientes en los que no se pudo obtener la información completa de la historia clínica (n=4).
Las características de los pacientes elegibles para recibir profilaxis (n=272) fueron las siguientes: edad media 63±10 años, sexo masculino 65% (177/272), cirugías de revascularización miocárdica aislada 67% (182/272); uso de â-bloqueantes en el preoperatorio 59% (160/272); fracción de eyección del ventrículo izquierdo (FEVI) media 54±11%.
De los pacientes elegibles a recibir la profilaxis, 33% (89/272) presentaron criterios de exclusión postopertorios (tabla 2).
Para los pacientes incluidos se definieron criterios de suspensión de la profilaxis (tabla 1). La distribución de los pacientes se muestra en la figura 1.
FIGURA 1. Distribución de los pacientes intervenidos en el período octubre 2006 a setiembre de 2007.
SEGUIMIENTO
Se realizó el seguimiento clínico de los pacientes hasta el alta quirúrgica (mediana de 32 días).
PROTOCOLO DE PROFILAXIS
El protocolo de profilaxis consistió en la administración de amiodarona intravenosa en infusión continua, comenzando en forma tan precoz como fuese posible durante las primeras 24 horas del postoperatorio. El ritmo de infusión inicial fue de 42 mg/h durante 24 horas (1.008 mg), continuando a 30 mg/h hasta completar 48 horas de infusión (1.728 mg), o hasta el alta de la UCIPo. La dosis mínima objetivo fue de 1.000 mg. Si el paciente completaba 1.000 mg y cumplía con las condiciones para ser dado de alta de la UCIPo, la administración de amiodarona se suspendía (esto no se consideró como criterio de suspensión).
MONITORIZACIóN ELECTROCARDIOGRáFICA
Se realizó monitorización electrocardiográfica continua y con electrocardiograma (ECG) seriado durante la internación en la UCIPo, mientras que en sala se realizó ECG en forma diaria y ante la presencia de síntomas o signos sugestivos de arritmia. Los controles en policlínica hasta el alta quirúrgica incluyeron la realización de ECG de 12 derivaciones.
DIAGNóSTICO DE FA
El contexto clínico y de monitoreo en que se realizó el protocolo y se efectuó el diagnóstico de FA fue en todo similar al de la práctica clínica habitual de los meses previos del servicio.
El diagnóstico de FA fue realizado por el médico responsable del sector (intensivista, cardiólogo, residente de cardiología) y documentado con ECG. El diagnóstico fue corroborado por el equipo médico encargado de la recolección de los datos. Se definió como caso incidente todo paciente en el que se diagnosticara por lo menos un episodio de FA, de manera que se consideraron número de casos incidentes y no episodios de FA.
VALORACIóN DEL OBJETIVO
La factibilidad se estimó utilizando como indicadores las proporciones de pacientes excluidos en el preoperatorio y postoperatorio.
El efecto de la intervención se estimó por medio de la incidencia acumulada de FA, la tasa de incidencia de FA y la mediana de los días de internación.
CONSIDERACIONES ESTADíSTICAS
La aplicación del protocolo de profilaxis y los criterios de exclusión dividieron naturalmente la población objetivo en tres estratos de intervención.
Un grupo sin profilaxis compuesto por los pacientes excluidos en el postoperatorio.
Un grupo con profilaxis incompleta integrado por aquellos pacientes que iniciaron la profilaxis pero debieron suspenderla.
Un grupo con profilaxis completa formado por pacientes en que se aplicó el protocolo en tiempo y forma.
La frecuencia del diagnóstico FA se determinó mediante la incidencia acumulada (IA) en el período y la tasa de incidencia (TI, persona.día-1) para toda la población y cada uno de los estratos antes mencionados.
Se calculó la duración de la estadía hospitalaria a través de la mediana de los días de internación luego de la cirugía para todos los pacientes y cada estrato de profilaxis, y para los pacientes con y sin diagnóstico de FA. Para la comparación de los resultados se utilizó la prueba de la U de Mann-Whitney. En todos los casos a=0,05.
RESULTADOS
De 272 pacientes elegibles, fueron incluidos 183 (67%). La profilaxis pudo completarse en 134 (73%) de ellos.
La bradicardia sinusal fue la principal causa de suspensión, alcanzando 61% (30/49) (tabla 2).
La incidencia acumulada de casos de FA en la población elegible fue de 28% (IC95%: 23-34%). Los pacientes incluidos presentaron una incidencia acumulada de FA de 21% (IC95%: 15-27%), siendo de 15% (IC95%: 9-21%) en el grupo profilaxis completa y de 37% (IC95%: 24-41%) en el grupo de profilaxis incompleta. En el grupo sin profilaxis la IA de FA fue de 44% (IC95%: 33-53%) (figura 2).
FIGURA 2. Incidencia acumulada de FA en el POCC distribuida según estratos de profilaxis. *post.: postoperatorio
Las tasas de incidencia de FA postoperatoria fueron de un caso cada 218 días-paciente para el grupo profilaxis completa; un caso cada 89 días-paciente para el grupo profilaxis incompleta, y un caso cada 75 días-paciente para el grupo sin profilaxis.
La mediana de internación fue de 7 días para los pacientes incluidos, y de 9 días para el grupo sin profilaxis, p=0,001. Esta diferencia se mantiene para los grupos de profilaxis completa (7 días) e incompleta (7 días) respecto al grupo sin profilaxis (9 días), p=0,002 y p=0,022, respectivamente.
Los pacientes en los que se diagnosticó FA en el postoperatorio presentaron una internación más prolongada que aquellos que no la tuvieron, con una mediana de 11 versus 7 días, p=0,00.
Entre los pacientes con diagnóstico de FA, no hubo diferencias significativas en el tiempo de internación entre los estratos de profilaxis.
DISCUSIóN
La FA es la complicación arrítmica más común del POCC. Al ser causa de morbilidad y aumentar los tiempos de internación y costos hospitalarios, aquellas acciones tendientes a disminuirla podrían tener fuerte impacto en los resultados de los servicios de cirugía cardíaca. A pesar de la multiplicidad de estrategias empleadas, su manejo continúa siendo dificultoso. Parece claro que la administración de agentes â-bloqueantes en pacientes sin contraindicaciones es recomendable. Esta indicación es clase I para las últimas guías de manejo de FA (2), si bien no se especifica en qué momento ni por qué vía administrarlos. Con respecto al uso de amiodarona, como puede observarse en la tabla 3, en distintos estudios que la han comparado con placebo se obtuvo una reducción significativa en la incidencia de FA (18-22).
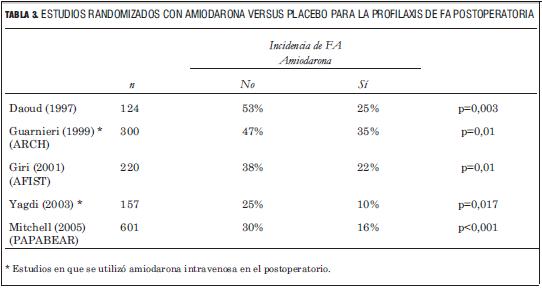
La recomendación actual respecto al uso de amiodarona en el POCC se refiere a pacientes con alto riesgo de desarrollar FA, administrándola en forma preoperatoria y por vía oral (clase IIa) (2). Esta recomendación se fundamenta principalmente en dos estudios randomizados que compararon amiodarona con placebo, administrada por vía oral e iniciada al menos seis días antes de la cirugía (18,22). Por su metodología, ambos estudios excluyeron los pacientes intervenidos de urgencia o emergencia.
Estos esquemas de uso de amiodarona por vía oral tendrían la ventaja de evitar algunos de los efectos hemodinámicos y cronotrópicos negativos de la amiodarona intravenosa. Sin embargo, son poco prácticos y no permiten ser utilizados en todos los pacientes intervenidos.
En nuestro caso se propuso desarrollar un protocolo que fuese aplicable al mayor número posible de pacientes intervenidos, incluyendo las urgencias y emergencias, para lo cual se descartaron los esquemas de administración preoperatoria. Debido a que la FA ocurre con mayor frecuencia en los primeros días del postoperatorio con un pico máximo en el segundo día (2,3), se estableció que la profilaxis debía comenzar precozmente en el postoperatorio (primeras 24 horas). Si bien la administración de β-bloqueantes se utiliza en nuestro servicio como profilaxis antiarrítmica, su uso durante las primeras horas del postoperatorio es limitado. Teniendo en cuenta todo lo anterior y siguiendo esquemas similares (20), es que se eligió a la amiodarona como agente antiarrítmico a utilizar en las primeras horas del postoperatorio, administrándola por vía intravenosa y en infusión continua para lograr efectos clínicos en menor tiempo. Debido a que es deseable la administración de este fármaco por vía venosa central, y teniendo en cuenta la mayor ocurrencia de la FA en los primeros días del postoperatorio, se pensó en un esquema de breve duración que fuese empleado en la UCIPo.
El protocolo comenzó a utilizarse en octubre de 2006 y hasta setiembre de 2007 pudo iniciarse en dos terceras partes de los pacientes, y completarse en la mitad. La incidencia acumulada de diagnóstico de FA en ese período fue de 28% (IC 95%: 23-34%). La menor incidencia se observó en los pacientes que completaron el protocolo y la mayor en aquellos que no lo recibieron.
En un estudio randomizado que incluyó 300 pacientes, Guarnieri y colaboradores investigaron el efecto de la amiodarona intravenosa contra placebo en la incidencia de FA en el POCC (20). Se utilizó un esquema similar al utilizado por nuestro grupo (1 g por vía intravenosa en 24 horas durante las primeras 48 horas del postoperatorio). La incidencia de FA en toda la población fue de 41%. El grupo tratado con amiodarona presentó una reducción significativa en la incidencia de FA respecto al grupo placebo (20).
Como puede deducirse de la figura 1 y de la tabla 2, se obtuvo un porcentaje elevado (51%) de pacientes con criterios de exclusión o suspensión de amiodarona, en su mayor parte debido a bradicardia sinusal y BAV. Si tenemos en cuenta que a todos los pacientes sometidos a cirugía cardíaca del servicio se les colocan electrodos transitorios epicárdicos, es probable que el número de pacientes que pudieron haber recibido amiodarona fuese mayor si a los pacientes con bradicardia o BAV se les hubiese estimulado externamente al mismo tiempo que se continuase la infusión de amiodarona como fue realizado en el estudio ARCH (20). Sin embargo, en esta primera experiencia se prefirió considerarlos como criterios de exclusión/suspensión.
Por otro lado, los criterios de suspensión de la infusión de amiodarona no deben interpretarse exclusivamente como efectos colaterales del fármaco. Debe tenerse en cuenta, por ejemplo, que los episodios de hipotensión arterial son comunes en el POCC independientemente del uso de amiodarona.
Cuando se analizan las características clínicas de los pacientes que presentaron contraindicaciones para iniciar la profilaxis con amiodarona, puede observarse que se trata de una población con más factores de riesgo de FA que aquellos que sí la recibieron. Las características de ambos grupos de pacientes se ilustran en la tabla 4.
Como puede observarse, quienes no recibieron amiodarona fueron pacientes de mayor edad, sometidos con más frecuencia a cirugía valvular o de aorta, y recibieron con menos frecuencia b-bloqueantes en el preoperatorio. Estos hechos se asocian a mayor riesgo de FA en el postoperatorio.
Por otra parte, los pacientes sometidos a cirugía valvular presentan con más frecuencia trastornos de conducción auriculoventricular, por lo que es esperable que esta población complete el protocolo con menor frecuencia que los pacientes coronarios.
En la tabla 5 se muestran las características clínicas y el porcentaje de profilaxis con amiodarona de los pacientes con y sin FA en el POCC. Puede observarse que los pacientes que desarrollaron FA eran más añosos, con mayor porcentaje de hombres, mayor porcentaje de cirugías no coronarias y recibieron profilaxis con amiodarona en menor proporción que los que no tuvieron FA (51% y 74%, respectivamente).
Como fue mencionado anteriormente, uno de los inconvenientes principales de la ocurrencia de FA en POCC es que por sí misma aumenta el tiempo de internación y los costos hospitalarios, como ha sido demostrado en múltiples estudios (4,6,7,10,21,23,24). En nuestro caso, los pacientes que desarrollaron FA tuvieron un aumento significativo del tiempo de internación, independientemente de haber recibido profilaxis.
Al analizar los estratos de profilaxis, los pacientes con profilaxis completa y profilaxis incompleta tuvieron un tiempo de internación menor que los pacientes sin profilaxis.
Por lo tanto, la presencia de FA o la ausencia de profilaxis se asociaron con mayor tiempo de internación, si bien por la metodología de este estudio, no podemos establecer una relación de causalidad.
LIMITACIONES
Este estudio muestra los resultados de la aplicación de un protocolo de profilaxis de FA en el POCC, en el que se utiliza un fármaco antiarrítmico que ha demostrado ser eficaz para este propósito. El protocolo se diseñó para ser aplicado al mayor número de pacientes intervenidos en el servicio. Debido a que no hubo una randomización de pacientes, no contamos con un grupo control. La comparación de la incidencia y la tasa de incidencia de FA, así como del tiempo de internación, se realiza entre poblaciones con características clínicas diferentes, por lo tanto no se pueden atribuir estos resultados al efecto de la amiodarona.
CONCLUSIONES
En condiciones clínicas habituales, el protocolo propuesto fue factible en dos terceras partes de los pacientes, si bien pudo realizarse en forma completa sólo en la mitad. El alcance del protocolo estuvo limitado principalmente por la bradicardia sinusal y los trastornos de conducción auriculoventricular.
La incidencia de la FA postoperatoria en la población elegible continúa siendo alta.
Si bien la incidencia de FA y el tiempo de internación fueron menores en aquellos pacientes en los cuales se realizó la profilaxis, no se puede concluir que haya sido por efecto de la amiodarona.
Deben desarrollarse estrategias diferentes de profilaxis, principalmente para aquellos pacientes de mayor riesgo de desarrollar FA.
BIBLIOGRAFíA
1. Sanjuán Mañez R, Blasco Cortés M, Carbonell Monleón NE, Carrera Hueso JA, Belda Nacher FJ. Fibrilación auricular post-cirugía cardíaca: mecanismos, factores predictivos, prevención y tratamiento. En: Otero Coto E, Rufilanchas Sánchez JJ, Belda Nacher FJ, editores. Riesgo y complicaciones en cirugía cardíaca. Madrid: Panamericana; 2004. p. 255-69.
2. ACC/AHA/ESC 2006 Guidelines for the Management of Patients UIT Atrial Fibrillation. Circulation 2006; 114: e257-e354.
3. Hogue C, Creswell L, Gutterman D, Fleisher L. Epidemiology,Mechanisms and Risks. American College of Chest Physisians Guidelines for the Prevention and Management of PostoperativeAtrial Fibrillation After Cardiac Surgery.Chest 2005; 128: 9S-16S.
4. Villareal R, Hariharan R, Liu B, Kar B, Lee V, Mc Arthur E, et al. Clinical Research: Complications of Bypass Surgery. J Am Coll Cardiol 2004; 43: 742-8.
5. Creswell L, Schuessler R, Rosenbloom M, Cox J. Hazards of postoperative atrial arritmias. Ann Thorac Surg 1993; 56: 539-49.
6. Aranki S, Shaw D, Adams D, Rizzo R, Couper G, VanderVielt M, Collins J, Cohn L, Burstin H. Predictors of atrial fibrillation after coronary artery surgery. Current trends and impact on hospital resources. Circulation 1996; 94: 390-7.
7. Mathew J, ParksR, Savino J, Friedman A, Koch C, Mangano D, et al. Atrial fibrillation following coronary artery bypass surgery: predictors, outcomes and resource utilization. JAMA 1996; 276: 300-6.
8. Borzak S, Tisdale J, Amin A, Goldberg A, Frank D, Padhi I, et al. Atrial fibrillation after bypass surgery: does the arrhythmia or the characteristics of the patients prolong hospital stay? Chest 1998; 113: 1489-91.
9. Tamis-Holland J, Kowalski M, Rill V, Firoozi K, Steinberg J. Patterns of Atrial Fibrillation After Coronary Artery Bypass Surgery. Ann Noninvasive Electrocardiol 2006; 11: 139-44.
10. Auer J, Weber T, Berent R, Ng C, Lamm G, Eber B. Postoperative Atrial Fibrillation Independently Predicts Prolongation on Hospital Stay After Cardiac Surgery. J Cardiovascular Surg 2005; 46: 583-8.
11. Funk M, Richards S, Desjardins J, Bebon C, Wilcox H. Incidence,Timing,Symptoms and Risk Factorsfor Atrial Fibrillation After Cardiac Surgery. Am J Crit Care 2003; 12: 424-33.
12. Hayashida N, Shojima T, Yokokura Y, Hori H, Yoshikawa K, Tomoeda H, et al. P-wave Signal-Averaged Electrocardiogram for Predicting Atrial Arrhytmia Alter Cardiac Surgery. Ann Thorac Surg 2005; 79: 859-64.
13. Amar D, Shi W, Hogue C, Zhang H, Passman R, Thomas B. Clinical Prediction Rule for Atrial Fibrillation After Coronary Artery Bypass grafting. J Am Coll Cardiol 2004; 44: 1248-53.
14. Bradley D, Creswell L, Hogue C, Epstein A, Prystowsky E, Daoud E. Pharmacologic prophylaxis. American College of Chest Physisians Guidelines for the Prevention and Management of PostoperativeAtrial Fibrillation After Cardiac Surgery.Chest 2005; 128: 39S-47S.
15. Maisel W, Epstein A. The role of cardiac pacing. American College of Chest Physisians Guidelines for the Prevention and Management of PostoperativeAtrial Fibrillation After Cardiac Surgery.Chest 2005; 128: 36S-38S.
16. Levy T, Fotopoulos G, Walker S, Rex S, Octave M, Paul V, et al.Randomized controlled study investigating the effect of biatrial pacing in prevention of atrial fibrillation after coronary artery bypass surgery. Circulation 2000; 102: 1382-7.
17. Marin F, Pascual D, Arribas J, Ahumada M, Tornel P,Oliver C, et al.Statins and postoperative risk of atrial fibrillation following coronary artery bypass grafting. Am J Cardiol 2006; 97: 55-60.
18. Daoud E, Strickberger A, Man C, Goyal R, Deeb M, Bolling S, et al. Preoperative Amiodarone as Prophylaxis against Atrial Fibrillation after Heart Surgery. N Eng J Med 1997; 337: 1785-91.
19. Giri S, White CM, Dunn A, Felton K, Freeman-Bosco L, Reddy P, et al. Oral Amiodarona for prevention of atrial fibrillation after open heart surgery, the Atrial Fibrillation Suppression Trial (AFIST): a randomized placebo controlled trial. Lancet 2001; 357: 830-6.
20. Guarnieri T, Nolan S, Gottlieb S, Dudek A, Lowry D. Intravenous Amiodarone for the Prevention of Atrial Fibrillation After Open Heart Surgery: The Amiodarona Reduction in Coronary Heart (ARCH) Trial. J Am Coll Cardiol 1999; 34: 343-7.
21. Yagdi T, Nalbantgil S, Ayik F, Apaydin A, Islamoglu F, Posacioglu H, et al. Amiodarone reduces the incidence of atrial fibrillation after coronary artery bypass grafting. J Thorac Cardiovasc Surg. 2003; 125: 1420-5.
22. Mitchel L, Exner D, Wyse D, Connolly C, Prystai G, Bayes A, et al. Prophylactic Oral Amiodarone for the Prevention of Arrhythmias That Begin After Revascularization, Valve Replacement, or Repair. PAPABEAR a Randomized Controlled Trial. JAMA 2005; 294: 3093-100.
23. Gillespie E, White CM, Kluger J, Rancourt J, Gallagher R, Coleman C. Cost-effectiveness of amiodarone for prophylaxis of atrial fibrillation after cardiothoraci surgery. Pharmacotherapy 2006; 26: 499-504.
24. Borzak S, Tisdale J, Amin N, Goldberg A, Frank D, Padhi I, et al. Atrial fibrillation after bypass surgery: does the arrhythmia or the characteristics of the patients prolongs hospital stay? Chest 1998; 113: 1489-91.















