Services on Demand
Journal
Article
Related links
Share
Revista Uruguaya de Cardiología
On-line version ISSN 1688-0420
Rev.Urug.Cardiol. vol.22 no.2 Montevideo Sept. 2007
ARTíCULO ORIGINAL
Incidencia de la fibrilación auricular poscirugía de revascularización miocárdica: asociación con uso de circulación extracorpórea
DRES. JAVIER IRIGOIN 1, YANINA ZóCALO 2, ZULY CORTELLEZZI 1, VERóNICA GONZáLEZ 1,
WALTER REYES CAORSI 3, GONZALO VARELA 4, NICOLáS RUSSO 5, FAVIO GUTIéRREZ 6,
OMAR MONTES DE OCA 7, JORGE POUSO 8, DANIEL BIGALLI 9
2. Asistente (Grado 2), Departamento de Fisiología, Facultad de Medicina, Universidad de la República. Postgrado de Cardiología, becario del Centro Cardiovascular Casa de Galicia.
3. Ex Profesor Adjunto de Cardiología, Jefe del Servicio de Electrofisiología de Casa de Galicia.
4. Ex-Asistente del Depto. de Cardiología de la Facultad de Medicina, Cardiólogo del Servicio de Electrofisiología de Casa de Galicia.
5. Coordinador de Insuficiencia Cardíaca y Trasplante de CICU.
6. Profesor Adjunto de Cirugía Cardíaca, Cirujano Cardíaco de CICU.
7. Coordinador de la Unidad de Cuidados Coronarios de CICU.
8. Jefe de Estadística del Departamento de Cardiología de Casa de Galicia.
9. Cirujano Cardíaco, Jefe de Cirugía Cardíaca de CICU.
Centro de Investigación Cardiovascular Uruguayo (CICU).
Servicio de Electrofisiología de Casa de Galicia.
Correspondencia: Dr. Javier Irigoin. General Espartero 1489. Montevideo, Uruguay. Correo electrónico: javoirigoin@adinet.com.uy
Recibido abril 16, 2007; aceptado agosto 13, 2007.
RESUMEN
La fibrilación auricular (FA) es una de las complicaciones más frecuentes en el postoperatorio de cirugía de revascularización miocárdica (CRM). Identificar los factores de riesgo asociados con la FA post CRM podría contribuir al conocimiento de su fisiopatología y al desarrollo de estrategias de prevención adecuadas. Distintos estudios han evaluado la relación de la FA post CRM con factores quirúrgicos, como el uso de circulación extracorpórea. Los resultados obtenidos son controversiales.
Objetivo: determinar la incidencia del diagnóstico de FA en el postoperatorio de CRM, estratificada según el uso o no de circulación extracorpórea.
Material y método: se determinó la incidencia del diagnóstico de FA en pacientes a los que se les realizó primera cirugía de revascularización miocárdica, de coordinación, entre los años 1995 y 2004 (n=2.459). Se estratificó la incidencia de FA, según el uso o no de circulación extracorpórea.
Resultado: el riesgo relativo (RR, IC 95%) de FA acumulada (con circulación extracorpórea) en el período abril de 1995 a diciembre de 2004 fue de 1,57 (1,18-2,02). Los RR anuales muestran valores en general por encima de 1, pero sus IC 95% no permiten rechazar la hipótesis nula.
Conclusión: el uso de circulación extracorpórea se asoció con mayor incidencia de diagnóstico de FA en el postoperatorio de CRM, aunque con escaso significado clínico.
PALABRAS CLAVE:
FIBRILACIÓN AURICULAR
REVASCULARIZACIÓN MIOCÁRDICA
CIRCULACIÓN EXTRACORPÓREA
SUMMARY
Atrial fibrillation (AF) is one of the most common complications in the post-operative period of coronary artery bypass grafting. The detection of the risk factors for the development of post-operative AF could help to understand its physiopathology, and to develop useful prevention strategies. Many studies have assessed the relation between postoperative AF and surgical factors as the use of cardiopulmonary bypass. The studies’ results differ.
Aims: to assess the incidence of the diagnosis of AF in the postoperative period of coronary artery bypass surgery, and its relation with the use of cardiopulmonary bypass.
Methods: incidence of the diagnosis of AF was calculated in patients undergoing first and elective coronary artery bypass surgery from April 1995 to December 2004 (n=2459). Incidence of AF was calculated for patients undergoing on-pump and off-pump coronary artery bypass grafting. Results: The cumulative relative risk (CI 95%) of AF with on-pump surgery is 1.57 (1.18-2.02). The annual relative risks showed values over 1, but the confidence intervals did not allow rejecting the null hypothesis.
Conclusion: the use of cardiopulmonary bypass was associated to an increased incidence in the diagnosis of postoperative AF, although with poor clinical significance.
KEY WORDS:
ATRIAL FIBRILLATION
MYOCARDIAL REVASCULARIZATION
EXTRACORPOREAL CIRCULATION
INTRODUCCIóN
La fibrilación auricular (FA) es la arritmia más común en el postoperatorio de cirugía cardíaca. La incidencia descrita en la literatura se encuentra entre el 10% y el 65% de los pacientes intervenidos. Esta variabilidad puede explicarse, al menos parcialmente, por diferencias en las poblaciones estudiadas y las estrategias metodológicas empleadas. En una revisión reciente se describe una incidencia global de 26,7% (1), reconociéndose que cuando se trata de cirugía de revascularización miocárdica (CRM) aislada, la incidencia es menor que en el caso de cirugía valvular o combinada (1,3).
La importancia de la FA en el postoperatorio de cirugía cardíaca radica fundamentalmente en que por sí misma prolonga el tiempo de internación, con el consiguiente aumento de los costos hospitalarios (4-10). Por otra parte, se ha asociado a mayor morbilidad, principalmente relacionada a accidentes cerebrovasculares, compromiso hemodinámico y requerimiento de anticoagulación (1,3,10,11). Finalmente, algunos trabajos han encontrado un aumento en la mortalidad en los pacientes que presentan FA en el postoperatorio de cirugía cardíaca (8,10).
La etiopatogenia de esta arritmia en el contexto del postoperatorio de cirugía cardíaca no se conoce. Se plantea que existen en el miocardio auricular áreas con diferente refractariedad, favorecidas por múltiples factores, como la inflamación por manipulación auricular (cuando se realiza atriotomía y canulación venosa), isquemia y distensión del músculo auricular, disionías y cambios del medio interno, descarga adrenérgica y uso de fármacos simpaticomiméticos (12-14). Estudios dirigidos a identificar factores de riesgo para el desarrollo de FA han encontrado asociación con la edad, el sexo masculino, la cirugía valvular o combinada, el antecedente de FA, el tiempo de circulación extracorpórea y la historia de insuficiencia cardíaca, entre otros (4-9,15-17).
Desde que comenzó a utilizarse en forma más amplia la CRM sin circulación extracorpórea se ha sugerido que su utilización se asociaría a una menor tasa de FA en el postoperatorio. Sin embargo, los trabajos en los que se estudió esta asociación muestran resultados discordantes (18-22).
Sabiendo que desde el punto de vista clínico la significación estadística no contesta todas las preguntas a responder (una asociación estadísticamente significativa puede no ser clínicamente relevante y, además puede no ser causal), y que podemos encontrar asociaciones estadísticamente posibles y conceptualmente estériles, el objetivo de este trabajo fue determinar la incidencia del diagnóstico de FA postoperatoria en una población de pacientes sometidos a primer cirugía de by-pass coronario de elección, según el uso de circulación extracorpórea. La población a estudiar fue elegida por considerarla de menor riesgo de morbilidad y mortalidad postoperatoria.
MATERIAL Y MéTODO
Se realizó un estudio observacional utilizando la base de datos del servicio (SUMMIT, The Society of Thoracic Surgeons-STS). Los datos se recogieron en forma prospectiva durante la internación del paciente y hasta el alta quirúrgica (generalmente a los 30 días de la cirugía). Se incluyeron todos los pacientes sometidos a primera cirugía de revascularización, de elección, en el período comprendido entre abril de 1995 y diciembre de 2004. Los pacientes en los que se inició la cirugía sin circulación extracorpórea, pero que durante el procedimiento la requirieron (conversión), se incluyeron en el grupo con circulación extracorpórea. Aquellos pacientes que presentaban FA en el preoperatorio fueron excluidos.
Se utilizó la definición de FA establecida por la STS para la base de datos (23). El diagnóstico de FA se realizó en las condiciones clínicas habituales, esto es, con monitorización electrocardiográfica continua durante la internación en el área de cuidados intensivos, y con electrocardiograma diario y seguimiento clínico durante el resto de la internación y el seguimiento en policlínica. Por lo tanto, los episodios de FA diagnosticados fueron aquellos clínicamente evidentes.
CONSIDERACIONES ESTADíSTICAS
a) Tasas de incidencia y riesgo relativo
Se determinó la tasa de incidencia anual acumulada del diagnóstico de FA en todas las CRM de elección, a través del cociente de nuevos casos de diagnóstico de FA en esta clase de cirugías y el total anual de las mismas (24). Del mismo modo se calculó la incidencia del diagnóstico de FA en las CRM de elección sin CEC. La razón de ambas tasas permitió calcular el riesgo relativo (RR) de FA en CRM de elección, considerando como potencial factor de riesgo la CRM de elección con CEC, con su correspondiente IC95% a través de las series de Taylor (25), donde H0 = 1. Finalmente se determinaron las correspondientes tasas de incidencia acumulada del diagnóstico de FA en CRM de elección, con y sin CEC, en el decenio 1995-2004, con sus correspondientes IC95% para la proporción según la estimación cuadrática de Fleiss (26) y teniendo en cuenta el efecto de diseño (27) en un modelo de conglomerados. Con los datos de RR anuales y el acumulado del decenio se construyó la figura 2.
b) Comparaciones de tasas
Dada la variabilidad de los denominadores anuales y la alta posibilidad de error b las comparaciones se establecieron según el criterio de RR y de los IC95% correspondientes de las proporciones según estuviera o no presente el atributo considerado como factor de riesgo. Igual criterio se utilizó con las comparaciones de tasas en el decenio.
También se procedió a la determinación de: a) la reducción de riesgo absoluto de FA en las cirugías sin CEC, a través de la diferencia entre las tasas de incidencia con y sin circulación extracorpórea. En base a ella se estimó el número de pacientes (primera CRM, de elección) que habría que operar sin CEC para evitar un caso de diagnóstico de FA (1/reducción de riesgo absoluto), y b) la reducción proporcional del riesgo relativo como complemento a 1 del RR obtenido al considerar la cirugía sin CEC como factor de riesgo, por 100.
RESULTADOS
En el período de estudio se realizaron 2.459 cirugías de revascularización coronaria de elección. La edad media de la población estudiada fue de 63,5±9,4 años. El 74,2% de los pacientes fue de sexo masculino. A 482 (19,5%) pacientes se les diagnosticó nuevo episodio de FA en el postoperatorio. Los pacientes que desarrollaron FA tuvieron una edad media de 66,9±7,9 años. Se realizaron 2.109 cirugías utilizando bomba de circulación extracorpórea. En este grupo, 432 (20,5%) pacientes presentaron FA. De los 350 pacientes intervenidos sin circulación extracorpórea, 50 (14%) desarrollaron FA (figura 1). La edad de los pacientes que desarrollaron FA fue de 66,8±7,8 y 67,7±8,7 años para los operados con y sin circulación extracorpórea, respectivamente.
Figura 1. Población sometida a primera CRM, de elección entre abril de 1995 y diciembre de 2004. Se muestra la tasa de incidencia acumulada del diagnóstico de fibrilación auricular (FA) en el postoperatorio. CRM: cirugía de revascularización miocárdica, CEC: circulación extracorpórea.
Las incidencias anuales acumuladas, con el IC95% para cada proporción del diagnóstico de fibrilación auricular en el período considerado, se muestran en la figura 2. El RR acumulado de FA luego de la CRM con CEC fue de 1,57 (IC 95%; 1,18-2,02), como se muestra en la figura 3.
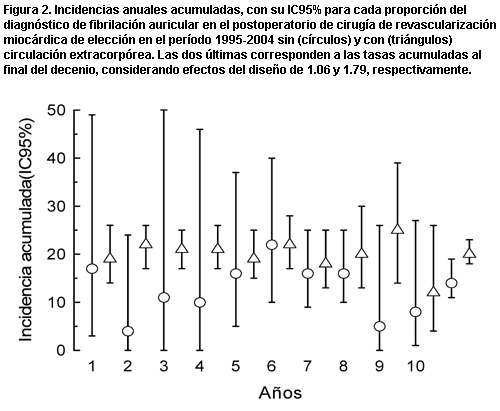
Figura 2. Incidencias anuales acumuladas, con su IC95% para cada proporción del diagnóstico de fibrilación auricular en el postoperatorio de cirugía de revascularización miocárdica de elección en el período 1995-2004 sin (círculos) y con (triángulos) circulación extracorpórea. Las dos últimas corresponden a las tasas acumuladas al final del decenio, considerando efectos del diseño de 1.06 y 1.79, respectivamente.
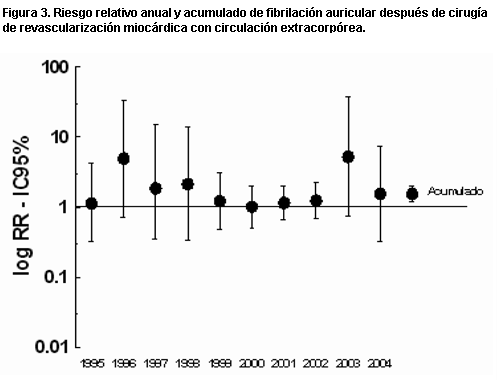
Figura 3. Riesgo relativo anual y acumulado de fibrilación auricular después de cirugía de revascularización miocárdica con circulación extracorpórea.
La reducción absoluta de riesgo fue de 6,5% (cada 100 personas operadas sin CEC evitamos casi siete nuevos casos de diagnóstico de FA) y, por lo tanto, habría que operar a 15 pacientes (CRM primera operación de elección) sin CEC para evitar un nuevo caso de FA en el postoperatorio.
DISCUSIóN
La FA es la arritmia más frecuente en el postoperatorio de cirugía cardíaca. Su incidencia no ha disminuido a pesar de los avances en las técnicas quirúrgicas y en los cuidados postoperatorios. Incluso se ha descrito un paradójico aumento de la FA, que podría explicarse, al menos parcialmente, por cambios en las características de la población que se opera y en las técnicas de monitoreo y diagnóstico. En este estudio, realizado en 2.459 pacientes sometidos a CRM de elección, en un período de diez años, la incidencia del diagnóstico de FA fue de 19,5%, similar a la descrita en la bibliografía (1). El RR acumulado para el desarrollo de FA postoperatoria en los pacientes sometidos a circulación extracorpórea fue de 1,57 (IC 95% 1,18-2,02). La edad de los pacientes que desarrollaron FA fue similar en los dos grupos (CRM con y sin CEC).
Se han descrito diferentes factores de riesgo para el desarrollo de FA en el postoperatorio de cirugía cardíaca, algunos de ellos directamente relacionados con el tipo de cirugía y la técnica quirúrgica utilizada. El uso de la bomba de CEC en la cirugía coronaria se ha propuesto como uno de los factores de riesgo para el desarrollo de FA. Esto se explicaría porque la CEC expondría al paciente a los factores que se plantea contribuyen a la génesis de la arritmia (atriotomía, isquemia y distensión auricular, mayor requerimiento de fármacos inotrópicos). Sin embargo, los estudios realizados para determinar la incidencia de la FA y su relación con la CEC han mostrado resultados dispares (tabla 1). En un estudio con distribución aleatoria, prospectivo, que incluyó 70 pacientes sometidos a cirugía coronaria con y sin CEC, Mariscalco y colaboradores no encontraron diferencias en la incidencia de FA entre los grupos (p=0,797) (18). Asimismo, Marasco y colaboradores, en un estudio retrospectivo observacional, compararon 80 pacientes sometidos a primera CRM, electiva sin CEC y 80 pacientes, de similares características, intervenidos con CEC y no encontraron diferencias significativas en la incidencia de FA entre los dos grupos (p=0,74) (19). Finalmente, en un estudio observacional, Salamon y colaboradores no encontraron diferencias en la incidencia de FA postoperatoria al comparar 252 pacientes sometidos a CRM sin CEC, con 841 pacientes, con similar número de by-pass realizados, pero intervenidos con CEC (8,8% versus 9,4%) (20). Por el contrario, Panesar y colaboradores, en un metaanálisis de pacientes mayores de 70 años sometidos a CRM, encontraron una menor incidencia de FA en el grupo intervenido sin CEC (OR 0,77, IC 95% 0,61-0,97), si bien al analizar individualmente los estudios incluidos no hubo diferencias significativas en 10 de 11 estudios (21). Banach y colaboradores, en un estudio que incluyó 1.200 pacientes, encontraron el uso de CEC como predictor de FA postoperatoria, mientras que el no uso de CEC se identificó como un factor de protección (22).
Como se puede observar en la tabla 1, fueron los estudios con menor número de pacientes los que no mostraron diferencias significativas en la incidencia de FA entre pacientes intervenidos con CEC y aquellos en los que no se utilizó CEC. Algo similar se puede observar al analizar los datos obtenidos en este estudio. Como se muestra en la figura 3, los RR anuales no mostraron diferencias significativas entre el grupo de pacientes intervenidos con CEC y aquellos sin CEC. Sin embargo, cuando se incluyeron todos los pacientes y se calculó el RR acumulado, se observó una diferencia significativa entre los grupos. Esto probablemente indica que la no utilización de CEC tiene cierto beneficio en relación con el desarrollo de FA en el postoperatorio, que adquiere significancia sólo cuando el número de pacientes es alto (figuras 3 y 4).
Figura 4. Evolución del RR de FA considerando como factor de riesgo la cirugía con CEC, desde 1995 a 2004, a medida que se acumulan las CRM, representadas dentro del gráfico en bastardilla. Son necesarios nueve años, 2.391 CRM para alcanzar significación estadística de beneficio de la CRM sin CEC. CEC: circulación extracorpórea; CRM: cirugía de revascularización miocárdica; FA: fibrilación auricular en el postoperatorio.
La CRM sin CEC tiene múltiples beneficios en el período postoperatorio, y, entre ellos, podría estar la disminución de la FA, como se muestra en este trabajo. En este sentido, la no utilización de CEC podría considerarse uno de los mecanismos por los que se podría reducir la incidencia de FA en el postoperatorio. De todas maneras, es evidente que entre los factores que determinan la utilización o no de CEC no se encuentra el riesgo de desarrollar FA en el postoperatorio, y, además, no todos los pacientes pueden ser operados sin CEC. En este estudio el porcentaje de pacientes intervenidos sin CEC fue de sólo 14%, pero se debe tener en cuenta que están incluidos años en los cuales el uso de esta técnica no se había popularizado. En la medida en que la experiencia en esta técnica aumente, es probable que en los próximos años crezca la proporción de pacientes intervenidos sin CEC.
SIGNIFICADO CLíNICO
La relevancia clínica de un fenómeno va más allá de cálculos aritméticos y está determinada por el juicio clínico. Depende, entre otros elementos, de la magnitud de la diferencia encontrada, la gravedad del problema investigado, la vulnerabilidad, la morbimortalidad generada por el mismo, su costo y su frecuencia. La reducción relativa del riesgo es una medida de utilidad en el cálculo de la relevancia clínica. Reducciones del riesgo relativo de 50% casi siempre y de 25% con frecuencia, son consideradas como clínicamente relevantes (28,29), independientemente de la significación estadística. En este estudio se evidenció que en nuestro servicio las CRM primera operación, de elección, sin CEC, significaron una reducción relativa de riesgo de FA de 32%.
Para finalizar, considerando la situación actual, parece claro que de aplicarse alguna medida de profilaxis de FA postoperatoria, deberá hacerse para todos los pacientes, independientemente de la técnica quirúrgica empleada, valorando el riesgo-beneficio de la medida a adoptar, sabiendo que los pacientes sometidos a circulación extracorpórea podrían obtener mayor beneficio.
LIMITACIONES
Entre las limitaciones de este estudio se encuentran las de ser un estudio observacional y el hecho de que no se realizó el ajuste de variables confundentes. Si bien esta última es una limitación importante, el ajuste de otras variables excede el objetivo del estudio. De todas maneras, la edad, el factor de riesgo que más se ha vinculado con el desarrollo de FA en el postoperatorio de cirugía cardíaca, no mostró diferencia significativa entre los pacientes de los grupos estudiados.
CONCLUSIONES
La incidencia del diagnóstico de FA post CRM obtenida en nuestro centro fue de 19,5%, similar a la descrita en la bibliografía. Los RR anuales no permiten rechazar la hipótesis nula, por lo que no podríamos concluir que el uso de CEC se asocia a mayor FA en el postoperatorio de CRM. Sin embargo, el RR acumulado para el desarrollo de FA en el postoperatorio de CRM con uso de CEC fue de 1,57 (IC 95%; 1,18-2,02). Como se puede observar, el intervalo de confianza se encuentra por encima del 1, aunque muy próximo a él. Para una enfermedad con una alta incidencia, como es la FA en el postoperatorio de CRM, estos intervalos de confianza no nos permiten establecer una relación de causalidad.
BIBLIOGRAFíA
1. Mc Keown P. Introduction. American College of Chest Physisians guidelines for the prevention and management of postoperative atrial fibrillation after cardiac surgery. Chest 2005; 128: 6S-8S.
2. Daoud E, Strickberger A, Man C, Goyal R, Deeb M, Bolling S, et al. Preoperative amiodarone as prophylaxis against atrial fibrillation after heart surgery. N Engl J Med 1997; 337: 1785-91.
3. Creswell L, Schuessler R, Rosenbloom M, Cox J. Hazards of postoperative atrial arritmias. Ann Thorac Surg 1993; 56: 539-49.
4. Aranki S, Shaw D, Adams D, Rizzo R, Couper G, VanderVielt M, et al. Predictors of atrial fibrillation after coronary artery surgery. Current trends and impact on hospital resources. Circulation 1996; 94: 390-7.
5. Mathew J, Parks R, Savino J, Friedman A, Koch C, Mangano D, et al. Atrial fibrillation following coronary artery bypass surgery: predictors, outcomes and resource utilization. JAMA 1996; 276: 300-6.
6. Borzak S, Tisdale J, Amin A, Goldberg A, Frank D, Padhi I, et al. Atrial fibrillation after bypass surgery: does the arrhythmia or the characteristics of the patients prolong hospital stay? Chest 1998; 113: 1489-91.
7. Tamis-Holland J, Kowalski M, Rill V, Firoozi K, Steinberg J. Patterns of atrial fibrillation after coronary artery bypass surgery. Ann Noninvasive Electrocardiol 2006; 11(2): 139-44.
8. Banach M, Rysz J, Drozdz J, Okonski P, Misztal M, Barylski M, et al. Risk factors of atrial fibrillation following coronary artery bypass grafting. A preliminary report. Circulation Journal 2006; 70: 438-41.
9. Auer J, Weber T, Berent R, Ng C, Lamm G, Eber B. Postoperative atrial fibrillation independently predicts prolongation on hospital stay after cardiac surgery. J Cardiovascular Surg 2005; 46(6): 583-8.
10. Villareal R, Hariharan R, Liu B, Kar B, Lee V, Mc Arthur E, et al. Clinical research: complications of bypass surgery. J Am Coll Cardiol 2004; 43: 742-8.
11. Ommen S, Odell J, Stanton M. Atrial arrhytmias after cardiothoracic surgery. N Engl J Med 1997; 336: 1429-34.
12. Hogue C, Creswell L, Gutterman D, Fleisher L. Epidemiology, mechanisms and risks. American College of Chest Physisians guidelines for the prevention and management of postoperativeatrial fibrillation after cardiac surgery. Chest 2005; 128: 9S-16S.
13. Ishii Y, Schuessler R, Gaynor S, Yamada K, Fu A, Boineau J, et al. Inflammation of atrium alter cardiac surgery is associated with inhomogeneity of atrial conduction and atrial fibrillation. Circulation 2005; 111: 2881-8.
14. Tselentakis E, Woodford E, Chandy J, Gaudette G, Saltman A. Inflammation effects on the electrical propertiesof atrial tissue and inducubility of postoperative atrial fibrillation. J Surg Res 2006 Sep; 135(1): 68-75.
15. Funk M, Richards S, Desjardins J, Bebon C, Wilcox H. Incidence, timing, symptoms and risk factors for atrial fibrillation after cardiac surgery. Am J Crit Care 2003; 12: 424-33.
16. Hayashida N, Shojima T, Yokokura Y, Hori H, Yoshikawa K, Tomoeda H, et al. P-wave signal-averaged electrocardiogram for predicting atrial arrhytmia alter cardiac surgery. Ann Thorac Surg 2005; 79: 859-64.
17. Amar D, Shi W, Hogue C, Zhang H, Passman R, Thomas B. Clinical prediction rule for atrial fibrillation after coronary artery bypass grafting. J Am Coll Cardiol 2004; 44: 1248-53.
18. Mariscalco G, Engstrom K, Ferrarese S, Cozzi G, Bruno V, Sessa F, et al. J Thorac Cardiovasc Surg 2006; 131(6): 1364-72.
19. Marasco S, Goldblatt J, McDonald M, Tatoulis J. No Decrease in Incidence of Atrial Fibrillation in Patients Undergoing Off-Pump Coronary Artery Bypass Grafting. Heart Lung Circ 2002; 11(2): 102-6.
20. Salamon T, Michler R, Knott K, Brown D. Off-pump coronary artery bypass grafting does not decrease the incidence of atrial fibrillation. Ann Thorac Surg 2003; 75: 505-7.
21. Panesar S, Athanasiou T, Nair S, Rao C, Jones C, Nicolaou M, et al. Early outcomes in the eldery: a meta-anlisis of 4921 patients undergoing coronary artery bypass grafting-comparison between off-pump and on-pump techniques. Heart 2006; 92: 1808-16.
22. Banach M, Rysz J, Drozdz J, Okonski P, Misztal M, Barylski M, et al. Risk factors of atrial fibrillation following coronary artery bypass grafting. Circ J 2006; 70: 438-41.
23. STS Adult cardiac database definition of terms versión 2.41. [monografía en línea]: Society of Thoracic Surgeons. Disponible en: http://www.sts.org/file/CoreDef241Book.pdf (Consultado 24/8/07).
24. Hennekens CH, Buring JE. Mayrent Epidemiology in medicine. Boston: Little, Brown: 77-96, 254-7.
25. Bernard PM, Lapointe C. Mesures statiques en épidemiologie. Quebec: Press de l' Université du Quebec, 1987; 2861.
26. Fleiss JL.Statistical methods for rates and proportions. 2nd ed :John Wiley & Sons; 1981: 14-15.
27. Lemeshow S. Sampling terchniques for evaluating health parameters in developing countries. A working paper, Atlanta: Departament of Health and Human Services, CDC,1988: 7-81.
28. Silva Ayçaguer LC. Cultura estadística e investigación científica en el campo de la salud: una mirada crítica. Madrid: De Díaz Santos, 1997: 43-57.














