Services on Demand
Journal
Article
Related links
Share
Revista Uruguaya de Cardiología
On-line version ISSN 1688-0420
Rev.Urug.Cardiol. vol.20 no.1 Montevideo May 2005
Cierre percutáneo de la fenestración en cirugía de Fontan-Kreutzer
DRES. PEDRO CHIESA 1, CARLOS PELUFFO 1, PEDRO DUHAGÓN 1, JAVIER GIÚDICE 2,
RAFAEL ANZÍBAR 3, JORGE TAMBASCO 3, RUBEN LEONE 3, R CANESSA 4, S GELÓS 4, JORGE MORALES 4
2. Pediatra.
3. Cirujano cardíaco.
4. Cardiólogo. Ecocardiografista.
Instituto de Cardiología Infantil
Correspondencia: Instituto de Cardiología Infantil. Montevideo, Uruguay
E-mail: icardinf@adinet.com.uy
Los autores agradecen al Departamento de enfermería del ICI. Téc. Neumocardióloga Daniela Denegri. Asistente en Informática Elizabeth Izquierdo. Bibliotecóloga Elena Campiotti.
RESUMEN
La fenestración del túnel cavopulmonar forma parte de la táctica operatoria en la cirugía de Fontan-Kreutzer. En la evolución alejada puede suceder que no se produzca su cierre espontáneo, determinando un cortocircuito hacia la aurícula sistémica con la consiguiente desaturación arterial de oxígeno.
Se presenta la experiencia del Instituto de Cardiología Infantil en el cierre percutáneo de la fenestración permeable en cuatro pacientes con este tipo de cirugía mediante la utilización del dispositivo oclusor Amplatzer ASD.
Todos eran portadores de cardiopatías congénitas con circulación univentricular, que fueron sometidos a derivación cavopulmonar total, y que presentaron a mediano plazo desaturación arterial sistémica de oxígeno. El ecocardiograma Doppler color reveló la existencia en todos los casos de una fenestración permeable con importante cortocircuito a su nivel. El cateterismo cardíaco permitió confirmar que esta era la causa de la desaturación arterial de O2, descartando otras causas de hipoxemia.
Utilizando la técnica para el cierre percutáneo de la comunicación interauricular se procedió a ocluir la fenestración mediante implante de un dispositivo oclusor Amplatzer ASD, con notable ascenso de la saturación arterial de oxígeno y sin cambios en la presión del sistema cavopulmonar.
No tuvimos complicaciones. El alta fue otorgada a las 18 hs de efectuado el procedimiento.
En suma, la oclusión de la fenestración quirúrgica mediante cateterismo cardíaco está indicada cuando la misma constituye la causa fundamental de desaturación en la evolución de la cirugía de Fontan-Kreutzer. El procedimiento resulta práctico, eficaz, con breve período de internación y escasa agresión sicofísica para el paciente.
PALABRAS CLAVE:
CATETERISMO CARDÍACO
PROCEDIMIENTO DE FONTAN
DISPOSITIVOS PARA SOPORTE CARDÍACO
SUMMARY
Cavopulmonary tunnel fenestration is involved in the Fontan-Kreutzer surgical technique. In the long-term, spontaneous closure might not take place, leading to a shunt to the systemic atrium, therefore causing arterial oxygen desaturation. We present the experience of the Institute of Pediatric Cardiology in percutaneous closure of permeable fenestration, with four patients who underwent this procedure, using the ASD Amplatzer occluder device. All patients had congenital heart disase with univentricular physiology, underwent total cavopulmonary anastomosis and showed signs of arterial oxygen desaturation in the medium-term follow-up. Color Doppler echocardiography revealed in all cases the existence of a fenestration with a significant right to left shunt. Cardiac catheterization lead to the confirmation of this as the cause of the arterial oxygen desaturation, as other causes of hypoxemia were discarded.
Using the percutaneous closure of the atrial septal defects approach, we then occluded the fenestration through the implantation of an ASD Amplatzer occluder device, which was followed by a remarkable increase in arterial oxygen saturation and no changes for the cavopulmonary systemic pressure, No complications were observed. The patients were discharged home 18 hours after the procedure was performed. In conclusion, percutaneous closure of surgical fenestrations is suggested when such fenestration represents the prime cause of oxygen desaturation in postoperative Fontan-Kreutzer patients. This procedure has shown to be practical, effective, represents a brief in-hospital stay and reduced psycho-physical aggression for the patient.
KEY WORDS:
HEART CATHETERIZATION
FONTAN PROCEDURE
HEART-ASSIST DEVICES
INTRODUCCIÓN
En el periodo neonatal, las cardiopatías congénitas complejas con fisiología univentricular presentan una gran diversidad anatómica, la cual a su vez condiciona el plan terapéutico inicial (1). Además del tratamiento médico de la insuficiencia cardíaca y el mantenimiento de la permeabilidad ductal con el uso de las prostaglandinas en los casos de circulación ductus dependiente, se plantean diversas opciones quirúrgicas paliativas (2).
Una vez sorteada esta etapa y llegado el momento de la cirugía “correctiva-paliativa-definitiva” se deben realizar las cirugías de derivación cavopulmonar (3-7), las que se suceden en dos etapas, una primera de derivación de la circulación venosa sistémica de vena cava superior a la arteria pulmonar y posteriormente una segunda etapa para completar la derivación de la sangre venosa sistémica de vena cava inferior (cirugía de Fontan-Kreutzer) a la circulación arterial pulmonar mediante la tunelización intra o extra cardíaca, habitualmente acompañada de la creación de una fenestración ó perforación en dicha pared que funcione a modo de descompresión de la circulación cavopulmonar en el postoperatorio inmediato. En la evolución debe ocurrir el cierre espontáneo; si esto no sucede, la fenestración puede ser una de las causas de la desaturación arterial que suele observarse en estos pacientes. El cateterismo terapéutico se ha empleado con éxito para solucionar este problema (8-12).
Se muestra la experiencia del Instituto de Cardiología Infantil en el cierre de la fenestración en la cirugía de Fontan-Kreutzer, mediante el implante percutáneo de dispositivos oclusores Amplatzer ASD (AGA Medical Corporation, Golden Valley, MN USA).
MATERIAL Y MÉTODO
Cuatro pacientes que cursaban el postoperatorio alejado de cirugía de Fontan-Kreutzer fueron llevados a cateterismo cardíaco por presentar desaturación arterial de oxígeno sistémica. El ecocardiograma Doppler color mostraba función normal del ventrículo único y demostraba la presencia de una fenestración del tunel intraauricular con shunt significativo hacia la aurícula sistémica.
Las características de la población estudiada se muestran en la tabla 1.
El cateterismo cardíaco se realizó bajo anestesia general e intubación orotraqueal con ventilación asistida. Las vías de acceso fueron arterial y venosa femoral en todos los casos, obtenidas por punción transcutánea. A todos se les realizó heparinización sistémica con heparina sódica a 100 U/K. Se realizó medición de presión a nivel de todo el sistema cavo-pulmonar y angiografías de los sectores vena cava superior y vena cava inferior para descartar conexiones venovenosas que deriven sangre desde el sector cavopulmonar hacia la circulación sistémica y confirmar la presencia de una fenestración permeable con cuantificación del shunt de sangre desaturada hacia la aurícula sistémica. En el primer caso se requirió del apoyo del ecocardiograma transesofágico.
Una vez confirmado el diagnóstico se procedió a realizar el cierre de la fenestración utilizando la técnica descrita para el cierre de la comunicación interauricular (13-16) empleando dispositivos Amplatzer ASD, que se caracterizan por ser autoexpandibles, conformados por dos discos unidos entre sí por un núcleo central (cuyo tamaño determina el tamaño del dispositivo) fabricados con Nitinol (aleación de níquel y titanio) rellenos con un material de poliéster (figura 1), eligiéndose el tamaño correspondiente mediante la medición realizada con un catéter-balón. En todos los casos se observó que la presión en el sistema cavo pulmonar no se modificaba al realizar la maniobra de oclusión transitoria del defecto, antes de decidir el implante del dispositivo.
FIGURA 1. Dispositivos Amplatzer ASD. A: dispositivo desplegado con sus tres componentes y sostenido por el cable de liberación. B: dispositivo ubicado en posición correcta ocluyendo el defecto septal. C: despliegue del dispositivo por el operador previo a su ensamble.
El implante de cada dispositivo fue realizado con éxito, sin incidentes.
Se realiza profilaxis antibiótica con cefradina. Se mantiene bajo antiagregación plaquetaria con ácido acetilsalicílico.
El alta fue otorgada con un promedio de 18 horas de internación. No se presentaron complicaciones.
DESCRIPCIÓN DE LOS CASOS CLÍNICOS
PACIENTE 1
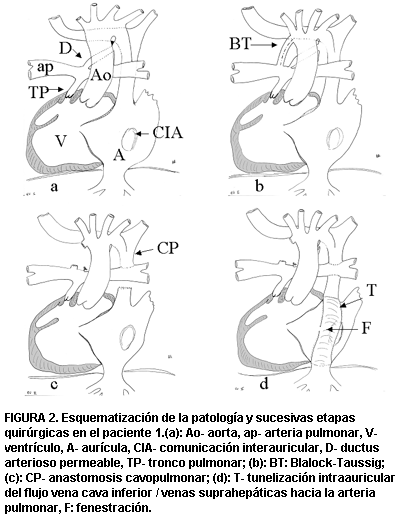
Ingresa al servicio a los 8 días de vida, portador de una cardiopatía congénita compleja cianótica ductus dependiente que requiere de la infusión de prostaglandinas para lograr una adecuada oxigenación y estabilización del paciente al reabrir el ductus. Se hace diagnóstico de isomerismo derecho con doble tracto de salida del ventrículo derecho, severa estenosis pulmonar y malposición de los grandes vasos (figura 2). Una vez estabilizado el paciente se realiza una anastomosis entre la circulación arterial sistémica y la circulación arterial pulmonar (anastomosis de Blalock-Taussig derecho) que se lleva a cabo a los nueve días de vida. Posteriormente presenta una buena evolución realizando la anastomosis cavo-pulmonar bidireccional a los siete meses y a los 20 meses se completa la cirugía de Fontan dejando una fenestración permeable, con buena evolución inicial y progresiva desaturación arterial sistémica de oxígeno (figura 3a).
FIGURA 2. Esquematización de la patología y sucesivas etapas quirúrgicas en el paciente 1.(a): Ao- aorta, ap- arteria pulmonar, V- ventrículo, A- aurícula, CIA- comunicación interauricular, D- ductus arterioso permeable, TP- tronco pulmonar; (b): BT: Blalock-Taussig; (c): CP- anastomosis cavopulmonar; (d): T- tunelización intraauricular del flujo vena cava inferior / venas suprahepáticas hacia la arteria pulmonar, F: fenestración.
FIGURA 3. Angiografías previa y posterior a la oclusión de la fenestración en el paciente 1. (a): Fenestración, T-túnel. (b): ETE: sonda para ecocardiograma transesofágico, T- túnel, D- dispositivo.
PACIENTE 2
Ingresa al servicio al mes y medio de edad, haciéndose diagnóstico de ventrículo único con L malposición de grandes arterias, atresia mitral, aorta originada desde camareta anterosuperior, con flujo pulmonar sin obstrucción y comunicación interauricular restrictiva por lo que requiere de un Rashkind y posterior Banding de la arteria pulmonar con buena evolución (figura 4). A los 7 meses se realiza la derivación cavo-pulmonar mas cirugía de Damus-Kaye- Stansel. A los dos años se completa la cirugía de Fontan fenestrado con buena evolución inicial, observándose progresiva desaturación arterial sistémica de oxígeno (figura 5a).
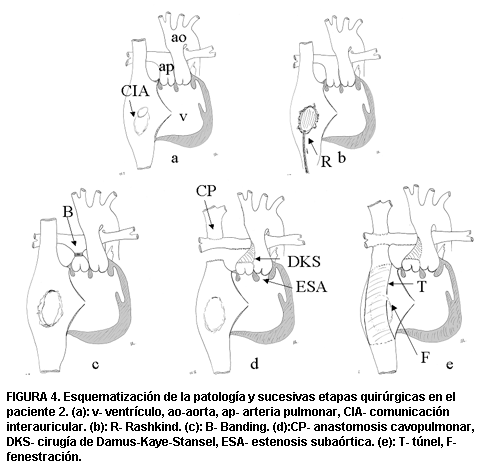
FIGURA 4. Esquematización de la patología y sucesivas etapas quirúrgicas en el paciente 2. (a): v- ventrículo, ao-aorta, ap- arteria pulmonar, CIA- comunicación interauricular. (b): R- Rashkind. (c): B- Banding. (d):CP- anastomosis cavopulmonar, DKS- cirugía de Damus-Kaye-Stansel, ESA- estenosis subaórtica. (e): T- túnel, F- fenestración.
FIGURA 5. Angiografías previa y posterior a la oclusión de la fenestración en el paciente 2. (a): aprd- arteria pulmonar rama derecha, apri- arteria pulmonar rama izquierda, as- aurícula sistémica, F- fenestración, T- túnel. (b): aprd- arteria pulmonar rama derecha, apri- arteria pulmonar rama izquierda, T- túnel, D- dispositivo.
PACIENTE 3
Ingresa al servicio al mes y medio de edad, haciéndose diagnóstico de cardiopatía congénita compleja dada por canal aurículo ventricular completo con ventrículos disbalanceados, estenosis infundibular pulmonar y aurícula única, por lo que se efectúa una anastomosis de Blalock-Taussig a derecha, buena evolución inicial (figura 6). A los 11 meses se realiza la anastomosis cavo-pulmonar bidireccional con plastia de los ramos pulmonares y posteriormente, a los 4 años, se completó la cirugía de Fontan fenestrado con buena evolución inicial y progresiva desaturación arterial sistémica de oxígeno (figura 7a).
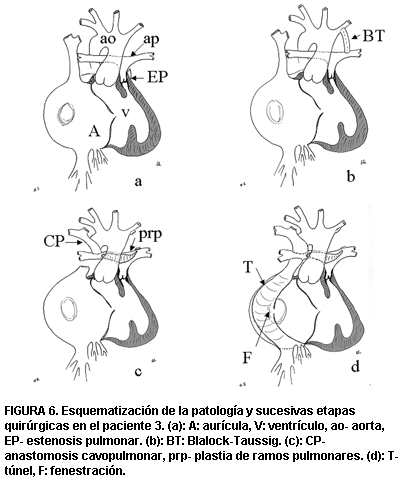
FIGURA 6. Esquematización de la patología y sucesivas etapas quirúrgicas en el paciente 3. (a): A: aurícula, V: ventrículo, ao- aorta, EP- estenosis pulmonar. (b): BT: Blalock-Taussig. (c): CP- anastomosis cavopulmonar, prp- plastia de ramos pulmonares. (d): T- túnel, F: fenestración.
FIGURA 7. Angiografías previa y posterior a la oclusión de la fenestración en el paciente 3. (a): T- túnel, as- aurícula sistémica, F- fenestración. (b): T- túnel, D- dispositivo.
PACIENTE 4
Ingresa al servicio a los 8 meses de edad haciéndose diagnóstico de cardiopatía congénita compleja dada por ventrículo único derecho con atresia pulmonar y desconexión de la arteria pulmonar rama derecha siendo la arteria pulmonar rama izquierda alimentada por un ductus arterioso permeable. Se efectúa una primera cirugía de cierre del ductus, reconexión de rama pulmonar derecha y anastomosis cavopulmonar bidireccional con buena evolución (figura 8), llevándose a cabo el Fontan fenestrado a los 3 años y 10 meses, con buena evolución inicial y progresiva desaturación arterial sistémica de oxígeno (figura 9a).
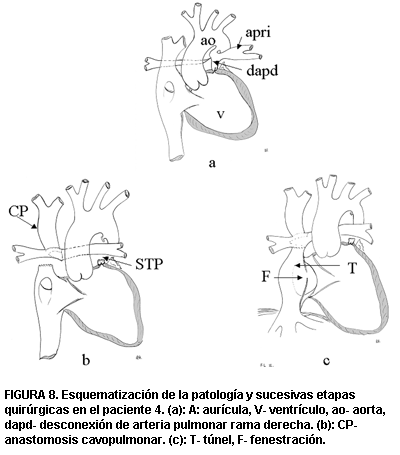
FIGURA 8. Esquematización de la patología y sucesivas etapas quirúrgicas en el paciente 4. (a): A: aurícula, V- ventrículo, ao- aorta, dapd- desconexión de arteria pulmonar rama derecha. (b): CP- anastomosis cavopulmonar. (c): T- túnel, F- fenestración.
FIGURA 9. Angiografías previa y posterior a la oclusión de la fenestración en el paciente 4. (a): aprd- arteria pulmonar rama derecha, apri- arteria pulmonar rama izquierda, T- túnel, F- fenestración, as- aurícula sistémica. (b): T- túnel, D- dispositivo.
RESULTADOS
En los cuatro pacientes tratados se logró el cierre total de la fenestración mediante el implante del dispositivo oclusor Amplatzer ASD, presentando en todos los casos un shunt residual mínimo a la salida de sala de hemodinamia, hecho normal con este tipo de dispositivos (figuras 3b, 5b, 7b y 9b). El control con ecocardiogramadoppler color realizado a las 24 horas del implante evidenció la ausencia de shunt residual.
La saturación arterial sistémica de oxígeno pasó de: 70-74-75 y 82% en el control precierre, a valores de: 96-93-92 y 96% respectivamente, en el control postcierre de la fenestración (tabla 1).
Las presiones en el sistema cavopulmonar estaban dentro del rango normal para este tipo de modelo circulatorio y no hubieron modificaciones significativas de las mismas post cierre de la fenestración con dispositivo.
No tuvimos complicaciones.
Tuvimos un promedio de internación de 18 hs por paciente, siendo otorgada el alta a domicilio en todos los casos.
DISCUSIÓN
La presencia de desaturación arterial de oxígeno (saturación medida por oxímetro de pulso menor al 90%) en el postoperatorio alejado de la cirugía de Fontan-Kreutzer puede deberse a diversos mecanismos: a) presencia de fístulas arteriovenosas intrapulmonares; b) desarrollo de conexiones veno-venosas entre la sangre del sistema cava (con bajo contenido de oxígeno) y la aurícula sistémica, que se presentan con gran diversidad de formas anatómicas; c) persistencia de una fenestración quirúrgica permeable (17-21).
Ante esta situación está indicado el cateterismo cardiaco con fines diagnósticos y terapéuticos: embolizaciones de canales veno-venosos y/o oclusión de la fenestración.
Clásicamente se han utilizado diferentes dispositivos para realizar el cierre de la fenestración permeable, en nuestro país solo están financiados (por el Fondo Nacional de Recursos) para su utilización: las espirales embolizantes (coils) y los dispositivos oclusores de CIA Amplatzer.
Los resultados obtenidos en nuestros pacientes con el uso de dispositivos Amplatzer ASD para efectuar el cierre percutáneo de las fenestraciones coinciden con los publicados en la literatura (22-24). La utilización de un dispositivo oclusor Amplatzer ASD es práctica y sencilla y con mayor rango de seguridad en el implante que frente al uso de un coil.
El procedimiento es eficaz, con minima morbilidad y se considera de elección en el momento actual, frente al cierre quirúrgico (25-28).
BIBLIOGRAFÍA
1. Nelson DP, Schwartz SM, Chang AC. Neonatal physiology of the functionally univentricular heart. Cardiol Young 2004; 14(Suppl. 1): 52-60.
2. Fontan F, Baudet E. Surgical repair of tricuspid atresia. Thorax 1971; 26: 240-8.
3. Sanders SP, Wright GB, Keane JF, et al. Clinical and hemodynamic results of the Fontan operation for tricuspid atresia. Am J Cardiol 1982; 49: 1733-1740.
4. Laks H, Milliken JC, Perloff JK, et al. Experience with the Fontan procedure. J Thorac Cardiovasc Surg 1984; 88: 939-51.
5. Mair DD, Rice MJ, Hagler DJ, et al. Outcome of the Fontan procedure in patients with tricuspid atresia. Circulation 1985; 72 (suppl II): II-88-II-92.
6. De Leon SY, Ilbawi MN, Idriss FS, et al. Fontan type operation for complex lesions: surgical considerations to improve survival. J Thorac Cardiovasc Surg. 1986; 92: 1029-37.
7. Mayer JE Jr, Helgason H, Jonas RA, et al. Extending the limits for modified Fontan procedures. J Thorac Cardiovasc Surg 1986; 92: 1021-8.
8. Kirklin JK, Blackstone EH, Kirklin JW, et al. The Fontan operation: ventricular hypertrophy, age and date of operation as risk factors. J Thorac Cardiovasc Surg 1986; 92: 1049-64.
9. Bartmus DA, Driscoll DJ, Offord KP, et al. The modified Fontan operation in children less than 4 years old. J Am Coll Cardiol. 1990; 15: 429-435.
10. Bridges ND, Lock JE, Castaneda AR. Baffle fenestration with subsequent transcatheter closure: modification of the Fontan operation for patients at increased risk. Circulation 1990; 82: 1681-9.
11. Fontan F, Kirklin JW, Fernández G, et al. Outcome after a “perfect” Fontan operation. Circulation 1990; 81: 1520-36.
12. Laks H, Pearl JM, Haas GS, et al. Partial Fontan: advantages of an adjustable interatrial communication. Ann Thorac Surg 1991; 52: 1084-1095.
13. King TD, Mills NL. Nonoperative closure of atrial septal defects. Surgery 1974; 75: 383-8.
14. King TD, Mills NL. Secundum atrial septal defects: nonoperative closure during cardiac catheterization. JAMA 1976; 235: 2506-9.
15. Lock JE, Rome JJ, Davis R, VanPraagh S, Perry SB, VanPraagh R, Keane JF. Transcatheter closure of atrial septal defects: experimental studies. Circulation 1989; 79: 1091-9.
16. Chiesa P, Peluffo C, Duhagón P, Giúdice J, Díaz P, Durán A, et al. Cierre de la comunicación interauricular con dispositivo oclusor implantado mediante cateterismo cardíaco. Rev Urug Cardiol 2004; 19: 73-80.
17. Bridges ND, Lock JE, Mayer JE Jr, et al. Cardiac catheterization and test occlusion of the interatrial communication after the fenestrated Fontan operation. J Am Coll Cardiol 1995; 25: 1712-7.
18. Hijazi ZM, Fahey JT, Kleinman CS, Kopf GS, Hallenbrand WE. Hemodynamic evaluation before and after closure of fenestrated Fontan: An acute study of change in oxygen delivery. Circulation 1992, 86, 196-202.
19. Bridges ND, Mayer JE Jr, Lock JE, et al. The effect of baffle fenestration on outcome of the modified Fontan operation. Circulation 1992; 86: 1762-9.
20. Mavroudis C, Zales VR, Backer CL, et al. Fenestrated Fontan with delayed catheter closure: effects of volume loading and baffle fenestration on cardiac index and oxygen delivery. Circulation 1992; 86 (suppl II): II-85-II-92.
21. Kuhn MA, Jarmakani JM, Laks H, et al. Effect of late postoperative atrial septal defect closure on hemodynamic function in patients with a lateral tunnel Fontan procedure. J Am Coll Cardiol. 1995; 26: 259-265.
22. Driscoll DJ, Offord KP, Feldt RH, et al. Five- to fifteen-year follow up after the Fontan operation. Circulation 1992; 85: 469-96.
23. Gentles TL, Mayer JE, Gauvreau K, et al. Fontan operation in five hundred consecutive patients: factors influencing early and late outcome. J Thorac Cardiovasc Surg 1997; 114: 376-91.
24. Tofeig M, Walsh KP, Chan C, et al. Occlusion of Fontan fenestrations using the Amplatzer septal occluder. Heart 1998; 79: 368-370.
25. Schneider DJ, Levi DS, Serwack MJ, Moore SD, Moore JW. Overview of interventional pediatric cardiology in 2004. Minerva Pediatrica 2004; 56: 1-28.
26. Moore JW, Murdison KA, Baffa GM, Kashow K, Murphy JD. Transcatheter closure of fenestrations and excluded hepatic veins after Fontan: versatility of the Amplatzer device. Am Heart J 2000; 140: 534-40.
27. Sommer RJ, Recto M, Golinko RJ, et al. Transcatheter coil occlusion of surgical fenestration after Fontan operation. Circulation. 1996; 94: 249-52.
28. Ruiz CE, Austin EH III, Cheatham JP, et al. First Food and Drug Administration approval under humanitarian device exemption of a septal occluder for fenestrated Fontan and muscular ventricular septal defects. Circulation 2000; 101: E9042.