Introducción
La técnica de imagen híbrida de SPECT-CT permite la adquisición secuencial de información funcional de la imagen de la tomografía por emisión de fotón único (SPECT) y anatómica del estudio de tomografía computada (TC), de esta forma se obtienen imágenes que combinan información funcional y morfoestructural en un solo estudio1.
Los equipos SPECT/CT más utilizados en la actualidad consisten en un equipo de tomografía computada multicorte y una gammacámara de doble cabezal. Estos sistemas permiten caracterizar y localizar anatómicamente los hallazgos centellográficos, detectar lesiones anatómicas no detectadas mediante SPECT y mejorar la calidad técnica de las imágenes centellográficas mediante la corrección de atenuación y radiación dispersa2,3).
Por otra parte, los estudios SPECT-CT determinan la exposición del paciente a una dosis adicional de radiación proveniente del componente TC. En el SPECT-CT la dosis de radiación que recibe el paciente es la sumatoria de las dosis proveniente del radiofármaco administrado para el estudio centellográfico SPECT y la dosis de radiación del estudio TC.
Las recomendaciones actuales de la Comisión Internacional de Protección Radiológica publicadas en 20074 definen que los procedimientos diagnósticos que emplean radiaciones ionizantes se deben regir bajo los principios de protección radiológica de justificación y optimización, teniendo en cuenta el principio de ALARA (por las siglas de as low as reasonable achievable o tan bajo como sea razonablemente posible, traducido al español)5.
En el Centro de Medicina Nuclear e Imagenología Molecular (CMNIM) del Hospital de Clínicas las principales indicaciones de SPECT-CT en población adulta abarcan el estudio de centellograma de perfusión miocárdica en pacientes con obesidad, estudios de patologías óseas, estudio de ganglio centinela en el cáncer de mama y patologías endocrinológicas (paratiroides y tiroides).
Los objetivos del presente estudio son estimar la dosis efectiva total en los protocolos SPECT-CT empleados en el CMNIM en la población adulta y determinar el aporte adicional del estudio TC sobre la dosis efectiva total para lograr su optimización.
Material y métodos
Se realizó un estudio retrospectivo, observacional y descriptivo de 258 pacientes adultos, mayores de 18 años, que fueron evaluados mediante la técnica SPECT-CT con un equipo híbrido Mediso© AnyScan 16 en el Centro de Medicina Nuclear e Imagenología Molecular del Hospital Universitario de Clínicas Dr. Manuel Quintela en el período comprendido entre enero 2017 y octubre 2019 en Montevideo, Uruguay.
Se tomó una muestra representativa de los pacientes mediante muestreo aleatorio simple de los siguientes procedimientos: perfusión miocárdica, óseo y ganglio centinela de mama, siendo estos los estudios SPECT-CT más utilizados en la práctica clínica. Por otro lado se incluyeron todos los estudios consecutivos de centellograma tiroideo y paratiroideo con SPECT-CT del período mencionado ya que son los estudios híbridos menos frecuentemente realizados en nuestro centro.
Criterios de inclusión
- Edad igual o mayor a 18 años
- Pacientes evaluados mediante centellograma y protocolo de SPECT-CT de uso clínico frecuente (perfusión miocárdica, óseo, paratiroides, tiroides, ganglio centinela de mama).
- Pacientes que firmaron el consentimiento informado
De los pacientes incluidos, se registraron del estudio SPECT-CT: el radiofármaco y actividad administrada (A) (MBq), tipo de estudio SPECT, región corporal explorada del estudio SPECT-CT, CTDIvol, longitud del scan y DLP (producto dosis longitud por sus siglas en inglés). Se calculó media, desvío estándar para la media muestral de las variables antes mencionadas. Se realizaron tablas, gráficos y los datos fueron procesados mediante software estadístico SPSS versión 25.
Se calculó la dosis efectiva aportada por el radiofármaco administrado (ERF) utilizando la actividad administrada (A) y factores de conversión específico para cada radiofármaco (hE1) publicados en las recomendaciones ICRP 128 (ecuación 1)6. Por otra parte se calculó la dosis aportada por la tomografía computada (ETC) mediante el producto de los valores de producto dosis-longitud (DLP) y los factores de conversión para cada región (hE2) (ecuación 2)7-9.
Ecuación 1
ERF(mSv) = (A(MBq) x hE1(µSv/MBq))/1000
Ecuación 2
ETC(mSv) = DLP(mGy/cm) x hE2(mGy/mSv*cm)
Donde A es la actividad administrada, hE1 es el factor de ponderación de dosis efectiva según tipo de radiofármaco, DLP es es producto dosis-longitud y hE2 es el factor de ponderación de dosis efectiva para TC según región explorada.
Posteriormente se calculó la dosis efectiva total y la media del porcentaje de cada componente (TC y RF) por paciente respecto de la dosis efectiva total.
El presente estudio fue aprobado por el comité de ética del Hospital de Clínicas. La base de datos fue anonimizada para proteger la identidad de los participantes.
Resultados
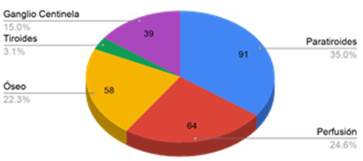
Los procedimientos evaluados correspondieron a estudios de paratiroides (n=91), perfusión miocárdica (n=62), óseo (n=58), ganglio centinela de mama (n=39) y centellograma tiroideo (n=8).
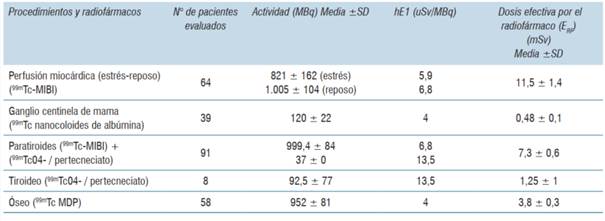
La (tabla 1) muestra los radiofármacos utilizados en cada procedimiento, la actividad administrada (MBq), el coeficiente de conversión hE1 (uSv/MBq) para cada radiofármaco y la dosis efectiva aportada por la administración de los radiofármacos ERF (mSv). El rango de dosis efectiva interna por paciente en los distintos procedimientos fue 0,48-11,5 mSv.
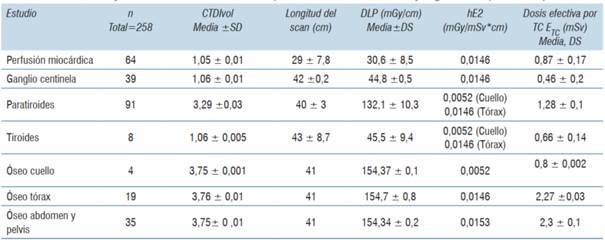
La (tabla 2) muestra la media y DS de CTDIvol, longitud del scan, DLP, el coeficiente de conversión hE2 (mGy/mSv*cm) y la dosis efectiva por paciente de los estudios TC. El rango de dosis efectiva por paciente en los estudios TC fue 0,46-2,3 mSv.
Tabla 2: CTDIvol, DLP y dosis efectiva externa en los procedimientos SPECT-CT y regiones corporales exploradas.
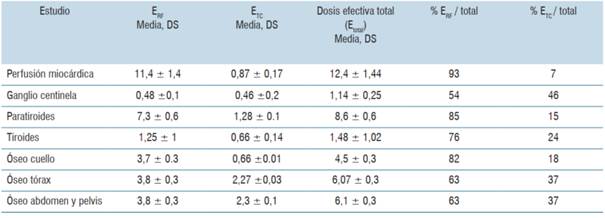
La dosis efectiva y porcentajes de cada componente sobre la dosis efectiva total calculados se muestran en la (tabla 3). En la (figura 1) se visualizan los porcentajes de la dosis efectiva aportados por cada componente (TC y RF) sobre la dosis efectiva total.
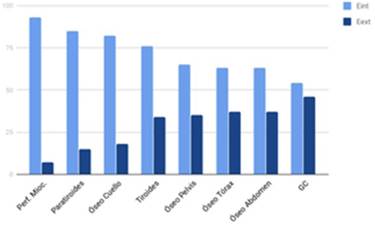
Figura 1: Dosis efectiva interna y externa como porcentaje de dosis efectiva total de cada procedimiento. Se visualiza un mayor porcentaje de dosis efectiva externa en el SPECT-CT de ganglio centinela, óseo de tórax, abdomen, pelvis y tiroides, siendo menor este porcentaje en el centellograma de perfusión miocárdica, paratiroideo y óseo de cuello.
Los procedimientos que reportaron mayor dosis efectiva total fueron el estudio de perfusión miocárdica y el centellograma paratiroideo (media 11,4 y 7,3 mSv, respectivamente) mientras que los estudios con menor dosis efectiva total fueron el centellograma tiroideo y ganglio centinela (media de 1,25 y 0,48 mSv, respectivamente) como se muestra en la tabla 3. El procedimiento con mayor aporte del componente TC a la dosis efectiva total fue el estudio de ganglio centinela (46%) mientras que el estudio con menor porcentaje es el centellograma de perfusión miocárdica (7%) (figura 2).
Discusión
La técnica de imagen híbrida de SPECT-CT combina información funcional del SPECT y la información anatómica del CT, lo cual implica un impacto clínico inmediato para un amplio rango de enfermedades al mejorar la precisión diagnóstica, especificidad y valor predictivo positivo de los estudios de medicina nuclear. El uso de SPECT-CT se encuentra actualmente en crecimiento y se está extendiendo a nuevas situaciones clínicas10.
A pesar de las ventajas del uso de la técnica SPECT-CT, el protocolo de estudio TC implica la adición de una dosis baja de radiación ionizante para los pacientes estudiados mediante esta técnica. La medida de la radiación y la protección deben convertirse en una consideración fundamental a la hora de emplear fuentes radiactivas. Los efectos reales de la radiación pueden no ser completamente conocidos, pero en general toda radiación es potencialmente nociva y por lo tanto deben tomarse medidas para prevenir exposiciones innecesarias. La exposición a la radiación del paciente puede ser estimada a través del cálculo de dosis efectiva a partir del promedio de la dosis equivalente (cantidad que toma en cuenta el daño biológico producido en un tejido por diferentes tipos de radiación) recibida por cada órgano y tejido irradiado11.
En las técnicas híbridas, el cálculo de dosis efectiva total que reciben los pacientes es la suma de la dosis efectiva derivada del radiofármaco administrado y la dosis efectiva por el estudio CT.
De acuerdo al sistema de protección radiológica propuesto por la Comisión Internacional de Protección Radiológica (ICRP), el uso de la radiación debe estar sujeto a tres criterios principales: el beneficio neto del individuo o la sociedad expuesta debe al menos compensar el daño por la exposición (justificación); la cantidad de exposición y la cantidad de personas expuestas deben mantenerse tan bajas como sea razonablemente posible teniendo en cuenta los factores sociales y económicos (optimización y principio ALARA)4, y la exposición de los pacientes debe estar sujeta a dosis diagnósticas de referencia (DRLs)14.
El cálculo de dosis efectiva es útil para comparar diferentes procedimientos diagnósticos y el riesgo asociado al efecto acumulativo de la dosis empleada de radiaciones ionizantes.
Los riesgos de la exposición en el cuerpo humano se clasifican según el tipo de célula en efectos genéticos que se presentan en la descendencia del individuo o somático manifestados en el mismo. Además, según la probabilidad de aparición se los agrupa como efectos determinísticos (radio dermitis) o estocásticos (cáncer).
Los efectos determinísticos están relacionados con la muerte celular a partir de un umbral de dosis por encima del cual estos se manifiestan. Los efectos estocásticos son aleatorios, probabilísticos y pueden aparecer tras la acumulación de exposición a pequeñas dosis de radiación ionizante. Al aumentar la dosis se incrementa la probabilidad de que ocurran siendo de tipo tardío y los más relevantes para este estudio15.
Los protocolos de estudio son optimizados teniendo en cuenta varios parámetros y aspectos, como la radiosensibilidad de cada paciente. Esta es mayor en pacientes pediátricos, debido al proceso de desarrollo celular activo que aumenta la probabilidad de los efectos, y en pacientes geriátricos dado que su desarrollo celular se ve limitado en la reparación de células afectadas.
Por otro lado, hay órganos más radiosensibles que otros según el tipo de función fisiológica que cumplan y la población celular que compone sus tejidos. Son más radiosensibles las células menos diferenciadas y con mayor capacidad de división, como las que forman parte de las glándulas tiroides, mamarias y gonadales. Por lo tanto las regiones corporales donde se encuentran requieren de mayor cuidado al exponerse a las radiaciones ionizantes y es de suma importancia utilizar todas las herramientas que se encuentren a nuestro alcance para disminuir la dosis tanto como sea posible y así bajar la probabilidad de aparición de los efectos negativos16.
En nuestro estudio los procedimientos que aportaron mayor dosis efectiva por el radiofármaco fueron el centellograma de perfusión miocárdica, el centellograma paratiroideo y el centellograma óseo, debido a que son los estudios con mayor actividad administrada al paciente.
Por otro lado, los protocolos TC que aportaron mayor dosis efectiva fueron el estudio TC de las regiones de tórax y abdomen-pelvis en el centellograma óseo y el TC de las regiones de cuello y tórax en el centellograma paratiroideo, dado que la dosis recibida se relaciona con el espesor y composición de la región censada por el equipo16.
Las regiones exploradas mediante SPECT-CT en los distintos protocolos fueron: cráneo, cuello, tórax, abdomen y pelvis o abarcando más de una región como en el caso de estudios óseos y de ganglio centinela, que abarcan tórax y abdomen.
El presente estudio encontró que la dosis efectiva media atribuible al componente TC de diferentes estudios SPECT-CT se encuentra entre 0,46 y 2,3 mSv. La dosis efectiva media del componente TC fue la más baja en el ganglio centinela de mama y la más alta en el estudio SPECT-CT óseo de la región abdomen y pelvis, esto se explica a que la región del tórax requiere dosis menores de radiación por el contraste natural entre las estructuras mientras que la dosis es mayor al estudiar dos regiones como abdomen y pelvis en un sólo estudio, lo que reafirma la importancia de delimitar adecuadamente la zona de estudio16.
El aporte adicional en la dosis efectiva de exposición medido como porcentaje de la dosis efectiva total atribuible al componente TC en los procedimientos SPECT-CT se encontró en el rango comprendido entre 7% para el estudio de perfusión miocárdica y 46% para el estudio ganglio centinela de mama. Debemos recordar que este porcentaje depende de la actividad y el radiofármaco administrado al paciente. La dosis adicional derivada del componente TC en los protocolos SPECT-CT encontrada en nuestra población es menor a la reportada en literatura12.
En Uruguay no se han establecido aún hasta la fecha niveles de referencia diagnósticos (DRLs, por las siglas de diagnostic reference levels)13 y el presente estudio representa el primer aporte a la literatura nacional sobre el cálculo de dosis efectiva en estudios híbridos.
Debemos tener en cuenta como limitantes de nuestro estudio que es un estudio retrospectivo, se tomó una serie de casos consecutivos para los casos de centellograma paratiroideo y tiroides y una muestra aleatoria del resto de los estudios y que las variables en estudio se expresan en valores promedio por lo cual cada caso particular puede diferir de los resultados.
Conclusiones
Se logró estimar la dosis efectiva en los protocolos SPECT-CT de uso clínico más frecuente en población adulta y el aporte de los estudios TC a la dosis efectiva total siendo relativamente baja comparado con la dosis aportada por los radiofármacos administrados con la excepción del estudio de ganglio centinela donde la contribución del componente TC es aproximadamente la mitad de la dosis efectiva total.