Introducción
Más de 150 millones de personas en todo el mundo padecen diabetes, y todos corren el riesgo de desarrollar una úlcera de pie diabético (UPD) de diverso grado, más del 15% realmente desarrollará dichas úlceras1,2. La mala vascularización y la matriz tisular inadecuada a menudo afectan el manejo de las úlceras diabéticas, entre varios factores. Diversos tratamientos son utilizados para manejar las UPD, los métodos empleados tradicionalmente incluyen cambios rigurosos de apósito con observación cuidadosa, desbridamiento del tejido necrótico, control de infecciones y reducción de la presión sobre el pie diabético2-4.
La revascularización de las extremidades inferiores también es considerada en algunos casos4. La falla en el resultado de los tratamientos puede provocar amputaciones hasta en un 20% de las UPD infectadas, con aumento de la morbimortalidad y alteración en la calidad de vida del paciente5.
Determinar los métodos de tratamiento para evitar las amputaciones en todos los pacientes es un problema de calidad de vida y un desafío financiero para los sistemas de salud. Las terapias celulares emergentes, como el plasma rico en plaquetas (PRP), pueden tener un papel complementario en el tratamiento de las UPD.
Han sido múltiples las experiencias clínicas en relación con el empleo de PRP autólogo en el ámbito de la otorrinolaringología, cirugía plástica, medicina deportiva, traumatología6. Ensayos clínicos han investigado la eficacia del PRP en la cicatrización de heridas crónicas7-12. Una revisión de Cochrane observó que el PRP puede mejorar la curación en UPD en dos estudios clínicos aleatorizados13. Otra revisión actual también informa del beneficio14. Las proteínas contenidas en los gránulos alfa poseen una fuerte influencia sobre los fenómenos reparadores de las heridas. Entre dichas proteínas se encuentran los factores de crecimiento derivados de plaquetas (PDGF), el factor de crecimiento transformante beta (TGF-ß), el factor plaquetario 4 (FP4), interleuquina 1 (IL-1), el factor angiogénico derivado de plaquetas (PDAF), el factor de crecimiento endotelial vascular (VEGF), el factor de crecimiento epidérmico (EGF), el factor de crecimiento endotelial derivado de plaquetas (PDEGF), el factor de crecimiento celular epitelial (ECGF), el factor de crecimiento tipo insulina (IGF), osteocalcina, osteonectina, fibrinógeno, fibronectina y trombospondina (TSP). Algunas de estas proteínas se encuentran ausentes en heridas crónicas que no sanan adecuadamente15.
En la UPD crónica se alteran las etapas de cicatrización, presentando una fase inflamatoria prolongada, defectos en la remodelación de la matriz extracelular, formación de radicales libres e inhibición de la generación de factores de crecimiento celular y de la migración celular. El PRP puede definirse como un volumen de plasma autólogo que contiene una concentración de plaquetas superior al nivel basal.
Luego de la aplicación de PRP el 95% de los factores de crecimiento se liberan en el lapso de una hora. Adicionalmente, la síntesis y secreción de proteínas dura entre 5 a 10 días más. Luego, los macrófagos que llegan al foco debido al crecimiento vascular promovido por las plaquetas, asumen la regulación de la reparación tisular mediante la secreción de sus propios factores. El uso de PRP autólogo es un tratamiento efectivo y seguro, con escasos efectos adversos leves16,17. Aún no se ha determinado cuál es el mejor método de preparación y conservación de PRP para aplicaciones clínicas18.
Objetivo general
Evaluar la capacidad del PRP autólogo para cicatrizar UPD crónicas refractarias como una modalidad complementaria de tratamiento, valorando su seguridad y efectos adversos. Evaluar el porcentaje de reducción del área de la herida en un plazo de 12 semanas.
Material y método
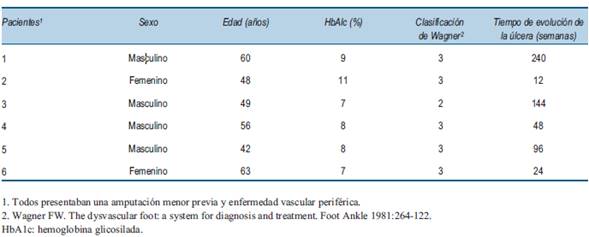
Estudio abierto, prospectivo, observacional. Pacientes con UDP provenientes del sistema de salud público, derivados del primer nivel de atención, policlínica de cirugía, emergencia e internación y que se asisten en la Unidad de Pie Diabético del Hospital de Clínicas, junto al Servicio de Hemoterapia y la Escuela de Tecnología Médica, área de Podología, entre marzo de 2018 y diciembre de 2019. Luego de calificar para los criterios de inclusión (tabla 1), se enrolaron UDP crónicas estadificadas con la clasificación de Wagner como grado II, III, con al menos 12 semanas de retraso en su cicatrización19,20. Se registraron datos demográficos, como edad y sexo (tabla 2), historial de lesiones previas, antecedentes comórbidos y uso de fármacos que interfirieran con el proceso de reparación (corticoides, anticoagulantes, quimioterapia). Los pacientes seleccionados tuvieron un período de preinclusión de 12 semanas con tratamiento estándar, en base a desbridado y suero fisiológico (SF) con un resultado pobre en cuanto a disminución del diámetro de la úlcera. Se evaluó la infección clínica y la terapia antibiótica empírica apropiada se inició al diagnóstico, controlando que ésta hubiera remitido antes del tratamiento con PRP. Se valoró la perfusión con estudio Doppler en conjunto con cirugía vascular. Para confirmar un recuento plaquetario normal solicitamos hemograma, función renal y hepática por métodos convencionales, así como serología de enfermedades transmisibles HIV 1-2, HTLV 1-2, VDRL, Chagas, hepatitis B Core, Ag de superficie y hepatitis C. Los pacientes continuaron con el control y las prescripciones para su diabetes dirigidas por endocrinólogo tratante. Hemoglobina A1c (HbA1c), se solicitó en el seguimiento (medida por inhibición de aglutinación de látex equipamiento DCA 2000 Bayer-Siemens). En cada consulta se realizó el control clínico y estado general del paciente, glucemia capilar, valoración de la úlcera y el pie, pesquisando la presencia de efectos adversos de la aplicación de PRP: alergias, dermatitis, inflamación, infección, dolor en el sitio de aplicación o cicatriz fibrosa16. Cumplieron con los criterios de inclusión y exclusión para la elegibilidad del estudio seis pacientes con antecedentes de amputación menor y diverso grado de enfermedad vascular asintomática21. Se excluyeron seis pacientes con infección no controlada.
Obtención y aplicación de PRP
La fase de centrifugación se realizó por médico hemoterapeuta entrenado en la obtención de hemocomponentes, para posibilitar el máximo rendimiento del producto. Se les extrajo un volumen de sangre total de 15 a 50 ml, las muestras se obtuvieron mediante sistema de tubos vacutainer en tubo citratado a 3,8%. Mediante un proceso que utiliza el principio de separación celular por centrifugación diferencial, se obtuvo PRP en estrictas condiciones de asepsia en cámara de flujo laminar para evitar la contaminación del producto en el laboratorio de hemoterapia (figura 1). Se realizó el control microbiológico de cada producto de PRP, sin obtener desarrollo microbiológico. Se realizó una primera centrifugación de la sangre total a 22 ºC, a una velocidad de 1.800 rpm en 5 minutos, separando los glóbulos rojos del plasma con las plaquetas; éste se sometió a una segunda centrifugación a 22 ºC, a una velocidad de 2.500 rpm, durante 8 minutos, descartando los dos tercios superiores del plasma pobre en plaquetas, obteniendo así el PRP. El producto fue destinado a inyectarse directamente o a la aplicación como gel plaquetario. En el PRP, nuestro objetivo fue llegar a concentrar las plaquetas al menos tres veces su valor basal22,23. La cantidad de PRP utilizado se definió según el tamaño y la profundidad de la úlcera. Decidimos no activar previamente el producto inyectable, sabiendo que la activación se realiza al contacto de las plaquetas con el tejido cruento de los bordes y el fondo desbridado de la úlcera. El gel se produjo activando el PRP con gluconato de calcio a 10% y dejándolo a 37 ºC hasta obtener su gelificación. Se aplicó PRP mediante inyección y como gel sobre la úlcera (figura 2) en tres pacientes consecutivos y únicamente como gel en los restantes tres pacientes (tabla 3). Luego de la aplicación, se realizó una compactación suave con apósitos de gasa seca para cubrir la superficie y absorber cualquier descarga. El apósito se retiró a las 24 horas continuando con curaciones diarias en domicilio con SF. La aplicación de PRP se realizó una vez por semana hasta el cierre de la úlcera o hasta completar 12 semanas. Antes de aplicar el PRP, la UPD se preparó utilizando un desbridamiento cuidadoso y riego vigoroso con SF. Se realizó el registro fotográfico y medida del área de la UPD al inicio del estudio y previo a cada aplicación de PRP. La longitud máxima y el ancho de cada herida se determinaron usando una regla esterilizada, se realizaron dos medidas y la media se utilizó para el cálculo. Se registró el área de la úlcera en cm2 mediante Mobile Wound Analyzer (MOWA), software de análisis de imágenes de úlceras (figura 3). Se calculó el porcentaje de reducción de la úlcera utilizando la fórmula:
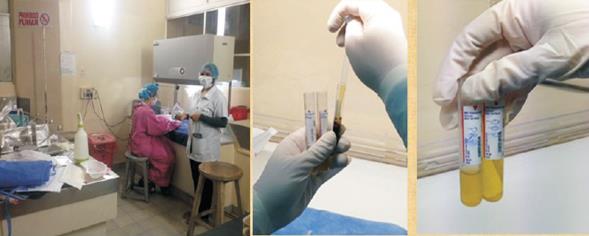
Figura 1: Obtención de PRP por método de doble centrifugación. Laboratorio de Hemoterapia del Hospital de Clínicas. Universidad de la República.
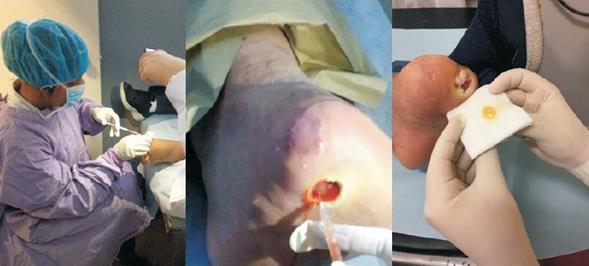
Figura 2: Aplicación del PRP. Inyección en bordes de úlcera y aplicación de gel en forma de coágulo. Pacientes con úlceras Wagner III.

Figura 3: MOWA, software de análisis de imágenes de úlcera. Análisis planar de la imagen; evaluación cualitativa y cálculo del área.
El protocolo de estudio se ajustó a las pautas éticas de la Declaración de Helsinki y fue aprobado por el Comité de Ética del Hospital Universitario. Los pacientes firmaron el consentimiento informado.
Criterio de valoración y análisis estadístico
Se consideró exitoso una reducción >70% del área de la úlcera. El crecimiento total del tejido o reepitelización sin secreción, constituyó una curación completa. La presencia de infección clínica motivó la suspensión del tratamiento. Los datos recopilados se analizaron mediante el software JMP 15.2.1 (análisis de datos) Inc. 2020, versión 15.2.1. Se calculó estadística descriptiva, medidas de resumen central y de dispersión (media, desviación estándar e intervalos de confianza con 95% de confiabilidad) con el método binomial.
Resultados
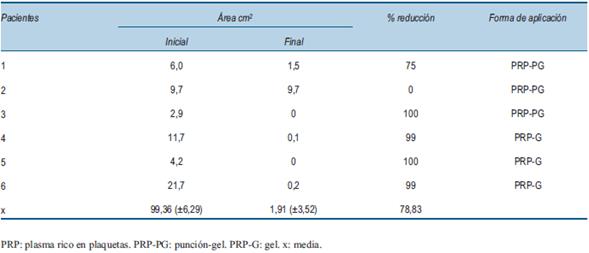
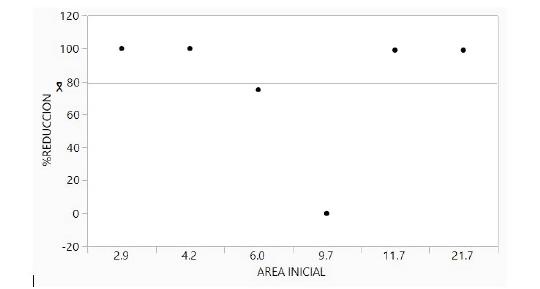
Se realizaron 48 procedimientos en seis pacientes de forma consecutiva, el conteo plaquetario preprocedimiento de fracción F1 y del producto de PRP tuvo un enriquecimiento plaquetario dentro de lo esperado, los cultivos para aerobios y anaerobios de todos los productos realizados fueron estériles. Predominó el sexo masculino (4/6), la media de edad fue de 53 años, DE: 8,0 (42 a 63 años). Dos úlceras eran categoría II y cuatro categorías III de la clasificación de Wagner, con una media en el retraso de su cicatrización de 94 semanas (DE: 86,6; R 12-240). El control glucémico durante el seguimiento fue deficiente, con una media de HA1c: 8,33% (DE: 1,50; R 7-11). En la valoración del resultado primario a las 12 semanas, cinco pacientes tratados lograron un porcentaje de cicatrización mayor al 70% de la superficie de la úlcera con una reducción media del área de 78,83 % (DE: 39,8) (figura 4). Antes del uso de PRP la media del área de la úlcera para todos los pacientes fue de 9,36 cm2 (DE: 6,29; R: 2,9-21,7), al final de las 12 semanas fue de 1,91 cm2 (DE: 3,52; R: 0,0-9,7) (tabla 3). Según la forma de aplicación del PRP, la respuesta obtenida fue: punción y gel redujo 75%, 0% y 100%, compactación con gel redujo 99%,100% y 99% respectivamente (tabla 3). Hubo dos cicatrizaciones completas (figura 5) y dos reducciones de 99% (figura 6). Un paciente redujo el área en 75% luego del tratamiento con PRP, en una úlcera de cinco años de evolución. Otro paciente requirió una amputación por sobreinfección con Staphylococcus aureus resistente a meticilina. No observamos efectos adversos secundarios a la aplicación del PRP.
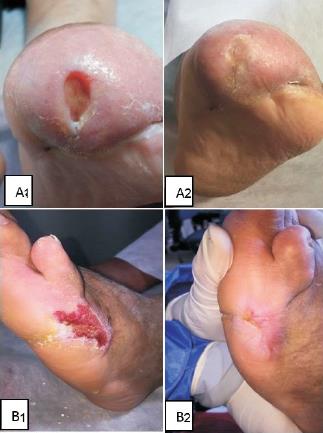
Figura 5: Pacientes representativos. (A1) Estado inicial, úlcera Wagner grado II sobre cicatriz de amputación transmetatarsiana (A2), úlcera completamente curada (día 90). (B1) Estado inicial, úlcera Wagner II del lecho de amputación en rayo del quinto dedo. (B2) Úlcera completamente curada (día 90).
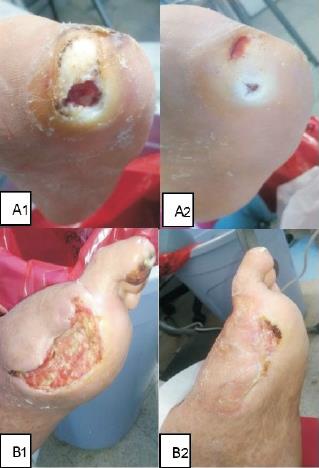
Figura 6: Pacientes representativos. (A1) Estado inicial, úlcera Wagner grado 3 sobre tercer radio del metatarsiano, en cicatriz de amputación transmetatarsiana. (A2) Úlcera cicatrizada en 99% (día 90). (B1) Estado inicial, úlcera Wagner grado 3 del lecho de amputación en rayo del primer dedo. (B2) Se logró una reepitelización significativa en 99% (día 90).
Discusión
Las UPD se caracterizan por su cronicidad y recaída24. La imposibilidad para curar por completo puede provocar amputaciones del pie o de la extremidad25. Aquellas úlceras con más de cuatro semanas de duración se consideran crónicas, siendo este un factor crítico porque la formación de biopelículas y la desecación del tejido subyacente pueden exacerbar las condiciones y dificultar el proceso de epitelización26 , derivando en una infección del pie, primera causa de amputación en UPD. El desafío es generar técnicas suplementarias para superar la insuficiencia vascular y de regeneración tisular inherentes. El uso de PRP ha mostrado una mayor cicatrización en heridas crónicas de espesor total de las extremidades inferiores27-30. Se han ensayado diversos métodos de centrifugación para obtener una buena concentración de PRP y sus factores de crecimiento31. La formulación de PRP que utilizamos logró promover la cicatrización de la úlcera tomando como punto final un período de tratamiento de 12 semanas. Nuestros pacientes no recibieron PRP en su primera visita. Para ser consistente con los resultados de nuestra Unidad de Pie, donde el 69% de los pacientes cicatrizan con una mediana de tiempo de cierre de tres meses (RIC 1-4,5) (Unidad de Pie Diabético. Hospital de Clínicas, octubre 2014 - setiembre 2016. Observación no publicada), realizamos el tratamiento convencional previo a la inclusión. Desde esta perspectiva, 31% de nuestros pacientes se consideran refractarios al tratamiento más allá de este tiempo (10,4% se amputan y 20,6% continúan con una úlcera activa). En otras palabras, incluimos úlceras refractarias con un tiempo medio de retraso en la cicatrización de 94 semanas que no habían tenido beneficio con el tratamiento estándar. Sin embargo, cinco de estos pacientes con UPD Wagner II, III, reactivaron el proceso de cicatrización efectivamente en las siguientes 12 semanas, cuando agregamos el uso complementario de PRP. Esto es consistente con estudios en que se utilizó PRP para el tratamiento de úlceras refractarias32-34, o que examinan la eficacia de los tratamientos utilizando el punto de corte menor a 20 semanas de terapia35,36. En un paciente, los fenómenos reparativos se encontraban ausentes o enlentecidos durante un período de cinco años y los múltiples procedimientos habían fracasado. Cuando utilizamos PRP en forma concomitante al tratamiento habitual, resultó muy favorecedor al reiniciar los procesos de reparación reduciendo el área de la úlcera en 75%. En otro paciente con una amputación de dedo previa, no fue posible evitar la sobreinfección de la úlcera, requiriendo una reamputación transmetatarsiana. Se ha propuesto que PRP promueve la quimiotaxis de macrófagos y contiene una pequeña cantidad de leucocitos que sintetizan interleuquinas, previniendo infecciones37. Al ser un producto realizado a partir de la sangre del propio paciente, es un producto no tóxico, sin posibilidades de rechazo, alergias o contagio de enfermedades infecciosas. Una revisión que incluye 12 artículos16 , así como otros estudios, analizan estas complicaciones que se describen como efectos adversos de carácter leves, en general cutáneos10,17,21,30. No registramos eventos adversos relacionados con la aplicación de PRP en nuestros pacientes, enfatizamos las ventajas de contar con personal médico entrenado en producción de hemocomponentes bajo estándares de bioseguridad y control de calidad.
Cuando aplicamos PRP como gel, el producto semifluido mantuvo los beneficios durante el proceso de curación (figura 2). Similar a otros componentes biológicos de reparación, el gel fluye fácilmente desde una jeringa y permanece estructuralmente cohesivo. Estas características permiten una cobertura completa de las úlceras que varían en forma y profundidad, incluidas aquellas con arquitecturas geométricas o de túnel38, garantizando una matriz adecuada para la migración celular y el posterior contacto de célula a célula. El aumento en la concentración de los PDGF estimula significativamente la proliferación de fibroblastos y la expresión de colágeno tipo I39, estimula la granulación, la angiogénesis y la proliferación celular, promoviendo la reepitelización40.
Avanzar en la cicatrización de la úlcera es de gran importancia, pues los factores que cronifican la lesión, asociado a condiciones comórbidas, hace que el proceso de curación sea impredecible, aumentando la morbilidad y los costos de tratamiento.
La literatura revela escasez de estudios económicos que evalúen el tratamiento con PRP en heridas crónicas. Se ha informado que este tratamiento es coste-efectivo o incluso dominante comparado con los cuidados habituales.
Su eficacia determina una menor utilización de los recursos al evitar tratamientos de una úlcera activa o sus complicaciones, como ingresos hospitalarios, infecciones, amputaciones, recurrencias y segundas amputaciones41,42.
Un estudio que evaluó el tratamiento durante 12 semanas con PRP (aplicado dos veces por semana) demostró que es más efectivo en términos de año de vida ganado ajustado por calidad (AVAC) y menos costoso (15.159 dólares) que el tratamiento estándar41. El costo total esperado por paciente cuya úlcera se logra epitelizar con PRP es menor que el tratamiento estándar de una úlcera refractaria12.
Realizamos 48 procedimientos aplicando PRP una vez por semana durante 12 semanas, logrando epitelizar la mayoría de las úlceras que tenían una media de retraso de cicatrización de 94 semanas (2 años).Un paciente debió amputarse.
En nuestra unidad el costo directo por paciente para una mediana de tiempo de epitelización de tres meses (RIC 1-4,5) asciende a 3.707 dólares. Cada procedimiento adicional en úlceras refractarias cuesta 325.910 dólares, llevando a un costo anual por úlcera que no cicatriza aproximadamente 15.600 dólares/paciente. El ingreso hospitalario lo incrementa en 14.643, una amputación menor en 12.385 y una amputación mayor en 32.003 dólares. (Gastos en Unidad de Pie Diabético. Hospital de Clínicas, octubre 2014 - setiembre 2016. Observación no publicada).
Acortar la duración de la úlcera disminuye estos costos al evitar la necesidad de procedimientos sobre la úlcera refractaria y sus complicaciones (amputaciones). Más importante aún, disminuye la morbimortalidad, pues aquellos pacientes con UPD tienen una mortalidad a cinco años de 42%-48%43,44.
Al año de seguimiento, no hubo recidiva de la lesión en cuatro pacientes y en uno de ellos persistió una úlcera de menor diámetro. Datos de un estudio que valora la recurrencia en lesiones tratadas con PRP, encontró recidivas a los 2,2 meses (rango 0,25 - 7 meses) mayor en pacientes con úlceras de evolución prolongada y descarga inadecuada del calzado poscicatrización, proponiendo que se obtendría con PRP una piel menos resistente al traumatismo en el sitio de la lesión propensa a la recidiva45.
Esto nos recuerda la importancia de la descarga como prevención primaria y secundaria sobre las alteraciones crónicas de la biomecánica del pie diabético que genera sitios de hiperpresión preulcerosos.
La metodología del presente trabajo (observacional, no aleatorizado) implica inevitablemente limitaciones a la hora de interpretar los datos. Sin embargo, el tratamiento fue efectivo en cinco pacientes luego de la aplicación del PRP, reduciendo el área de la úlcera en forma significativa, teniendo en cuenta que los pacientes fueron tratados previamente sin lograr avances en el proceso de cicatrización.
La efectividad se refiere a la capacidad en el mundo real de que un tratamiento proporcione un beneficio. Dado que los pacientes rara vez son sometidos a las condiciones idealizadas de los estudios controlados aleatorizados, las estimaciones de efectividad pueden ser tan útiles como las estimaciones de eficacia al momento de decidir las mejores opciones de tratamiento para los pacientes individuales46.
El PRP puede considerarse en úlceras con escasa o nula respuesta a los tratamientos convencionales. Presenta un costo accesible y es de fácil generación y aplicación.
Es necesario protocolizar la generación del PRP y la frecuencia de su aplicación, de esta forma podremos diseñar trabajos de investigación prospectivos que evalúen la efectividad del tratamiento asociado a PRP comparado con el tratamiento estándar. Limitaciones: necesitamos un número mayor de pacientes para poder validar el uso de PRP en el manejo de las UPD, por lo cual se siguen incluyendo pacientes. Sería interesante incluir en la investigación un soporte histológico que detalle los aspectos microscópicos de la reparación.
Conclusiones
Nuestros resultados muestran los efectos reparativos del PRP autólogo en UPD Wagner grados II y III refractarias al tratamiento estándar, mejorando las perspectivas de epitelización, sin haberse presentado efectos adversos a su uso. Se requieren más pruebas clínicas y monitoreo de seguimiento para confirmar su importancia en el manejo de las UPD difíciles de curar.