Resumen de recomendaciones
- Recomendamos que los pacientes con enfermedad renal en todas sus etapas (ERC etapas 1-5, diálisis, trasplante renal) sea una población priorizada en el plan de vacunación contra SARS-CoV-2.
- Recomendamos que en todos los casos la vacunación sea administrada sin importar si los pacientes tuvieron previamente COVID-19 o si tienen títulos IgG positivos para SARS-CoV-2.
- Recomendamos la vacunación de todos los pacientes con ERC avanzada en plan de diálisis crónica o fuera de ella con los esquemas habituales propuestos para las diferentes vacunas disponibles en nuestro medio.
- Recomendamos la vacunación de todos los pacientes en lista de espera de trasplante renal. En quienes se encuentran coordinados para trasplante intervivo es deseable que completen la vacunación un mes previo al procedimiento.
- Recomendamos la vacunación de todos los pacientes receptores de trasplante renal luego del primer mes de trasplantado y aprovechando las situaciones clínicas de estabilidad y menor requerimiento de inmunosupresión. En las situaciones en que se administra timoglobulina o rituximab al trasplante, se recomienda diferir la vacunación hasta el tercer mes. Cuando se indica tratamiento antirrechazo (metilprednisolona, recambio plasmático terapéutico, gammaglobulinas), se recomienda diferir la vacunación al menos dos semanas.
- Recomendamos la vacunación de los pacientes con enfermedades autoinmunes (enfermedades autoinmunes sistémicas, glomerulopatías), con o sin tratamiento inmunosupresor, preferentemente en el momento en que la enfermedad de base esté estable y eligiendo el mejor momento de la inmunosupresión.
Propósito de esta recomendación
Este documento de recomendación elaborado por la Sociedad Uruguaya de Nefrología (SUN), la Cátedra de Nefrología de la Universidad de la República y el Programa de Salud Renal tiene como objetivo orientar a los médicos nefrólogos y no nefrólogos que asisten a pacientes con enfermedad renal crónica (ERC) en todas las etapas de la misma (ERC de cualquier causa en seguimiento, diálisis o trasplante renal) en el proceso de vacunación contra el SARS-CoV-2. Como consecuencia de la situación epidemiológica y de los tiempos del proceso de elaboración de las vacunas disponibles, no se ha generado evidencia lo suficientemente potente, por lo que las recomendaciones no se acompañan del nivel de evidencia. Pese a ello, se partió de la premisa de que la priorización de la vacunación, dado el contexto epidemiológico local y mundial, es más beneficiosa que los potenciales efectos adversos. Estas recomendaciones se organizaron según grupos de asistencia y se consideraron situaciones especiales no excepcionales en la asistencia de pacientes con enfermedad renal.
Infección por SARS-CoV-2 / COVID-19 y enfermedad renal
Los pacientes con ERC avanzada, en diálisis crónica y trasplante renal particularmente, constituyen una población susceptible para la infección por SARS-CoV-2, para el desarrollo de la enfermedad (COVID-19) y para presentar una evolución más desfavorable cuando se los compara con la población general1. La exposición e infección por SARS-CoV-2 en la población con ERC avanzada, y particularmente en los pacientes en hemodiálisis crónica es muchísimo más elevada que en la población general. A la fragilidad impuesta por la ERC avanzada, se suma la necesidad de mayor asistencia y permanencia de este grupo en centros de salud (consultas ambulatorias, centros de hemodiálisis, controles en diálisis peritoneal y policlínica de trasplante). Durante la “primera ola” de la infección, surge de reportes de centros europeos que entre 5% y 20% de los pacientes que concurren a centros de hemodiálisis se infectarán con SARS-CoV-22. Esta prevalencia fue significativamente más baja en la población en diálisis peritoneal y trasplante renal por ser tratamientos que transcurren predominantemente en el domicilio3. Un grupo importante de pacientes cursa la infección de forma asintomática. En estudios de seroprevalencia se ha objetivado que 28%-36% de pacientes en centros de hemodiálisis (Londres, Nueva York) tienen anticuerpos contra SARS-CoV-2, y hasta 70% cuando se considera a los pacientes que además concurren a centros de rehabilitación física4. La elevada prevalencia de infección asocia una altísima tasa de muerte. Cuando se compara el riesgo de morir por COVID-19 de los pacientes con ERC, con el de la población sin ERC que requiere hospitalización por COVID-19, se objetiva que es entre 30% y 130% más elevado5 , con una tasa de mortalidad reportada entre 16% y 32%5-7. El riesgo de muerte es excepcionalmente elevado en pacientes jóvenes en diálisis cuando se compara con población sana de la misma edad8. La mortalidad reportada es incluso más alta (1,28 veces mayor) en receptores de trasplante renal cuando se compara con pacientes en programa de diálisis crónica6. Este incremento en la mortalidad se explica, al menos en parte, por el compromiso inmunológico vinculado a la ERC y a la inmunosupresión que reciben los trasplantados, sumado a que este grupo de pacientes asocia con frecuencia otras comorbilidades como diabetes, obesidad, hipertensión arterial e insuficiencia cardíaca, entre otras, que le imprimen más riesgo de enfermar y evolucionar peor2,8,9.
La pandemia por SARS-CoV-2 ha generado también efectos indirectos poco reconocidos8, principalmente en la población en diálisis crónica. El miedo frente a la amenaza de la infección ha determinado en todo el mundo un mayor número de inasistencias a las sesiones de hemodiálisis, una disminución en el número de consultas programadas de seguimiento en diálisis peritoneal y trasplante, y una reducción en el número de consultas emergentes en esta población. Este cambio en las conductas de asistencia a diálisis y controles programados también se asocia a incremento en la mortalidad8,10.
Vacunación contra SARS-CoV-2
Existe cierta “actitud pasiva” de la comunidad médica mundial respecto a la vacunación de algunos grupos de pacientes con ERC, principalmente quienes están en diálisis crónica, debido a la escasez de datos sobre seguridad y eficacia de las vacunas contra el SARS-CoV-2 en esta población. Esto responde, en parte, a que no se ha incorporado ningún paciente en diálisis crónica en ninguno de los ensayos de vacuna a nivel mundial8. En una reciente revisión sistemática sobre la seguridad y eficacia de la vacunación contra COVID-19 en pacientes con enfermedad renal11, se identificó que 16% de los estudios excluyeron explícitamente a pacientes con ERC (en cualquier estadio y circunstancia), 33% excluyeron pacientes con enfermedad renal grave, y en 44% de los estudios se dejó a la “discreción del investigador” la incorporación de pacientes con enfermedad renal. Solo 6% de los estudios utilizaron un umbral de filtrado glomerular específico (>60 ml/min/1,73m2) para determinar la elegibilidad de los pacientes a incluir. Específicamente en ensayos en fase 3 se incluyó a 39,4% de pacientes con ERC leve a moderada y en el 60,6% restante se dejó abierta la posibilidad para su exclusión. El 78% de los estudios que incluían virus atenuados no vivos y atenuados vivos excluyeron a pacientes que recibían inmunosupresión para trasplante renal o glomerulopatías, no siendo explícita la exclusión en el resto de los estudios. En los estudios en fase 3, el 93,5% excluyó a pacientes inmunodeprimidos; 64,5% excluyó a quienes recibían algún tipo de inmunosupresión, y 32,3% excluyó a quienes recibían inmunosupresión más allá de una dosis de prednisona de 10-20 mg/día11.
Sin embargo, algunos datos indirectos dan la pauta de que la vacunación puede ser efectiva. Pacientes en diálisis que han sobrevivido al COVID-19 tienen títulos de IgG contra el SARS-CoV-2 detectables hasta dos meses después de la infección12. Esto sugiere fuertemente que una seroconversión vinculada a la vacunación es también esperable en este grupo de pacientes. Adicionalmente, hay vasta experiencia con la vacunación contra influenza, hepatitis B y neumococo en pacientes con ERC avanzada, en diálisis y trasplantados renales, en donde se objetivan tasas de seroconversión de 33%-80% para influenza, por ejemplo13.
Vacunas disponibles contra SARS-CoV-2
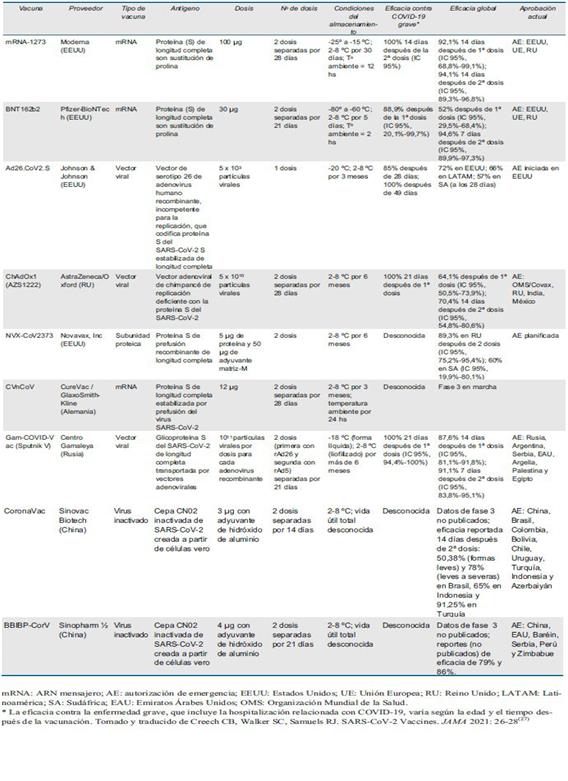
Las vacunas disponibles pertenecen a cuatro grupos: basadas en ácidos nucleicos (ARN o ADN), basadas en vectores virales, basadas en subunidades proteicas y de virus inactivados14. Las vacunas basadas en partículas de ARN, una vez que entran en las células del huésped, determinan la producción de la proteína S de SARS-CoV-2 estimulando al sistema inmune a producir anticuerpos contra ésta. Dentro de este grupo se encuentran las vacunas elaboradas por Pfizer (ARN Comirnaty©(BNT162b2)), Moderna y CureVac. Las vacunas basadas en partículas de ADN utilizan el mismo mecanismo descrito para las ARN, estando en etapa de evaluación la Inovio. Las vacunas basadas en vectores virales combinan sectores del SARS-CoV-2 y los incorporan a vectores virales (otros virus, por ejemplo, adenovirus) que son inoculados al huésped. En este grupo están las vacunas de vector viral no replicativo de AstraZeneca (AZD-1222 / ChAdOx1), Janssen, CanSino y Sputnik V. Las vacunas inactivadas y de subunidades proteicas utilizan para producir inmunogenicidad virus inactivados o un conjunto de subunidades proteicas de éstos. Dentro de este grupo se encuentran la vacuna a virus inactivado CoronaVac (Sinovac), Sinopharm, Barath y Novavax14. En la (tabla 1) se resumen las vacunas disponibles y sus principales características.
Recomendaciones según grupos de pacientes
Pacientes con ERC-no diálisis y pacientes en diálisis crónica (hemodiálisis y diálisis peritoneal)
Al igual que otros grupos de pacientes con enfermedad renal, no fueron incluidos en los ensayos clínicos que evaluaron la efectividad de las vacunas. El hallazgo de títulos elevados de IgG dirigidos contra SARS-CoV-2 en pacientes bajo tratamiento con diálisis infectados previamente12 podría sugerir que la vacuna tendrá también un efecto protector en esta población.
- Recomendamos la vacunación de todos los pacientes con ERC avanzada (en plan de diálisis crónica o fuera de ella) con los esquemas propuestos para las diferentes vacunas. No está definido aún si esta población requerirá un aumento de la dosis de inoculación, tal como ocurre con otras vacunas en este grupo, o si requerirán revacunación temprana.
- El grupo de pacientes en plan de hemodiálisis crónica puede ser vacunado en el contexto del procedimiento en su centro (previo o después de la hemodiálisis), sin necesidad de cambiar el régimen de anticoagulación (ver apartado de situaciones especiales), ni de suspenderse otros tratamientos que habitualmente recibe (eritropoyetina, etc.).
- Recomendamos optimizar el acceso a la vacunación de los pacientes con ERC avanzada, diálisis y trasplante mediante el aprovechamiento de los medios logísticos existentes para el control de pacientes trasplantados, programas de ERC-avanzada y unidades de hemodiálisis.
- En aquellos casos que reciban inmunosupresión por alguna causa, se actuará según lo recomendado en ese grupo particular.
- Recomendamos que en todos los casos la vacunación sea administrada sin importar si los pacientes tuvieron previamente COVID-19 o si tienen títulos IgG positivos para SARS-CoV-2.
Pacientes con trasplante renal funcionante y en lista de espera
Los receptores de trasplante renal son pacientes que presentan elevado riesgo de consecuencias graves por la infección por SARS- Cov-2, incluyendo la muerte en un alto porcentaje de casos (20% a 30%, según las series)6,15,16. Estas consecuencias adquieren más relevancia en los primeros meses del trasplante6,15,16. Si bien los receptores de trasplantes no se incluyeron en los ensayos clínicos, dada la experiencia con otras vacunas, no hay evidencia que sugiera que alguna de las vacunas disponibles contra COVID-19 no sea segura y protectora en este grupo de pacientes. El antecedente de que se ha objetivado seroconversión en más del 70% de pacientes con trasplante renal que se han infectado por SARS-CoV-2, apoya la hipótesis de que la vacunación puede ser efectiva en este grupo17. Sin embargo, se ha observado que hasta en 20% hay un descenso del título de anticuerpos en el tiempo. Los factores asociados a este descenso fueron el uso de inhibidores de la calcineurina y los esteroides18. Por lo tanto, al igual que otros grupos de pacientes bajo tratamiento inmunosupresor, es posible que la respuesta esperada frente a la vacunación sea atenuada en su magnitud y duración en comparación con la población general19,20. Independientemente de las consideraciones realizadas, esta población debe vacunarse contra SARS-CoV-217,21.
- Recomendamos la vacunación de todos los pacientes en lista de espera de trasplante. En quienes se encuentran coordinados para trasplante intervivo es deseable que completen la vacunación un mes previo al procedimiento y al menos dos semanas antes del trasplante renal como plazo mínimo.
- No se recomienda excluir al paciente de lista de trasplante durante ningún período tras la primera o segunda dosis de la vacuna. Riesgos y beneficios deben ser individualizados en cada caso.
- Recomendamos la vacunación de todos los receptores de trasplante renal luego de transcurrido el primer mes del trasplante.
- En las situaciones en que se administra timoglobulina o rituximab al trasplante, recomendamos diferir la vacunación hasta el tercer mes luego del trasplante.
- Si el paciente ha recibido tratamiento antirrechazo (bolos de metilprednisolona, recambio plasmático terapéutico, gammaglobulina), recomendamos diferir la vacunación al menos dos semanas.
- Recomendamos aprovechar las situaciones clínicas de estabilidad y menor requerimiento de inmunosupresión para proceder a la vacunación. Sin perjuicio de ello, no es recomendable retrasar excesivamente la vacunación.
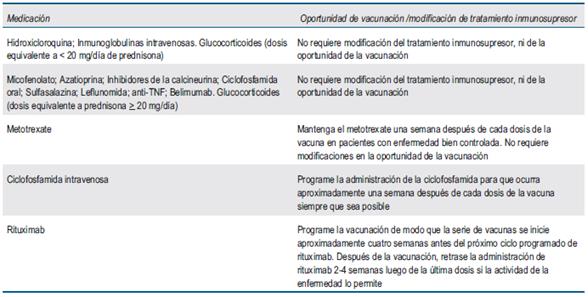
- Las consideraciones en referencia a la oportunidad y eventuales modificaciones del tratamiento inmunosupresor son recogidas en la (tabla 2).
- Recomendamos que en todos los casos la vacunación sea administrada sin importar si los pacientes tuvieron previamente COVID-19 o si tienen títulos IgG positivos para SARS-CoV-2.
Pacientes con enfermedades autoinmunes/inflamatorias y/o bajo tratamiento inmunosupresor (enfermedades autoinmunes sistémicas, glomerulopatías, -no trasplante renal-)
Los pacientes bajo tratamiento inmunosupresor han presentado en todo el mundo una mayor prevalencia de hospitalización por COVID-19 y una tasa de mortalidad más elevada cuando se comparó con la población general19,22. Los pacientes inmunodeprimidos no han sido incluidos en la mayoría de los ensayos clínicos de las vacunas para COVID-1922. Es posible que la respuesta esperada frente a la vacunación para muchos pacientes bajo tratamiento inmunosupresor/inmunomodulador sea atenuada en su magnitud y duración en comparación con la población general19,20,22; sin embargo, ello no constituye un argumento de peso para no indicarles la vacunación19,20,22. Existe un riesgo teórico de “brote” o empeoramiento de la enfermedad autoinmune después de la vacunación, no obstante, el beneficio de la vacuna para los pacientes con enfermedades autoinmunes supera el riesgo potencial de cualquier posible manifestación de autoinmunidad19,20,22. En función de lo analizado y basados en las recomendaciones del Colegio Americano de Reumatología (ACR) y de la Liga Europea contra el Reumatismo (EULAR)19,20:
- Recomendamos que los pacientes con enfermedades autoinmunes reciban vacunación contra SARS- CoV-2 de acuerdo a lo planificado según su grupo de edad y comorbilidades.
- Recomendamos, de preferencia, la vacunación en un momento en que la enfermedad de base esté estable y/o sin actividad reciente. En la tabla 2 se realizan las consideraciones pertinentes sobre el mejor momento de indicar la vacunación en función del tratamiento inmunosupresor, así como eventuales modificaciones en caso de requerirse.
- Los pacientes (con o sin enfermedades autoinmunes/inflamatorias) que reciben tratamiento inmunosupresor deben recibir vacunación contra SARS- CoV-2 de acuerdo a lo planificado según su grupo de edad y comorbilidades.
- A excepción de las vacunas con virus vivos o con vectores replicantes (que no se recomiendan en este grupo de pacientes), no existe preferencia de una vacuna sobre otra para ser administrada. En Uruguay las vacunas disponibles pueden ser administradas sin preferencias en este grupo.
- No recomendamos cambios en la pauta de administración (dosis, distancia entre dosis) en este grupo de pacientes.
- No recomendamos realizar test serológicos en busca de anticuerpos contra SARS-CoV-2 en forma previa ni posterior a la vacunación. Tampoco se recomienda evaluar sistemáticamente con estudios de laboratorio la presencia de “brote” de su enfermedad autoinmune si no hay otras manifestaciones que así lo indiquen.
- No recomendamos interrumpir el tratamiento inmunosupresor para la administración de la vacuna. Esto implicaría riesgo de “brote” o empeoramiento de su enfermedad. Tampoco se recomienda modificar la pauta de administración del tratamiento inmunosupresor.
- Recomendamos que en todos los casos la vacunación sea administrada sin importar si los pacientes tuvieron previamente COVID-19 o si tienen títulos IgG positivos para SARS-CoV-2.
Situaciones particulares
Pacientes anticoagulados, con trombocitopenia u otras situaciones que los predispongan al sangrado
Existe amplia experiencia sobre la vacunación por vía intramuscular en este grupo de pacientes. Regularmente reciben vacunación antigripal (anual), así como otras vacunas por esa vía sin que ello determine complicaciones mayores23. Ninguno de estos escenarios supone una contraindicación para la vacunación.
Antagonistas de la vitamina K (warfarina)
- En los pacientes anticoagulados con antagonistas de la vitamina K (warfarina), no debe suspenderse la anticoagulación para administrarse la vacuna24,25.
- En los pacientes que están recibiendo fármacos antivitamina K (warfarina), es conveniente confirmar que se encuentran dentro de su rango de INR objetivo al administrarse la vacuna24,25.
Anticoagulantes orales de acción directa (dabigatrán, rivaroxabán, apixabán)
- En los pacientes anticoagulados con anticoagulantes directos (dabigatrán, rivaroxabán, apixabán), no debe suspenderse la anticoagulación para administrarse la vacuna24,25.
- En los pacientes en tratamiento con anticoagulantes orales de acción directa (dabigatrán, rivaroxabán, apixabán), se debe de evitar el momento de pico máximo del fármaco al programar la vacunación24,25. Para ello, se puede retrasar la dosis del anticoagulante el día de la vacunación hasta después de administrada la vacuna26.
Antiagregantes plaquetarios (AAS, clopodogrel, ticagrelor, plasugrel)
- Se puede mantener el tratamiento habitual sin requerirse ningún ajuste el día de la vacunación26.
Trombocitopenia
- En pacientes con trombocitopenia persistente se recomienda25:
- Si el recuento plaquetario > 50.000/mm3 no se requieren medidas especiales.
- Si el recuento plaquetario es de 30.000 a 50.000/mm3, se recomienda comprimir la zona de punción (sin frotar) durante al menos tres minutos.
- Si el recuento es < 30.000/mm3, se recomienda consultar al hematólogo para que haga las indicaciones específicas adecuadas a la situación.
- En todos los casos se recomienda la administración con aguja fina (no más de 23G) y presionar la zona de punción (sin frotar) al menos durante 3 minutos24,25.
- En pacientes con otras patologías hematológicas (hemofilia, etc.), se recomienda consultar al hematólogo para que haga las indicaciones específicas adecuadas a la situación24,25.