Introducción
El drenaje lumbar externo (DLE) consiste en la colocación de un catéter en el espacio subaracnoideo espinal a nivel lumbar con el objetivo de extraer líquido cefalorraquídeo (LCR), usualmente con fines diagnósticos y terapéuticos.
Existen dos procedimientos para el drenaje externo de LCR. Uno es la colocación de un drenaje ventricular externo (DVE), y el otro es, precisamente, la colocación de un drenaje lumbar. En relación al DVE, existen algunas dificultades en su uso: los ventrículos cerebrales muchas veces son pequeños en situaciones de hipertensión intracraneana (HIC), con escaso volumen de LCR para drenar y su cateterización puede ser compleja; es conocido, además, el alto riesgo de infección que el DVE conlleva (9%-20% según las diferentes series); hay también cierto riesgo de trauma con hemorragia intracraneana tanto en su emplazamiento como en su remoción, lo que no es raro durante la curva de aprendizaje (aproximadamente 5% a 7%)1-4. Por otro lado, y en relación al DLE, el espacio subaracnoideo espinal es de un volumen mayor al espacio ventricular (75 ml vs 35 ml) y de forma más regular, comunicándose ampliamente a través del foramen magno con todo el espacio subaracnoideo intracranenano.
Por décadas, la punción lumbar y fundamentalmente el DLE han sido estrictamente contraindicados en situaciones de sospecha o confirmación de elevación de la presión intracraneana (PIC)5,6. De hecho, en la última edición de las guías de la Brain Trauma Foundation el DLE no es ni siquiera citado7. Tampoco se lo recomienda en el más reciente consenso de Seattle para el manejo de la hipertensión intracraneal (HIC), figurando, en cambio, en las guías pediátricas8,9. Sin embargo, en los últimos años se ha acumulado evidencia clínica importante a favor de su uso seguro en diversos tipos y severidad de neuroinjurias agudas. En este sentido, y siguiendo el estudio pionero de Korein y colaboradores que revaluó el drenaje de LCR a través de la punción lumbar en situación de HIC, fueron Baldwin y Rekate en 1991 los primeros en publicar el uso del DLE para el tratamiento de la HIC refractaria en el trauma encefalocraneano, fundamentalmente en los casos de HIC difusa (sin lesión focal, desviación de línea media o masa quirúgica evacuable)10-13. En otra situación clínica, como la hemorragia subaracnoidea (HSA), el estudio pionero de Klimo y colaboradores mostró un beneficio clínico significativo mediante el aumento del aclaramiento de sangre por medio de un DLE14.
En este manuscrito, realizaremos una revisión no sistemática del manejo del DLE en los pacientes neurocríticos, poniendo especial énfasis en sus aspectos prácticos (indicaciones, descripción técnica y complicaciones), así como en la evidencia clínica existente.
Indicaciones y manejo en diferentes escenarios clínicos
Los principales usos del DLE, de donde surgen las indicaciones de éste, son:
a)La remoción de sangre a través de la extracción de LCR hemático. Esta indicación surge en casos de HSA, especialmente de origen aneurismático. Dado que la sangre derramada en el espacio extravascular se considera un factor etiopatogénico clave en el desarrollo de los fenómenos isquémicos diferidos en esta patología, se plantea que el lavado progresivo del LCR hemorrágico podría mitigar la isquemia cerebral diferida.
b)El control de la HIC. Si bien en un tiempo fue contraindicada en esta situación clínica, puede actualmente ser un recurso a usar en formas refractarias de HIC si cumplen a priori ciertas exigencias. Al mismo tiempo es indicación específica y de elección en la HIC con cisternas basales presentes, cuya forma más típica es la HIC en la criptococosis meníngea. También puede verse en el trauma encefalocraneano (TEC), HSA y otras infecciones meningoencefálicas. Cabe aclarar que está contraindicado cuando el origen de la HIC son lesiones masa a nivel hemisférico o de fosa posterior.
c)El propio drenaje de LCR independiente de la HIC. Existen tres situaciones clínicas: 1) Protección de isquemia medular en cirugía compleja o procedimientos endovasculares sobre aorta torácica. También se postula en la injuria medular de cualquier origen. En todos estos casos, el objetivo es bajar la presión intraespinal (PIS) y aumentar la presión de perfusión medular (PPM); 2) Drenaje temporal de una hidrocefalia comunicante, muy frecuente posdescompresiva, y 3) Disminución del gasto de una fístula de LCR encefalocraneana. En esta situación es importante aclarar que si bien el DLE puede favorecer el cierre espontáneo de la fístula, tiene el riesgo de crear una presión negativa y, si la solución de continuidad es grande, permitir la entrada de aire provocando un neumoencéfalo que puede ser grave en los casos que se presente a tensión. También en las fístulas de piso anterior, con comunicación con senos o etmoides, puede favorecer la entrada de microorganismos y con esto meningitis o colecciones supuradas.
d)Medida de la PIS. En todas las situaciones de DLE puede realizarse la medida de la PIS, la cual debería ser igual a la PIC con el paciente en decúbito dorsal a 0º (tomando como referencia del cero hemodinámico el trago y la línea medio-axilar, cuyos niveles coinciden en esa posición). La maniobra de Queckenstedt consiste en la compresión biyugular, la cual debe provocar un ascenso de la PIS antes de los 10 segundos en caso de ausencia de obstrucción del canal espinal. La PIS extrapolable a la PIC es la PIS, cuyo cero se mide a nivel del trago, en caso de haber descartado obstrucción espinal con la maniobra de Queckenstedt en los pacientes que están semisentados a distintos grados.
e)Administración de fármacos intraespinales. En general, pensando en su efecto encefálico o espinal. Así se administran: antibióticos, anestésicos locales, baclofeno, etc.
A continuación, veremos algunas de las situaciones clínicas citadas en donde es frecuente el uso del DLE.
Disminución del riesgo de isquemia cerebral diferida en la HSA
La cantidad de sangre volcada en las cisternas basales se considera un factor pronóstico mayor luego de una HSA, estando fuertemente asociada a complicaciones como la isquemia cerebral diferida y el vasoespasmo cerebral15. La entidad del sangrado ha sido cuantificada por diferentes escalas tomográficas, siendo la escala de Fisher la más utilizada (tabla 1)16. La remoción rápida de la sangre derramada, entre otras acciones beneficiosas, evita los múltiples procesos que esta sangre desencadena y que condicionan la injuria isquémica tardía, así como el riesgo de hidrocefalia crónica pos-HSA. En este sentido, el drenaje lumbar de LCR agrega un beneficio fisiológico al manejo de estos pacientes, lo que ha sido mostrado en resultados de estudios clínicos de variada evidencia en los últimos años.
Tabla 1: Escala de Fisher para la evaluación tomográfica de la cantidad del sangrado en la hemorragia subaracnoidea aneurismática16.

El estudio ya citado sobre este tema de Klimo y colaboradores analizó retrospectivamente 167 pacientes con HSA. Los pacientes tratados con DLE experimentaron menos vasoespasmo cerebral (17% vs 51%), menos infartos vinculados al vasoespasmo (7% vs 27%), así como una mejor evolución neurológica a los tres meses (71% vs 35%) comparados con los pacientes en los que no se colocó DLE. Todos estos resultados fueron estadísticamente significativos en el estudio univariado y multivariado, excepto la evolución neurológica14.
El trabajo de Maeda y colaboradores mostró mediante volumetría tomográfica que el DLE puede ser más efectivo que la DVE para el aclaramiento de sangre en la HSA17.
El estudio LUMAS, publicado por Al-Tamimi y colaboradores en 2012, consistió en un ensayo prospectivo randomizado unicéntrico que analizó el uso del DLE en 210 pacientes con HSA18. El DLE redujo la incidencia de déficit isquémico diferido (35% vs 21%) y mejoró la evolución neurológica inmediata, si bien esta mejoría no fue estadísticamente significativa a los seis meses. Una de las limitaciones más importantes de este estudio es que no incluyó a los pacientes con mal grado clínico, los que a su vez tienen mayor riesgo de vasoespasmo cerebral y déficit neurológico diferido.
Otro estudio, realizado por Fang y colaboradores, comparó específicamente los beneficios del DLE en las HSA con diferente cantidad de sangre cisternal. Fue un trabajo retrospectivo de 193 pacientes19. En las HSA Fisher 3 o 4, el DLE redujo el riesgo de vasoespasmo, isquemia cerebral diferida e hidrocefalia, mejorando asimismo los resultados neurológicos a los tres meses. Esto no ocurrió en las HSA con poco sangrado (Fisher 0-2), lo que apoya el concepto de que son los pacientes con mayor sangrado los que se benefican de DLE.
En un metaanálisis publicado por Alcalá-Cerra y colaboradores en 2016, se encontraron seis estudios clínicos relacionados al DLE en la HSA, de los cuales tres eran controlados y randomizados y tres observacionales14,17-23. El análisis mostró que el DLE se asoció con un menor riesgo significativo de aparición de nuevos infartos cerebrales en la tomografía computada (TC) o resonancia magnética (RM), así como de deterioro neurológico relacionado a isquemia cerebral tardía, sin observarse heterogeneidad significativa entre los estudios.
En otro metaanálisis publicado por Qian y colaboradores en 2016, el drenaje de LCR en pacientes con HSA mostró reducir en forma significativa la incidencia de vasoespasmo cerebral angiográfico y sintomático, comparado con aquellos en los que no se realizó dicho procedimiento (18,8% vs 41,4%, p<0,01)24. Asimismo, se encontró que el DLE redujo significativamente la ocurrencia de déficit neurológico isquémico diferido (DNID) e infarto cerebral, y se asoció con una mejor recuperación neurológica a largo plazo (80,9% vs 63,5%, OR 2,86, p<0,01). Comparado con el otro método utilizado para el drenaje de LCR, como es la derivación ventricular externa (DVE), los pacientes con DLE tuvieron una mejor evolución a largo plazo en forma significativa (85,8% vs 81,7%, OR 3,11, p=0,02). Por otro lado, en este mismo estudio, se halló una incidencia de complicaciones asociadas al DLE de 5,3%, las cuales no impactaron negativamente en la evolución neurológica de estos pacientes.
Probablemente el estudio EARLYDRAIN, ya finalizado, aunque aún pendiente su publicación, arroje más certeza en la evidencia clínica del DLE en la HSA. Se trata de un estudio randomizado controlado y multicéntrico de 300 pacientes que, a diferencia del LUMAS, incluyó todos los grados clínicos de HSA25.
Otro beneficio potencial que se le ha atribuido al DLE es la disminución del riesgo de desarrollar hidrocefalia en la evolución a través de la eliminación de productos hemáticos del espacio subaracnoideo que podrían obstruir las vellosidades aracnoideas de Pacchioni. Sin embargo, este metaanálisis no mostró diferencias en la necesidad de requerir derivación ventricular definitiva en este tipo de pacientes con el uso de DLE23.
En suma, en el escenario de HSA el DLE tiene indicación fundamentalmente en aquellos pacientes que tienen mucho sangrado o hidrocefalia de tipo comunicante. Se drenará un volumen constante de LCR entre 5-10 ml/h durante 5-7 días luego de asegurado el aneurisma (clipado o embolizado).
Tratamiento de la HIC refractaria con DLE
La HIC es un factor principal de mal pronóstico en los pacientes neurocríticos. Las medidas terapéuticas de la HIC llamadas de primer nivel (drenaje ventricular de LCR, sedación y analgesia, osmoterapia e hiperventilación moderada) han sido consensuadas por la mayoría de los autores4-6. Cuando la PIC se mantiene mayor de 25 mmHg y no responde a estas medidas de primer nivel, nos encontramos frente a una HIC refractaria, la cual asocia una significativa morbimortalidad. En este sentido, las medidas de segundo o tercer nivel (barbitúricos, craniectomía descompresiva, hipotermia) continúan siendo controversiales, variables en su implementación entre los diferentes centros, y asociadas a mayores efectos adversos dada su invasividad.
En algunas situaciones específicas de pacientes con HIC refractaria, el DLE ha mostrado una buena relación riesgo-beneficio. Varios trabajos retrospectivos sustentan esto tanto a nivel de niños como de adultos26-31. La mayoría de estos autores concuerdan que se deben reunir ciertas condiciones previas para decidir la colocación del DLE, entre las que se destacan: a) la ausencia de una lesión ocupante de espacio con indicación quirúrgica; b) la existencia de cisternas basales presentes o discernibles, y c) la ausencia de desviación de línea media mayor a 5 mm32,33.
Algunos autores, como Manet y colaboradores, agregan a estas condiciones el desarrollo gradual de colecciones subaracnoideas o subdurales localizadas en la cisura de Silvio o interhemisférica, o en los surcos de la convexidad. Esto se basa en el mecanismo fisiopatológico planteado por estos autores como causa de esta situación y que consiste en la denominada hidrocefalia externa34-36.
Cuando se coloque un DLE en esta situación clínica, se drenará LCR cuando la PIC sea mayor a 25 mmHg, siempre contra una altura de 15-20 cm H2O, o presión de drenaje de 15 mmHg. Para que esta maniobra sea más segura, es importante que el paciente esté en decúbito dorsal a 0º y drenar la menor cantidad de LCR para descender la PIC por debajo de 20 mm de Hg, no superando un volumen de drenado mayor a 20 ml/h. La posición en decúbito supino a 0º atenuará el peligro de descenso y hundimiento del neuroeje con enclavamiento paradojal de éste al extraer LCR espinal. Un DLE controlado por dispositivo LiquoGuard-7®, con alarmas de seguridad de presión y de volumen drenado, teóricamente podría contribuir a la seguridad de esta técnica. Es importante aclarar que el drenaje aspirativo de LCR por el DLE está contraindicado en casos de manejo de HIC.
Tratamiento de la HIC con cisternas basales presentes
Esta situación, un tiempo atrás ignorada, ha comenzado a ser reconocida con frecuencia en varias entidades clínicas. Una de las primeras entidades donde se la reconoció fue la HIC en el contexto de la meningitis producida por criptococo en el paciente con VIH-SIDA. Otras entidades en las que se identificó este mecanismo son: algunos casos de HIC en el TEC, algunas situaciones posdescompresivas, algunos casos de HSA, en el pseudotumor cerebral y en otras infecciones meningoencefálicas. Fisiopatológicamente no parece que haya un solo mecanismo en su génesis. Se postula que hay trastornos de circulación del LCR, junto con cambios en las propiedades mecánicas del parénquima cerebral por edema o por otro proceso agudo (isquemia) o crónico cerebral, que imposibilita que el encéfalo se expanda desde el centro, como en una hidrocefalia habitual. Esto lleva a que el LCR se acumule en el espacio subaracnoideo de la convexidad (hidrocefalia externa), lo que habitualmente es subestimado por la TC y, en cambio, es bien observado en la RM. La apariencia aparentemente normal (pseudonormal) de la TC en cuanto al buffer espacial, así como el desconocimiento de esta entidad, lleva con frecuencia a confusiones diagnósticas, desconfianza de la medida invasiva de la PIC y conductas terapéuticas inadecuadas. El diagnóstico se basa en los siguientes elementos: alto índice de sospecha cuando se presenta una patología como las citadas; presencia de HIC con cisternas presentes y conservación del buffer espacial, o los métodos no invasivos (medida ultrasonográfica de la vaina del nervio óptico o el Doppler transcraneal) detectan hallazgos sugestivos de HIC. En todos estos casos el DLE es de elección para el control de la HIC y debe ser considerado la primera medida a realizar34-38.
Meningitis criptocócica en paciente con sida
Aproximadamente el 50% de los pacientes con esta infección oportunista presentan como complicación HIC, la cual se transforma, además, en uno de los factores pronósticos más importantes. Las causas del aumento de la PIC en esta enfermedad no se conocen con certeza, si bien se cree que se vinculan a alteración de la absorción o aumento de la producción de LCR provocados por el microorganismo y su cápsula de polisacáridos39. Asimismo, hay modificaciones simultáneas del parénquima cerebral, por lo que esta patología adopta con frecuencia el patrón de HIC con tomografía pseudonormal (cisternas basales presentes). Un elemento importante a destacar es la poca o nula dilatación ventricular en estos casos. Cuando esta complicación se sospecha o se presenta, se recomienda por los diferentes autores la realización de una punción lumbar para medir la presión de apertura del LCR. Si esta presión es mayor a 25 mmHg, la mayoría de los autores recomienda la extracción terapéutica de 10-20 ml de LCR40. Cuando esta situación de presión mayor a 25 mmHg (HIC) se repite en varias oportunidades o se mantiene en el tiempo, algunos autores plantean la colocación de un DLE para su mejor control. Esta técnica ha demostrado ser una medida segura y efectiva en el manejo de la HIC refractaria en este grupo de pacientes, asociándose a un rápido y mantenido descenso de la PIC, así como al control de los signos y síntomas vinculados41-43. En las series referidas, los autores mantuvieron el drenaje de LCR a través del DLE si el mismo superaba una altura de 20 cm H2O, como control terapéutico y de seguridad clínica.
Protección de isquemia medular en cirugía de aorta torácica compleja
Los déficit neurológicos vinculados fundamentalmente a isquemia medular, constituyen una complicación poco frecuente pero dramática de la cirugía de reparación de la aorta torácica y tóraco-abdominal, con una incidencia entre 3%-7% y una elevada morbimortalidad. Esto se vincula tanto a cirugía a cielo abierto como, aunque en menor grado, a los procedimientos endovasculares a nivel de la aorta torácica. Existen factores de riesgo perioperatorios asociados a mayor riesgo de isquemia medular: cirugía de emergencia, disección, lesiones extensas a nivel de la lesión, edad avanzada, cirugía aórtica abdominal previa, insuficiencia renal, oclusión de la arteria subclavia sin previa revascularización y la necesidad de utilizar más de tres stents endovasculares44,45.
En este sentido, existen varias estrategias perioperatorias disponibles para reducir la incidencia y severidad de la isquemia medular, siendo el drenaje de LCR mediante un DLE la medida más efectiva44,46. Esto se explica por varios factores operatorios (tanto en cirugía convencional como endovascular) que pueden contribuir a la isquemia medular, como la oclusión de arterias perforantes aórticas que irrigan la médula espinal, así como elevación de la presión del LCR espinal por retracción quirúrgica del arco aórtico. Esto generará una disminución de la PPM a través tanto de la disminución del flujo o presión arterial (PAM) como del aumento de la PIS (PPM = PAM - PIS). Esto puede ocurrir inmediatamente a la cirugía (isquemia intraoperatoria) o en forma diferida hasta varios días después (probablemente por edema medular debido a fenómenos de isquemia-reperfusión). Con la utilización de este procedimiento, la incidencia de isquemia medular en centros especializados ha disminuido a menos de 1%, ya que disminuye uno de los factores de riesgo mencionados como es la hipertensión del LCR espinal47.
En esta situación clínica, el DLE se colocará en el preoperatorio inmediato y se monitorizará la presión de LCR (PLCR) en forma continua durante el acto operatorio y las primeras 48-72 horas del posoperatorio. Se buscará como objetivo una PAM mayor o igual a 80 mmHg y una PIS menor a 10-12 mmHg, con una PPM de 70 mmHg. La aparición de un déficit espinal motor o sensitivo debe hacer sospechar la isquemia medular. Si los signos clínicos no mejoran con los objetivos anteriormente citados, se puede aumentar la PAM con vasopresores a más de 90 mmHg, como prueba terapéutica para lograr una mejor PPM.
Contraindicaciones del DLE
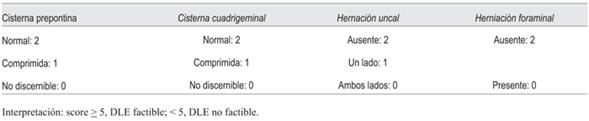
Está absolutamente contraindicado colocar un DLE cuando existe compresión de las cisternas basales o desviación de línea media encefálica mayor a 5 mm en la TC, dado el riesgo de desencadenar una herniación encefálica descendente durante el procedimiento. Asimismo, está contraindicado cuando existe un proceso expansivo de un hemisferio cerebral con efecto de masa o cuando hay HIC secundaria a un proceso expansivo de fosa posterior. El Score de Reserva Intracraneana de Innsbruck, descrito recientemente por Bauer y colaboradores, constituye un método basado en la imagen de TC el cual puede predecir la seguridad clínica del DLE, evitando la presentación de la complicación más temida de este método como es la herniación encefálica descendente. Se basa en la caracterización tomográfica de cuatro parámetros: cisterna prepontina, cisterna cuadrigeminal, herniación uncal y herniación foraminal, con un puntaje de 0 a 2 para cada uno de ellos. Un score de 5 puntos o más, se asoció con un drenaje lumbar de LCR efectivo y seguro para el tratamiento de hipertensión intracraneana, de acuerdo con un estudio de cohorte con un número pequeño de pacientes publicado por dichos autores48. En la (tabla 2) se esquematiza dicho score.
Existe contraindicación para la colocación de un DLE en un paciente que presente plaquetopenia (menor a 50.000/mm3) o alteración de la coagulación (tasa de protrombina menor a 50%).
Descripción del método
En cuanto a la colocación del catéter se deben seguir algunos pasos importantes, a saber: posición adecuada del paciente, decúbito lateral o sentado y flexionado; realización del procedimiento estándar de punción lumbar con una aguja Tuohy (14 o 16 gauge); una vez en el espacio subaracnoideo, se avanza el catéter especialmente diseñado para DLE (17 o 18 gauge) unos 20 cm, retirándose posteriormente la aguja; tunelización subcutánea del catéter, y conexión al sistema de drenaje, adhiriendo el catéter al flanco del paciente para evitar acodamientos. La tunelización subcutánea larga > 10 cm es un factor importante para reducir el riesgo de fístula de LCR pericatéter y fundamentalmente de infección, así como para reducir la migración o salida del catéter. Es conveniente usar sets diseñados específicamente para DLE. Los catéteres de analgesia peridural son demasiados finos para su uso intraespinal, y aunque pueden ser usados, suelen obstruirse en caso de LCR hemorrágico o purulento. Por la misma razón, además, no permiten un buen registro de la PIS.
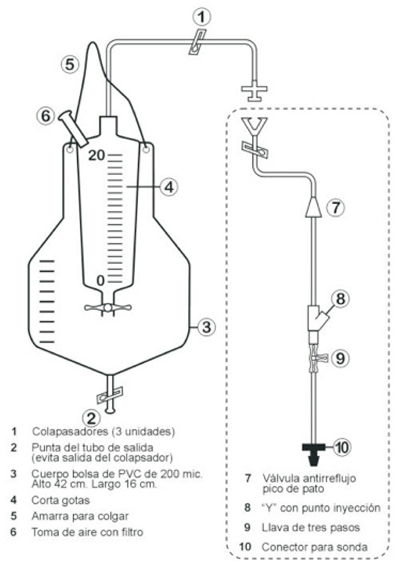
El sistema de recolección de LCR debe reunir cuatro características esenciales: 1) sistema cerrado, hermético, con gotero y receptáculo no colapsable; 2) toma de aire, con filtro antibacteriano; 3) válvula antirreflujo en la línea prerreceptáculo; 4) tapones de goma, incluidos en pequeñas colaterales de la línea de conexión (figura 1)3. El transductor de presión debe colocarse y cerarse a la altura de la aurícula derecha (línea medioaxilar). Esto medirá la presión de LCR espinal lumbar (PIS lumbar).
Existe la posibilidad de realizar DLE con un sistema computarizado especialmente diseñado para ese fin (LiquoGuard-7®), que permite monitorizar la presión del LCR y drenar en forma simultánea49. Se trata de un sistema modular, automático, seguro, que no necesita de regulación de alturas, ni ninguna otra manipulación. Cuenta con dos sensores de presión integrados al sistema. Este método asegura un drenaje de LCR cuando supera exactamente un nivel de presión de LCR predeterminado y con un límite máximo de volumen drenado (nunca superior a 15-20 ml/h). Cuenta con control de flujo de LCR y límites con alarmas de presión y de volumen de LCR, que permiten la detección precoz de oclusiones inadvertidas del catéter a la vez que evitan los sobredrenajes peligrosos.
Los objetivos de la cantidad de LCR a drenar, la velocidad de drenaje así como los límites de presiones y volúmenes correspondientes, dependerán de la razón por la cual se colocó el drenaje lumbar. Éstos fueron analizados previamente, y por separado, en los diferentes escenarios clínicos planteados.
Se deben realizar controles clínicos durante el DLE que incluyen:
a) nivel de conciencia: cualquier disminución sin una causa evidente debe hacer revisar el funcionamiento del mismo, buscando, por ejemplo, el sobredrenaje;
b) cambios pupilares (anisocoria o midriasis): su aparición debe determinar como primera medida emergente el cierre inmediato del DLE, dada la sospecha clínica de herniación encefálica descendente (ver Complicaciones).
En todos los casos de puesta en marcha de un DLE es recomendable y más seguro mantener al paciente en decúbito supino a 0º o, en su defecto, a no más de 10º, a efectos de evitar hundimientos peligrosos del neuroeje. Se debe subrayar que la colocación del paciente con DLE en decúbito supino a 0º aumenta la seguridad del procedimiento.
En los casos que exista HIC o el paciente presente riesgo de herniación encefálica descendente debe realizarse un control más específico y precoz de la presión lumbar de LCR, colocando un transductor al extremo del catéter espinal lumbar. Esto permite medir el gradiente de presión craneolumbar (PIC - presión lumbar) para ambos monitores cerados a un mismo nivel (a nivel del trago, por ejemplo). Cuando dicho gradiente es mayor de 5 mmHg, se recomienda detener el drenaje de LCR lumbar. Se recomienda retirar el catéter luego que la PIC se controló al menos 24 horas con el DLE cerrado25,50.
Existe controversia sobre si la utilización del DLE debe ser continua o intermitente. Excepto para la situación de HIC refractaria, en nuestra opinión, el drenaje continuo ofrece varias ventajas, como un mayor aclaramiento de sangre y un mejor drenaje de LCR, y eventualmente control de la PIC.
Durante la instauración de DLE debe monitorizarse el descenso del neuroeje mediante dos parámetros:
a) clínicamente, con caída del nivel de GCS, cefaleas y aparición de compromiso de pares craneanos III y VI.
b) en la TC, con caída del score de Innsbruck y aumento del sag ratio o índice de Komotar.
Éste consiste en el cociente entre el diámetro máximo anteroposterior y el diámetro máximo lateral del tronco encefálico medido a nivel interpeduncular del mesencéfalo. Normalmente este cociente o índice es menor a 0,9 (más ancho que largo). Cuando existe hundimiento del tronco encefálico por hipotensión o hipovolemia de LCR, el tronco se alarga y este cociente pasa a ser mayor a 0,9 (en general se hace mayor a 1)51.
En su descripción original, Komotar define el síndrome de hundimiento encefálico o brain sag en base a la existencia de los siguientes tres criterios diagnósticos41:
1. Desaparición de las cisternas basales en la TC.
2. Rápida mejoría clínica con la posición de Trendelenburg.
3. Imagen de TC o RM que muestre elongamiento y descenso del tronco cerebral (medido por el sag ratio).
En la (figura 2) se muestran las imágenes tomográficas de un caso clínico de un paciente con HSA en el que se colocó DLE y se midió el sag ratio descrito por Komotar y colaboradores.
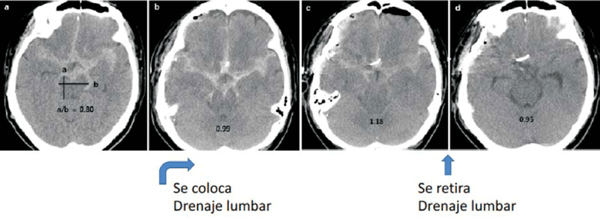
Figura 2: Medida tomográfica del sag ratio descrito por Komotar y colaboradores51. Se muestran las imágenes seriadas de un paciente con HSA en el que se colocó un DLE. a) TC inicial, antes de colocar el DLE; b) TC a las 24 horas de colocado el DLE; c) TC a las 48 horas de colocado el DLE (se observa la desaparición de las cisternas basales y aumento del sag ratio a 1,18); d) TC 12 horas luego de retirado el DLE.
Complicaciones
1. La complicación más grave asociada al DLE es la herniación encefálica descendente de las amígdalas cerebelosas a través del foramen magnum debido a hipotensión intracraneana o a la generación de un gradiente de presión cráneo-espinal significativo. Si bien se trata de una situación muy poco frecuente, puede tener consecuencias devastadoras52. El punto más importante para prevenir o detectar precozmente esta complicación es el estudio detallado de la TC, como ya se analizó previamente con el score de reserva intracraneana. La aparición durante el DLE de hundimiento encefálico o brain sag en la TC o RM es otro elemento imagenológico que debe advertir al clínico sobre el riesgo de esta complicación, como ya se analizó. Su presentación, a veces con la instalación de una anisocoria, constituye una emergencia terapéutica que requerirá las siguientes medidas: detención inmediata de drenaje de LCR, colocación del paciente en posición de Trendelenburg, con descenso del nivel de la cabeza por debajo del tronco a -20º a -30º; si en 15 a 20 minutos no retrocede la semiología, se pueden hacer movimientos de flexo-extensión cervical a efectos de desenclavar el neuroeje. No deben realizarse medidas dirigidas a tratar una HIC (osmoterapia, hiperventilación), dado que esto pueda agravar la situación clínica del paciente.
2. Puede presentarse declinación funcional neurológica o cefalea, por hipotensión intracraneana o hipovolemia de LCR, sin cambios pupilares ni otros elementos clínicos de alteración del tronco encefálico. Esto determinará la detención del DLE para reevaluar posteriormente su continuidad o no, de acuerdo a la situación clínica y tomográfica del paciente.
3. El DLE conlleva un riesgo aumentado de infecciones del LCR, como meningitis. Si bien es bajo (2% según el estudio LUMAS) y claramente inferior al drenaje ventricular externo, se asocia a un aumento de la morbilidad y de la estadía hospitalaria de estos pacientes18. Todas las medidas anteriormente descritas durante la inserción y manipulación del DLE se resumen en el concepto de paquete o bundle de medidas, las cuales tienen como objetivo final disminuir las complicaciones relacionadas a su uso, principalmente las infecciones. Las mismas han sido descritas y validadas para el drenaje ventricular externo, por lo que planteamos extrapolarlas al manejo del DLE53. Son una serie de medidas que deben aplicarse en conjunto, dado que la no aplicación de alguna de ellas, llevará a la falla de su efectividad. Se agrupan en cuatro ítems:
a) reeducación del personal de salud;
b) manipulación aséptica y meticulosa del DLE;
c) toma de muestra solo cuando se sospeche infección;
d) la menor duración posible del catéter lumbar, preferentemente menos de 7-10 días.
4. Si bien es poco frecuente, puede producirse un hematoma epidural espinal con compresión de la cola de caballo luego de la colocación de un drenaje lumbar.
5. Con baja incidencia, también, pueden producirse hemorragias cerebrales, extracerebrales o intraventriculares por hiperdrenaje o descenso del neuroeje.
Conclusiones
El DLE se presenta como una opción terapéutica novedosa y basada en conceptos fisiológicos y fisiopatológicos relevantes para pacientes que presentan diversas situaciones patológicas encefálicas o medulares agudas. Si bien la evidencia clínica de alto nivel aún es escasa, su perfil de seguridad, cuando se siguen las recomendaciones analizadas, permite sugerir su utilización con las consideraciones anteriormente expuestas hasta que existan recomendaciones definitivas basadas en estudios clínicos randomizados controlados concluyentes.