Introducción
La pancreatitis aguda (PA) resulta de la activación de las enzimas pancreáticas dentro del páncreas y la autodigestión del tejido pancreático como consecuencia de un proceso inflamatorio catastrófico del páncreas exocrino; es una de las patologías gastrointestinales más comunes que requieren hospitalización aguda y presenta una incidencia anual creciente de 30-45 por cada 100.000 habitantes1,2. La etiología de la PA difiere entre los países, los cálculos biliares y el alcohol son los principales responsables de alrededor del 40% y 30% de los casos, respectivamente, seguidos por otras etiologías tales como las que se desencadenan posteriormente a una colangiopancreatografía endoscópica retrograda (5% a 10%), aquellas secundarias a hipertrigliceridemia (2% a 5%) y secundarias a fármacos (menos de 5%). La PA de etiología traumática y otras etiologías menos frecuentes son responsables de menos del 1% de los episodios de PA3. La disfunción orgánica múltiple persistente (más allá de las 48 horas) y la necrosis pancreática infectada son los principales determinantes de un mal resultado, elevando la mortalidad de la PA grave (PAG) hasta valores cercanos a 35% independientemente de la etiología2.
La litotricia extracorpórea por ondas de choque (LEOC) es un método estándar no invasivo ampliamente aceptado para el tratamiento de la urolitiasis4,5. Las complicaciones asociadas con este procedimiento son en su mayoría leves y transitorias; sin embargo, existen algunas complicaciones que aunque infrecuentes (menos de 1%), son graves. En este sentido, se han informado episodios de hemorragia subcapsular hepática potencialmente mortal y hematoma perirrenal, sepsis nefrourológica, trombosis venosa, obstrucción biliar, abscesos del psoas y de la pared abdominal, perforación intestinal, lesiones e infecciones pulmonares, ruptura de aneurisma aórtico y arritmias cardíacas6,7. En la literatura existen escasos informes aislados de PA después de la LEOC y no se conoce el mecanismo exacto de la pancreatitis. Aunque la posibilidad de PA pos-LOEC es extremadamente baja (0,4% a 0,7%), los médicos deben estar conscientes de esta complicación grave.
Presentamos el caso de un paciente joven que desarrolló una PA luego de someterse a un procedimiento de LEOC para el tratamiento de urolitiasis renal derecha.
Caso clínico
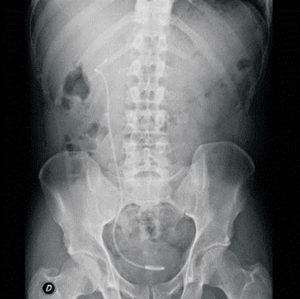
Paciente de sexo masculino de 42 años, fumador intenso, sin antecedentes personales. En enero de 2019, consultó por cólico nefrítico, en esa oportunidad le diagnosticaron discreta ureterohidronefrosis y urolitiasis derecha radiopaca de 8 milímetros. La litiasis migró al cáliz inferior del riñón derecho durante colocación de catéter doble J, el 18 de enero de 2019 (figura 1). Recibió tratamiento con LOEC, la primera sesión resultó inefectiva y se suspendió el procedimiento a los 1.253 disparos a 1,5 de energía dada la imposibilidad de focalización del cálculo por tratarse de un riñón muy móvil. Posteriormente se coordinó un segundo procedimiento, que se realizó el 21 de marzo de 2019, durante el cual se administraron 3.500 disparos a 4 de energía. No se registraron incidentes ni eventos adversos durante el procedimiento, el paciente fue dado de alta a domicilio asintomático.
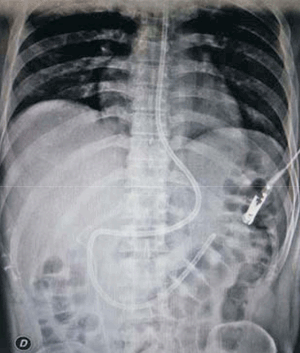
A las ocho horas posteriores al procedimiento de LEOC, instala vómitos incoercibles y dolor abdominal a predominio de hemiabdomen superior, sin fiebre. Se solicitó paraclínica de valoración general que evidenció hiperleucocitosis de 19.270 uL y amilasemia de 579 U/l; se le realizó una tomografía de abdomen que evidenció: alteraciones de la grasa peripancreática, escasa cantidad de líquido a nivel del espacio perigastroduodenal y escaso liquido libre intraabdominal; el sector cefalopancreático se observó levemente aumentado de tamaño con densidad heterogénea y se observó el catéter doble J normo posicionado a derecha. A las 48 horas, el paciente incrementó los síntomas de intolerancia digestiva, agregó distensión abdominal difusa e intensificó el dolor abdominal. En las siguientes horas instaló polipnea, taquicardia sinusal y fiebre. Se solicitó nueva paraclínica de la que se destaca una amilasemia de 1.047 U/l, proteína C reactiva (PCR) de 196 mg/l, hematocrito (HTO) de 48%, hiperleucocitosis de 21.300 µL, hiperazoemia 1,48 g/l con creatininemia de 2,24 mg/dl, funcional y enzimograma hepáticos normales. Se repitió la tomografía de abdomen que evidenció parénquima pancreático aumentado de tamaño a predominio cefálico, importante alteración de la grasa adyacente, menos de 30% de necrosis y una colección aguda peripancreática (figura 2). No se encontró evidencia de litiasis biliar ni dilatación de la vía biliar principal por ecografía ni por tomografía. El paciente se mantuvo lúcido, con elementos de síndrome de respuesta inflamatoria persistente (polipnea, taquicardia, fiebre e hiperleucitosis), presentó hipotensión arterial que fue transitoria. Durante las primeras 72 horas presentó elementos de disfunción gastrointestinal aguda grado 2, como ausencia de ruidos abdominales, vómitos persistentes y volumen residual gástrico aumentado, hipertensión intraabdominal (presión intraabdominal > o igual a 12 mmHg). El dolor se controló con opiáceos y antiinflamatorios no esteroideos; se realizó reposición de fluidos con cristaloides balanceados (suero ringer lactato) precozmente y dirigida por objetivos. Al cuarto día se inició nutrición enteral (NE) por vía yeyunal a través de una sonda naso yeyunal (SNY), con una fórmula enteral completa, polimérica, isocalórica, isonitrogenada y sin fibras (figura 3). El paciente no presentó elementos de intolerancia a la NE.
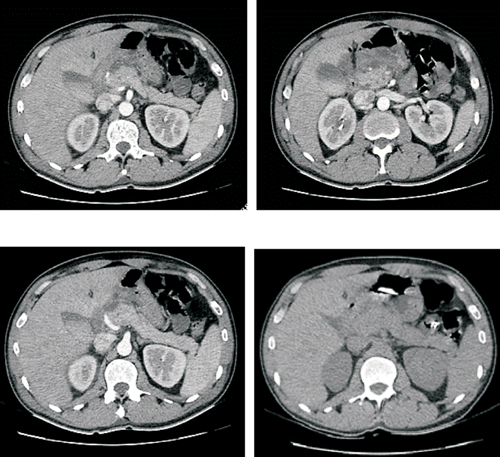
Figura 2: Tomografia de abdomen. Se observa la cabeza pancreática aumentada de tamaño, presenta contornos mal definidos y realce heterogéneo (< de 30% de necrosis). Cuerpo y cola de aspecto conservado. Leve dilatación difusa del conducto de Wirsung. Importante alteración de la grasa peripancreática en relación con el sector cefálico que se extiende al mesenterio adyacente y mesocolon transverso. Se identifica colección adyacente a la cabeza pancreática que acompaña las alteraciones de la grasa mesentérica, mide aproximadamente 60 mm cefalo-caudal y en el sector más voluminoso 35 mm T por 32 mm AP. Están engrosadas las fascias retroperitoneales, en particular a derecha, existiendo escasa cantidad de líquido en el espacio renal anterior. También se observa líquido libre en reducida cantidad en la gotera parietocólica derecha y en saco de Douglas.
No se desarrollaron otras complicaciones relacionadas a la PA, ni otras complicaciones extrapancreáticas; el paciente evolucionó a la mejoría de las disfunciones descritas, no requirió terapia de reemplazo de la función renal, asistencia respiratoria mecánica, vasopresores ni nutrición parenteral, y se otorgó el alta a sala de cuidados moderados al decimosegundo día del ingreso.
Discusión
El páncreas es un órgano que raramente se lesiona en el traumatismo. Esto ocurre en menos del 2% de los casos de traumatismo cerrado; esta lesión se asocia con una morbilidad y mortalidad considerablemente altas en los casos de diagnóstico tardío, clasificación incorrecta de la lesión o retraso en el tratamiento8.
La LEOC es un procedimiento seguro en todo el mundo, sin embargo, se han informado algunos incidentes posteriores al procedimiento, como la lesión gastrointestinal en el 1,8% de los casos9. Se han reportado traumas pancreáticos después de la LEOC, se informaron lesiones en el colédoco y en el páncreas debido a LEOC para el tratamiento de litiasis renales derechas, o hematoma pancreático autolimitado tres meses después de la LEOC para cálculos renales izquierdos10,11.
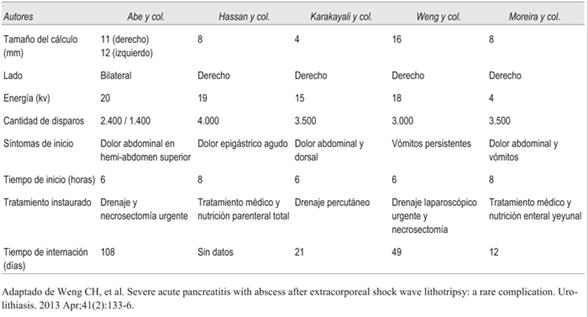
La PA pos-LEOC es poco frecuente, sin embargo, se han comunicado algunos casos que comparten algunas características como se observa en la (tabla 1). Todos los casos reportados ocurrieron precozmente en las horas siguientes al procedimiento; la forma de presentación fue similar al caso que comunicamos, predominando el dolor abdominal y los vómitos posprocedimiento, todas desarrollaron colecciones agudas peripancreáticas12. Todos los casos recibieron la LEOC sobre el riñón derecho, excepto la que se sometió a una LEOC bilateral13. Tres casos necesitaron intervenciones quirúrgicas, siendo la necrosis infectada la principal indicación9. El caso que presentamos, de acuerdo con la clasificación tomográfica de Baltazar, corresponde a una PA de grado D (por presentar alteraciones extrapancreáticas incluyendo una colección extrapancreática única), además, presentó menos del 30% de necrosis del páncreas en la tomografía de abdomen, lo que le confiere un índice de severidad tomográfico de entre 4 y 6 puntos. Presentó hemoconcentración, hiperazoemia, una PCR elevada y una creatinina en sangre mayor de 1,8-2,0 mg/l, lo que le confirió criterios de severidad de la PA14-16, sin embargo, el compromiso hemodinámico fue transitorio y no requirió terapias de soporte vital. Existe una serie de predictores, incluidos marcadores clínicos y de laboratorio y varios sistemas de puntuación que se han desarrollado para mejorar el juicio clínico y poder predecir la severidad de la PA, siendo útiles porque se asocian con un aumento del riesgo de complicaciones o muerte independientemente de la etiología3. El grado de elevación de la amilasa sérica o del nivel de lipasa no tienen valor pronóstico, siendo la persistencia de la disfunción orgánica múltiple y la infección de la necrosis pancreática los principales determinantes de mortalidad, que puede alcanzar el 35% en estos casos3.
El mecanismo por el cual las ondas de choque pueden generar lesión pancreática no se conocen con exactitud, teóricamente las fuerzas de rotura y cizallamiento y la actividad de cavitación producida por las ondas de choque en tejidos y vasos pueden causar lesión17. Posiblemente como resultado de la ampliación del foco durante la LEOC, una parte del páncreas estuvo expuesta a ondas de choque extracorpóreas que provocaron daño celular agudo (efecto traumático), que causó un hematoma pequeño, daño microvascular y finalmente pancreatitis aguda7,18. Algunos estudios evaluaron los marcadores séricos relacionados con el páncreas después de la LEOC para la urolitiasis y no mostraron cambios significativos de amilasa y lipasa en pacientes después de la LEOC para cálculos renales unilaterales19,20. Mientras que Kirkail y colaboradores, entre 150 casos con cálculos en el tracto urinario superior, evidenciaron un ligero aumento de la amilasa y la lipasa séricas, las cuales todavía estaban dentro del rango normal21.
El manejo apropiado de la PA es independiente de la etiología, se basa en un diagnóstico preciso, una clasificación apropiada para definir un ingreso precoz a la unidad de cuidados intensivos, un sostén de alta calidad que incluye tratamiento adecuado del dolor, la reposición hidroelectrolítica apropiada y una terapia nutricional óptima. A esto se suma el tratamiento adecuado de las complicaciones y la prevención de recaídas22. El agotamiento del volumen intravascular por tercer espacio es la base de muchas de las características predictivas negativas de la PA, la hemoconcentración (Hto > 44%) y la hiperazoemia son el sustento para la reposición hidroelectrolítica cuyo objetivo es resolver el déficit y evitar los daños de la hiperreposición22. La reanimación con líquidos “liberal” o “agresiva” siempre ha sido uno de los pilares de la terapia, pero esto ha sido cuestionado recientemente. La terapia con fluidos vigorosa es más importante durante las primeras 12 a 24 horas después del inicio de los síntomas y tiene poco valor después de las 24 horas23. Una solución cristaloide balanceada a una velocidad de 200 a 500 ml/h, o de 5 a 10 ml/kg/h sería apropiada, dado que se asocia a menor respuesta inflamatoria24. Una estrategia nutricional adecuada ha sido uno de los factores clave durante el apoyo sistemático en pacientes con PA, existe evidencia suficiente que apoya el uso de nutrición enteral por sobre la nutrición parenteral en pacientes que no toleran la dieta oral, dado que mejora la supervivencia25. En pacientes con PAG, la NE se administra habitualmente mediante una SNY para minimizar la estimulación pancreática; sin embargo, la NE por sonda nasogástrica (SNG) representa una ruta segura. Existe evidencia que demuestra que la administración de NE con fórmula semielemental por SNG no es inferior a la nutrición por SNY en términos de reducción de mortalidad y puede ser eficaz en el 90% de los pacientes. Aunque la nutrición enteral se ha convertido en una de las terapias estándar para pacientes con PA, las fórmulas óptimas para la nutrición enteral han sido objeto de debate. Sobre el supuesto de que la fórmula elemental es adecuada para el tratamiento de estos pacientes porque tiene menos efectos estimulantes para las secreciones exocrinas del páncreas, al mismo tiempo que mantiene la inmunidad intestinal; sin embargo, los estudios clínicos que corroboran este supuesto han sido escasos. Actualmente, no existe evidencia suficiente para recomendar un tipo de fórmula específica para PA. En nuestro medio contamos con fórmulas poliméricas, motivo por el cual optamos por la vía yeyunal en este paciente. La presencia de disfunción gastrointestinal aguda en el caso que presentamos fue otro motivo para preferir esta vía26-28.
No existe evidencia suficiente de los efectos de la inmunonutrición en los resultados de eficacia y seguridad en esta patología, el papel de la suplementación de la NE con agentes inmunomoduladores potenciales sigue en duda, y se requiere más investigación en esta área. Con el fin de prevenir la translocación bacteriana, se hicieron intentos para influir en el microbioma intestinal utilizando antibióticos profilácticos y bacterias probióticas. Los estudios que evaluaron el uso de probióticos proyectaron resultados inconsistentes y contradictorios, especialmente con respecto a la seguridad y los eventos adversos, y sus hallazgos no respaldan el uso rutinario en la práctica clínica habitual. Sin embargo, se deben realizar investigaciones adicionales para tratar de determinar la eficacia potencial o los daños de los probióticos29. La profilaxis antibiótica no se recomienda para ningún tipo de PA, a menos que se sospeche una infección o se haya confirmado23,30. No fueron utilizadas estas estrategias en el caso que presentamos.
Los escasos reportes existentes en la literatura y la ausencia de una explicación fisiopatológica clara no hacen posible demostrar la relación causal entre la PA y la LEOC, sin embargo, la ubicación anatómica de la lesión pancreática predominantemente cefálica, los síntomas inmediatos y posteriores a la LOEC apoyan el planteo de PA como una complicación de dicho procedimiento en nuestro paciente. En los casos de dolor abdominal súbito e inesperado con náuseas y vómitos después de un procedimiento de LEOC, se debe prestar atención a la posibilidad de una PA, y se debe posponer el procedimiento inmediatamente para evitar el daño pancreático en estos pacientes. La PA se debe considerar como una complicación temprana después de la LOEC para urolitiasis, principalmente derechas. Debe recordarse que los casos graves de PA se caracterizan por una alta mortalidad, y a pesar de las mejoras en el manejo de cuidados intensivos, ningún tratamiento específico ha mejorado radicalmente los resultados clínicos de la enfermedad, por lo que todos los esfuerzos destinados a su prevención y diagnóstico precoz están justificados.