Introducción
El trasplante pulmonar (TP) es una terapéutica válida en enfermedades respiratorias crónicas que no responden a pesar del tratamiento médico o quirúrgico optimizados, cuya expectativa de vida es muy reducida1. En estas enfermedades suele ser la única intervención capaz de modificar el pronóstico, la supervivencia y la calidad de vida. El TP se ha consolidado en los últimos 30 años; el número de trasplantes realizados tiende a crecer cada año, pasando de unos 15 por año realizados a mediados de la década de 1980 a 4.122 reportados en el mundo durante el 20152.
En América Latina los resultados distan notablemente de ser óptimos y la tasa de donantes por millón de población (pmp) se encuentra lejos de las posibilidades máximas de la región. A modo de ejemplo, mientras que en América Latina, con 531,1 millones de habitantes, en el año 2016 se realizaron 167 TP, en Europa, con una población menor (505,9 millones) se realizaron 1.916, casi 11 veces más3. La escasez relativa de donantes atenta contra la formación de programas específicos. Actualmente, los únicos países que han reportado datos de TP realizados en América Latina en 2016 han sido Argentina, Brasil, Chile, Perú, Costa Rica y Uruguay3.
En nuestro país, con un bajo número de habitantes, se ha optado hasta el momento por un programa de trasplante en colaboración con un centro regional de referencia en TP (Fundación Favaloro para la Docencia e Investigación Médica, Buenos Aires, Argentina), mediante un convenio binacional con dicha República.
Los objetivos del presente trabajo son describir las características del programa de TP en Uruguay, mostrar sus resultados y avances, así como las herramientas en curso para mejorar la procuración pulmonar y aspectos operativos del mismo.
Material y método
Trabajo descriptivo de los antecedentes y situación actual del programa, así como de los avances en curso. Para la sección Resultados se realizó revisión retrospectiva de historias clínicas y análisis de base de datos del programa. El análisis estadístico se realizó mediante IBM SPSS Statistics v.20.
Características del programa
El programa funciona desde el año 2003 mediante un convenio binacional con la República Argentina a través de sus organismos reguladores INCUCAI (Instituto Nacional Central Único Coordinador de Ablación e Implante, Argentina) e INDT (Instituto Nacional de Donación y Trasplante, Uruguay)4.
En el marco de este convenio, en Uruguay se realizan los módulos de evaluación pretrasplante y seguimiento postrasplante. La ablación se realiza en territorio uruguayo por parte de un equipo quirúrgico proveniente de Fundación Favaloro que también realiza el implante en territorio argentino.
Este convenio establece que los pacientes uruguayos en situación de espera para trasplante electivo o de urgencia se trasplantarán con órganos procurados en nuestro país, mientras que en condición de emergencia los pacientes ingresan a lista argentina para trasplantarse con órganos procurados en el país vecino. Cada vez que esto último sucede, el INDT, en atención al principio de reciprocidad, se compromete a enviar al INCUCAI un órgano equivalente procurado en Uruguay con el objetivo de contribuir al programa de trasplante del cual se hizo usufructo.
El convenio binacional ha permitido el desarrollo y crecimiento de dicho programa en Uruguay gracias a la solidaridad y el trabajo en conjunto con los colegas argentinos.
El entrenamiento de recursos humanos ha sido continuo. Se progresó en el entrenamiento del equipo médico quirúrgico con pasantías de los cirujanos de tórax en uno de los principales centros europeos de referencia en TP, como lo es la Universidad de Lovaina. El equipo médico neumológico ha realizado su entrenamiento en forma permanente desde el año 2004 en el centro de referencia regional Hospital Universitario Fundación Favaloro.
El desarrollo del programa, necesario para abordar la alta demanda médica sanitaria dado el crecimiento sostenido de los potenciales receptores y la elevada mortalidad en lista de espera, presenta limitantes.
Las principales limitantes asociadas a la logística de los operativos de donación e implante son multicausales e incluyen tiempos prolongados del operativo, coordinación de la participación de técnicos de ambos países, coordinación de operativos de donación multiorgánica y otros imponderables, como la situación climática para el traslado o disponibilidad de aeropuertos durante las 24 horas.
Otra limitante no menor del programa es la falta de centralización asistencial en un centro único nacional de referencia en TP. Dicha centralización, que se encuentra en proceso de resolución administrativa, resulta indispensable para racionalizar la asistencia, optimizar el uso de recursos humanos, recursos tecnológicos asociados y costos económicos relacionados con la práctica. El abordaje de pacientes de la mayor complejidad en la trasplantología, como el TP, debe realizarse necesariamente en un centro asistencial de referencia que asegure los insumos, la tecnología, la logística y los recursos humanos interdisciplinarios de las especialidades involucradas.
Discusión y resultados del programa
Entre el 2003 y 2017, el incremento de pacientes remitidos para evaluación ha sido exponencial, debido principalmente a la mayor difusión de esta posibilidad terapéutica y sus resultados entre los neumólogos del país. Durante los cuatro primeros años ingresaron a lista 15 pacientes5, mientras que considerando solo el 2017 ingresaron 9 pacientes. En total, han ingresado 70 pacientes a lista de espera desde el inicio del programa.
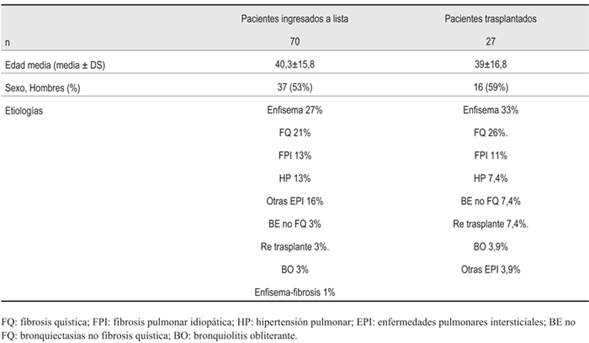
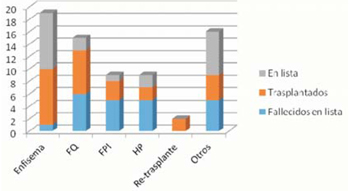
En cuanto a las características epidemiológicas y etiológicas de los pacientes ingresados en lista, las mismas se describen en la (tabla 1). De los pacientes ingresados a lista, el 36% se trasplantó, 4% se excluyó de lista, 2% requirió retrasplante, 32% falleció en lista y 26% se mantiene en lista. El enfisema y la fibrosis quística (FQ) fueron las causas más frecuentes de ingreso. El tiempo medio de espera en lista fue de 18,5 ± 18,24 meses. La mortalidad global en lista fue elevada (32%). Si analizamos la mortalidad según la patología, vemos que FQ, fibrosis pulmonar idiopática (FPI) y la hipertensión pulmonar (HP) fueron las de mayor mortalidad (figura 1).
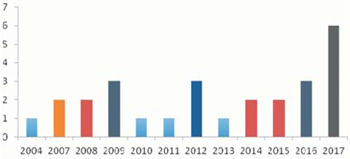
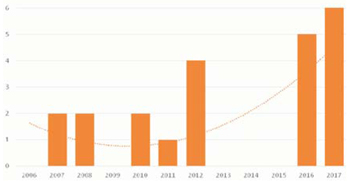
En cuanto a la evolución del número de trasplantes por año, luego del primero en 2004, la cifra ha variado entre 1 y 3 al año, logrando un salto a seis trasplantes en 2017 (figura 2) gracias a estrategias en la procuración que luego detallaremos. En total, en los 14 años del programa se han realizado 27 trasplantes. De estos, más de 50% se han realizado en los últimos tres años, lo que muestra el cambio cuantitativo secundario a la aplicación de nuevas estrategias de procuración (figura 3)6. Las características de los pacientes trasplantados se detallan en la (tabla 1). Predominan los trasplantes bipulmonares (78%) y fueron en condición electiva 56%, en urgencia 11% y en emergencia 33%.
Las patologías trasplantadas más frecuentes fueron enfisema, FQ y FPI. Esta distribución presenta grandes semejanzas con lo publicado internacionalmente, donde el enfisema también representa el 33% de los trasplantes, seguido por la enfermedad pulmonar intersticial (30%), con predominio de la FPI (24,8%), y en tercer lugar la enfermedad bronquiectásica FQ (16%) y no FQ (2,7%)2.
Las infecciones respiratorias han sido las complicaciones más frecuentes en nuestra casuística, seguidas de las complicaciones de la vía aérea (33% de los pacientes), en su mayoría a modo de estenosis bronquial.
En cuanto a los aspectos psicosociales, el 95% de los pacientes trasplantados lograron reinserción total a tareas laborales o educativas. Utilizando la escala Likert para la autovaloración de la calidad de vida (rango de 0 a 10), la media antes del trasplante se sitúa en 3,13 contrastando con una media de 9 postrasplante, reflejando el gran impacto positivo en los pacientes.
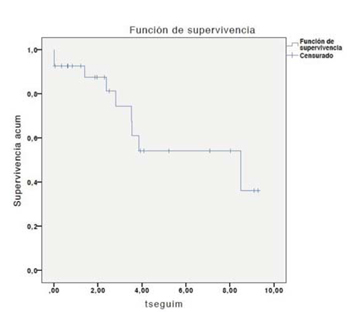
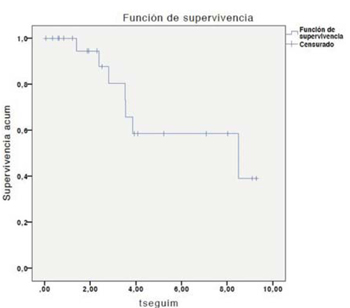
Hasta el momento analizado se trasplantaron 25 pacientes, dos se retrasplantaron. De los 25 pacientes, 18 se mantienen vivos (72%). La mortalidad postrasplante se sitúa en 34%, mientras que la mediana de supervivencia global y condicionada (excluyendo mortalidad del primer año postrasplante) por Kaplan-Meier coinciden en 8,48 años (figura 4a) y (figura 4b). Esta coincidencia responde al pequeño número de pacientes y la baja mortalidad (7 en 27). Según el reporte 2017 del Journal of Heart and Lung Transplantation (JHLT), la supervivencia media global del TP entre 1990 y 2016 ha sido de 6,0 años, y la supervivencia media condicional de 8,1 años. Con este análisis, podemos afirmar que nuestros resultados son comparables a los reportados internacionalmente2, si bien en nuestra serie existe el sesgo de ser un número escaso de pacientes. Debemos recordar que en las últimas tres décadas la supervivencia del TP se ha incrementado mundialmente, sobre todo a corto plazo, a expensas principalmente de las mejoras en el manejo perioperatorio de los pacientes, incluyendo la incorporación del soporte vital avanzado con el uso de la membrana de oxigenación extracorpórea (ECMO).
Respecto a las causas de muerte, dos pacientes fallecieron en el postrasplante inmediato (disfunción primaria severa del injerto y lesión vascular intraoperatoria), un paciente falleció por disfunción crónica del injerto (CLAD)6 y los cuatro restantes por causa infecciosa, constituyendo la principal causa de muerte de nuestra serie. Dentro de los microorganismos involucrados, destacamos el aislamiento de Scedosporium en dos de ellos, Pseudomonas aeruginosa, Staphylococcus aureus, herpes virus y virus influenza A.
Según la literatura, a pesar de la mejoría en los números globales de supervivencia, las causas de muerte no han variado significativamente con el correr de los años8,9. Las principales causas de muerte en el primer mes postrasplante son la disfunción primaria del injerto y las infecciones respiratorias, si bien contribuyen las complicaciones quirúrgicas y las causas cardiovasculares. Si consideramos el primer año, la principal causa de muerte se centra en las infecciones. Finalmente, pasado el primer año, cobra importancia el rechazo crónico7, principalmente bajo la forma de síndrome de bronquiolitis obliterante (SBO/BOS, bronchiolitis obliterans syndrome), acompañado de infecciones. Aún dentro del primer año las enfermedades neoplásicas contribuyen en buen número a las causas de muerte9.
Estrategias para incrementar el número de donantes pulmonares
En todos los programas de TP el crecimiento de pacientes ingresados a lista de espera es desproporcionadamente alto respecto al número de trasplantes. Este disbalance producido por la elevada demanda y la escasez relativa de donantes es el principal responsable de la excesiva mortalidad en lista de espera. La escasez relativa de donantes es la mayor limitante para el desarrollo y la aplicación generalizada de esta terapéutica10.
En Uruguay, como se mencionó previamente, desde el inicio del programa hasta el año 2015, se realizaron 13 trasplantes con una media anual que oscilaba entre 0 y 2, realizándose excepcionalmente cuatro trasplantes en el año 2012. Entre los años 2013 y 2015 el número de donantes pulmonares ablacionados en el país fue cero, lo que obligó al equipo de trasplante pulmonar, junto al INDT, a diseñar nuevas estrategias de procuración pulmonar.
Como primera medida, durante el 2015, se realizó un seguimiento prospectivo de todos los donantes reales menores de 65 años en quienes se analizaron las causas de descarte para pulmón. Se detectó que las principales causas de descarte fueron: tiempos de procuración previstos excesivamente largos (logística), el planteo no confirmado de aspiración del donante y el deterioro del intercambio gaseoso expresado por la relación PaO2/FiO2. Estas tres causas se asociaron a más del 60% de los pulmones descartados. Las restantes eran causas no corregibles de descarte (contraindicaciones absolutas).
Se establecieron entonces las siguientes estrategias:
- Se implementó un programa de seguimiento prospectivo de pacientes menores de 65 años comunicados al INDT como pasibles de evolucionar a muerte encefálica con el objetivo de minimizar el escape de donantes pulmonares mediante seguimiento longitudinal.
- Se descendió el umbral de convocatoria al equipo de evaluación pulmonar a PaO2/FiO2 de 200 mmHg con una PEEP hasta 8 cm H2O. En aquellos pacientes con PaO2/FiO2 aceptable en gasometrías arteriales previas y un deterioro de la PaO2/FiO2 posterior a la prueba de apnea se planteó la realización de maniobras de homogeneización pulmonar mediante PEEP para minimizar la participación de posibles atelectasias vinculadas a los períodos de desconexión de la asistencia respiratoria mecánica (ARM). En Uruguay son necesarios dos tests de apnea para el diagnóstico de muerte encefálica. Estos habitualmente se realizan sin válvula de PEEP y desconectado de la ARM, lo que deteriora el intercambio gaseoso. La realización de maniobras de reclutamiento alveolar ha demostrado incrementar el número de pulmones válidos para trasplante11.
- Se generalizó la realización de fibrobroncoscopía en el potencial donante pulmonar procurando confirmar o descartar el planteo clínico de aspiración. Destacamos que no en todos los pacientes en los que se planteó clínicamente aspiración, se confirmó por broncoscopía.
- En cuanto a los aspectos logísticos se describieron las diferentes fases de los procesos de ablación, traslado del receptor y del órgano para implante. Se minimizaron los tiempos, independizando los traslados del receptor y del equipo de ablación.
- Conformación de un equipo quirúrgico uruguayo, actualmente en entrenamiento, con el objetivo de contar en un futuro próximo con un equipo de ablación y posterior implante en nuestro territorio. Se comenzó el entrenamiento mediante la ablación pulmonar en donantes no óptimos rechazados como donantes reales y asimismo la realización de ablaciones en donantes óptimos por el equipo quirúrgico uruguayo supervisado por el equipo argentino. Esta incorporación tiene un doble propósito: realizar la curva de aprendizaje de ablación pulmonar y minimizar el escape de donantes pulmonares al generar un segundo control mediante el análisis macroscópico y gasométrico intraoperatorio12,13. Asimismo, se generó un protocolo de investigación que correlaciona los hallazgos clínicos, gasométricos, microbiológicos, anatomopatológicos y fisiopatológicos de los pulmones rechazados. Creemos que este protocolo en el futuro ayudará a la toma de decisiones en cuanto al rechazo de donantes pulmonares. Ya en los primeros operativos bajo esta modalidad hemos detectado discordancias en gasometrías realizadas mediante punción de arteria radial y gasometrías realizadas en venas pulmonares a tórax abierto, hecho previamente reportado por otros grupos de trabajo14,15. También hemos detectado la presencia de macrotrombos pulmonares en pacientes con baja probabilidad clínica de tromboembolismo pulmonar, hecho también reportado previamente por otros grupos de trabajo16. Estos hallazgos, de ser confirmados, pueden abrir la puerta a futuros algoritmos de decisión en cuanto a terapéutica de donantes y rechazo o aceptación. Una vez entrenado el equipo quirúrgico local y validada su experiencia por parte del equipo quirúrgico de referencia, se minimizarán aún más los tiempos operativos. Esto permitirá la valoración in situ de pulmones con criterios límites de aceptación a priori.
- En busca de nuevas fuentes de donantes se encuentra en desarrollo un programa de donación pulmonar en asistolia en un hospital de referencia nacional (Hospital Maciel). Este programa se encuentra en fase de reevaluación y expansión a nuevos centros.
A raíz de estas nuevas estrategias, si bien queda mucho trabajo por realizar, ya se comienzan a visualizar algunos resultados esperanzadores: la procuración pulmonar en Uruguay pasó de 0 pmp durante los años 2013, 2014 y 2015 a 1,2 pmp en 2016, lo que la ubicó en el segundo lugar de América Latina después de Chile3, y 1,8 pmp en 2017.
Conclusiones y desafíos futuros
El Programa Uruguayo de Trasplante Pulmonar, gracias al trabajo en conjunto entre el equipo técnico local y el del centro de referencia, ha tenido importantes avances desde su inicio en 2003. Los últimos dos años han sido claves para el crecimiento de la procuración pulmonar. Los resultados en los pacientes trasplantados en cuanto a características, morbimortalidad, calidad de vida y supervivencia son comparables con los descritos internacionalmente. Dentro de los desafíos a corto plazo, destacamos la posibilidad de consolidación del equipo quirúrgico de ablación uruguayo, así como centralizar la actividad de seguimiento pre y postrasplante en un centro asistencial de referencia. Esta centralización es imperiosa y es la única forma de abordar un tratamiento y seguimiento integral e inter y multidisciplinario a pacientes de gran complejidad en todas sus etapas. Asimismo y en forma simultánea se deberá realizar el entrenamiento del equipo multidisciplinario involucrado en los distintos aspectos asistenciales (anestesia, terapia intensiva, anatomía patológica, entre otros). Estos aspectos serán claves para poder pensar en un eventual programa independiente incluyendo la ablación y el manejo posoperatorio en nuestro país en un futuro próximo.