Introducción
Las pandemias metabólicas del siglo XXI, como la diabetes mellitus tipo 2 (DT2) y la obesidad, siguen aumentando dramáticamente en el mundo occidental. Se estima que la incidencia mundial de DT2 asciende a 382 millones de casos, y se predice que la DT2 alcanzará a 600 millones de personas en el año 20351. Se estima que 35 millones de personas a lo largo del mundo sufren enfermedad de Alzheimer (EA) en este momento y que este número se duplicará en pocas décadas2. En Uruguay, la Asociación Uruguaya de Alzheimer y Similares (AUDAS) estima que existen 50.000 uruguayos con EA3.
La DT2 es causada por la insulino-resistencia (IR) en el 90% de los casos. La DT2 es considerada un importante factor de riesgo para demencia vascular y EA después de los estudios epidemiológicos de Rotterdam3,4. Existe una sumatoria del daño vascular e inflamatorio en el cerebro del paciente diabético. Ambos afectan el estatus cognitivo5,6.
La DT2 es considerada una enfermedad inflamatoria crónica y sistémica de bajo grado de intensidad (EICSBI) que promueve otras afecciones inflamatorias como enfermedad cardiovascular, cáncer y demencia8. Existe evidencia de que la EICSBI aumenta la inflamación cerebral9. Defectos en el receptor de insulina, alterado por la EICSBI, determina insuficiencia energética para las neuronas así como mayor vulnerabilidad a la oxidación, otros insultos metabólicos y dificultad en la plasticidad sináptica10. Un importante estudio realizado por Konrad Talbot analizó muestras postmortem de tejido cerebral de pacientes no diabéticos con EA. Este investigador demostró por primera vez resistencia a la insulina en el cerebro asociada a la desregulación de IRS-1 e IGFs-. Estos datos destacan la importancia de la IR en la etiología de la EA11. Es bien sabido que marcadores de EICSBI están relacionados con IR en obesidad y DT212,13.
Ejercicio y cerebro
Está bien demostrado que la actividad física mejora el nivel cognitivo y puede retrasar la pérdida de memoria vinculada a la edad en humanos y roedores14-17. El ejercicio regular es un pilar terapéutico en la DT2, dado que mejora la IR y el nivel de glucosa18. Una revisión sistemática sobre los efectos del ejercicio sobre el nivel cognitivo en individuos mayores de 55 años demostró mejoría en la atención auditiva y la velocidad de procesamiento cognitivo19. Se piensa que la mejoría cognitiva y metabólica del ejercicio está vinculada a la mejoría del EICSBI, el cual puede menoscabar el señalamiento de IGF-1 e insulina en sus respectivos receptores, tanto a nivel sistémico como dentro del cerebro20. El hallazgo de citoquinas y mioquinas antiinflamatorias, emitidas por la contracción muscular durante el ejercicio, ha dado más luz a la comprensión del efecto beneficioso del ejercicio regular en la salud general21. El mecanismo exacto del efecto terapéutico del ejercicio en la mejoría cognitiva permanece desconocido. La evidencia actual posiciona al ejercicio regular y moderado como una de las mejores armas para combatir la declinación cognitiva y la EA, probablemente por el control de la EICSBI, y el incremento de la insulino sensibilidad en el cerebro, promoviendo, además, la neurogénesis y la sinaptogénesis22.
Al igual que el ejercicio, la nutrición afecta la función cerebral. Se ha demostrado que la dieta mediterránea mejora el estado cognitivo23. Se analizó la relación entre una dieta pro inflamatoria, v. g., “dieta occidental”, y enfermedad cardiovascular y metabólica con resultados muy significativos (24. Varios estudios han subrayado la relación entre los ácidos grasos saturados de la dieta con enfermedades inflamatorias como DT2, obesidad, enfermedad cardiovascular y dislipemias25.
La mayoría de los estudios cognitivos en DT2 han sido realizados en pacientes con DT2 de largo tiempo de evolución y fueron todos estudios de cohorte. La prevención del declive cognitivo debe iniciarse precozmente luego del diagnóstico de DT226.
Objetivos del estudio
El principal objetivo del estudio fue explorar el impacto de un programa de 20 semanas de ejercicio controlado (PVSEC) sobre el estatus cognitivo, calidad de vida y marcadores de inflamación en una muestra de pacientes DT2 de relativo reciente diagnóstico (= 10 años), asistidos por nuestro Sistema Nacional Integrado de Salud (SNIS). El segundo objetivo fue evaluar los efectos del PVSEC sobre el riesgo metabólico y cardiovascular de la muestra. El estudio fue aprobado por el Comité de Ética del Hospital de Clínicas, Hospital Universitario del Uruguay.
Método
Diseño del trabajo y pacientes
Se realizó un ensayo clínico, abierto, randomizado y controlado, en acuerdo con los protocolos CONSORT27), de 20 semanas de ejercicio programado y controlado en pacientes asistidos en el primer nivel atención.
En la (figura 1) se ve el flujo del diagrama de randomización.
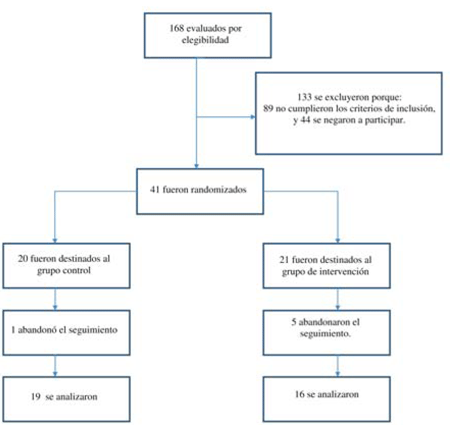
Figura 1: Diagrama de flujo del progreso a través de las fases de un ensayo paralelo y randomizado en dos grupos.
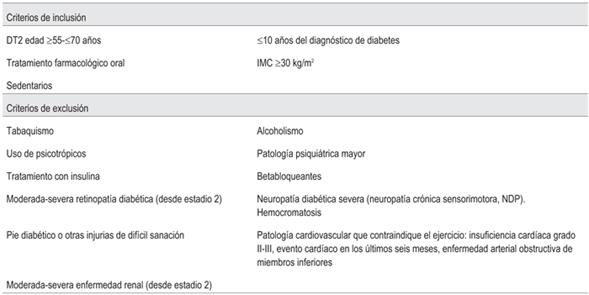
Se reclutaron 168 pacientes DT2 del SNIS de Uruguay bajo la evaluación de uno de los endocrinólogos, miembro del grupo de investigadores del estudio; 41 cumplieron con los criterios de inclusión. Véase criterios de inclusión / exclusión (tabla 1).
Todos los participantes fueron informados sobre las características del estudio y firmaron su consentimiento. El estudio fue aprobado por el Comité de Ética del Hospital de Clínicas, Hospital Universitario del Uruguay.
Todos los pacientes llenaron un cuestionario sobre edad, sexo, nivel educativo según la Clasificación Internacional Normalizada de la Educación (UNESCO) 2011 28 y el nivel económico, según el último censo uruguayo29. Se registró el nivel de actividad física en los 14 días previos, según las recomendaciones de la CDC y el Colegio Americano de Medicina del Deporte30, y otros ítems que se detallan en la (tabla 2).
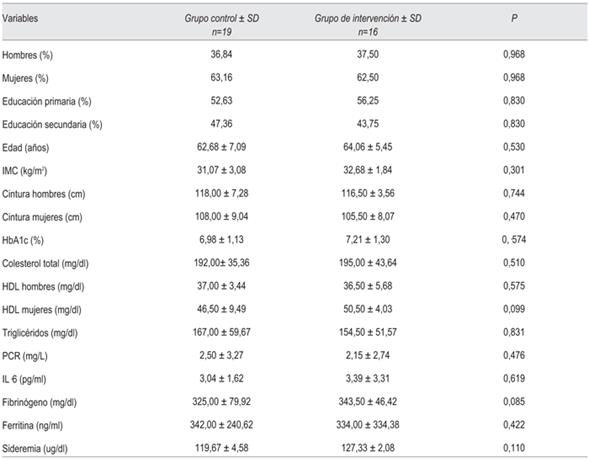
Tabla 2: Comparación de variables demográficas, antropométricas, metabólicas e inflamatorias al comienzo del estudio en ambos grupos.
Todos los participantes fueron asignados al grupo de intervención o grupo de control por técnica de muestreo simple. La asignación aleatoria fue realizada por el coordinador del proyecto, que no tuvo contacto con los pacientes o sus datos, utilizando la función RANDOM del software Microsoft Excel.
El análisis se realizó según intención de tratar.
Evaluación
Todos los pacientes seleccionados eran sedentarios, según las recomendaciones de la CDC y del Colegio Americano de Medicina del Deporte.
Se realizaron mediciones antropométricas, peso, altura, índice de masa corporal (IMC) y cintura abdominal.
Se realizó una evaluación metabólica con hemoglobina A1c (HbA1c), (medida por inhibición de aglutinación de látex equipamiento DCA 2000 Bayer-Siemens); el colesterol total, lipoproteínas de alta densidad, triglicéridos y la sideremia fueron realizados por métodos convencionales.
Los marcadores inflamatorios medidos fueron la proteína C-reactiva, por Inmmunturbimetric Cobas equipo C 311; la interleukina 6, por Electroquimioluminicency Cobas Equipo E 411 Roche; el fibrinógeno, por Clauss equipo ACL 200 IZAZA, y la ferritina, por Electroquimioluminicency Cobas Equipo E 411 Roche.
Luego de un reposo de 10 minutos en posición supina, se midió la presión sanguínea sistólica y diastólica en el brazo derecho con un estetoscopio estándar y un tensiómetro anaeroide dial. Todos lo individuos fueron evaluados por un cardiólogo del SNIS.
Todas las medidas antropométricas del estado metabólico, marcadores inflamatorios y del estatus cognitivo, psicológico y de calidad de vida se realizaron antes y después de la finalización del estudio. Para el tamizaje de depresión se utilizó la versión española del test de depresión geriátrica de Yesavage31, considerando el punto de corte en 5. La evaluación de la calidad de vida se realizó usando el cuestionario WHOQOL-BREF32. La valoración cognitiva se realizó con la versión validada al español del examen cognitivo de Adenbrooke (ACE), considerando un punto de corte de 86 para niveles de educación media y alta y de 68 para un nivel de educación baja33.
Programa de 20 semanas de ejercicio controlado
Antes y después del PVSEC fue evaluada la capacidad aeróbica de los sujetos por un médico deportólogo mediante la prueba de Rockport34.
El grupo de intervención cumplió con un programa de 20 semanas de ejercicio. Se siguieron las recomendaciones del CDC y del Colegio Americano de Medicina del Deporte.
En el primer mes caminaron 45 minutos seis días por semana, con una intensidad moderada, y los 2 minutos finales (es decir, a partir de los 43 minutos) con intensidad enérgica. El segundo mes se incrementó a 4 minutos de intensidad enérgica, el tercer mes a 6 minutos, el cuarto a 8 minutos y el quinto mes (20 semanas) a 10 minutos.
Una enfermera caminó con los pacientes y controló la presión arterial, el pulso y los valores de glicemia con tirilla reactiva al principio y al final del ejercicio diario. Al grupo control se le aconsejó caminar.
Una vez al mes un médico deportólogo evaluó a ambos grupos de pacientes.
Una enfermera perteneciente al SNIS obtuvo la extracción de las muestras antes y después del PVSE.
La nutrición de la muestra de DT2 fue controlada, en ambos grupos, por nutricionistas profesionales del SNIS en acuerdo con las recomendaciones de la American Diabetes Asociation 201735.
Cuando el estudio hubo finalizado se alentó a los pacientes a continuar con hábitos saludables. Abandonaron seis pacientes, uno en el grupo control y cinco en el grupo de intervención.
Métodos estadísticos
En el análisis descriptivo se utilizaron medidas resumidas de tendencia central (media y mediana), dispersión (desviación estándar SD y rangos intercuartiles) y frecuencias.
En el análisis bivariado inferencial las variables continuas fueron estudiadas con la prueba de Anderson para verificar la normalidad de la prueba de Barttlet y comprobar la homogeneidad de los grupos, ANOVA o Kruskal-Wallis, según correspondiera, para la comparación de la tendencia central.
En la comparación de las variables categóricas y dicotómicas la prueba de chi cuadrado por Mantel-Haenszel se sostuvo; cuando los valores esperados fueron inferiores a 5, se usó la prueba exacta de Fischer.
Para el procesamiento estadístico se utilizó el paquete R 3.3.2 y Microsoft Excel.
Resultados
Capacidad aeróbica
Antes del PEVSC el grupo de intervención mostró 18,20% de baja capacidad aeróbica (CA); menor al promedio un 9%; promedio 26%, y mayor al promedio 54%; alta 0%. Después del PEVSC: baja CA 18,2%; menor al promedio 0%; promedio 27,3%, mayor al promedio 18,2% y alta AC 36,4%.
Al inicio del estudio tanto el grupo de intervención como el grupo control fueron homogéneos en referencia a la evaluación demográfica, antropométrica, metabólica, inflamatoria y psicológica (tabla 2).
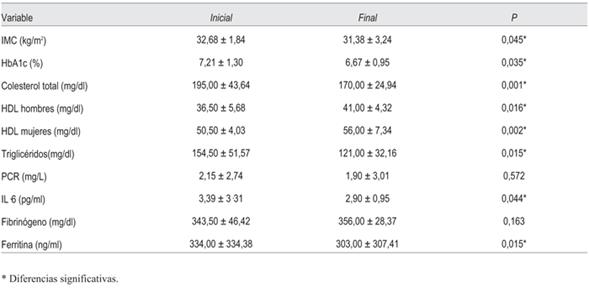
Después de 20 semanas, el grupo de intervención tuvo una disminución de 4% (p = 0,045) del peso corporal y una mejoría significativa de los marcadores metabólicos, con una disminución de 7,5% (p = 0,035) en niveles de HbA1c, 13% (p = 0,001) del colesterol total, y 21% (0,015) de triglicéridos, con un aumento asociado entre 10% y 12% en los niveles de HDL (p = 0, 016 y p = 0,015) hombres y mujeres, respectivamente.
En el estado inflamatorio se encontró una disminución significativa en los niveles de IL-6 (p = 0,044) y de ferritina (p = 0,15), pero no hubo cambios en los niveles de proteína C reactiva (CRP) y fibrinógeno (tabla 3).
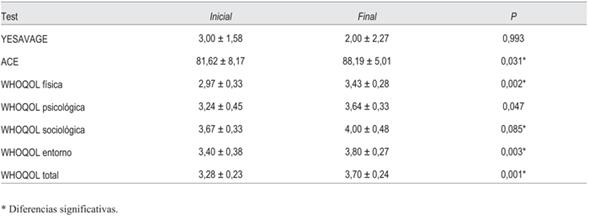
En la evaluación psicológica no se encontraron diferencias en la detección de depresión, según la prueba de Yesavage.
Se encontró una mejora en la calidad de la vida global (p = 0,001) y especialmente en la dimensión física (p = 0,002), psicológica (0,047) y del entorno (0,003).
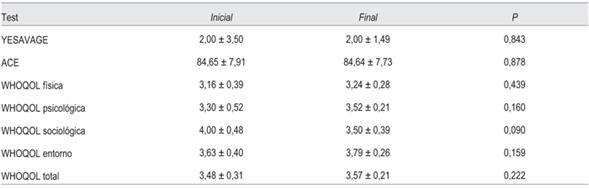
La valoración con la prueba ACE demostró una mejora significativa en el estado cognoscitivo después del período de la intervención (p = 0,031) (tabla 4).
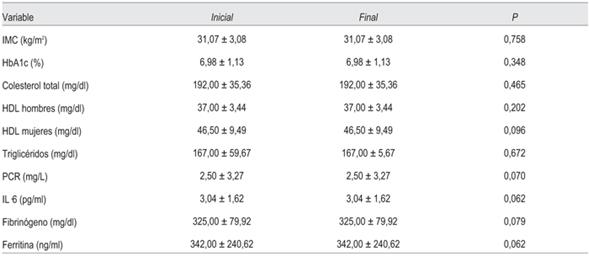
En contraste, el grupo control no mostró diferencias en ninguno de los aspectos investigados: antropométricos, metabólicos, inflamatorios y psicológicos (tabla 5) y (tabla 6).
Comparando la valoración cognitiva en el grupo de intervención no se encontraron diferencias entre la educación primaria y la secundaria, ya sea al principio (78,17 vs. 83,70 p = 0,200), e incluso después de la intervención (88,00 vs. 88,33 p = 0,912).
No hubo eventos adversos en ninguno de los dos grupos.
Discusión
Trabajamos con una muestra de pacientes con DT2 (10 años de diagnosticados por criterios ADA estándar con el objetivo de tomar acciones relativamente tempranas para prevenir el deterioro cognitivo. Es bien sabido que por lo menos diez años previos al diagnóstico de DT2 transcurren con prediabetes, riesgo cardiovascular y resistencia a la insulina y EICBI. Este estudio toma medidas tempranas para prevenir el deterioro cognitivo de acuerdo con Nooyens y colaboradores.
En el estudio Edinburgh Diabetes 2 Study, la IL-6 fue considerada un marcador confiable de inflamación crónica de bajo grado en el cerebro. Los niveles de IL-6 también fueron asociados con declinación cognoscitiva durante el curso de la vida6.
En otro estudio de cohorte se demostró que los marcadores séricos de inflamación, especialmente IL-6 y PCR, se asocian prospectivamente con disminución cognitiva en personas mayores36.
La IL-6 fue uno de los marcadores de inflamación cerebral que alcanzó significancia en nuestro estudio.
En ausencia de depleción de hierro o hemocromatosis la ferritina ha demostrado ser un buen marcador de inflamación aguda y de inflamación crónica de bajo grado. Varios estudios relacionaron la ferritina con el síndrome metabólico, diabetes y otras enfermedades inflamatorias37. En el estudio prospectivo de EPIC-Norfolk los niveles elevados de ferritina sérica predicen la DT2 de nueva aparición38.
La ferritina sérica es un marcador importante de enfermedad inflamatoria. La ferritina sérica alcanzó significación en el grupo de intervención al final de nuestro estudio.
Casi todos los pacientes reclutados para la investigación no se encontraban en equilibrio metabólico en la etapa basal, a pesar de ser tratados por médicos del SNIS.
Al final del estudio el grupo de intervención alcanzó una diferencia estadísticamente significativa en algunos aspectos de la cognición, marcadores inflamatorios como IL-6 y la ferritina, medidas antropométricas y marcadores metabólicos.
No pudimos explicar la ausencia de mejoría en los valores de PCR y fibrinógeno, a pesar de que sus valores están regulados por IL-6.
Conclusiones
Según nuestro conocimiento este es uno de los primeros estudios con el diseño de un ensayo controlado y aleatorizado en demostrar que un programa corto de ejercicio, en el contexto de pacientes con DT2, con ≤ 10 años de diagnóstico -asistidos por nuestro SNIS-, mejora de los marcadores metabólicos, inflamatorios, cognición y calidad de vida.
Destacamos como fortalezas del mismo la valoración integral que incluyó medidas clínicas, de laboratorio, así como el estatus cognitivo y la calidad de vida de los pacientes.
La aplicación temprana y sistemática de un programa de ejercicio de VSEC, u otro programa similar de ejercicio, en el tratamiento habitual de pacientes con DT2 por las instituciones de salud puede contribuir a prevenir el declive cognitivo asociado a la diabetes, así como al estado de salud general de estos pacientes.