Introducción
En el mundo el cáncer de cuello uterino (CCU) es el cuarto cáncer en incidencia y la segunda causa de muerte por cáncer en la mujer.
El CCU es uno de los principales ejemplos sanitarios de inequidad. El 85% de los mismos corresponde a los países subdesarrollados y dependientes con los mayores índices de inequidad social. En cuanto a mortalidad a nivel mundial casi 9 de cada 10 muertes por CCU corresponden a regiones en desarrollo1. En Uruguay el CCU es el tercer cáncer más frecuente en las mujeres, luego del de mama y colorrecto. Aproximadamente se registran en promedio unos 327 casos nuevos cada año, correspondiendo a una tasa de incidencia para CCU por 100.000 de 15,28 y de mortalidad de 5,47, lo cual representa aproximadamente unas 134 muertes anuales2,3.
Desde la década de 1970, cuando Zur Hausen describe por primera vez el vínculo etiológico de la infección por el virus del papiloma humano (VPH) y el CCU, el desarrollo del conocimiento ha permitido el impulso de estrategias de prevención en todos los niveles4.
Estrategias de prevención
La Organización Mundial de la Salud (OMS) recomienda desarrollar un enfoque integral para prevenir y controlar el CCU5. Recomienda abordar las medidas preventivas en el ámbito comunitario con la educación y sensibilización sobre el tema, la vacunación, tamizaje y detección precoz, tratamiento adecuado y cuidados paliativos.
Establece que se incluyan los planes de vacunación contra el VPH como parte de una estrategia nacional de salud pública que adopte un enfoque integral de prevención del CCU.
En la guía de control integral del CCU de la OMS6 se destacan como principales directrices:
Administrar a las niñas, entre los 9 y los 13 años, dos dosis de la vacuna contra los VPH.
Utilizar las pruebas de detección de VPH como método de cribado para prevenir el CCU.
Difundir información de forma más amplia.
En esta guía también se destacan las acciones necesarias para combatir las desigualdades socioeconómicas y de género, garantizando el derecho a la salud de las mujeres.
Uruguay cuenta desde el año 1994 con un Programa de Prevención del Cáncer de Cuello Uterino (PPCCU) que funciona en la órbita de la Comisión Honoraria de Lucha contra el Cáncer y que desde el año 2006, a partir de un acuerdo con el Ministerio de Salud Pública (MSP), funciona en todo el país. El objetivo general de este programa es disminuir la incidencia y mortalidad por CCU en Uruguay. Este programa ha funcionado en el terreno de la asistencia pública y ha sido el responsable del desarrollo e implementación de manera ordenada y controlada y con control de calidad de la colpocitología oncológica en nuestro país7.
En el año 2011, ya en el marco del Sistema Nacional Integrado de Salud (SNIS) y con el principal objetivo de obtener datos para el desarrollo e implementación de medidas tendientes a disminuir la incidencia y mortalidad por CCU en Uruguay, el MSP realizó una auditoría sobre la situación, posteriormente, y a partir de estos insumos, un análisis técnico de las medidas de prevención primaria y secundaria. Una de las principales conclusiones de dicha auditoría fue que el país no contaba con un programa de prevención que funcionara en la órbita del rectorado y que abarcara todos los niveles de prevención de este cáncer. Finalmente, en marzo del 2012, el MSP determina las principales líneas estratégicas en medidas preventivas del CCU en el país y en agosto del mismo año se desarrolla el Plan Nacional de Prevención Integral del Cáncer de Cuello Uterino (PNPICCU). Este plan pretendía convertirse en la herramienta estructurada e implementada desde el MSP que abarcase prestaciones educacionales, de tamizaje, diagnóstico, tratamiento y rehabilitación. Se proyectaron y realizaron actividades en el período 2012-2015. Específicamente en lo referente a las medidas de prevención primaria del CCU se desarrollaron las siguientes actividades: campañas de educación, difusión e información referente a la vacunación contra el VPH; actividades formativas con docentes de centros de educación secundaria; material escrito con los contenidos para el abordaje educativo en Secundaria de prevención primaria y secundaria; material informativo escrito para profesionales médicos que pueden indicar la vacuna contra el VPH; se oficializaron y analizaron los trabajos sobre serotipos circulantes de VPH en población sana, así como en los cánceres invasores de Uruguay; desarrollo de estudio costo-efectividad de la implementación de la vacuna contra VPH en el medio local; desarrollo e implementación, en conjunto con el Departamento de Inmunizaciones del MSP, de un plan de vacunación contra el VPH, así como un sistema de fármaco-vigilancia y de recordatorio para lograr la cobertura adecuada (con tres dosis) dada la dificultad de una vacuna con la necesidad de tres dosis8.
Virus del papiloma humano
Hace más de 30 años que se conoce y estudia el papel oncogénico del VPH como factor etiológico9.
La infección por el VPH es la infección de transmisión sexual más frecuente.
Existen más de 100 tipos de VPH, entre 30 a 40 se pueden aislar del tracto genital. Los VPH se categorizan, según la capacidad oncogénica in vitro, como de bajo y alto riesgo10. Los VPH de alto riesgo, relacionados con lesiones de alto grado, CCU, vagina, vulva, son: 16, 18, 31, 33, 35, 39, 45, 51, 55, 56, 58, 59, 66, 68. Los VPH de bajo riesgo, vinculados con el desarrollo de lesiones benignas, son: 6, 11, 26, 42, 44, 54, 70, 73.
A diferencia de otras enfermedades infecciosas, la presencia del germen no provoca de manera irremediable la infección, sino que por el contrario la inmensa mayoría se resuelve espontáneamente. Al analizar la historia natural común de la afección se describe que primero existe el contagio, luego la infección y solo en los casos de persistencia de la misma se avanza a una lesión orgánica denominada neoplasia intraepitelial, genéricamente descrita como lesión premaligna. El CCU es la etapa final de una infección con VPH de alto riesgo en un determinado huésped.
Hay que destacar el comportamiento de la infección por VPH: a lo largo de la vida hasta el 80% de las personas sexualmente activas podrán desarrollar una infección por algún VPH, con un pico de incidencia en la adolescencia y juventud. A pesar de que las infecciones transitorias disminuyen con la edad, aumentan las posibilidades de infecciones persistentes, y cuando estas corresponden a los VPH 16 o 18 son las que tienen mayor riesgo de desarrollar CCU11.
El desarrollo de un CCU no solo depende de la evolución de la infección por VPH, sino también de las condiciones de salud de la mujer y esto se encuentra establecido por los determinantes sociales de la salud y las diferencias socioeconómicas12.
En Uruguay se conocen las cepas de los VPH de alto riesgo relacionadas con el desarrollo del CCU, identificándose en 65,9% de las muestras analizadas de CCU VPH 16, y en 7,4% el 1813.
Epigenética
La frecuencia y facilidad de transmisión de los VPH lo convierten en una infección que coexiste con el humano. Así, es importante conocer el comportamiento tanto por parte de los profesionales de la salud, pero sobre todo por la sociedad, para evitar la culpa y estigmati zación de la infección.
Los eventos epigenéticos son cada vez más conocidos y estudiados. En particular la epigenética en la carcinogénesis es cada vez más estudiada y su conocimiento seguramente abra más puertas y posibilidades en el conocimiento y tratamiento del CCU14. Se han estudiado eventos de metilación tanto a nivel de los genes del huésped como de los genes del VPH. La metilación de regiones promotoras es un mecanismo que favorece la carcinogénesis mediante la inactivación de genes supresores de tumor15.
Dos de las principales oncoproteínas virales, E6 y E7, están relacionadas en la interacción del virus y la célula e inducen concomitantemente cambios epigenéticos en las células infectadas y en las que evolucionan a la transformación maligna. Estas proteínas interactúan con proteínas relacionadas con regulación epigenética, incluyendo ácido desoxirribonucleico (ADN), metiltransferasas, enzimas modificadoras de histonas y subunidades de complejos de remodelación de la cromatina, influyendo así en el programa de transcripción de la célula huésped. Además, las oncoproteínas del VPH modulan la expresión de micro ácido ribonucleico (ARN) celular. La mayoría de estas acciones epigenéticas son las relacionadas con la infección persistente y la transfor mación celular maligna16.
Se cree que los factores ambientales y de estilo de vida están implicados en el desarrollo de una amplia gama de cánceres humanos provocando cambios epigenéticos. Eventos epigenéticos aberrantes asociados con factores de estrés ambiental juegan un papel importante en el inicio y la progresión de diferentes neoplasias humanas. En particular si analizamos el comportamiento y la distribución del CCU y su clara relación con los determinantes sociales de la salud, no es difícil pensar que los eventos epigenéticos tienen necesariamente que incorporarse en el proceso etiopatogénico de la enferme dad17).
Vacunas contra los virus del papiloma humano
Las vacunas contra VPH han demostrado eficacia para prevenir infecciones persistentes y lesiones precancerosas. Estos resultados son mejores en mujeres que completaron el esquema de vacunación y negativas para la infección por VPH en el tracto genital previo a la inmunización18,19.
Todos los análisis de eficacia se realizan a partir de variables subrogadas, decisión que fue tomada en el año 2003 a partir de una recomendación de la OMS20, por lo cual, si bien las lesiones precancerosas son consideradas precursoras del CCU, no es exacto ni correcto afirmar que son vacunas contra el CCU. Destacando, además, que la infección por VPH no es la única condición para la progresión al cáncer, sino que son necesarios los denominados cofactores. La presencia de estos cofactores (infecciones de transmisión sexual, tabaquismo, paridad, ingesta de anticonceptivos orales, etcétera) es muy variable entre diferentes realidades socioeconómicas y culturales21.
Por otra parte, es importante transmitir que el 30% de los CCU están relacionados etiopatológicamente con serotipos de VPH no vacunales.
Las vacunas actualmente habilitadas para la prevención primaria no son terapéuticas, destacándose que la inmunidad que generan es de tipo humoral y no celular. Se ha demostrado que no hay diferencias significativas en el desarrollo de lesiones vinculadas con VPH 16 y 18 en mujeres que eran positivas a estos virus previo a la vacunación22. Esto significa que su capacidad de acción se refiere a la posibilidad de evitar infecciones persistentes al momento de la exposición, pero no el de eliminar una displasia o cáncer existente, o evitar su progresión.
En el campo de la inmunoterapia se encuentran en estudio las vacunas terapéuticas, para las cuales las características inmunogénicas del objetivo deben ser: tener una expresión única dentro del tumor o diferencial al tejido normal; debe expresarse y mantenerse durante todo el proceso de carcinogénesis, y debe ser altamente inmunogénica. En particular las proteínas E6 yE7 del proceso de reproducción de los VPH cumplen con estos criterios23.
El perfil de seguridad a largo plazo es adecuado24.
En nuestro país están registradas y disponibles dos vacunas contra el VPH con las siguientes indicaciones:
Gardasil®: prevención de lesiones genitales premalignas (cervicales, vulvares y vaginales), cáncer cervical y verrugas genitales externas (condiloma acuminado) causalmente relacionadas con los serotipos 6, 11, 16 y 18 del VPH;
Cervarix®: prevención de lesiones cervicales premalignas y cáncer de cérvix causadas por los serotipos 16 y 18 del VPH, en mujeres de 15 a 25 años de edad.
Desde el año 2012 y en el marco de las diferentes estrategias de prevención primaria desarrolladas en el PNPICCU, el Programa Nacional de Inmunizaciones introduce la vacuna contra VPH asumiendo lo relevante de las recomendaciones de la OMS, destacando:
1. La necesidad de que las estrategias de prevención primaria como la vacunación sean parte de estrategias coordinadas para la prevención del CCU y otras enfermedades vinculadas a la infección por VPH. Debería incluir educación sexual para la disminución de las conductas de riesgo para la adquisición de la infección por VPH e información sobre el diagnóstico y tratamiento de las lesiones precancerosas y el CCU.
2. La implementación de la vacunación no debe desviar los esfuerzos para el financiamiento de un programa efectivo de tamizaje del CCU.
3. La vacunación no elimina la necesidad del tamizaje de las personas vacunadas debido a que con las vacunas disponibles no se cubren todos los tipos de VPH que causan CCU (se estima que se cubre el 70% de los CCU producidos por VPH).
4. Debe incluir una vigilancia estricta posintroducción de la vacuna para monitorizar el impacto sobre la prevalencia de serotipos de VPH, incidencia de lesiones precancerosas y CCU, incidencia de mortalidad por cáncer invasor y vigilancia de efectos adversos vinculados a la vacuna. La medida del impacto de la vacunación sobre lesiones precancerosas y CCU requiere monitorización por décadas.
Desde entonces se implementó una estrategia de vacunación, con la vacuna contra VPH en forma gratuita en adolescentes de 12 años, pasando luego de avanzar en la educación, promoción y análisis del comportamiento local del VPH, del tamizaje a nivel nacional, así como en la proyección y análisis de costo efectividad de la medida, a ser una estrategia recomendada.
Claro está que en esta estrategia de incorporación de la medida en el programa nacional de inmunizaciones, la clave está en los educadores y en el propio sistema sanitario que debe incorporar en el cuerpo de profesionales encargados de la promoción y atención la importancia de la recomendación y la promoción en salud para lograr una amplia cobertura, así como la incorporación de todo el arsenal de medidas preventivas que existen para esta enfermedad.
Las políticas públicas y la vacunación obligatoria
Una de las responsabilidades de los gobiernos es definir cuáles son los criterios para incluir determinada vacuna en los programas nacionales y bajo qué condiciones se hace. Las políticas de vacunación deben generar tanto beneficios colectivos como individuales25.
El Estado debe proteger la salud pública y en este contexto las infecciones que ponen en riesgo la misma se deben prevenir. La protección contra agentes que se puedan adquirir en el medio ambiente o que se puedan adquirir involuntariamente son uno de los objetivos de los planes de vacunación. Se podrían considerar criterios de definición de planes de vacunación:
Que se trate de infecciones que causen importantes consecuencias en la población, ya sea por la severidad del caso individual o por la posibilidad de afectar a grandes grupos de personas. En este punto podemos decir que estas vacunas son justificadas por la potencialidad, por un lado, de poder disminuir la incidencia del CCU y eventualmente la mortalidad por esta causa. Por otro lado, pueden tener grandes impactos poblacionales disminuyendo costos individuales y poblacionales por lesio nes tan frecuentes como las verrugas genitales.
Contar con vacunas con probada efectividad y seguridad. Las vacunas contra el VPH han mostrado su efectividad en reducir la posibilidad de desarrollar lesiones premalignas de cuello uterino sobre todo en mujeres VPH negativas. En cuanto a la seguridad, los organismos de referencia no han encontrado hasta el momento eventos graves relacionados directamente con la vacuna que superen el beneficio.
Ser costo-efectiva, es decir que el balance económico de los beneficios obtenidos sea positivo o sea menor que otras medidas con iguales beneficios. En este punto en particular no contamos con un análisis a nivel local.
Una tarea esencial a la hora de las definiciones es la evaluación de la carga o riesgo individual de la enfermedad para poder definir si el acceso a las vacunas es un punto relevante para lograr la igualdad de acceso sanitario de la población. En este sentido la disponibilidad de las mismas en forma gratuita es una definición que apunta a respetar dicho principio26.
Es responsabilidad de los gobiernos definir programas ordenados y generar confianza y compromiso en los mismos, tanto por parte de la población como por parte de los profesionales. Esta es una estrategia fundamental a la hora de cualquier medida sanitaria ofrecida, ya que se debe contar con la aceptación poblacional, así como con la responsabilidad profesional a la hora de educar e indicar27.
Discusión
Las políticas de recomendación de la vacunación son importantes para lograr altas tasas de cobertura. Para el éxito de las mismas, como dijimos, son necesarias la educación y confianza de la población, y el conocimiento y compromiso del sistema sanitario para asumir la responsabilidad del accionar proactivo y la indicación rutinaria. Estas indudablemente no son políticas que persuadan a las personas. Otra estrategia probable para lograr la cobertura deseada o el impacto poblacional es la vacunación obligatoria.
Creemos que la definición de una política u otra está de la mano de dos conceptos; primero, la definición de si se está ante un riesgo sanitario poblacional y, segundo, si es necesario promover decisiones informadas para lograr un mayor impacto. En este sentido lo fundamental es definir si se considera abordar la infección por el VPH dentro de una estrategia integral de prevención como enfermedad de transmisión sexual. De esa forma se debería discutir firmemente la obligatoriedad para todos los involucrados en la cadena de transmisión y vacunar también a los varones.
También debemos pensar cuál va a ser el argumento que se tendrá cuando alguien no acepte vacunarse, dado que no se trata de una infección que exponga a riesgos a la sociedad. ¿Cuál es, entonces, el sustento de una medida sanitaria obligatoria en particular cuando no hay un riesgo poblacional en juego?
Las medidas de persuasión no necesariamente requieren manejo de información por los implicados, lo cual en una enfermedad como el CCU, donde otras medidas de prevención (tamizaje, educación sexual, métodos de barrera) han demostrado su efectividad en la disminución de su incidencia, puede conspirar en contra de estrategias integrales de impacto en las sociales.
La vacunación contra el VPH se recomienda dentro de programas integrales de educación, prevención secundaria, terciaria y aun cuaternaria. Se deben ofrecer iguales condiciones de protección poblacional contra el CCU, y en este sentido es sustancial que el Estado se responsabilice de estas acciones y del acceso a todas ellas, es decir que la equidad se debería alcanzar en el acceso a la vacuna pero también en las otras medidas de prevención recomendadas.
Sabemos que existen estrategias que han demostrado disminuir el CCU, como los programas de tamizaje dirigidos, por lo cual también deberíamos invertir en esto.
Lo discutible es que, como respuesta a nuestra imposibilidad de evitar muertes evitables con medidas que ya conocemos, implementemos una medida obligatoria que nos excusa de la responsabilidad que no hemos cumplido con el resto de las acciones recomendadas.
Conocemos acciones poblacionales con impacto demostrado en la incidencia y mortalidad por CCU, y por lo tanto debemos cuestionarnos si los gobiernos no deberían estar obligados a implementarlas o promoverlas. Sabemos que:
Los programas dirigidos de tamizaje disminuyen significativamente la incidencia de CCU y la muerte. Nuestro país tiene condiciones geográficas, poblacionales, sanitarias, que nos acercan a lograr estas características.
Está confirmado que el tamizaje con test de VPH aumenta la sensibilidad diagnóstica y la aceptabilidad del método28,29. La OMS lo recomienda como test de tamizaje. Aún no hemos puesto en el punto de evaluación su incorporación dentro de la estrategia nacional.
El diagnóstico precoz y el tratamiento adecuado evitan la muerte por la enfermedad. Por lo tanto, deberíamos poder auditar y asegurar el acceso y control de calidad de los procedimientos diagnósticos y terapéuticos.
Se recomienda que la vacunación se inscriba dentro de una estrategia global de prevención y con programas de tamizaje funcionando. Aún no hemos logrado un programa de tamizaje con cobertura adecuada.
Desde que se descubrió la relación entre las relaciones sexuales y el riesgo de cáncer de cuello30 la afección marca un estigma social que las mujeres relacionan con sus comportamientos sexuales y sus creencias religiosas.
Como sabemos, el estigma genera miedo y construye barreras, muchas veces insalvables, para el acceso a los servicios de salud, lo que impide realizar acciones preventivas, retrasa diagnósticos e impide tratamientos oportunos.
Sin embargo, un reciente estudio realizado en Holanda cambia radicalmente la perspectiva31. El denominado estudio HELIUS se propuso como objetivo evaluar la prevalencia de infecciones por serotipos oncogénicos de VPH y su relación con la presencia de CCU en seis diferentes grupos étnicos que viven en Ámsterdam. Se encontró que la población de las mujeres holandesas, de Surinam y africanas presentan el mayor comportamiento sexual de riesgo y esto se releja en la prevalencia de los serotipos oncogénicos de VPH holandés (40%), Surinam-África (32%), Turquía (29%), Ghana (27%), Marruecos (26%) y Surinam-Sur de Asia (18%). Sin embargo, esta mayor prevalencia global VPH de alto riesgo y el comportamiento sexual de riesgo más alto en la población nativa holandesa no se relaciona con la mayor prevalencia de CCU, que es mayor en las poblaciones no locales, por lo cual se necesitan más investigaciones para desentrañar la compleja problemática relativa a las disparidades del CCU. Factores probablemente vinculados son las diferencias en la participación en el programa de cribado de CCU, o diferencias en el acla ramiento y la persistencia de VPH de alto riesgo.
Lo que se puede concluir de este estudio es que la disminución de la prevalencia de la infección por VPH no garantiza la disminución de la incidencia del CCU; entonces, el corolario sería que la infección por VPH y el CCU no necesariamente son direccionales. Así, la infección dependería más que de la acción viral de la acción inmune que puede llevar o bien al aclaramiento (cuando es exitosa) o bien a la persistencia (cuando es defectuosa). El sistema inmune ignora o al menos muestra fallas para detectar la infección por VPH básicamente por tres grandes causas: en primer lugar, por déficit de la inmunidad general, vinculada al estado de salud integral de la mujer (bio-psico-social); en segundo lugar, a cambios locales, por ejemplo, provocados por el embarazo, adolescencia, y en tercer lugar a factores de riesgo, como, por ejemplo, a la exposición precoz. Esto nos hace pensar que el CCU, más que una enfermedad infecciosa es una afección de etiología infecciosa que requiere de una inmunidad deficiente relacionada de manera directa con los determinantes sociales de la salud, la discriminación, el estigma social y la vulneración de derechos, sobre todo sexuales y reproductivos.
Es imprescindible entonces priorizar la prevención integral sobre cada uno de sus componentes:
Prevención primaria: educación en salud y derechos sexuales y reproductivos (inicio precoz de relaciones sexuales, número de parejas, métodos de barrera, vacu nas).
Prevención secundaria: examen ginecológico periódico, screening (colpocitología oncológica, incorporación de otros métodos como la detección de VPH) para proponerse como objetivo general disminuir la inci dencia y mortalidad.
Prevención terciaria: tratamiento oportuno y adecuado al estadio, rehabilitación y cuidados paliativos.
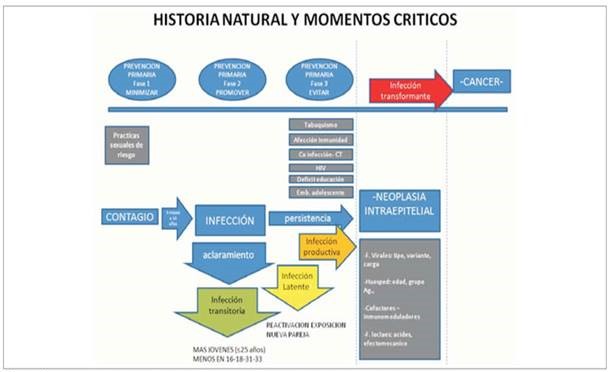
Se podrían proponer medidas clave en los diferentes momentos de la historia natural de la afección, como se muestra en la (figura 1), donde se proponen tres fases de prevención primaria. Fase 1: minimizar el contagio; fase 2: promover el aclaramiento, y fase 3: evitar la persisten cia.
El cáncer de cuello es una afección mucho más compleja de lo previsto y, por lo tanto, a la hora de abordar, en particular la prevención primaria, en lo que denominamos fase 1 (minimizar el contagio), la educación en salud y derechos sexuales y reproductivos, así como la existencia de alternativas y proyectos para adolescentes y jóvenes son la clave.
Con respecto a impedir el contagio de serotipos 16 y 18 se considera una acción muy pertinente y por ende debe ser recomendada por la rectoría. Sin embargo, la presencia de serotipos no vacunales en un alto porcentaje de los CCU32 hace que sea un riesgo importante crear una falsa seguridad de protección que de ninguna manera se asimila a la protección de las inmunizaciones del certificado de esquema de vacunación (CEV) nacional.
Bloquear la acción de algunos tipos de VPH sin mejorar el marco general de aclaramiento del virus en la población general implica riesgos potenciales de mantenimiento de acción deletérea de genotipos no vacunales; disminución de políticas de screening.
Por último, el objetivo de erradicar la circulación de los cuatro serotipos oncogénicos es factible con la vacuna nanovalente que cubre las cuatro cepas de alto riesgo, y para lograrlo se debería vacunar a niñas, niños y adolescentes. Mientras tanto la recomendación es adecuada, pero la obligatoriedad es riesgosa.
Podemos implementar un sinnúmero de medidas sanitarias obligatorias o compulsivas que seguramente impactarán en los indicadores sanitarios. La pregunta es: ¿ese es el camino?