Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Médica del Uruguay
versión impresa ISSN 0303-3295versión On-line ISSN 1688-0390
Rev. Méd. Urug. vol.32 no.3 Montevideo set. 2016
Diez años del Registro Uruguayo de Peritonitis en Diálisis Peritoneal
Liliana Gadola*, Teresa Gómez†, Lucía Saez‡, Daniel Pérez§, Lucía Orihuela¶, Virginia Ramella**, Emma Bugstaller††, Alejandra Canon‡‡, Carlota González-Bedat§§, Patricia Larre-Borges¶¶, Mariela Mautone***, Anabella Rébori†††, Alicia Sans‡‡‡, Natalia Orihuela¶¶¶, Mario Forselledo****, María Eugenia Torres Debat††††, Verónica Seija‡‡‡‡
Resumen
La peritonitis es una complicación grave de la diálisis peritoneal (DP), por lo que interesa conocer la incidencia y sensibilidad antibiótica de los gérmenes causantes. En Uruguay, desde el 1° de enero de 2004, se realiza un registro nacional de las peritonitis en DP, gérmenes, sensibilidad y evolución. Método: se analizaron los registros desde el 1° de enero de 2004 al 31 de diciembre de 2013. El registro fue aprobado por comités de ética institucionales. Resultados: en el período se registraron 850 peritonitis, con una incidencia que descendió de 0,49/paciente-año (2004-2005) a 0,37/paciente-año (2013). La incidencia de Staphylococcus aureus y Staphylococcus coagulasa negativo (SCoN) fue menor en 2009-2013 vs 2004-2005 (0,2 vs 0,12 peritonitis/paciente-año, test Poisson p<0,05). En 2009-2013: 14/54 S. aureus y 26/71 SCoN fueron meticilinorresistente, similar al período previo. El 98% de los gérmenes gramnegativos fueron sensibles a amikacina. En 145/467 (31%) episodios no se identificó germen. Se logró cura primaria en 71% de las peritonitis por grampositivos y en 45% por gramnegativos (chi2 p<0,05). En 2013 se observó mayor incidencia de peritonitis en los centros en los que no se controló el estado de portador nasal. Comentarios y conclusiones: se justifica implementar el control de portador de Staphylococcus aureus. La incidencia de peritonitis por S. aureus y SCoN meticilinorresistentes, la incidencia sostenida de gérmenes gramnegativos (con peor evolución), y el elevado porcentaje de cultivos sin desarrollo justifica mantener el protocolo antibiótico empírico inicial con vancomicina y amikacina. El descenso de la incidencia de S. aureus + SCoN podría ser atribuido a una mejor educación de los pacientes en DP.
Palabras clave: PERITONITIS
DIÁLISIS PERITONEAL
Key words: PERITONITIS
PERITONEAL DYALISIS
* Profesora Agregada de Nefrología, Facultad de Medicina, Universidad de la República.
† Nefróloga, Grupo de Diálisis Peritoneal, Sociedad Uruguaya de Nefrología.
‡ Ex Asistente de Nefrología, Facultad de Medicina, Universidad de la República.
§ Nefrólogo, Grupo de Diálisis Peritoneal, Sociedad Uruguaya de Nefrología.
¶ Ex Asistente de Nefrología, Facultad de Medicina, Universidad de la República.
** Nefróloga y Pediatra, Grupo de Diálisis Peritoneal, Sociedad Uruguaya de Nefrología.
†† Nefróloga, Grupo de Diálisis Peritoneal, Sociedad Uruguaya de Nefrología.
‡‡ Ex Asistente del Centro de Nefrología, Facultad de Medicina, Universidad de la República.
§§ Nefróloga, Grupo de Diálisis Peritoneal, Registro Uruguayo de Diálisis, Sociedad Uruguaya de Nefrología.
¶¶ Profesora Adjunta de Nefrología, Facultad de Medicina, Universidad de la República.
*** Profesora Adjunta de Nefrología, Facultad de Medicina, Universidad de la República.
††† Jefa del Servicio de Nefrología Pediátrica, Centro Hospitalario Pereira Rossell, ASSE, Grupo de Diálisis Peritoneal, Sociedad Uruguaya de Nefrología.
‡‡‡ Ex Asistente de Nefrología, Facultad de Medicina, Universidad de la República.
§§§ Asistente de Nefrología, Facultad de Medicina, Universidad de la República.
¶¶¶ Nefróloga, Grupo de Diálisis Peritoneal, Sociedad Uruguaya de Nefrología.
**** Nefrólogo, Grupo de Diálisis Peritoneal, Sociedad Uruguaya de Nefrología.
†††† Microbióloga, Ex Profesora Adjunta de Bacteriología y Virología, Ex Profesora Adjunta de Laboratorio Clínico, Facultad de Medicina, Universidad de la República. Laboratorio de Bacteriología CASMU-IAMPP.
‡‡‡‡ Microbióloga, Profesora Agregada Laboratorio de Patología Clínica, orientación Bacteriología, Facultad de Medicina, Universidad de la República.
Colaboraron con el registro:Lilián Costa, Gianella Ghelfi, Rossana Laborda, Fátima Mastandrea, Mariela Vieira, Carla Poggi Licenciadas de Enfermería, Grupo de Diálisis Peritoneal, Sociedad Uruguaya de Enfermería Nefrológica.
Correspondencia: Dra. Liliana Gadola. 18 de Julio 2103/802, Montevideo, Uruguay Correo electrónico: lilianagad@gmail.com
Los autores declaran que no existe conflicto de intereses.
Recibido: 1/10/15 Aprobado: 23/11/15.
Introducción
La peritonitis es la principal complicación, vinculada al tratamiento, de los pacientes en diálisis peritoneal (DP). La incidencia ha disminuido a lo largo de las décadas desde el inicio de esta modalidad terapéutica, vinculada a mejoras en los sistemas de conexión, control y tratamiento de portadores de Staphylococcus aureus y a la mejor educación de los pacientes para realizar este autotratamiento domiciliario(1,2).
Sin embargo, las complicaciones derivadas de episodios de peritonitis son una de las principales causas de abandono de la técnica dialítica y de mortalidad en este grupo de pacientes(3,4).
El tratamiento precoz y adecuado de los episodios de peritonitis es una piedra angular del éxito del mismo, por lo que conocer la prevalencia de los distintos gérmenes y su sensibilidad antibiótica tiene fundamental importancia. Los protocolos empíricos iniciales propuestos por las guías internacionales tuvieron variaciones a lo largo de los años, de acuerdo a cambios en los gérmenes prevalentes y al aumento de la resistencia a antibióticos entre los gérmenes grampositivos. Así, de las cefalosporinas de primera generación utilizadas inicialmente en la década de 1980, se pasó a recomendar el uso de vancomicina y luego, por temor a la aparición de resistencia a ésta, las guías internacionales la desaconsejaron. Finalmente, desde 2006, recomiendan basar el tratamiento empírico inicial en el conocimiento de la sensibilidad a antibióticos de los gérmenes prevalentes en cada centro o región(5,6). Entre los antibióticos utilizados en los protocolos empíricos iniciales el uso de vancomicina y aminoglucósidos ha sido particularmente debatido, por lo que el conocimiento de la sensibilidad de los gérmenes prevalentes en una determinada región adquiere una relevancia que ha sido destacada en las guías internacionales desde 2006(5-8). Con el objetivo de conocer la situación nacional el Grupo de estudio de DP de la Sociedad Uruguaya de Nefrología (DP-SUN) realizó un registro de todos los episodios de peritonitis observados en pacientes en DP crónica en el país desde 2004, en el que participaron todos los centros de DP (ocho de adultos y uno pediátrico). El Grupo DP-SUN realizó un análisis anual de los resultados y en 2006, basado en los resultados de los dos años previos(9), estableció como protocolo empírico inicial nacional la asociación de vancomicina y amikacina intraperitoneales, en dosis ajustadas al peso del paciente y a los niveles plasmáticos de los mismos. Se realizaron jornadas conjuntas con microbiólogos a los efectos de establecer recomendaciones para uniformizar las técnicas de los estudios microbiológicos de líquido peritoneal (figura 1) de acuerdo a las recomendaciones internacionales, las que se ajustaron en 2013(4).
Objetivos
Los objetivos del presente estudio fueron: a) conocer la incidencia de peritonitis asociada a DP; b) determinar los gérmenes causales y su sensibilidad antibiótica para optimizar el protocolo terapéutico empírico inicial; c) evaluar los posibles factores de riesgo de contaminación peritoneal; d) conocer la evolución de las peritonitis en DP en el país.
Material y método
Diseño: se realizó un estudio observacional, prospectivo, de cohorte.
Población: se incluyeron todos los pacientes en DP de Uruguay, entre el 1° de enero de 2004 y el 31 de diciembre de 2013 y se estudiaron los episodios de peritonitis que se diagnosticaron en esta población.
Metodología: se analizó el registro de todos los episodios de peritonitis observados en pacientes en DP crónica en el país realizado por el Grupo de estudio de DP-SUN. Participaron todos los centros de DP de Uruguay (ocho de adultos y uno pediátrico). Cada vez que se diagnosticó un episodio de peritonitis se envió al laboratorio clínico la bolsa o muestra de drenado peritoneal obtenida al momento de la consulta(4,5) para realizar recuento celular y cultivos, previo al inicio de la terapia antimicrobiana. Además, se solicitó el registro de las siguiente variables: edad del paciente al momento del evento reportado, tiempo en DP, fecha del episodio, germen y su sensibilidad antibiótica, tratamiento antibiótico inicial y si se realizó cambio del mismo, así como evolución (cura primaria, cura con cambio antibiótico, retiro de catéter peritoneal o fallecimiento). Exclusivamente en los episodios del año 2013 se registraron algunos factores considerados de riesgo de adquirir infecciones en DP: edad, sexo, diabetes, tiempo en DP, estación del año del episodio y si en el centro se realizaban controles periódicos del estado de portador nasal de S. aureus.
Las peritonitis en niños en DP se registraron desde 1° de enero de 2009 y fueron analizadas en forma independiente.
Procesamiento en laboratorio: una vez llegada la muestra se procedió a agitar la misma de manera de homogeneizar el contenido. Se utilizaron volúmenes no inferiores a 50 ml para centrifugación y para cultivo de bacterias y hongos en medios sólidos y enriquecimientos. En el caso de pacientes pediátricos se procesó el total de volumen recibido. Se centrifugó líquido para confeccionar frotis para examen microscópico (figura 1). La investigación de micobacterias se realizó en casos seleccionados. En los aislamientos de Staphylococcus sp. se reportó la sensibilidad a los siguientes antibióticos: oxacilina, cefoxitín, gentamicina y vancomicina. Aquellas cepas resistentes a oxacilina o cefoxitín fueron definidas como meticilinorresistentes y por lo tanto resistentes a todos los betalactámicos, incluida cefazolina. En los aislamientos de bacterias gramnegativas se reportó la sensibilidad a ciprofloxacina, ceftazidime y amicacina. Se dividieron los agentes causales en cuatro grupos: bacterias grampositivas, gramnegativas, hongos y polimicrobianas. Dentro de los primeros se distinguieron tres grupos: Staphylococcus aureus, Staphylococcus coagulasa negativos (SCoN) y otras bacterias grampositivas (no Staphylococcus).
Definiciones
Para el diagnóstico de peritonitis asociada a DP se utilizó la definición de la International Society of Peritoneal Dialysis(4), o sea la presencia de al menos dos de tres criterios: 1. Síntomas y signos de inflamación peritoneal. 2. Líquido peritoneal turbio con recuento leucocitario superior a 100 cel/mm3 con al menos 50% de polimorfonucleares. 3. Presencia de gérmenes en el líquido peritoneal drenado.
“Cura primaria” se definió como la curación (regresión de síntomas, signos y polimorfonucleares en líquido peritoneal) con el protocolo antibiótico empírico inicial. No se registraron las recaídas/recidivas de peritonitis, por lo que el episodio inicial se consideró “curado” y la recidiva/recaída como un nuevo episodio. Se consideraron fallecidos como “consecuencia de la peritonitis” a quienes fallecieron antes del alta por el episodio o hasta un mes del episodio.
Ética: el proyecto fue aprobado por el Comité de Ética del Hospital de Clínicas y de las instituciones participantes. Los datos recabados de las historias clínicas se registraron en una base independiente, sin datos identificatorios de los pacientes ni de las instituciones de acuerdo a la normativa legal vigente (ley de Habeas Data).
Estadística: la incidencia de peritonitis se expresó como episodios por paciente-año, conociendo el número de episodios y el tiempo de exposición (suma de los meses en tratamiento con DP de toda la población en DP en el período considerado).
Los datos continuos se expresan como media y desvío estándar o mediana y rango, según corresponda a su distribución. Se utilizaron test de t o chi2 según correspondiera. Las incidencias de episodios se compararon con el test de Poisson. Se considera significativa una p < 0,05.
Resultados
A. Incidencia de peritonitis
Se analizaron los datos del registro en el período señalado y se compararon por períodos a los efectos de analizar posibles cambios en los gérmenes causales o en la evolución.
Se registraron 850 episodios de peritonitis, con una incidencia global de 0,47 episodios/paciente-año. En el primer período (2004-2008) se observaron 383 episodios, con un tiempo de exposición total de 9.903 meses (incidencia 0,46 peritonitis por paciente-año) y en el segundo período (2009-2013) 467 peritonitis en un tiempo de exposición total de 11.810 meses (0,47 peritonitis por paciente-año). La incidencia fue similar en ambos períodos, test Poisson (NS) (tabla 1). Al comparar la incidencia de peritonitis en los dos primeros años (2004-2005) (144 episodios en 3.552 meses de exposición, incidencia 0,49 episodios/paciente-año) con el año 2013 (74 episodios, tiempo de exposición 2.398 meses, incidencia 0,37 episodios/paciente-año) (tabla 3) se observa un descenso significativo (test Poisson, p < 0,05) que, sin embargo, ha sido irregular en los diferentes años observados.
B. Incidencia de peritonitis por tipo de germen (figura 2)
En el período 2009-2013 se observa una leve mayor incidencia, aunque no significativa, de bacterias gramnegativas (0,1 peritonitis/pac-año) comparado con el período previo (0,09 peritonitis/pac-año) (test de Poisson NS) y una significativa menor incidencia de SCoN (diversas especies de Staphylococcus coagulasa negativo) y S. aureus (0,2 vs 0,12 peritonitis/paciente-año) (test de Poisson p < 0,05) (tabla 1 y figura 2).
C. Etiología de la peritonitis y sensibilidad antibiótica
En la tabla 1 se pueden observar los agentes causales y su susceptibilidad a los antibióticos reportados. En el período 2009-2013 se observaron 14/54 S. aureus y 26/71 SCoN meticilinorresistentes. Respecto a los gérmenes gramnegativos, 98% eran sensibles a amikacina y globalmente 28/162 (17%) de gérmenes testados eran resistentes a ciprofloxacina. Se observaron 31% de episodios (145/467) en los que no se logró identificar germen, similar al período 2004-2008 (Poisson NS).
Entre los gérmenes gramnegativos se destaca la baja incidencia de Pseudomonas aeruginosa (tabla 1) en todo el período (14/850 episodios, la incidencia 2004-2008 fue de 0,008 peritonitis/paciente-año y en 2009-2013 de 0,007 peritonitis/paciente-año). La sensibilidad antibiótica de los gérmenes gramnegativos estudiados fue amplia, con escasas cepas resistentes a ciprofloxacina (11/115) y a ceftazidime (12/112) (tabla 1) y casi no se identificó resistencia en Pseudomonas spp. (excepto un caso de resistencia a meropenem).
La incidencia de peritonitis fúngicas se ha mantenido baja durante el período analizado (se realiza tratamiento empírico con antifúngico en recaída/recidiva de peritonitis o si la peritonitis aparece en un paciente que ha recibido tratamiento antibiótico reciente o prolongado).
D. Evolución
Se observó cura primaria con el protocolo empírico inicial de vancomicina y amikacina intraperitoneal en 259/363 (71%) de peritonitis causadas por bacterias grampositivas y en un número menor en los episodios causados por bacterias gramnegativas: 67/171 (39%) (chi2 p<0,05) (tabla 2).
Se observó una “mala evolución” (retiro catéter y fallecimiento) en 78/171 (45%) de peritonitis por gramnegativos, significativamente mayor que en los episodios por grampositivos (58/363, 16%) (chi2 p<0,005). En 6/14 (43%) peritonitis a Pseudomonas spp. se logró curación con tratamiento antibiótico intraperitoneal ajustado a sensibilidad, en 7/14 (50%) se retiró el catéter peritoneal y un paciente (7%) falleció.
En el período 2009-2013 se retiraron 97 catéteres peritoneales (21%) y fallecieron 22 pacientes (4,7%). En el período total se retiraron 185 catéteres peritoneales (por peritonitis consideradas refractarias al tratamiento médico) y fallecieron 42 pacientes (4,9%).
E. Peritonitis en población pediátrica
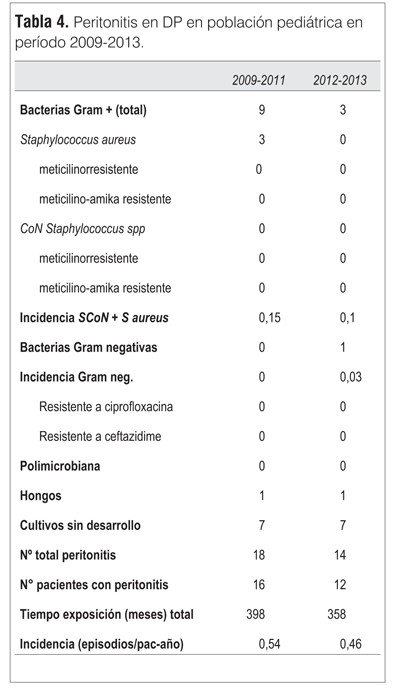
En el período 2009-2013 se registraron también las peritonitis en la población menor de 18 años en DP (tabla 4). Se observaron 34 episodios en 28 niños, de los 79 pacientes en DP en Uruguay en el período (edad entre 2 y 17 años). El tiempo de exposición total fue de 756 meses, por lo que la incidencia fue de un episodio cada 22 meses-paciente (o 0,5 episodios/paciente-año) Los gérmenes más frecuentes identificados fueron grampositivos (incidencia 0,19 episodio/paciente-año), pero en 14 episodios no se identificó germen, probablemente vinculado a los bajos volúmenes de líquido peritoneal utilizados (acorde al peso de los pacientes). Ningún paciente falleció como consecuencia de una peritonitis en el período.
F. Factores de riesgo de adquisición y evolutivos
En los episodios del año 2013 se analizaron factores de riesgo: edad, sexo, diabetes, tiempo en DP, estación del año del episodio y si en el centro se realizaban controles periódicos y tratamiento del estado de portador nasal de S. aureus. Se registraron 74 episodios (un episodio fue una recaída de un episodio previo) en 66 pacientes, 23 hombres y 43 mujeres (65% mujeres) con edad media de 55,9 ± 17,5 años (entre 19 y 85 años) y un tiempo en DP al episodio de 31,7 ± 28 meses (1-120 meses). Comparado con la población global en DP, según datos del Registro Uruguayo de Diálisis (RUD) 2013: edad media 51,5 ± 20,3 años, 55% mujeres), quienes presentaron peritonitis tenían una edad superior (edad con peritonitis: 55,9 ± 17,5 años vs edad de pacientes que no cursaron peritonitis: 51,2 ± 19,8 años [test de t NS], y mayor predominio femenino [chi2 NS]), pero estas diferencias no fueron estadísticamente significativas. La incidencia de peritonitis fue de 0,37 episodios/paciente-año (un episodio cada 32 meses-paciente). En los meses de primavera-verano (2013) se registraron 34 episodios y 40 en otoño-invierno. No se observaron episodios vinculados a infección del orificio de salida o del túnel subcutáneo del catéter peritoneal. La condición de diabetes no aumentó el riesgo de adquisición de peritonitis: la incidencia en diabéticos fue de 0,34 peritonitis/paciente-año (20 episodios en 709 meses de exposición) y en los no diabéticos de 0,38 peritonitis/paciente-año (52 episodios en 1.641 meses de exposición) (test de Poisson NS).
Se observó una incidencia significativamente mayor de peritonitis a S. aureus en los cuatro centros que por dificultades operativas no pudieron realizar los controles periódicos con exudado nasal, y, por ende, tampoco el tratamiento en caso de resultar positivo, como está recomendado en las guías internacionales. Se observaron 9 episodios en 1.271 meses vs 1 episodio en 1.127 meses de exposición (incidencia 0,08 vs 0,01 peritonitis a S. aureus / paciente-año) (test de Poisson, p < 0,05) (tabla 3).
En el año 2013 se correlacionó la evolución (curación o retiro catéter/fallecimiento) según edad al episodio (? 65 años), sexo, diabetes y germen causante (tabla 3). En el análisis univariado los gérmenes gramnegativos tuvieron una peor evolución (retiro de catéter peritoneal o fallecimiento (7/12 vs 2/27 Gram +), así como los hombres (17/20 vs 11/38 mujeres) (chi2 p<0,05), pero en el análisis multivariado solo el sexo masculino se correlacionó con peor evolución (retiro de catéter peritoneal o fallecimiento).
Discusión
La peritonitis continúa siendo un factor de riesgo de morbi y mortalidad a pesar de que ha disminuido su incidencia a nivel mundial, vinculado esto a la introducción de mejoras en la conexión-desconexión de las bolsas con las soluciones de diálisis peritoneal. El diagnóstico de peritonitis se basa en la presencia de al menos dos de tres criterios: síntomas y signos de inflamación abdominal, líquido peritoneal turbio (con recuento leucocitario en líquido peritoneal mayor a 100 células/?L, 50% polimorfonucleares, luego de una permanencia mínima de dos horas) y cultivo con desarrollo bacteriano(4-6).
Dado que los pacientes con enfermedad renal crónica (ERC) son inmunodeprimidos, es importante un alto grado de sospecha y un adecuado entrenamiento a los pacientes, para que la consulta y el tratamiento empírico sean precoces(10-12).
La incidencia de peritonitis observada en nuestro país se encuentra en un nivel aceptable comparada con reportes internacionales(10), pues se consideraba que 0,67 episodio/paciente-año era tolerable; sin embargo, numerosos centros reportan incidencias de 0,36 episodios/paciente-año y algunos aún menores: 0,06-0,24 episodios/paciente-año(6).
Una técnica de cultivo de líquido peritoneal correcta es fundamental, dado que frecuentemente existe un bajo número de gérmenes en la muestra obtenida, lo que puede dificultar el hallazgo del mismo. La identificación del germen causal y su sensibilidad antibiótica no solo serán una guía del tratamiento, sino que también pueden orientar hacia la causa o foco de origen(8). En Uruguay se realizaron jornadas de consenso entre bacteriólogos y nefrólogos con el fin de homogeneizar y optimizar los métodos utilizados en la práctica clínica en 2004 y 2013, que incluyeron desde las condiciones de recolección y transporte de la muestra hasta los métodos de cultivo e identificación. El envío de la bolsa de DP y no únicamente una pequeña muestra del líquido permite sembrar mayores volúmenes y efectuar procedimientos de enriquecimiento y concentración de la muestra, lo que contribuye a aumentar las probabilidades de aislar el agente etiológico.
A pesar de estos esfuerzos aún es elevado el número de cultivos sin desarrollo (tabla 1), por lo que a nivel nacional no se alcanzan las metas establecidas, por ejemplo, por el Grupo de la Sociedad Española de Nefrología(13), que ha fijado en menos de 20% el máximo aceptable de episodios sin identificación de germen causal.
Incidencia según gérmenes y período. Existe consenso en que el tratamiento de las peritonitis en DP se debe iniciar en forma empírica, inmediatamente luego de obtenida la muestra de líquido peritoneal (LP) para cultivo(4-6). El protocolo propuesto, como ya fue mencionado, ha variado a lo largo de los años y desde 2006 la International Society of Peritoneal Dialysis (ISPD) propone que debe estar guiado por los gérmenes incidentes en cada lugar y la sensibilidad de los mismos. El Registro Uruguayo de Peritonitis en DP se inició con el objetivo de disponer de evidencia nacional para decidir el protocolo de tratamiento antibiótico empírico inicial. El protocolo propuesto a partir de los datos de 2004-2005 consiste en la administración intraperitoneal, en las dosis recomendadas en las guías(6), de vancomicina y amikacina. Esta elección se basó en la incidencia observada en dichos años de bacterias Gram positivas(9), con un elevado porcentaje de meticilinorresistencia, lo que limita el uso de cefalosporinas como tratamiento inicial (tabla 1). Si bien la incidencia de Gram positivos ha disminuido (figura 2), persiste elevado el porcentaje de meticilinorresistencia, por lo que se decidió mantener vancomicina en el protocolo empírico inicial. El descenso en la frecuencia de SCoN y S. aureus se vincula en general a una mejor técnica de conexión del sistema de DP realizado por los pacientes en sus domicilios, por lo que su descenso en los últimos cinco años probablemente sea consecuencia de mejoras en el entrenamiento/educación terapéutica(14). Los reportes internacionales coinciden en señalar una tendencia similar de disminución de la incidencia de bacterias Gram positivas, vinculado a una mejora en la conectología de los sistemas de DP y otras medidas preventivas(6,10). Se ha descrito resistencia intermedia a vancomicina, por lo cual es imperativo el control de los niveles plasmáticos alcanzados durante el tratamiento(12) para evitar niveles plasmáticos subóptimos que comprometan la evolución.
En este estudio se observa un aumento relativo de la incidencia de bacterias gramnegativas, si bien no significativo, por lo que se ha acordado implementar medidas de prevención, por ejemplo en situaciones de alteraciones del tránsito intestinal o estudios endoscópicos abdominales de acuerdo a las recomendaciones internacionales(15,16). La resistencia antibiótica observada entre los gérmenes gramnegativos ha sido menor (tabla 1), aunque no disponemos del análisis completo de la sensibilidad antibiótica, que fue menos frecuentemente informada que la de los estafilococos. A nivel internacional la incidencia de peritonitis causadas por bacterias gramnegativas se mantiene estable, con una incidencia aproximada de 0,16 episodios/paciente-año(10).
Factores de riesgo de adquirir peritonitis
La prevención de infecciones en DP es fundamental para el éxito de todos los programas. La incidencia tiene una amplia variación a nivel mundial, e incluso en un mismo país en los diferentes centros. La ISPD ha publicado recientemente Recomendaciones para la prevención(6). La mejoría de la conectología disponible a nivel mundial y nacional sería la principal explicación del descenso de incidencias de peritonitis que eran muy altas al inicio de la DP, cuando se usaba el sistema con espiga, a los niveles actuales. En nuestro país, en la experiencia piloto inicial en 1985 la incidencia alcanzó a 1,5 episodio/paciente-año, 2,6 veces más frecuente en diabéticos, probablemente porque se administraba insulina en las bolsas, práctica que se discontinuó luego del estudio referido(17). Piraino refiere que la prevención de la contaminación por S. aureus (con aplicación de mupirocina a nivel del sitio de salida del catéter peritoneal o nasal) reduce efectivamente la incidencia de peritonitis por este germen, que de otro forma sería la más frecuente y concluye que esta incidencia debería ser menor de 0,05 episodio/paciente-año. En nuestro medio encontramos que los centros que pudieron aplicar medidas de profilaxis en el año 2013 tuvieron una incidencia aun menor: 0,01 episodio/paciente-año. Este resultado estimula a solucionar los problemas a nivel nacional para extender esta práctica. Los pacientes diabéticos de nuestra población no tuvieron una incidencia mayor que los no diabéticos, acorde a lo reportado por Rodríguez-Carmona y colaboradores(18), quienes observaron mayor incidencia de infecciones del túnel y orificio de salida del catéter, pero no de peritonitis en relación con el control glucídico. Se ha reportado una variación estacional de las peritonitis, pero no todos los datos reportados son concordantes. Así, en Hong Kong, la incidencia aumenta durante los meses de mayor calor y humedad tanto para gérmenes grampositivos como negativos(19), similar a lo reportado en Brasil, pero diferente de los hallazgos en Norteamérica(19-21). Cho(22), en Australia, no encuentra diferencias estacionales en la incidencia global de peritonitis, aunque sí variaciones según el germen, por ejemplo los estafilococos coagulasa-negativos son más frecuentes en primavera-verano. En nuestro país, en el año 2013, observamos más episodios en los seis meses de otoño-invierno (40 episodios) que en primavera-verano (34 episodios) (tabla 3), pero los datos disponibles en el registro no nos permiten un análisis estadístico preciso de este aspecto.
Evolución
A nivel internacional el principal interés en la última década se ha enfocado en mejorar la evolución de las peritonitis, dado que en los principales centros la incidencia ya ha disminuido significativamente(23). El principal factor de mal pronóstico evolutivo han sido el germen (peor con gramnegativos, Mycobacterium sp, micosis o flora polimicrobiana, así como la asociación con tunelitis, bajo filtrado glomerular residual o persistencia de altos recuentos celulares peritoneales). Los hallazgos del presente estudio confirman el impacto negativo en el pronóstico de la presencia de gérmenes gramnegativos (tabla 2), a pesar de que la resistencia de gérmenes a la amikacina (usada en el protocolo empírico inicial) fue muy baja (2%). En el presente trabajo se observa que entre los gramnegativos fue más frecuente la cura con cambio antibiótico (tabla 2), lo que se explica porque de acuerdo a las pautas terapéuticas, cuando se confirma la presencia de un germen gramnegativo se suspende la vancomicina y se asocia a amikacina, otro antibiótico de acuerdo a la sensibilidad in vitro. Szeto y colaboradores(24) consideran que las peritonitis a gramnegativos son el talón de Aquiles de la DP, porque la resistencia antibiótica es frecuente y la respuesta al tratamiento es a menudo pobre. Los gérmenes gramnegativos más frecuentes reportados son Pseudomonas spp, Escherichia coli y Klebsiella. Pseudomonas spp se observa, en ocasiones, concomitante con infección de túnel u orificio de salida del catéter peritoneal. En particular, en un estudio australiano(25), la presencia de Pseudomonas se asocia a una mayor tasa de retiro de catéter peritoneal o transferencia definitiva a hemodiálisis, aunque con igual tasa de fallecimiento (3%), y encuentran mejor evolución cuando se asociaron dos antibióticos efectivos contra ese microorganismo(25). Escherichia coli y Klebsiella (integrantes de la familia de las enterobacterias) se observan con mayor frecuencia luego de tratamiento antibiótico prolongado(26), tienen peor evolución y requieren tratamiento con dos antibióticos, y si bien luego de resuelto el episodio es posible la colocación de un nuevo catéter peritoneal, es frecuente encontrar deterioro de la membrana peritoneal, con menor aclaramiento de solutos o pérdida de la capacidad de ultrafiltración. En un estudio español se observa(27) que las peritonitis a gramnegativos son un desafío, y se pronostica un aumento de la resistencia antibiótica en los próximos años. En un estudio brasileño(16) estudiaron la evolución de la sensibilidad antibiótica de gramnegativos aislados de peritonitis y observaron que entre los bacilos gramnegativos no fermentadores en los últimos años ha aumentado la resistencia a ceftazidime, en tanto que el perfil de la sensibilidad se mantiene estable entre las enterobacterias. La presencia de micobacterias es poco frecuente, y en el presente estudio, en los diez años, solo se observó un episodio causado por M tuberculosis, que determinó el retiro del catéter peritoneal y el tratamiento antibiótico correspondiente.
El impacto de la edad es discutido y algunos estudios muestran que los pacientes añosos tuvieron mayor mortalidad vinculada a la peritonitis(23,27), pero no todos coinciden en esta observación. En el presente estudio no se observó correlación entre edad mayor de 65 años y mala evolución, ni diferencia en la media de edad de la población con y sin peritonitis.
La mortalidad de los episodios de peritonitis es baja en sí misma, oscila en diferentes publicaciones entre 2% y 4%(25,27,28) y en el presente trabajo se encuentra en 4,7%. Muñoz y colaboradores destacan en el estudio multicéntrico español(27) que cada episodio de peritonitis se correlaciona con una menor supervivencia a largo plazo, y este riesgo varía según el germen de cada episodio: mayor para hongos, bacterias gramnegativas y menor para grampositivas. En el análisis univariado en este estudio encontramos una significativa peor evolución (retiro de catéter peritoneal o fallecimiento) en las peritonitis a gramnegativos, en relación con la observada en los episodios por grampositivos. Asimismo, la evolución fue peor en los hombres, pero no así en los añosos (tabla 2), pero en el análisis multivariado solo el sexo masculino se correlacionó con peor evolución. Tsai y colaboradores(29) observaron que los pacientes añosos tenían una peor evolución, así como los diabéticos. Respecto al sexo no hemos encontrado reportes con hallazgos similares a los del presente estudio, por ejemplo Kumar y colaboradores(30) encuentran mayor riesgo de adquisición de peritonitis entre las mujeres, pero no señalan diferencias en la evolución.
Población pediátrica
La incidencia global de peritonitis en los menores de 18 años en el país ha descendido progresivamente desde 2009 a 2013 (tabla 4). Según lo reportado en la literatura(31), la incidencia objetivo en niños sería de un episodio cada 18-20 meses-paciente. No se observaron gérmenes resistentes y la baja tasa de aislamiento de germen probablemente se vincule a los bajos volúmenes utilizados en esta población, acorde al peso del paciente. Se destaca la mejor evolución de los episodios en esta franja etaria, ya que ningún niño falleció por peritonitis en el período de estudio.
Conclusiones
1. La incidencia de peritonitis a S. aureus fue significativamente mayor cuando no fue posible controlar ni tratar el estado de portador nasal, lo que justifica implementar medidas preventivas nacionales.
2. La incidencia de peritonitis causadas por S. aureus y SCoN meticilinorresistentes, la incidencia sostenida de gramnegativos (con peor evolución) y el elevado porcentaje de cultivos sin desarrollo justifica mantener igual protocolo antibiótico empírico inicial, con vancomicina y amikacina.
3. El descenso significativo de la incidencia de S. aureus y SCoN en los diez años estudiados traduciría una mejora en la educación y en el entrenamiento de los pacientes en DP a nivel nacional.
Abstract
Peritonitis is a severe complication of peritoneal dialysis (PD), so it is important to learn about the incidence and antibiotic sensitivity of the germs that cause it. In Uruguay, since January 1, 2004, a national record is kept for peritonitis in PD, germs, sensitivity and evolution.
Method: the records from January 1, 2004 through December 31, 2013 were analyzed. The registry was approved by institutional ethical committes.
Results: during the above mentioned period, 850 cases of peritonitis were recorded, and incidence dropped from 0.49/patient-year (2004-2005) to 0.37/patient-year (2013). Incidence of Staphylococcus aureus and coagulase-negative staphylococci (SCoN) was lower in 2009-2013 vs 2004-2005 (0.2 vs 0.12 peritonitis/patient-year, test Poisson p<0.05). In 2009-2013: 14/54 S. aureus and 26/71 SCoN were methicillin-resistant, similar to the previous period. 98% of Gram-negative were sensitive to amikacin. No germ was identified in 145/467 (31%) of episodes. Primary cure was achieved in 71% of peritonitis for Gram-positive and 45% for Gram-negative bacteria (chi2 p<0.05). In 2013 a greater incidence of peritonitis was observed in those centers where the nasal carriage was not controlled.
Comments and conclusions: controlling Staphylococcus aureus nasal carriages is worth doing. The incidence of peritonitis by methicillin-resistant S. aureus y SCoN, the sustained incidence of Gram-negative germs (with a worse evolution), and the high percentage of cultures with no development justify keeping the initial empirical antibiotic protocol with vancomycin and amikacin. Reduction in the incidence of S. aureus + SCoN could be explained by a greater education in PD patients.
Resumo
A peritonite é uma complicação grave da diálise peritoneal (DP), sendo, portanto, importante conhecer a incidência e a sensibilidade antibiótica dos gérmens causadores. No Uruguai, desde 1 de janeiro de 2004, realiza-se um registro nacional das peritonites em DP, com dados sobre gérmens, sensibilidade e evolução.
Método: foram analisados os registros do período 1 de janeiro de 2004 - 31 de dezembro de 2013. O registro foi aprovado pelos comitês de ética das instituições envolvidas.
Resultados: foram registradas 850 peritonites no período estudado; a incidência diminuiu de 0,49/paciente-ano no período 2004-2005 a 0,37/paciente-ano em 2013. A incidência de Staphylococcus aureus e Staphylococcus coagulase negativo (SCoN) foi menor no período 2009-2013 comparada com 2004-2005 (0,2 vs 0,12 peritonite/paciente-ano, teste de Poisson p<0,05). No período 2009-2013: 14/54 S. aureus e 26/71 SCoN foram resistentes à meticilina, similar ao período prévio. 98% dos gérmens gramnegativos eram sensíveis a amicacina. Não se pode identificar o gérmen em 145/467 (31%) episódios. Em 71% das peritonites por grampositivos e em 5% por gramnegativos (chi2 p<0,05) foi possível obter cura primária. Em 2013 foi observada uma maior incidência de peritonite nos centros em que não se realizava controle de portador nasal.
Comentários e conclusões: justifica-se a realização de controle de portador de Staphylococcus aureus. A incidência de peritonite por S. aureus e SCoN resistentes à meticilina, a incidência constante de gérmens gramnegativos (com pior evolução), e a alta porcentagem de cultivos sem crescimento justificam manter o protocolo antibiótico empírico inicial com vancomicina e amicacina. A redução da incidência de S. aureus + SCoN poderia ser atribuída a melhor educação dos pacientes em DP.
Bibliografía
1. Bender FH, Bernardini J, Piraino B. Prevention of infectious complications in peritoneal dialysis: best demonstrated practices. Kidney Int Suppl 2006; (103):S44-54.
2. Ballerini L, Paris V. Nosogogy: when the learner is a patient with chronic renal failure. Kidney Int Suppl 2006; (103):S122-6.
3. Hsieh YP, Wang SC, Chang CC, Wen YK, Chiu PF, Yang Y. The negative impact of early peritonitis on continuous ambulatory peritoneal dialysis patients. Perit Dial Int 2014; 34(6):627-35.
4. Montenegro J, Correa-Rotter R, Riella M. Tratado de diálisis peritoneal. 2 ed. Barcelona: Elsevier, 2009.
5. Piraino B, Bailie GR, Bernardini J, Boeschoten E, Gupta A, Holmes C, et al; ISPD Ad Hoc Advisory Committee. Peritoneal dialysis-related infections recommendations: 2005 update. Perit Dial Int 2005; 25(2):107-31.
6. Piraino B, Bernardini J, Brown E, Figueiredo A, Johnson DW, Lye WC, et al. ISPD position statement on reducing the risks of peritoneal dialysis-related infections. Perit Dial Int 2011; 31(6):614-30.
7. Barretti P, Doles JV, Pinotti DG, El Dib R. Efficacy of antibiotic therapy for peritoneal dialysis-associated peritonitis: a proportional meta-analysis. BMC Infect Dis 2014; 14:445.
8. Akoh JA. Peritoneal dialysis associated infections: An update on diagnosis and management. World J Nephrol 2012; 1(4):106-22.
9. Gadola L, Orihuela L, Pérez D, Gómez T, Solá L, Chifflet L, et al. Peritonitis in peritoneal dialysis patients in Uruguay. Perit Dial Int 2008; 28(3):232-5.
10. Li PK, Chow KM. Infectious complications in dialysis: epidemiology and outcomes. Nat Rev Nephrol 2011; 8(2):77-88.
11. Ballinger AE, Palmer SC, Wiggins KJ, Craig JC, Johnson DW, Cross NB, et al. Treatment for peritoneal dialysis-associated peritonitis. Cochrane Database Syst Rev 2014; (4):CD005284.
12. Cho Y, Johnson DW. Peritoneal dialysis-related peritonitis: towards improving evidence, practices, and outcomes. Am J Kidney Dis 2014; 64(2):278-89.
13. Bajo Rubio MA, Selgas R, Remón C, Arrieta J, Álvarez-Ude F, Arenas MD, et al. Plan de calidad científico-técnica y de mejora continua de la calidad en diálisis peritoneal. Nefrología (Madr.) 2010; 30(1):28-45.
14. Gadola L, Poggi C, Poggio M, Sáez L, Ferrari A, Romero J, et al. Using a multidisciplinary training program to reduce peritonitis in peritoneal dialysis patients. Perit Dial Int 2013; 33(1):38-45.
15. Yip T, Tse KC, Lam MF, Cheng SW, Lui SL, Tang S, et al. Risks and outcomes of peritonitis after flexible colonoscopy in CAPD patients. Perit Dial Int 2007; 27(5):560-4.
16. Barretti P, Pereira D, Brasil MA, de Lourdes Cunha M, Caramori J, Montelli A. Evolution of gram-negative bacilli susceptibility in peritoneal dialysis-related peritonitis in Brazil: a single center’s experience over nine years. Perit Dial Int 2009; 29(2):230-3.
17. Gadola L, Schwedt E, Díaz A, Sola L, Falchi B, Verdaguer C, et al. Informe del Programa de Diálisis Peritoneal Continua Ambulatoria (Uruguay). En: I Congresso Latino Americano de Diálise Peritoneal. Florianópolis, 21-23 de outubro de 1988.
18. Rodríguez-Carmona A, Pérez-Fontán M, López-Muñiz A, Ferreiro-Hermida T, García-Falcón T. Correlation between glycemic control and the incidence of peritoneal and catheter tunnel and exit-site infections in diabetic patients undergoing peritoneal dialysis. Perit Dial Int 2014; 34(6):618-26.
19. Szeto CC, Chow KM, Wong TY, Leung CB, Li PK. Influence of climate on the incidence of peritoneal dialysis-related peritonitis. Perit Dial Int 2003; 23(6):580-6.
20. Stinghen AE, Barretti P, Pecoits-Filho R. Factors contributing to the differences in peritonitis rates between centers and regions. Perit Dial Int 2007; 27(Suppl 2):S281-5.
21. Núñez-Moral M, Sánchez-Álvarez JE, González-Díaz I, Peláez-Requejo B, Quintana-Fernández A, Rodríguez-Suárez C. Seasonal variations and influence of the weather on the appearance of peritoneal infection. Nefrología 2014; 34(6):743-8.
22. Cho Y, Badve SV, Hawley CM, McDonald SP, Brown FG, Boudville N, et al. Seasonal variation in peritoneal dialysis-associated peritonitis: a multi-centre registry study. Nephrol Dial Transplant 2012; 27(5):2028-36.
23. van Esch S, Krediet R, Struijk DG. Prognostic factors for peritonitis outcome. En: Ronco C, Rosner MH, Crepaldi C, eds. Peritoneal dialysis: state of the art 2012. Basel: Karger 2012. v.178:264-70.
24. Szeto CC, Chow KM. Gram-negative peritonitis—the Achilles heel of peritoneal dialysis? Perit Dial Int 2007; 27(Suppl 2):S267-71.
25. Siva B, Hawley CM, McDonald SP, Brown FG, Rosman JB, Wiggins KJ, et al. Pseudomonas peritonitis in Australia: predictors, treatment, and outcomes in 191 cases. Clin J Am Soc Nephrol 2009; 4(5):957-64.
26. Szeto CC, Chow VC, Chow KM, Lai RW, Chung KY, Leung CB, et al. Enterobacteriaceae peritonitis complicating peritoneal dialysis: a review of 210 consecutive cases. Kidney Int 2006; 69(7):1245-52.
27. Muñoz de Bustillo E, Borrás F, Gómez-Roldán C, Pérez-Contreras FJ, Olivares J, García R, et al. Impacto de las peritonitis en la supervivencia a largo plazo de los pacientes en diálisis peritoneal. Nefrología (Madr.) 2011; 31(6):723-32.
28. de Moraes TP, Olandoski M, Caramori JC, Martin LC, Fernandes N, Divino-Filho JC, et al. Novel predictors of peritonitis-related outcomes in the BRAZPD cohort. Perit Dial Int 2014; 34(2):179-87.
29. Tsai CC, Lee JJ, Liu TP, Ko WC, Wu CJ, Pan CF, et al. Effects of age and diabetes mellitus on clinical outcomes in patients with peritoneal dialysis-related peritonitis. Surg Infect (Larchmt) 2013; 14(6):540-6.
30. Kumar VA, Sidell MA, Yang WT, Jones JP. Predictors of peritonitis, hospital days, and technique survival for peritoneal dialysis patients in a managed care setting. Perit Dial Int 2014; 34(2):171-8.
31. Feneberg R, Warady BA, Alexander SR, Schaefer F; International Pediatric Peritonitis Registry. The international pediatric peritonitis registry: a global Internet-based initiative in pediatric dialysis. Perit Dial Int 2005; 25(Suppl 3):S130-4.














