Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Médica del Uruguay
versión On-line ISSN 1688-0390
Rev. Méd. Urug. vol.31 no.1 Montevideo mar. 2015
Linfoma cutáneo primario difuso de células B grandes tipo pierna: primer reporte de presentación como úlcera de Marjolin sobre úlcera venosa crónica
Cristian Morales*, Sandra Damiano†, Diego Bertini‡, Daniela De Boni§
Resumen
El linfoma cutáneo primario difuso de células B grandes tipo pierna (LCPDCBG-TP) constituye el 4% de los linfomas cutáneos primarios (LCP). Presenta un comportamiento agresivo con sobrevida a los cinco años cercana a 55%. La úlcera de Marjolin corresponde al desarrollo de una neoplasia sobre lesiones crónicas, siendo el carcinoma espinocelular el más frecuentemente desarrollado. Presentamos el caso de un paciente de sexo masculino, de 74 años, con insuficiencia venosa crónica bilateral, portador de una úlcera crónica de 15 años de evolución en pierna derecha. Desde hace tres años presenta dos lesiones tumorales exofíticas sobre el fondo de la úlcera, con acelerada progresión en últimos meses, planteándose el diagnóstico de úlcera de Marjolin. La histopatología mostró una proliferación celular atípica difusa de tejido linfoide de tipo blástico. En el análisis inmunohistoquímico se evidenció CD20+, CD10-, MUM1+, Bcl-2+, Bcl-6-, Ki67 90%. Los estudios fueron compatibles con el diagnóstico de LCPDCBG-TP. La valoración imagenológica no evidencia adenopatías profundas, ni visceromegalia. La biopsia de médula ósea no pudo ser completada por dificultades producidas por obesidad e intolerancia al dolor del paciente. Se realizó radioterapia local con una dosis total de 54 Gy, presentando excelente evolución con desaparición de las lesiones tumorales. Las opciones terapéuticas de primera línea para el LCPDCBG-TP son la quimioterapia CHOP asociada a rituximab, con o sin radioterapia agregada. Si el estado del paciente no permite un tratamiento agresivo, se considera realizar monoterapia con rituximab o radioterapia. El presente trabajo corresponde al segundo caso reportado en la literatura a nivel mundial de un LCP que surge como úlcera de Marjolin sobre el lecho de una úlcera venosa crónica, y al primero del subtipo LCPDCBG-TP.
Palabras clave: LINFOMA CARCINOMA DE CÉLULAS ESCAMOSAS ÚLCERA VARICOSA
Key words: LYMPHOMA CARCINOMA, SQUAMOUS CELL VARICOSE ULCER
* Posgrado de Cátedra de Dermatología Prof. Dr. Miguel Martínez. Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
† Hematóloga. Instituto Nacional del Cáncer. Uruguay.
‡ Oncólogo Radioterapeuta. Instituto Nacional del Cáncer. Asistente de Cátedra de Oncología Radioterápica Prof. Dr. Pedro Kasdorf. Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
§ Dermatóloga. Instituto Nacional del Cáncer. Profesora Adjunta de la Cátedra de Dermatología Prof. Dr. Miguel Martínez. Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
Correspondencia: Dr. Cristian Morales. Correo electrónico: cmovar@gmail.com
Recibido: 22/12/14 Aceptado: 9/2/15
Introducción
Los linfomas cutáneos primarios (LCP) son linfoproliferaciones malignas originadas en la piel y que al momento del diagnóstico no presentan evidencia de enfermedad sistémica extracutánea(1). Después del tracto gastrointestinal, la piel es el sitio más frecuente de localización extranodal de linfoma no Hodgkin(1,2). Los LCP de células T (LCPCT) y de células B (LCPCB) tienen a menudo un comportamiento y pronóstico muy diferentes a los linfomas sistémicos con histopatología similar, requiriendo también tratamientos diferentes(1,3).
La incidencia total de los LCP en países occidentales se estima en 0,5-1 caso por 100.000 personas al año(1,2,4). El 23% a 29% de los LCP corresponden a LCPCB, dentro de los cuales el más frecuente es el linfoma cutáneo primario de células B centrofolicular (LCPCBCF)(1,3,5). El linfoma cutáneo primario difuso de células B grandes tipo pierna (LCPDCBG-TP) constituye cerca de 4% de los LCP, correspondiendo a 20% del total de los LCPCB(1). El LCPDCBG-TP es una malignidad de comportamiento intermedio, con peor pronóstico comparado con los otros LCPCB, con una sobrevida a los cinco años en torno a 55%(1,3,6). Las opciones terapéuticas incluyen la quimioterapia CHOP (ciclofosfamida, doxorrubicina, vincristina y prednisona), radioterapia de campo afectado, rituximab, y asociaciones entre estas alternativas(1,7,8).
La úlcera de Marjolin corresponde al desarrollo de una neoplasia maligna sobre áreas que reflejan condiciones de irritación crónica, más frecuentemente en cicatrices de quemadura(9-12). El tumor que más frecuentemente se desarrolla es el carcinoma espinocelular, seguido del carcinoma basocelular(10,11). La aparición de un LCP como úlcera de Marjolin sobre el lecho de una úlcera venosa crónica es extremadamente infrecuente, existiendo a la fecha solo un reporte en la literatura de un LCP de células B grandes CD20 negativo, siendo el presente caso el primero del subtipo LCPDCBG-TP(13).
Caso clínico
Paciente de sexo masculino, de 74 años, portador de insuficiencia venosa crónica bilateral de larga data, el cual presenta una gran úlcera crónica de 15 años de evolución en mitad inferior de pierna derecha abarcando casi por completo toda su circunferencia. Desde hace tres años presenta dos lesiones tumorales exofíticas que asientan sobre el fondo de la úlcera, la mayor de 2,5 cm de diámetro, de lento crecimiento al inicio, pero con aumento de su velocidad de progresión en los últimos meses (figura 1).
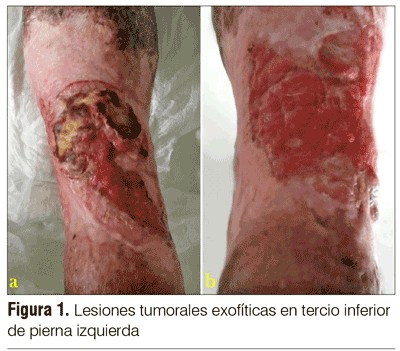
Tanto la piel circundante a la lesión, como la del miembro inferior contralateral, muestran signos de importante lipodermatoesclerosis. No se palpan linfadenopatías en territorios superficiales, los pulsos arteriales se encuentran presentes. Destacamos que el paciente se encuentra en buen estado general y en apirexia. Se plantea el diagnóstico de úlcera de Marjolin.
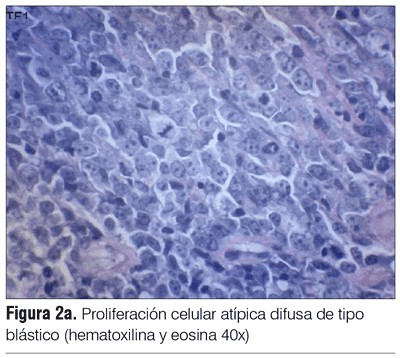
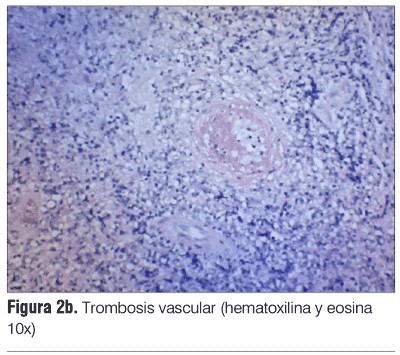
El estudio histopatológico de la lesión muestra proliferación celular atípica difusa de tejido linfoide de tipo blástico asociado a una marcada trombosis vascular (figura 2 a) y 2 b).
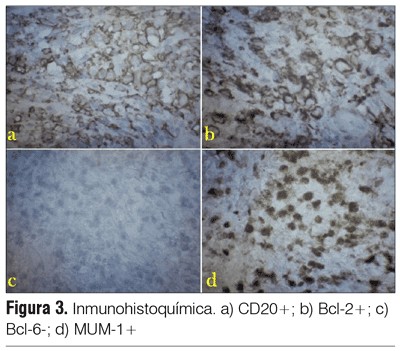
El análisis inmunohistoquímico mostró las siguientes características: CD20+, CD3-, CD10 no concluyente, CD30-, MUM1+, Bcl-2+, Bcl-6-, Ki67 90% (figura 3).El panel inmunohistoquímico, en conjunto con el estudio anatomopatológico, resultaron compatibles con el diagnóstico de LCPDCBG-TP. Se realizaron tomas biópsicas múltiples con el objetivo de mapear la úlcera y poder identificar los sectores correspondientes al linfoma, confirmando que los únicos sectores comprometidos eran las lesiones tumorales descritas. Los estudios de hemograma, LDH y proteinoelectroforesis no mostraron alteraciones, mientras que la proteína C reactiva resultó elevada (43 mg/L). La tomografía computada de cuello, abdomen y pelvis evidenció ausencia de adenopatías profundas, sin hepatomegalia ni esplenomegalia.
Se indica biopsia de médula ósea, sin embargo el procedimiento no se pudo completar debido a dificultades producidas por la obesidad del paciente y una marcada intolerancia al dolor, lo que motivó la negativa final del paciente.
Se realiza tratamiento con radioterapia local externa con haz de fotones de 6 Mv, por campos opuestos tangentes a la lesión inicial, con bloqueo de zona central ósea, utilizando bolus a una dosis/fracción de 1,8 Gy, a razón de una fracción/día, cinco fracciones por semana. Al completar 37,8 Gy se reevalúa clínicamente, persistiendo dos lesiones remanentes de menor tamaño. Se realiza terapia con haz de electrones de 6 MeV con igual esquema de fraccionamiento, adicionando 10,8 Gy a la dosis inicial. A la evaluación clínica posterior persiste sólo una lesión de menor tamaño en la cara anterior de la pierna, a la cual se agregaron tres fracciones de 1,8 Gy, completando una dosis total de 54 Gy. Se realizan controles semanales intratratamiento, constatándose una excelente tolerancia clínica.
Se decide no asociar a poliquimioterapia debido a que las lesiones se presentaban de forma localizada y a la ausencia de síntomas B, sumándose a esto elementos asociados a menor tolerancia como la edad avanzada y obesidad del paciente, y a que este provenía de un medio rural que dificultaba su seguimiento. El paciente presentó excelente evolución posradioterapia, con desaparición de las lesiones tumorales, comenzándose posteriormente un adecuado tratamiento de su úlcera e insuficiencia venosa, con elastocompresión y sulfadiazina de plata tópica, evidenciándose disminución de la superficie ulcerada (figura 4).
A los seis meses de realizada la radioterapia no se observó recidiva local ni evidencia de compromiso sistémico.Discusión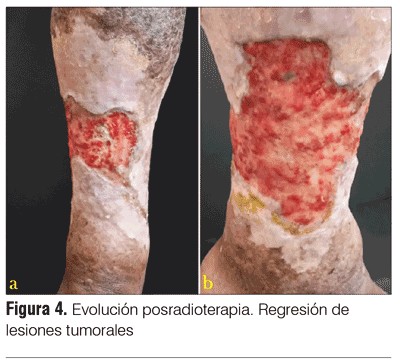
La úlcera de Marjolin es un término que se refiere al desarrollo de una neoplasia maligna sobre cicatrices de quemaduras u otras condiciones que reflejan irritación crónica, como úlceras venosas y por presión, fístulas, áreas de injerto, áreas irradiadas, hidrosadenitis supurativa, entre otras(9-12). El período de latencia entre el inicio de la injuria y el desarrollo del tumor es variable, y se ha propuesto diferenciar una forma aguda cuando la transformación maligna se desarrolla dentro del primer año luego de producida la injuria con un tiempo mínimo de latencia de un mes, y una forma crónica que se produciría después de ese período, más frecuente entre los 20 y 50 años posterior al inicio de la injuria(9-12). El tumor más frecuente desarrollado es el carcinoma espinocelular, seguido del carcinoma basocelular y menos frecuentemente, melanoma y tumores mesenquimales(9-11).
El LCPDCBG-TP es un LCP de células B de pronóstico intermedio, según la clasificación de consenso de la OMS-EORTC(1). Su etiología es desconocida y corresponde a una proliferación clonal de linfocitos B que forman un infiltrado celular denso formado predominantemente por centroblastos e inmunoblastos(1,3). La edad promedio de presentación se encuentra en la séptima década de la vida y es más frecuente en mujeres que en hombres, con una razón 3-4:1(14,15). Clínicamente se presenta generalmente como placas infiltradas y tumores eritematosos o azul rojizo, únicos o múltiples, aunque se han descrito formas inusuales(1,3,16). Generalmente se encuentra localizado en miembro inferior, predominantemente por debajo de las rodillas, pero en un 10%-15% de casos se pueden presentar en otras topografías, como tronco o cabeza(1,3,14,17,18).
En el estudio histopatológico del LCPDCBG-TP se observa un infiltrado dérmico difuso de centroblastos e inmunoblastos en láminas monótonas o confluentes, sin epidermotropismo, presentando núcleos redondos, de más del doble de tamaño que un linfocito normal, con una cromatina abierta y nucléolos prominentes(1,6,17). Es frecuente la presencia de mitosis y existe un escaso número de linfocitos T reactivos, los que se limitan a áreas perivasculares(1,3,6). El inmunofenotipo de LCPDCBG- TP expresa CD20, CD79a, y fuertemente Bcl-2, también marca en la mayoría de los casos la proteína MUM1/IRF4, pudiendo expresar o no Bcl-6, mientras que CD10 es generalmente negativo(3,19-22). El LCPDCBG- TP presenta una fuerte y amplia expresión inmunoglobulina M citoplasmática, la que es negativa en el LCPCBCF(23,24).
El análisis por técnica de hibridación fluorescente in situ (FISH) de los cromosomas en interfase frecuentemente revela translocaciones de c-MYC, Bcl-6 y en los genes de inmunoglobulina H, a diferencia del LCPCBCF(25). Se han detectado deleciones en regiones de los genes CDKN2A y CDKN2B en cromosoma 9p21.3 en 67% de los pacientes con LCPDCBG-TP(26).
Actualmente se consideran como opciones terapéuticas de primera línea la quimioterapia CHOP asociada con rituximab, con o sin radioterapia de campo afectado agregada; sin embargo, este enfoque terapéutico está aún poco documentado(1,7,8). En casos en que el paciente presente un tumor localizado o su estado no permita un tratamiento agresivo se puede considerar monoterapias con rituximab o radioterapia(1,7,8).
En la valoración del compromiso sistémico se recomienda la realización de tomografía computada, en especial en pacientes con linfadenopatías palpables, hemograma en sangre periférica y proteinoelectroforesis. Debido al peor pronóstico del LCPDCBG-TP, se recomienda incluir la biopsia de médula ósea como parte de la evaluación inicial(3).
El LCPDCBG-TP tiene un pronóstico desfavorable, presentando mayor riesgo de diseminación extracutánea, una baja tasa de respuestas completas con alto número de recaídas y rápida progresión, con una sobrevida específica a los cinco años de 55%(1,3,6,7,15). Los principales factores que se asocian a mal pronóstico son la localización en las piernas, la presencia de lesiones múltiples con afectación bilateral y la presencia de deleción en locus CDKN2A en cromosoma 9p21.3(15,17,26,27).
Destacamos el interés del presente caso por tratarse del único reporte en la literatura a nivel mundial de un LCPDCBG-TP que se presenta como úlcera de Marjolin sobre el lecho de una úlcera venosa crónica.
Abstract
Primary Cutaneous Diffuse Large B-cell Lymphoma, Leg-type (CBCL-LT) accounts for 4% of the primary cutaneous lymphomas (PCL). It is characterized by being aggressive, with a five-year survival rate of around 55%. Marjolin’s ulcer is a malignant neoplasms arising in an area of chronic lesions, being squamous cell carcinoma the most frequent one.
The study presents the case of a 74 year old male patient who suffered from bilateral chronic venous insufficiency, carrier of a chronic ulcer with 15 years of evolution in his right leg. Since three years ago he presents two exophytic lesions on the ulcer’s bottom, with accelerated progression in the last months, Marjolin’s ulcer being the possible diagnosis.
Histopathology showed an diffuse proliferation of atypical lymphoid cells of blastic type lymphoid cells. Immunohistochemistry evidenced CD20+, CD10-, MUM1+, Bcl-2+, Bcl-6-, Ki67 90%. Studies were compatible with a diagnosis of primary cutaneous diffuse large B-cell Lymphoma, Leg-type. Imagenology assessment failed to evidence deep adenopahties or visceromegally. Bone marrow biopsy could not be completed due to difficulties resulting from the patient’s obesity and pain intolerance. Local radiation therapy was used with a total dose of 54Gy, evolution being excellent and tumor lesions disappeared. Chemotherapy associated to rituximab is the first line therapy for primary cutaneous diffuse large B-cell Lymphoma, leg-type, with or without radiation therapy.
If the patient’s condition is not compatible with aggressive treatment, then rituximab monotherapy or radiation therapy are considered. This study corresponds to the second case of primary cutaneous lymphoma reported in the global literature, that debuts as Marjolin´s ulcer on a chronic venous lesion, and the first one of the primary cutaneous diffuse large B-cell lymphoma, leg- type sub-type.
Resumo
O linfoma cutâneo primário difuso de células B grandes tipo perna (LCPDCBG-TP) corresponde ao 4% dos linfomas cutâneos primários (LCP). Apresenta comportamento agressivo com sobrevida de aproximadamente 55% aos cinco anos. A úlcera de Marjolin corresponde ao desenvolvimento de uma neoplasia sobre lesões crônicas, sendo o carcinoma espinocelular o mais frequente. Apresentamos o caso de um paciente de sexo masculino, de 74 anos, com insuficiência venosa crônica bilateral, portador de uma úlcera crônica de 15 anos de evolução na perna direita. Apresenta, desde três anos atrás, duas lesões tumorais exofíticas sobre o fundo da úlcera, com progressão acelerada nos últimos meses, quando se propôs o diagnóstico de úlcera de Marjolin. A histopatologia mostrou uma proliferação celular atípica difusa de tecido linfoide de tipo blástico. Nos exames imunohistoquímicos foram observados CD20+, CD10-, MUM1+, Bcl-2+, Bcl-6-, Ki67 90%. Os exames eram compatíveis com o diagnóstico de LCPDCBG- TP. A avaliação imagenológica não mostrou adenopatias profundas, nem visceromegalia. A biopsia de medula óssea não pode ser completada por dificuldades devidas a intolerância à dor e a obesidade do paciente. Foi realizado tratamento com radioterapia local com uma dose total de 54Gy, apresentando excelente evolução com desaparecimento das lesões tumorais. As opções terapêuticas de primeira línea para o LCPDCBG-TP são a quimioterapia CHOP associada à rituximab, com ou sem radioterapia. Se o estado do paciente não permite tratamento agressivo, deve-se considerar monoterapia com rituximab ou radioterapia. Este trabalho corresponde ao segundo caso informado na literatura mundial de um LCP que surge como úlcera de Marjolin sobre o leito de uma úlcera venosa crônica, e o primeiro do subtipo LCPDCBG-TP.
Bibliografía
1. Willemze R, Jaffe ES, Burg G, Cerroni L, Berti E, Swerdlow SH, et al. WHO-EORTC classification for cutaneous lymphomas. Blood 2005; 105(10):3768-85.
2. Groves FD, Linet MS, Travis LB, Devesa SS. Cancer surveillance series: non-Hodgkin’s lymphoma incidence by histologic subtype in the United States from 1978 through 1995. J Natl Cancer Inst 2000; 92(15):1240-51.
3. Suárez AL, Pulitzer M, Horwitz S, Moskowitz A, Querfeld C, Myskowski PL. Primary cutaneous B-cell lymphomas: part I. Clinical features, diagnosis, and classification. J Am Acad Dermatol 2013 ;69(3):329.e1-13.
4. Dores GM, Anderson WF, Devesa SS. Cutaneous lymphomas reported to the National Cancer Institute’s surveillance, epidemiology, and end results program: applying the new WHO-European Organisation for Research and Treatment of Cancer classification system. J Clin Oncol 2005; 23(28): 7246-8.
5. Bradford PT, Devesa SS, Anderson WF, Toro JR. Cutaneous lymphoma incidence patterns in the United States: a population-based study of 3884 cases. Blood 2009; 113(21): 5064-73.
6. Vermeer MH, Geelen FA, van Haselen CW, van Voorst Vader PC, Geerts ML, Van Vloten WA, et al. Primary cutaneous large B-cell lymphomas of the legs: a distinct type of cutaneous B-cell lymphoma with an intermediate prognosis. Dutch Cutaneous Lymphoma Working Group. Arch Dermatol 1996; 132(11):1304-8.
7. Suárez AL, Querfeld C, Horwitz S, Pulitzer M, Moskowitz A, Myskowski PL. Primary cutaneous B-cell lymphomas: part II. Therapy and future directions. J Am Acad Dermatol. 2013; 69(3):343.e1-11.
8. Senff NJ, Noordijk EM, Kim YH, Bagot M, Berti E, Cerroni L, et al. European Organization for Research and Treatment of Cancer and International Society for Cutaneous Lymphoma consensus recommendations for the management of cutaneous B-cell lymphomas. Blood 2008; 112(5):1600-9.
9. Hahn SB, Kim DJ, Jeon CH. Clinical study of Marjolin’s ulcer. Yonsei Med J 1990; 31(3):234-41.
10. Smith J, Mello LF, Nogueira Neto NC, Meohas W, Pinto LW, Campos VA, et al. Malignancy in chronic ulcers and scars of the leg (Marjolin’s ulcer): a study of 21 patients. Skeletal Radiol 2001; 30(6):331-7.
11. Kowal-Vern A, Criswell BK. Burn scar neoplasms: a literature review and statistical analysis. Burns 2005; 31(4): 403-13.
12. Trent JT, Kirsner RS. Wounds and malignancy. Adv Skin Wound Care 2003; 16(1):31-4.
13. Cendras J, Sparsa A, Bedane C, Delage M, Touati M, Bonnetblanc JM. Primary cutaneous large B-cell lymphoma in chronic venous leg ulcer. Ann Dermatol Venereol 2007; 134(4 Pt 1):357-61.
14. Swerdlow SH, Campo E, Harris NL, Jaffe ES, Pileri SA, Stein H, et al, eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. 4 ed. Lyon: IARC Press, 2008.
15. Grange F, Beylot-Barry M, Courville P, Maubec E, Bagot M, Vergier B, et al. Primary cutaneous diffuse large B-cell lymphoma, leg type: clinicopathologic features and prognostic analysis in 60 cases. Arch Dermatol 2007; 143(9): 1144-50.
16. Kodama K, Massone C, Chott A, Metze D, Kerl H, Cerroni L. Primary cutaneous large B-cell lymphomas: clinicopathologic features, classification, and prognostic factors in a large series of patients. Blood 2005; 106(7):2491-7.
17. Grange F, Bekkenk MW, Wechsler J, Meijer CJ, Cerroni L, Bernengo M, et al. Prognostic factors in primary cutaneous large B-cell lymphomas: a European multicenter study. J Clin Oncol. 2001; 19(16):3602-10.
18. Thomas V, Dobson R, Mennel R. Primary cutaneous large B-cell lymphoma, leg type. Proc (Bayl Univ Med Cent) 2011; 24(4):350-3.
19. Geelen FA, Vermeer MH, Meijer CJ, Van der Putte SC, Kerkhof E, Kluin PM, et al. Bcl-2 expression in primary cutaneous large B-cell lymphoma is site-related. J Clin Oncol 1998; 16(6):2080-5.
20. Hoefnagel JJ, Dijkman R, Basso K, Jansen PM, Hallermann C, Willemze R, et al. Distinct types of primary cutaneous large B-cell lymphoma identified by gene expression profiling. Blood 2005; 105(9):3671-8.
21. Hoefnagel JJ, Vermeer MH, Janssen PM, Fleuren GJ, Meijer CJ, Willemze R. Bcl-2, Bcl-6 and CD10 expression in cutaneous B-cell lymphoma: further support for a follicle centre cell origin and differential diagnostic significance. Br J Dermatol 2003; 149(6):1183-91.
22. Paulli M, Viglio A, Vivenza D, Capello D, Rossi D, Riboni R, et al. Primary cutaneous large B-cell lymphoma of the leg: histogenetic analysis of a controversial clinicopathologic entity. Hum Pathol 2002; 33(9):937-43.
23. Demirkesen C, Tuzuner N, Esen T, Lebe B, Ozkal S. The expression of IgM is helpful in the differentiation of primary cutaneous diffuse large B cell lymphoma and follicle center lymphoma. Leuk Res 2011; 35(9):1269-72.
24. Koens L, Vermeer MH, Willemze R, Jansen PM. IgM expression on paraffin sections distinguishes primary cutaneous large B-cell lymphoma, leg type from primary cutaneous follicle center lymphoma. Am J Surg Pathol 2010; 34(7): 1043-8.
25. Hallermann C, Kaune KM, Gesk S, Martin-Subero JI, Gunawan B, Griesinger F, et al. Molecular cytogenetic analysis of chromosomal breakpoints in the IGH, MYC, BCL6, and MALT1 gene loci in primary cutaneous B-cell lymphomas. J Invest Dermatol 2004; 123(1):213-9.
26. Dijkman R, Tensen CP, Jordanova ES, Knijnenburg J, Hoefnagel JJ, Mulder AA, et al. Array-based comparative genomic hybridization analysis reveals recurrent chromosomal alterations and prognostic parameters in primary cutaneous large B-cell lymphoma. J Clin Oncol 2006; 24(2): 296-305.
27. Grange F, Petrella T, Beylot-Barry M, Joly P, D’Incan M, Delaunay M, et al. Bcl-2 protein expression is the strongest independent prognostic factor of survival in primary cutaneous large B-cell lymphomas. Blood 2004; 103(10):3662-8.