Services on Demand
Journal
Article
Related links
Share
Revista Médica del Uruguay
On-line version ISSN 1688-0390
Rev. Méd. Urug. vol.30 no.1 Montevideo Mar. 2014
Ataque cerebrovascular isquémico en Uruguay: comunicación de los primeros 34 casos trombolizados en el Hospital de Clínicas
Dres. Florencia Brunet*, Claudia Camejo†, Andrés Gaye‡, Lorena Castro§, Corina Puppo¶, Álvaro Niggemeyer**, Soledad Mateo**, Mariana Guirado††, Verónica Pérez††, Fabián Gómez‡‡, Federico Preve*, Irene Retamoso**, Rafael Mila§§, Lorena Viñole¶¶, Ricardo Silvariño**, Mariana Legnani***, Juan Gil†††, Heber Hackembruch‡‡‡, Carlos Ketzoian§§§, Ronald Salamano¶¶¶
Unidad de ACV (Centro Cardiovascular Universitario) y Departamento de Emergencia. Hospital de Clínicas. Facultad de Medicina, Universidad de la República. Uruguay
* Asistente de Neurología. Grupo de ACV. Instituto de Neurología. Departamento de Emergencia del Hospital de Clínicas. Facultad de Medicina, Universidad de la República. Uruguay.
† Ex Prof. Adj de Neurología. Coordinadora Grupo Enf. CerebroVascular. Instituto de Neurología. Facultad de Medicina, Universidad de la República. Uruguay.
‡ Prof. Adj. de Neurología. Grupo de ACV. Instituto de Neurología. Facultad de Medicina, Universidad de la República. Uruguay.
§ Ex Asistente de Neurología. Grupo de ACV. Instituto de Neurología. Facultad de Medicina, Universidad de la República. Uruguay.
¶ Prof. Agda. de Emergencia. Departamento de Emergencia del Hospital de Clínicas. Facultad de Medicina, Universidad de la República. Uruguay.
** Prof. Adj. de Emergencia. Departamento de Emergencia del Hospital de Clínicas. Facultad de Medicina, Universidad de la República. Uruguay.
†† Asistente de Emergencia. Departamento de Emergencia del Hospital de Clínicas. Facultad de Medicina, Universidad de la República. Uruguay.
‡‡ Residente de Neurología. Grupo de ACV. Instituto de Neurología. Departamento de Emergencia del Hospital de Clínicas. Facultad de Medicina, Universidad de la República. Uruguay.
§§ Prof. Adjunto de Cardiología, Centro Cardiovascular Universitario. Facultad de Medicina, Universidad de la República. Uruguay.
¶¶ Residente de Cardiología. Departamento de Cardiología. Facultad de Medicina, Universidad de la República. Uruguay.
*** Residente de Neurología. Grupo de ACV. Instituto de Neurología. Facultad de Medicina, Universidad de la República. Uruguay.
††† Prof. Agdo. del Departamento Métodos Cuantitativos, coordinador de la Sección Neuroepidemiología. Instituto de Neurología, Facultad de Medicina, Universidad de la República. Uruguay.
‡‡‡ Asistente del Departamento de Neurofisiología, integrante de la Sección de Neuroepidemiología. Instituto de Neurología, Facultad de Medicina, Universidad de la República. Uruguay.
§§§ Asistente de Dirección del Hospital de Clínicas. Ex coordinador de la Sección Neuroepidemiología. Instituto de Neurología, Facultad de Medicina, Universidad de la República. Uruguay.
¶¶¶ Profesor de Neurología, Instituto de Neurología, Facultad de Medicina, Universidad de la República. Uruguay. Grupo de ACV. Instituto de Neurología. Departamento de Emergencia del Hospital de Clínicas. Sección Neuroepidemiología. Instituto de Neurología. Departamento de Cardiología
Correspondencia: Dra. Claudia Camejo. Avda. General Flores 3461, Montevideo. Uruguay.
Correo electrónico: ccamejo@adinet.com.uy
Conflicto de intereses: los autores declaran no tener conflicto de intereses.
Recibido: 15/6/13 Aceptado: 10/3/14
Resumen
Introducción: el ataque cerebrovascular (ACV) constituye un problema de salud en Uruguay y en el mundo. Se ha comprobado que la trombolisis intravenosa disminuye la morbimortalidad y las secuelas en los pacientes con ACV isquémicos agudos (nivel de evidencia IA). Objetivos: analizar los casos de ACV isquémico trombolizados en el Hospital de Clínicas y valorar la utilidad de un score de predicción de sangrado intracraneano sintomático en esta población. Material y método: estudio descriptivo, observacional y prospectivo. Población: pacientes trombolizados en el Hospital de Clínicas en el período 2010-2013. Se aplicó score predictivo de hemorragia sintomática a toda la población de trombolizados. Tests estadísticos: test de chi cuadrado, test de student, test de Wilcoxon, se consideraron diferencias estadísticamente significativas aquellas con una p < 0,05. Resultados: treinta y cuatro pacientes trombolizados, promedio de edad 67 años, mayoría mujeres, alto porcentaje de ACV graves, National Institute of Health Stroke Scale (NIHSS) promedio al ingreso: 11, con mejoría estadísticamente significativa al alta. Etiología principal: cardioembolia. Tiempo síntoma aguja promedio: 170 minutos. Hemorragia intracraneana: ocho pacientes (23,5%), fallecieron cuatro de ellos. El puntaje del score de sangrado no predijo el sangrado intracraneano. Conclusiones: en el Hospital de Clínicas, desde la inauguración de la Unidad de ACV, el porcentaje de infartos cerebrales trombolizados ha ido en aumento, siendo actualmente comparable a cifras internacionales. El tiempo síntoma-aguja es menor que en otros estudios. La trombolisis generó un beneficio estadísticamente significativo en la escala de NIHSS. El porcentaje de sangrados fue similar al descrito en la literatura.
Palabras clave: ACCIDENTE CEREBROVASCULAR
TERAPIA TROMBOLÍTICA
Keywords: STROKE
THROMBOLYTIC THERAPY
Introducción
El ataque cerebrovascular (ACV) constituye un problema de salud en el mundo. En nuestro país es la segunda causa de muerte luego del infarto agudo de miocardio (IAM)(1) y genera una morbimortalidad muy importante con costos muy elevados para el sistema sanitario.
El 80% de los ACV son isquémicos(2) y solo existen dos tratamientos que disminuyen la morbimortalidad en la fase aguda con nivel de evidencia 1A: las unidades de ACV(3) y la trombolisis intravenosa con activador tisular recombinante del plasminógeno (r-TPA), con una ventana terapéutica de tres horas desde el inicio de los síntomas(4).
Las unidades de ACV, independientemente del uso de trombolíticos, demostraron fehacientemente disminuir la mortalidad, morbilidad y los costos de atención de los pacientes(3).
La introducción del rTPA como terapia de reperfusión ha causado un cambio dramático en el tratamiento agudo de la isquemia cerebral. La trombolisis ha sido evaluada en estudios controlados randomizados(4-6), pool de análisis(7,8) y estudios de monitorización y seguridad. Entre 10% a 20% de los ACV isquémicos son candidatos a fibrinolíticos intravenosos.
La trombolisis intravenosa con r-TPA fue aprobada por la Food and Drug Administration (FDA) de Estados Unidos en 1995(4), en base al estudio The National Institute of Neurological Disorders and Stroke 2 (NINDS 2) con una ventana terapéutica de tres horas.
En 1999 fue aprobado su uso en Canadá y en el 2002 por la European Medicine Agency (EMEA).
El estudio realizado por European Cooperative Acute Stroke Study (ECASS III)(9,10) extendió la ventana terapéutica a entre 3 y 4,5 horas y mostró un aumento no significativo de sangrados sin incremento de la mortalidad. La FDA no ha aceptado la extensión de dicha ventana, sí lo han hecho la Academia Americana de Neurología (AAN) y la EMEA.
Varios metaanálisis sugieren que el beneficio del tratamiento decrece con el tiempo que transcurre desde el comienzo de los síntomas hasta el inicio del rTPA intravenosa.
Su uso presenta múltiples limitaciones: corto tiempo de ventana terapéutica, baja tasa de recanalización, diversas causas de exclusión, sospecha de neurotoxicidad, vida media muy corta (5 minutos), y sustancial riesgo de hemorragia intracerebral.
La escala de NIHSS fue creada en 1995 para indicar y controlar la trombolisis en los pacientes con ACV isquémico. Es una forma de cuantificación universal del ACV al ingreso y en la evolución. Es indispensable su aplicación para la selección de pacientes candidatos a rTPA (anexo 1).
Tal como se mencionó, la hemorragia cerebral es la complicación más temida. En el 2012, en base al análisis de 31.627 pacientes tratados con trombolíticos, el estudio Safe Implementation of Treatments in Stroke (SITS) implementó una escala predictora de sangrados sintomáticos intracerebrales(11) que no excluye la realización del mismo.
Esta es la primera serie de pacientes con ACV tratados con trombolíticos reportada en nuestro país.
Objetivos
1. Describir una población de pacientes con ACV isquémico tratados con rTPA, su evolución durante la internación y sus complicaciones.
2. Evaluar el poder predictor de sangrado a través de la aplicación de la escala de sangrado sintomático en dichos pacientes(11).
Material y método
Estudio descriptivo, observacional y prospectivo. Se analizaron todos los pacientes trombolizados (34) desde enero del 2010 hasta diciembre del 2013. Se revisaron los protocolos de ingreso a la Unidad de ACV, en los cuales constan: datos clínicos, paraclínicos, el tratamiento realizado y la evolución. Se extrajeron datos como: sexo, edad, factores de riesgo, hora de instalación de síntomas, demora en la llegada a la Emergencia, tratamiento previo al ACV (anexo 2p1-2p2).
En la vertiente clínica se utilizaron clasificaciones como la Oxfordshire Community Stroke Project (OXFORD)(12), en la cuantificación de la severidad la escala de NIHSS anexo 2, etiológica por el Trial of Org 10172 in Acute Stroke Treatment (TOAST[13]) y en la evolución las escalas funcionales de Barthel y Rankin modificadas.
Los pacientes candidatos a trombolisis intravenosa se seleccionaron por criterios estrictos de inclusión y exclusión de acuerdo a normas internacionales vigentes(4,6,14). Inclusión: inicio de síntomas dentro de las 4,5 horas previas al comienzo del tratamiento (AAN, EMEA), déficit neurológico medible por escala de NIHSS (NIHSS mayor o igual a 3), síntomas neurológicos persistentes, tomografía (TAC) de cráneo sin evidencia de hemorragia. Exclusión: menos de 18 o más de 80 años, crisis epilépticas al inicio del cuadro si la TC o resonancia magnética (RM) hacen sospechar otra etiología, NIHSS > a 25, presión arterial (PA) sistólica >185 o diastólica > a 110 mmHg. Requerimiento de medidas agresivas para el manejo de la PA o situación hemodinámica o cardiovascular inestable, síntomas sugestivos de hemorragia meníngea, signos tomográficos de infarto extenso constituido (hipodensidad mayor a 1/3 del territorio de la arteria cerebral media), evidencia de sangrado activo o trauma agudo en el examen, antecedentes de hemorragia intracraneal, ACV o traumatismo encéfalo craneano (TEC) severo en los tres meses previos, IAM en los tres meses previos, cirugía mayor en los últimos 14 días, sangrado digestivo o urinario en los 21 días previos, punción arterial en sitio no compresible en los últimos siete días, tratamiento anticoagulante con INR mayor a 1,7, heparina en las últimas 48 horas si el KPTT es mayor a 40´´ o heparinas de bajo peso a dosis de anticoagulación, plaquetas menores a 100.000/mm3, glicemia menor a 50 o mayor a 400 mg/dl, gestación o parto en los últimos 30 días, enfermedad grave, terminal o con alto riesgo de sangrado (hepatopatías, etcétera).
Los estudios paraclínicos indispensables para el tratamiento fueron: TAC de cráneo, glicemia venosa o capilar, hemograma y crasis. Se solicitó la firma del consentimiento informado por parte del paciente o del familiar responsable en todos los casos.
La dosis utilizada de r-TPA fue de 0,9 mg/kg (máximo 90 mg) administrada el 10% en bolo y el 90% restante en bomba de infusión en 60 minutos.
La recepción del paciente y las primeras 24 horas de evolución se desarrollaron en el área de reanimación y en la Unidad de Cuidados Especiales del Departamento de Emergencia. De acuerdo a su nivel de conciencia y la TC de control se trasladaron a la Unidad de ACV o a centro de tratamiento intensivo (CTI).
Los pacientes fueron sometidos a evaluación estricta en las primeras horas luego de realizado el tratamiento (escala de NIHSS, escala canadiense por parte de enfermería, controles muy frecuentes de PA, hemoglucotest [HGT], vigilia y monitorización cardíaca durante las primeras 48 horas). La TC de control se realizó dentro de las primeras 24 a 36 horas.
Se aplicó el score predictor de hemorragia(11) a todos los pacientes trombolizados para valorar si los pacientes con hemorragia sintomática tenían un puntaje significativamente más elevado que los que no la presentaron. La escala no contraindica la realización del tratamiento. Dicha escala puntea tratamiento previo con ácido acetilsalicílico (AAS) y clopidogrel: 3 puntos (p); solo AAS: 2 p; edad >72 años:1 p; glicemia = 180mg/dl: 2 p; tiempo de demora en realizar rTPA >180 minutos:1 p; PA > 149: 1 p; peso > 95 kg: 1 p.
Riesgo bajo: 0-2, riesgo medio: 3-5, riesgo moderado: 6-8, riesgo alto más de 9.
Se consideró hemorragia sintomática con la definición más estricta (por el estudio NINDS): cualquier sangrado intracraneano, incluso petequial con agregado de síntomas neurológicos, cuantificado por un aumento del NISHH mayor a 1.
Para las variables cualitativas se utilizaron porcentajes, para las variables cuantitativas se utilizaron medidas de resumen (media y mediana) y de dispersión (rango, desvío estándar y varianza). Para las variables categóricas se estudió la existencia de asociación estadística mediante test de chi cuadrado o el test exacto de Fisher, según condiciones de aplicación. Para la comparación de valores pre y postratamiento de los scores o escalas se utilizaron los tests de Student muestras dependientes o el test de Wilcoxon. En todos los casos, el nivel de significación fue de ? = 0,05.
Resultados
Población
Se analizaron los primeros 34 pacientes con tratamiento trombolítico en el Hospital de Clínicas. El promedio de edad fue de 67 años (rango: 38-80 años).
Se realizaron fibrinolíticos en 20 mujeres (59%) y en 14 hombres (41%) con un promedio de edad de 67 y 68 años, respectivamente.
Con respecto a los factores de riesgo vascular, 97% eran hipertensos, 41% dislipémicos, 26% tenían arritmia como antecedente personal, 29% diabéticos, tabaquismo en 29% y alcoholismo en 18% (figura 1). Se destaca que el 32% de los pacientes tenían como antecedente personal un ACV previo y 18% un ataque isquémico transitorio (AIT).
Clínica
Clínicamente se presentaron como infarto total de la circulación anterior (TACI), 15 pacientes (44%); como infarto parcial de la circulación anterior (PACI), 9 (26,5%); como infarto lacunar (LACI), 9 (26,5%), y 1 paciente (3%) como infarto de la circulación posterior (POCI).
Al ingreso, la mediana del NIHSS fue de 11 puntos (3-24); a las 24 horas, 7 puntos (0-34), y al alta, 4 puntos (0-36), siendo el score al ingreso significativamente mayor que al alta (test de Wilcoxon, p = 0,049) (ver tabla 1 y figura 2).
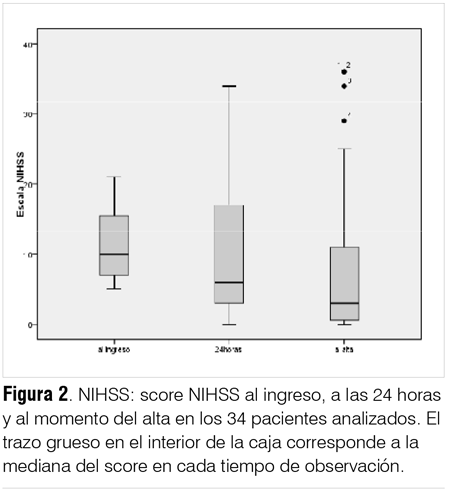
Etiopatogenia
Desde el punto de vista etiopatogénico, 35% fueron cardioembólicos, 23% ateromatosos, 6% oclusión de pequeño vaso, 12% indeterminados por estudios negativos, 6% indeterminados por dos causas y 18% indeterminados por estudios incompletos (figura 3).
Tiempos
El tiempo síntoma-aguja promedio fue de 170 minutos (rango: 60-270 minutos).
Con respecto a la demora de llegada a la puerta de urgencia, la media fue de 83 minutos (rango: 0-240 minutos).
Durante el 2010 se protocolizaron 125 ACV isquémicos y se les realizó rTPA a 3 (2,4%). En el 2011, 77 ACV isquémicos y 7 rTPA (9%). Durante el 2012, 84 ACV y 14 rTPA (16,6%) y durante el 2013 se protocolizaron 64 pacientes con ACV y 10 fueron tratados con rTPA (15,6%) (tabla 2).
Complicaciones
Mortalidad
Fallecieron 9 pacientes (26%) (3 hombres y 6 mujeres), en un promedio de 12 días. La mitad antes del décimo día de su ingreso.
El 100% de los fallecimientos se dio en pacientes con TACI, su puntaje promedio en la escala NIHSS fue de 18 (12-24) y ninguno logró reperfusión clínica ni imagenológica, configurando en todos los casos un infarto silviano total.
De los pacientes fallecidos, cuatro presentaron un sangrado intracraneano (uno de ellos fue una pequeña transformación hemorrágica), con score de sangrado promedio de 6, y un tiempo medio puerta-aguja de 183 minutos. En los restantes pacientes, dos fallecieron por neumonía aspirativa, uno por sepsis nefrourológica y otro por gastroenterocolitis que fallece al mes del alta.
Dos pacientes se presentaron como infarto silviano maligno y requirieron cirugía descompresiva.
Sangrados
De los 34 pacientes trombolizados, 9 sangraron: 8 hemorragias intracraneanas (23,5%) más un sangrado que fue extraneurológico (hematuria).
Dos de ellos se presentaron como transformación hemorrágica leve sin manifestaciones clínicas y en otro el sangrado fue un hallazgo en la TAC de cráneo de control.
De los ocho pacientes que presentaron sangrado intracraneal, la mitad de ellos fallecieron.
Estadía
Los pacientes trombolizados permanecieron internados en la Unidad de ACV un promedio de 5,5 días (1-11) y una estadía total en el hospital de 17 días (1-67).
Ingresaron ocho pacientes (23,5%) a CTI.
Desde el 2010 se trombolizaron 34 pacientes, durante ese período se asistieron 350 pacientes con ACV isquémico: 9,7%.
Score riesgo de sangrado
Aplicada la escala o score predictor de hemorragia sintomática el promedio fue de 5 puntos, nivel de riesgo medio.
Se aplicó la escala encontrando que tres pacientes (9%) tenían un riesgo entre 0-2; 18 pacientes (53%) entre 3-5; 13 pacientes (38%) entre 6-8, y ninguno mayor de 9.
En el subgrupo con score entre 3-5, sangraron seis pacientes (33%) y en el subgrupo con score entre 6-8, sangraron dos pacientes (15%).
No pudo ponerse en evidencia que aquellos pacientes que tuvieron sangrado intracraneal presentaran al ingreso valores del score más elevados respecto a los no sangrantes, presentando un valor mediano de score igual a 5 en ambos grupos (p = 0,984). La distribución de score de ambos grupos se resume en la figura 4.
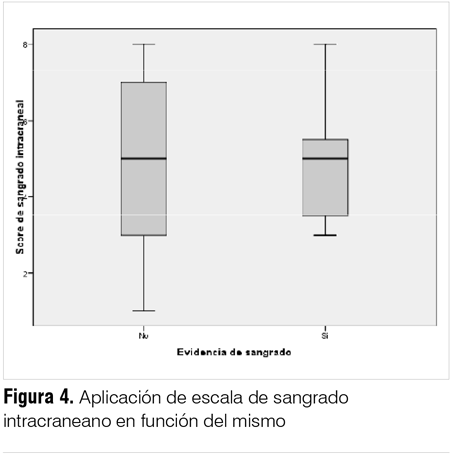
Discusión
Aunque la realización de trombolíticos está aprobada en el ACV isquémico, en nuestro país se ha realizado en forma aislada en algunas instituciones privadas y públicas.
El proceso de realización de trombolíticos en el Hospital de Clínicas transitó varias etapas. En el año 2007 se constituyó un equipo multidisciplinario conformado por neurólogos, internistas, fisiatras, que mediante protocolo captaban todos los pacientes que ingresaban al hospital, homogeneizando pautas de estudio y tratamiento aceptadas internacionalmente.
En una segunda etapa se abrieron dos camas en el piso 2 con el fin exclusivo del tratamiento agudo, incluido el tratamiento trombolítico. Posteriormente y ya en el centro cardiovascular se instauraron cuatro camas en forma definitiva. En todos estos años se han protocolizado más de 800 ACV, con 75% de ACV isquémicos.
Los datos que presentamos son de los primeros 34 pacientes con ACV tratados con trombolíticos en forma sistemática entre el 2010 y diciembre de 2013. Los resultados epidemiológicos son similares a otros trabajos realizados en América Latina(15) y en Europa(10).
Entre 10% a 20% del total de pacientes con ACV isquémicos son candidatos a tratamiento trombolítico. Esta población representó el 9,7%.
Durante el 2011 se realizó rTPA a 9% de los ACV isquémicos, y en 2012 y 2013 el número de pacientes trombolizados alcanzó el 16%, cifras que muestran que el entrenamiento del equipo médico y la inauguración de la Unidad de ACV han influido en forma favorable.
En esta población se destaca el alto número de pacientes hipertensos con un ACV previo, por lo que es recomendable el control de los factores de riesgo así como realizar una exitosa prevención secundaria.
Dada la vinculación directa del tiempo entre síntoma e inicio del tratamiento trombolítico, cuantificar el mismo se hace indispensable. Aún no se han implementado campañas con las emergencias móviles que permitan disminuir dicho tiempo.
La media del traslado o llegada a puerta fue de 83 minutos. La media de la demora en realizar el rTPA en Montevideo fue de 170; 198 en Chile(15 ) y 239 minutos en el ECASS III(10).
La media del NIHSS al ingreso fue de 11 puntos, en comparación con 16 en Chile y 12 puntos en el ECASS III. La mejoría del mismo en las primeras 24 horas a 7 puntos y al alta a 4 puntos fue estadísticamente significativa, demostrando que la realización del fibrinolítico y su control en el contexto de la Unidad de ACV es más seguro y efectivo.
El porcentaje de sangrados totales fue de 23,5%, mientras que en el ECASS III fue de 27%.
La mortalidad de 26% se explicó por los siguientes factores: a) una severidad clínica inicial con un NIHSS muy elevado, 18 (mucho más alto que en el total de la población trombolizada, 11); b) la presentación clínica como un infarto total (por la clasificación de Oxford todos eran TACI). Es reconocido que estos pacientes no tienen, en general, buena evolución con la trombolisis sistémica y que muchas veces requieren terapias intraarteriales de rescate, no disponibles en nuestro país. Además, ninguno reperfundió clínica ni imagenológicamente, configurando todos un infarto silviano total, cuadro sumamente grave y con altísima mortalidad más allá de si el paciente es o no trombolizado; c) varios pacientes fallecieron por complicaciones infecciosas no vinculables al tratamiento agudo del ACV.
La aplicación del score no mostró asociación estadísticamente significativa con el riesgo de sangrado, probablemente debido al bajo número de pacientes.
Conclusiones
El uso del rTPA es seguro y eficaz cuando se siguen cuidadosamente las guías, en el marco de Emergencia-Unidad de ACV.
El tiempo síntoma-aguja fue menor en nuestro trabajo que en otros estudios. La trombolisis generó un beneficio estadísticamente significativo en la escala de NIHSS. El porcentaje de sangrados es similar al descrito en la literatura y la escala predictora no resultó estadísticamente significativa.
La mortalidad no siempre fue consecuencia del tratamiento con rTPA.
Pocos pacientes son candidatos a trombolisis intravenosa, pero dadas las características del sistema de salud y geográficas de nuestro país, ese número puede llegar a ser mucho mayor; el porcentaje de infartos cerebrales trombolizados en el Hospital de Clínicas ha ido en aumento, siendo actualmente comparable con cifras internacionales.
La base del éxito está en la formación de equipos entrenados y adecuados a cada institución y a políticas sociales de difusión para la consulta precoz.
Abstract
Introduction: ischemic stroke is a health issue of paramount importance in Uruguay and the world. It has been proved that intravenous thrombolysis reduces morbi-mortality and sequels in patients with severe ischemic strokes (evidence level: severe ischemic stroke).
Objectives: to analyse the cases of thrombolized ischemic strokes at the Clinicas Hospital and to assess the usefulness of the risk score to predict symptomatic intracranial hemorrhage in this population.
Method: descriptive, observational and prospective study. Population: thrombolized patients at the Clinicas Hospital during the 2010-2013 period of time. A risk score to predict symptomatic intracranial hemorrhage was applied to the entire thrombolized population. Statistical tests: chi-square test, student test and Wilcoxon test. The study considered p < 0,05 reflected statistically significant differences.
Results: thirty four thrombolized patients, average age was 67 years old, most of them were women, high percentage of severe ischemic strokes, average National Institute of Health Stroke Scale value upon admittance was 11, with statistically significant improvement trends. Main etiology: cardioembolism. Average symptom-to-needle time: 170 minutes. Intracranial Hemorrhage: eight patients (23.5%), four of which died. The risk score failed to predict the intracranial hemorrhage.
Conclusions: the percentage of thrombolized ischemic strokes has been gradually increasing at the Clinicas Hospital since the Ischemic Stroke Department was open, and current national figures match the international ones. Thrombolysis resulted in a statistically significant benefit in the NIHSS scale. The hemorrhage was similar to that described in international literature.
Resumo
Introdução: o acidente vascular cerebral (AVC) é um problema de saúde no Uruguai e em todo o mundo. Foi demonstrado que a trombólise intravenosa reduz a morbimortalidade e as sequelas em pacientes com AVC isquêmicos agudos (nível de evidencia IA).
Objetivos: analisar os casos de AVC isquêmico trombolizados no Hospital de Clínicas e avaliar a utilidade de uma escala de predição de sangramento intracraniano sintomático nesta população.
Material e método: estudo descritivo, observacional e prospectivo. População: pacientes trombolizados no Hospital de Clínicas no período 2010-2013. Uma escala de predição de hemorragia sintomática foi utilizada em todos os pacientes trombolizados. Testes estatísticos: teste de qui quadrado, teste de Student, teste de Wilcoxon, Foram consideradas como diferenças estatisticamente significativas aquelas com p < 0,05.
Resultados: trinta e quatro pacientes trombolizados, com idade média 67 anos, maioria de sexo feminino, com alta porcentagem de AVC graves, média da National Institute of Health Stroke Scale (NIHSS) no momento da admissão: 11, com melhoria estatisticamente significativa no momento da alta. Etiologia principal: cardioembolia. Tempo sintoma agulha médio: 170 minutos. Hemorragia intracraniana: oito pacientes (23,5%), quatro falecidos. O valor da escala de sangramento não foi preditivo para sangrado intracraniano.
Conclusões: no Hospital de Clínicas, desde a inauguração da Unidade de AVC, a porcentagem de infartos cerebrais trombolizados está aumentando sendo atualmente comparável a cifras internacionales. O tempo sintoma agulha é menor que em outros estudos. A trombólise produziu um beneficio estatisticamente significativo na escala NIHSS. A porcentagem de sangramentos foi similar à descrita na literatura.
Bibliografía
1. Comisión Honoraria para la Salud Cardiovascular. Área de Epidemiología y Estadística. Uruguay. Mortalidad por enfermedades cardiovasculares en el Uruguay 2008. Montevideo: CHSC, 2010.
2. Castillo J, Zarranz JJ, Larracoechea J. Enfermedades vasculares cerebrales. En: Zarranz JJ. Neurología. 3 ed. Madrid: Elsevier Science, 2004:357-435.
3. Govan L, Langhorne P, Weir CJ; Stroke Unit Trialists Collaboration. Does the prevention of complications explain the survival benefit of organized inpatient (stroke unit) care?: further analysis of a systematic review. Stroke 2007; 38(9):2536-40.
4. The National Institute of Neurological Disorders and Stroke rt-PA Stroke Study Group. Tissue plasminogen activator for acute ischemic stroke. N Engl J Med 1995; 333(24):1581-7.
5. Hacke W, Kaste M, Fieschi C, Toni D, Lesaffre E, von Kummer R, et al. Intravenous thrombolysis with recombinant tissue plasminogen activator for acute hemispheric stroke. The European Cooperative Acute Stroke Study (ECASS). JAMA 1995; 274(13):1017-25.
6. Hacke W, Kaste M, Fieschi C, von Kummer R, Davalos A, Meier D, et al. Randomised double-blind placebo-controlled trial of thrombolytic therapy with intravenous alteplase in acute ischaemic stroke (ECASS II). Second European-Australasian Acute Stroke Study Investigators. Lancet 1998; 352(9136):1245-51.
7. Hacke W, Donnan G, Fieschi C, Kaste M, von Kummer R, Broderick JP, et al; ATLANTIS Trials Investigators; ECASS Trials Investigators; NINDS rt-PA Study Group Investigators. Association of outcome with early stroke treatment: pooled analysis of ATLANTIS, ECASS, and NINDS rt-PA stroke trials. Lancet 2004; 363(9411):768-74.
8. Lees KR, Bluhmki E, von Kummer R, Brott TG, Toni D, Grotta JC, et al; ECASS, ATLANTIS, NINDS and EPITHET rt-PA Study Group. Time to treatment with intravenous alteplase and outcome in stroke: an updated pooled analysis of ECASS, ATLANTIS, NINDS, and EPITHET trials. Lancet 2010; 375(9727):1695-703.
9. Del Zoppo GJ, Saver JL, Jauch EC, Adams HP Jr; American Heart Association Stroke Council. Expansion of the time window for treatment of acute ischemic stroke with intravenous tissue plasminogen activator: a science advisory from the American Heart Association/American Stroke Association. Stroke 2009; 40(8):2945-8.
10. Hacke W, Kaste M, Bluhmki E, Brozman M, Dávalos A, Guidetti D, et al; ECASS Investigators. Thrombolysis with alteplase 3 to 4.5 hours after acute ischemic stroke. N Engl J Med 2008; 359(13):1317-29.
11. Mazya M, Egido JA, Ford GA, Lees KR, Mikulik R, Toni D, et al; SITS Investigators. Predicting the risk of symptomatic intracerebral hemorrhage in ischemic stroke treated with intravenous alteplase: safe Implementation of Treatments in Stroke (SITS) symptomatic intracerebral hemorrhage risk score. Stroke 2012; 43(6):1524-31.
12. Wardlaw JM, Dennis MS, Lindley RI, Sellar RJ, Warlow CP. The validity of a simple clinical classification of acute ischaemic stroke. J Neurol 1996; 243(3):274-9.
13. Adams HP Jr, Bendixen BH, Kappelle LJ, Biller J, Love BB, Gordon DL, et al. Classification of subtype of acute ischemic stroke, definitions for use in a multicenter clinical trial, TOAST: Trial of Org 10172 in Acute Stroke Treatment. Stroke 1993; 24(1):35-41.
14. Wahlgren N, Ahmed N, Dávalos A, Ford GA, Grond M, Hacke W, et al; SITS-MOST investigators. Thrombolysis with alteplase for acute ischaemic stroke in the Safe Implementation of Thrombolysis in Stroke-Monitoring Study (SITS-MOST): an observational study. Lancet 2007; 369(9558):275-82.
15. Figueroa Reyes T, Sáez D, Mansilla E, Sánchez R, Nogales Gaete J, Delgado I. Experiencia de trombolisis sistematizada en infarto cerebral agudo en un hospital público de Chile. Rev Méd Chile 2011; 139(9):1118-27.














