Services on Demand
Journal
Article
Related links
Share
Revista Médica del Uruguay
On-line version ISSN 1688-0390
Rev. Méd. Urug. vol.29 no.2 Montevideo June 2013
Cohorte GEFA-HT-UY (GEnotipo, Fenotipo y Ambiente de la HiperTensión Arterial en UruguaY). Protocolo y primeros resultados
Leonella Luzardo*, Inés Lujambio†, Mariana Sottolano†, Alicia Da Rosa‡, Sebastián Robaina†, Federico Arce§, María Márquez¶, Valentina Agorrody**, Carlos Américo**, Mariela Garau††, Nadia Krul‡‡, Ana Carina Ríos§§, Lucía Florio¶¶, Alicia Olascoaga***, Óscar Noboa†††, Jan Albert Staessen‡‡‡, José Boggia¶
Unidad de Hipertensión Arterial. Centro de Nefrología. Departamento de Fisiopatología. Hospital de Clínicas. Facultad de Medicina. Universidad de la República
* Asistente del Departamento de Fisiopatología del Hospital de Clínicas. Postgrado del Centro de Nefrología del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
† Ayudante de Clase del Departamento de Fisiopatología del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
‡ Licenciada en Neumocardiología del Departamento de Fisiopatología del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
§ Estudiante de postgrado del Centro de Nefrología del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
¶ Profesor Adjunto del Departamento de Fisiopatología del Hospital de Clínicas. Facultad de Medicina. Asistente del Centro de Nefrología del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
** Residente del Departamento de Cardiología del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
†† Profesora Adjunta del Departamento de Métodos Cuantitativos de la Facultad de Medicina. Universidad de la República.
‡‡ Asistente del Departamento de Laboratorio de Patología Clínica del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
§§ Licenciada en Laboratorio del Departamento de Laboratorio de Patología Clínica del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
¶¶ Profesora Adjunta del Departamento de Cardiología del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
*** Profesora Agregada del Departamento de Laboratorio de Patología Clínica del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
††† Profesor Agregado del Centro de Nefrología del Hospital de Clínicas. Facultad de Medicina. Universidad de la República.
‡‡‡ Studies Coordinating Centre, Department of Cardiovascular Diseases, Division of Hypertension and Cardiovascular Rehabilitation, University of Leuven, Leuven, Belgium and Department of Epidemiology, Maastricht University, Maastricht, The Netherlands.
Fuentes de financiamiento: Comisión Sectorial de Investigación Científica (CSIC), Fondos I+D 2010; Agencia Nacional de Investigación e Innovación (ANII), Fondo María Viñas 2011 (Proyecto FMV_2_2011_1_6414) Programa para la Formación y Fortalecimiento de los Recursos Humanos de los Prestadores Públicos de Servicios de Salud (ASSE), y laboratorio Gramón-Bagó - Novartis a través de Ley de Fundaciones (Ley 16.462/94). El equipamiento utilizado en el estudio fue cedido en préstamo por OMRON (equipo para monitoreo domiciliario de presión arterial M10 HEM-7080IT-E), IEM (equipo de monitoreo ambulatorio de presión arterial Mobil-O-Graph PWA-24h) y AtCor (equipo para evaluación de rigidez arterial SphygmoCor). Conflicto de intereses: el Dr José Boggia, como responsable científico del estudio GEFA-HT-UY recibió equipos en calidad de préstamo por la duración del estudio de las empresas OMRON, IEM, AtCor y material plástico en donación de e-Medical.
Resumen
Introducción: la hipertensión arterial esencial es el resultado de complejas interacciones entre el genotipo, el fenotipo y el ambiente. El estudio GEFA-HT-UY busca analizar el papel de diferentes rasgos fenotípicos cardiovasculares y renales y su relación con factores genéticos y ambientales en una muestra aleatoria de una zona de Montevideo. Material y método: estudio de cohorte poblacional, observacional y analítico que inició su diseño y programación en 2011 y la recolección de datos en abril de 2012. La muestra consiste en 150 familias (aproximadamente 450 sujetos), seleccionados de forma aleatoria entre los habitantes de un área geográfica delimitada de Montevideo. Las determinaciones basales incluyen el registro de antecedentes médicos de relevancia, medidas antropométricas, determinaciones de presión arterial en domicilio, en consultorio, automonitoreo de presión arterial y monitoreo ambulatorio de presión arterial periférico y central. Se realiza registro electrocardiográfico, ecocardiográfico y de rigidez arterial. Se recogen muestras de sangre y orina para determinaciones bioquímicas con especial énfasis en los factores de riesgo cardiovascular y de enfermedad renal crónica y la evidencia de daño de órgano blanco. Durante el seguimiento se pesquisará la incidencia de nuevos eventos cardiovasculares y renales. Resultados: el objetivo de esta publicación es comunicar el protocolo, de todas formas se presentan los resultados de los primeros 36 sujetos que ya lo han completado. Discusión: el seguimiento de la cohorte aportará datos relevantes y originales sobre la hipertensión arterial y su relación con el desarrollo de enfermedad cardiovascular y renal.
Palabras clave: HIPERTENSIÓN ESTUDIOS DE COHORTES FACTORES DE RIESGO ENFERMEDADES CARDIOVASCULARES ENFERMEDADES RENALES
Keywords: HYPERTENSION COHORT STUDIES RISK FACTORS CARDIOVASCULAR DISEASES KIDNEY DISEASES
Correspondencia: Prof. Adj. Dr. José Boggia. Unidad de Hipertensión Arterial. Hospital de Clínicas. Av. Italia 2870, piso 15, ala central. Montevideo, Uruguay. Correo electrónico: jboggia@hc.edu.uy Recibido: 15/12/12 Aceptado: 2/4/13
Introducción
La hipertensión arterial (HTA) esencial es el resultado de complejas interacciones entre el genotipo, el fenotipo y el ambiente. La HTA no controlada, es decir el mantenimiento de cifras elevadas de presión arterial (PA) a lo largo del tiempo genera lesión a nivel vascular, cardíaco, cerebral y renal entre otros parénquimas: daño sobre órgano blanco. A su vez, en la generación de daño sobre órgano blanco participan interacciones, aún no del todo dilucidadas, entre el fenotipo hipertensivo y la predisposición genética del sujeto, modulada por la presencia de otros factores de riesgo (el ambiente). Un ejemplo de cómo interactúan genotipo, fenotipo y ambiente es el papel de los defectos congénitos y adquiridos del riñón en la patogenia de la HTA esencial(1). Así, el genotipo adquiere un doble rol, primero como factor potencial para el desarrollo de HTA y segundo como factor determinante de la severidad del daño sobre órgano blanco generado por la HTA. Por otra parte, el ambiente actúa exigiendo la capacidad de adaptación de la composición genética y modificando el fenotipo. Finalmente, la HTA que imprime cambios en el fenotipo de otros órganos tiene rasgos propios. Por ejemplo, en las últimas décadas cobran relevancia los conceptos de PA central y rigidez arterial como rasgos fenotípicos de algunas formas de hipertensión.
Uno de los principales objetivos de la conformación y seguimiento de la cohorte GEFA-HT-UY (Genotipo, Fenotipo y Ambiente de la HiperTensión Arterial en UruguaY) es analizar el papel de la PA central (en reposo y ambulatoria), la rigidez arterial medida a través de la velocidad de onda de pulso (VOP), el índice de aumentación sistólica (en reposo y ambulatorios) y la función renal evaluada por diferentes métodos como fenotipos particulares asociados a las cifras de PA, y su relación con factores genéticos y ambientales en una muestra aleatoria de la población de Montevideo. El objetivo de la presente publicación es comunicar el protocolo y los primeros resultados de la cohorte GEFA-HT-UY.
Material y método
Diseño del estudio
GEFA-HT-UY es el acrónimo para GEnotipo, Fenotipo y Ambiente de la HiperTensión arterial en UruguaY, cohorte prospectiva que comenzó el relevamiento de datos en abril del año 2012. Es un estudio poblacional, observacional y analítico elaborado y ejecutado por la Unidad de Hipertensión Arterial del Hospital de Clínicas Dr. Manuel Quintela, Universidad de la República. El protocolo de investigación fue aprobado por el Comité de Ética de dicho hospital y todos los sujetos deben firmar un consentimiento informado previo a su inclusión en el proyecto. Al inicio del estudio se recogen datos referentes a factores de riesgo cardiovascular (CV) así como antecedentes de enfermedad CV o renal, con particular interés en el accidente cerebrovascular, la cardiopatía isquémica, la insuficiencia cardíaca y la enfermedad renal crónica. Durante el seguimiento se pesquisará la incidencia de nuevos eventos CV o renales.
El objetivo del estudio es analizar los aspectos genotípicos, fenotípicos y del ambiente vinculados a la PA. Con la finalidad de evaluar la asociación entre exposición a factores de riesgo y aparición de eventos fatales y no fatales, CV o renales, se planificó el relevamiento de nuevos eventos con intervalo de dos años.
Población
Se seleccionaron 150 familias al azar entre los habitantes de un área geográficamente definida de Montevideo. La selección de casos se realizó utilizando el procedimiento de selección de casos al azar de un programa estadístico a partir de un listado de 500 viviendas de un área geográficamente definida. Las familias reclutadas deben incluir al menos a uno de los padres y dos hijos (límite inferior de edad 18 años, sin límite superior). Se incluyen en el estudio los integrantes del núcleo familiar que comparten la misma vivienda o viven a una distancia no mayor a los 10 kilómetros del área definida. La muestra inicial está constituida por 150 familias, aproximadamente 450 personas. Los sujetos seleccionados son invitados a participar del estudio mediante una llamada telefónica, posteriormente se les entrega en el domicilio información escrita detallada, y si aceptan, confirman su participación firmando un consentimiento. Posteriormente se concreta una primera entrevista en el domicilio. Al momento de presentar este reporte se han incluido 52 sujetos en la cohorte, de los cuales en este avance se incluyen aquellos que completaron todas las etapas del protocolo básico (n = 36).
Trabajo de campo
Entrevistas
En el domicilio del sujeto se completa un cuestionario diseñado para recoger información sobre indicadores socioeconómicos, antecedentes médicos personales y familiares, factores de riesgo para enfermedad cardiovascular y renal, nivel de actividad física, estrés mental, y tratamiento farmacológico y no farmacológico. Al final de la entrevista, luego de que el sujeto permanece cinco minutos sentado en reposo, el observador mide la PA del sujeto cinco veces consecutivas, como se detalla más adelante. Todos los encuestadores son médicos, entrenados específicamente para esta entrevista. Los cuestionarios que se aplican en el estudio GEFA-HT-UY están basados en cuestionarios validados en el estudio EPOGH(2-6) y fueron especialmente adaptados a nuestro medio.
Medidas antropométricas
Las medidas antropométricas así como el resto de los estudios se realizan un día diferente a la entrevista, pero dentro de las siguientes tres semanas a la misma, en la policlínica del área geográfica definida. Se solicita a los sujetos que no realicen ejercicio físico, no fumen y no beban café, mate o alcohol en las dos horas previas a la cita en policlínica.
El peso corporal se mide utilizando una balanza de impedancia (SECA Supraplus 720, Alemania) con el sujeto utilizando ropa liviana y sin zapatos. Se registran todas las variables indicadoras de la composición corporal por bioimpedancia, ajustadas para sexo, edad y biotipo. La altura se determina usando un tallímetro adosado a una pared, y los pliegues cutáneos son medidos en el lado izquierdo del cuerpo, a nivel del ángulo inferior de la escápula y de la porción media del tríceps, utilizando una pinza de presión constante (Harpender, Inglaterra).
En esta misma cita se procede a la medida de la PA en el consultorio con la técnica descrita más adelante.
Electrocardiograma
Con el sujeto acostado en posición supina se registra un electrocardiograma (ECG) estándar de 12 derivaciones, utilizando una computadora portátil y un amplificador Cardiax(r) (Mesa, Alemania). Las 12 derivaciones se graban de forma simultánea durante 32 segundos, siguiendo las guías actuales para registro electrocardiográfico(7).
Presión arterial por técnica auscultatoria
La PA periférica se mide por técnica ausculatoria utilizando esfigmomanómetro de mercurio, con el sujeto sentado en tres oportunidades diferentes; dos de ellas en el domicilio del participante separadas por dos a cuatro semanas (PA-dom) y una de ellas en el consultorio de la policlínica (PA-cons). Se realizan cinco mediciones cada vez (separadas por un minuto), las cuales se promedian para el análisis estadístico. En la mayoría de los sujetos se utilizan manguitos de tamaño estándar de 22 por 12 cm. Si la circunferencia del brazo es mayor a 31 cm, se utilizan manguitos de tamaño apropiado según lo recomendado por las guías vigentes(8). Los investigadores del estudio GEFA-HT-UY que participan de la medida de la PA fueron entrenados especialmente en el método auscultatorio para reconocer las fases I (sístole) y V (diástole) de Korotkoff y para medir con una precisión de 2 mmHg, de acuerdo con las guías de la British Hypertension Society(9). Cada seis meses se realizan sesiones para testear la precisión de las mediciones y reentrenar a los investigadores participantes. El reentrenamiento consiste en comparar las mediciones realizadas por el investigador con las de un panel de 20 expertos siguiendo un video de entrenamiento (Blood Pressure Measurement, British Medical Association, Inglaterra). Sus lecturas no deben diferir más de 5 mmHg con respecto a las determinadas por el panel de expertos.
Automonitoreo de la presión arterial
Para la realización del automonitoreo de la presión arterial (MAPA) en domicilio, los voluntarios son entrenados por un integrante del equipo de investigación. El investigador entrena y corrobora que el sujeto haya comprendido cada paso del procedimiento y sea capaz de reproducirlo en el domicilio de forma estandarizada. Los sujetos deben medir su PA sentados, tres veces en la mañana (antes del desayuno) y tres veces en la tarde (antes de la cena) durante siete días consecutivos. Para realizar este procedimiento cada participante recibe un aparato oscilométrico automatizado (Omron M10, Japón) programado para medir la PA tres veces consecutivas, separadas por un intervalo de un minuto. Adicionalmente, el participante recibe instrucciones escritas e ilustradas que ayudan a seguir el procedimiento de forma estandarizada y una planilla para completar con los valores de las mediciones. Al finalizar el período de medición (siete días) el participante entrega el equipo y los registros son extraídos de la memoria a una computadora (Omron Health Management Software). Para el análisis se utiliza el promedio de la PA sistólica y diastólica de los siete días.
Velocidad de onda de pulso e índice de aumentación sistólica por tonometría
Para la caracterización de la rigidez arterial por VOP e índice de aumentación sistólica (AIx) se utiliza el dispositivo SphygmoCor (AtCor Medical, Australia). Luego de 15 minutos de reposo en posición supina registramos la onda de pulso a nivel de la arteria radial derecha y de la arteria carótida común derecha mediante tonometría de aplanamiento utilizando un micromanómetro de alta fidelidad (SPC-301, Millar Instruments, Inc, Texas, Estados Unidos) interconectado con un equipo provisto del software SphygmoCor (versión 8.2, AtCor Medical, Australia) para el procesamiento de los datos. Este software calcula automáticamente el score del operador en base a la variabilidad sistólica y diastólica de ondas sucesivas, la uniformidad de la altura de la onda de pulso y la amplitud de la señal. Se consideran válidos para el análisis únicamente aquellos registros con un score de operador superior a 85%. A partir de la señal de pulso periférica (radial y carotídea), calibrada con la medida de PA a nivel braquial, el software calcula la onda de pulso central aórtica y la presión aórtica central (sistólica y diastólica), utilizando una función de transferencia que ha sido previamente validada en estudios poblacionales(10-12). La VOP aórtica se mide a través de registros secuenciales de la onda de pulso a nivel carotídeo y femoral, el tiempo de tránsito entre dos puntos se obtiene a partir de la diferencia entre el registro electrocardiográfico y la señal de pulso. A su vez, se miden las distancias entre el hueco supraesternal y el punto de registro carotídeo (distancia A) y entre el hueco supraesternal y el punto de registro femoral (distancia B). La distancia recorrida por la onda de pulso se calcula como distancia B menos distancia A. El tiempo de tránsito es el promedio de diez latidos consecutivos. La VOP es la distancia (en metros) dividida por el tiempo de tránsito (en segundos). Se considera el índice de aumentación sistólica periférico (radial) como la diferencia entre el segundo y el primer pico de la onda de pulso, expresado como porcentaje de la presión de pulso. El índice de aumentación (AIx) sistólico central (aórtico) se define como la relación entre el segundo y el primer pico de la onda de pulso, expresado como porcentaje de la presión de pulso aórtica.
Monitoreo ambulatorio de la presión arterial
El monitoreo ambulatorio de la presión arterial (MAPA) se obtiene con un dispositivo oscilométrico (Mobil-O-Graph 24h PWA Monitor, IEM, Alemania), utilizando manguitos seleccionados con el mismo criterio que para las mediciones de PA en consultorio y domicilio. Los equipos se programan para obtener registros cada 20 minutos durante la vigilia y cada 30 minutos durante el sueño. Se incluyen para el análisis únicamente las primeras 24 horas del registro ambulatorio de PA. El intervalo diurno se define como el período entre la hora 10.00 y la hora 20.00, y el nocturno entre la hora 0.00 y la hora 6.00, con la finalidad de eliminar los períodos de transición donde ocurren cambios rápidos de la PA en la mayoría de los sujetos. Todos los MAPA se realizan en días laborales, con el sujeto realizando su actividad habitual.
Velocidad de onda de pulso, índice de aumentación y presión arterial central ambulatoria
El monitor Mobil-O-Graph 24h PWA incluye la aplicación ARCSolver(13) que permite el análisis de la onda de pulso central y la estimación de la VOP aórtica. El algoritmo ARCSolver incluido en el monitor construye la onda de pulso central a través de la función de transferencia tal como ha sido descrito por Weber(14). Para el análisis ambulatorio de la onda de pulso, después de cada medición de la PA (cada 20 minutos en el día y cada 30 minutos durante la noche), se realiza automáticamente una segunda insuflación del manguito hasta el nivel de la PA diastólica y allí se registra la onda de pulso durante 10 segundos, utilizando un sensor de presión de alta fidelidad (MPX5050, Freescale, Tempe, Estados Unidos). Para la calibración de cada medida, el dispositivo utiliza la medición de la PA realizada inmediatamente antes. La función de transferencia incluida en el software ARCSolver cuenta con un algoritmo que permite comprobar la calidad de cada señal de pulso en base a parámetros similares a los del Sphygmocor, en una escala que va de 1 a 4. Los resultados calificados con 1 o 2 ("excelentes" y "buenos", respectivamente) implican que los registros fueron realizados en forma satisfactoria en más del 80% o del 50% de los ciclos cardíacos, respectivamente. Los registros calificados con puntaje 3 o 4 tienen menor porcentaje de ciclos grabados de forma satisfactoria y son considerados de mala calidad. En este estudio se incluyen únicamente los registros de calidad 1 o 2. El modelo utilizado por el software para estimar la VOP central considera la resistencia y la complacencia arteriales y calcula la VOP a partir de la reconstrucción de la onda de pulso central, la impedancia(15) y la edad(13), basado en el concepto de que el trabajo del ventrículo izquierdo está sujeto a un principio de optimización(16).
Ecocardiograma
Las imágenes son adquiridas en el Laboratorio de Ecocardiografía del Centro Cardiovascular Universitario del Hospital de Clínicas Dr. Manuel Quintela. Se utiliza un equipo SIEMENS modelo Sequoia con una sonda transtorácica de 4 MHz que permite adquirir imágenes en los modos M, bidimensional, doppler continuo, pulsado, color y tisular. Se utiliza el software para evaluar deformación miocárdica (strain y strain rate). Para la adquisición y la interpretación de los resultados obtenidos se aplican los criterios establecidos en las guías de ecocardiografía vigentes(17). Se guardan imágenes sincronizadas con ECG simultáneo, un latido. Posteriormente se procesan las imágenes obtenidas y se realiza la comparación interobservador de lo informado en cada caso con dos observadores cuya reproducibilidad ha sido demostrada. Se emplea el protocolo habitual de estudio transtorácico, con vistas paraesternal eje largo y eje corto, apical cuatro cámaras y cinco cámaras, apical dos cámaras y tres cámaras, supraesternal y subxifoidea.
Laboratorio
El día previo a la extracción de sangre cada sujeto recolecta orina de 24 horas utilizando un envase plástico de boca ancha (e-Medical, Uruguay). El día de la extracción de sangre el participante concurre a la policlínica con un ayuno de 8 horas y entrega la orina de 24 horas y una muestra de orina fresca. Un investigador mide la diuresis y realiza la extracción de sangre. Las muestras de sangre y orina se mantienen a una temperatura de 4 °C por no más de dos horas, hasta ser trasladadas al Laboratorio Central del Hospital Universitario. En las muestras de sangre frescas se determina: glicemia, insulinemia, creatinina, urea, ácido úrico, perfil lipídico, ionograma, funcional y enzimograma hepático y hemograma; y en las muestras de orina: iones, proteínas y creatinina. A su vez, las muestras son guardadas en alícuotas en freezer de -80 °C para determinaciones posteriores que incluyen cistatina C y albuminuria.
Filtrado glomerular
El filtrado glomerular se estima considerando: raza, sexo, edad y creatininemia utilizando la fórmula CKD-EPI(18). Adicionalmente, se mide el aclaramiento de creatinina, obteniendo la creatininuria de la muestra de orina de 24 horas. Para la determinación del aclaramiento de creatinina se le brinda a cada individuo instrucciones claras y un instructivo ilustrado sobre cómo realizar la recolección de orina de 24 horas.
La concentración de creatinina en las muestras de sangre y orina se obtiene utilizando la técnica de Jaffé(19), con las modificaciones descritas(20,21), utilizando un autoanalizador Cobas 6000 (Roche, Alemania) y utilizando los reactivos suministrados por el fabricante. El aclaramiento de creatinina (ClCr) ajustado a superficie corporal se calcula con la siguiente fórmula ClCr = [creatininuria (mg/dl) x diuresis (ml) x 1,73 (m2)] / [creatininemia (mg/dl) x tiempo de recolección (min) x superficie corporal (m2)]. El cálculo de la superficie corporal se realiza con fórmula de Mosteller(22). La determinación de cistatina -C se realiza mediante inmuno-turbidimetría utilizando un autoanalizador Cobas 6000 (Roche, Alemania) y los reactivos proporcionados por el fabricante. El filtrado glomerular estimado únicamente a partir de la cistatina -C plasmática o en combinación con creatininemia se estima utilizando ecuaciones descritas previamente en la literarura(23,24).
Análisis genético
Para el análisis genético se almacenan muestras de sangre en las que previamente se separó la capa leucocitaria mediante centrifugación a 1.500 g durante 10 minutos. Las muestras se almacenan a -80 °C. La extracción de ácido desoxirribonucleico (ADN) se realiza en nuestro laboratorio utilizando el kit comercial Quick- gDNA(r) Mini Prep (ZYMO Research, Estados Unidos). El análisis genético de las principales vías involucradas en el control de la PA (identificación de genes candidatos y caracterización genotípica) lo realizaremos utilizando un metabolochip con el que se procesa el conjunto de las muestras del consorcio EPOGH (Cattedra e Scuola di Nefrologia, Universita' Vita e Salute San Raffaele, Milán, Italia). El control de calidad de las muestras para ADN será realizado por duplicado en nuestro laboratorio y en el laboratorio del Study Coordinating Centre, Hypertension and Cardiovascular Rehabilitation Unit, Department of Molecular and Cardiovascular Research, de la Universidad Católica de Lovaina.
Eventos cardiovasculares y renales en el seguimiento
El seguimiento se iniciará a partir de los dos años de reclutamiento y a intervalos no mayores de tres años. Se pesquisará la ocurrencia de muerte y causa de muerte así como la ocurrencia de eventos cardiovasculares y renales no fatales. Dentro de los eventos cardiovasculares no fatales se buscará la ocurrencia de infarto agudo de miocardio, revascularización miocárdica, insuficiencia cardíaca y stroke. Dentro de los eventos renales pesquisaremos ingresos por insuficiencia renal, y desarrollo de alteraciones renales en ingresos por otras causas, episodios de cólicos nefríticos, ingresos por cirugía de las vías urinarias (prostatectomía, nefrectomía, litotomía, etcétera), derivación de la vía urinaria (nefrostomía, sonda vesical, etcétera) e ingreso a plan de sustitución de función renal en cualquier modalidad. La pesquisa se realizará mediante entrevista de seguimiento y se confirmará contra documento de historia clínica proporcionada por el sujeto o su institución de asistencia médica. Adicionalmente, las mediciones de PA en todas sus modalidades así como las medidas de rigidez arterial, ecocardiografía, filtrado glomerular y proteinuria durante el seguimiento nos permitirán detectar cambios en los resultados de estas pruebas funcionales independientemente de la ocurrencia de eventos clínicos. Las pérdidas de seguimiento deben minimizarse en el seguimiento de una cohorte, dado que habitualmente no ocurren al azar y por tanto son una fuente potencial de sesgo. Para minimizar este fenómeno se han diseñado las siguientes estrategias: se seleccionó una población que registra baja movilidad; cada participante tiene dos investigadores (duplicado) encargados de supervisar la recolección e ingresar los datos a la base (case database manager); al momento de invitarlo a participar del estudio se le entrega al candidato un material impreso que detalla todas las fases del proyecto y concientiza al participante sobre la importancia de aportar datos durante el seguimiento y se programaron devoluciones del avance del proyecto a intervalos anuales para mantener el contacto y la motivación de los participantes. Además, el diseño orientado a registrar familias contribuye a minimizar la pérdida de datos, ya que proporciona fuentes de información alternativa y cercana al sujeto. Finalmente, manteniendo estricta confidencialidad, se realizará cruzamiento con bases de datos que realizan seguimiento de eventos renales y cardiovasculares (Programa de Salud Renal, Registro Uruguayo de Diálisis, base de datos de procedimientos cardiovasculares del Fondo Nacional de Recursos, etcétera), para rastrear eventos en sujetos perdidos de seguimiento.
Análisis estadístico
Para el análisis estadístico se utilizó el software SAS 9.2. La comparación de medias entre ambos sexos para las variables continuas se realizó mediante test de t y para las variables categóricas mediante test de chi2 o test de Fisher si alguna de las frecuencias esperadas fue menor a 5%. Se consideró significativo un valor de p menor a 0,05.
Resultados
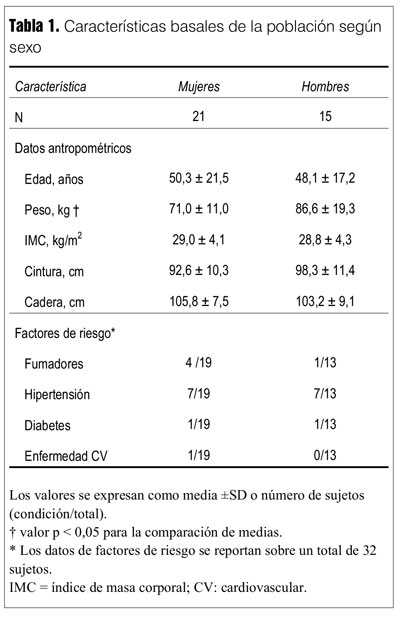
Al momento de este reporte hay 52 sujetos reclutados, 36 de los cuales (21/36 mujeres) han completado todo el protocolo y se incluyen en este análisis. El promedio (±SD) de edad fue de 49,4 ± 19,6 años, el peso corporal fue de 77,6 ± 14,7 kg, el índice de masa corporal (IMC) de 29,0 ± 4,1 kg/m2 y la circunferencia de la cintura de 94,9 ± 10,3 cm. Cinco de los participantes en el estudio eran fumadores activos (13,8%), nueve reportaron consumo frecuente de alcohol (25,0%), catorce eran hipertensos ya diagnosticados previamente (38,8%) y dos refirieron tener diabetes (5,5%). La tabla 1 muestra estas características generales por sexo. Encontramos diferencias significativas únicamente en el peso corporal (mujeres 71,0 ± 11,0 kg versus hombres 86,6 ± 19,3 kg; p = 0,01).
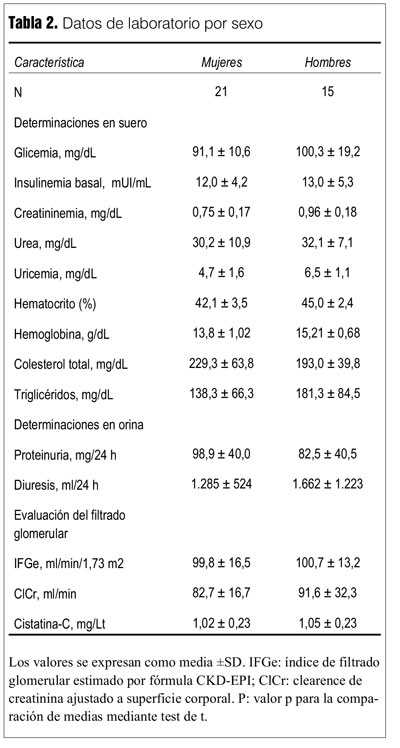
Con respecto a los resultados de laboratorio el promedio (±SD) de glicemia de ayuno fue de 94,5 ± 14,8 mg/dL; el colesterol total fue de 215,7 ± 58,1 mg/dL y la uricemia de 5,4 ± 1,7 mg/dl. El valor promedio de creatininemia (±SD) fue de 0,84 ± 0,20 mg/dl; el filtrado glomerular estimado (CKD-EPI) fue de 100 ± 14 ml/min/1,73m2; el clearence de creatinina medido y ajustado a superficie corporal (n = 25) fue de 86,3 ± 24,0 ml/min y la concentración de cistatina -C fue de 1,05 ± 0,23 mg/L. La recolección de orina de 24 horas mostró un volumen promedio de 1.435 ± 885 ml y la excreción diaria de proteínas fue de 93 ± 41 mg/día. Al momento de este reporte ningún participante presentó filtrado glomerular estimado (CKD-EPI) inferior a 60 ml/min/1,73 m2 (rango 74-132 ml/min/1,73m2) ni proteinuria de 24 horas superior a 300 mg/día (rango 20-190 mg/día). Sin embargo, la evaluación del filtrado glomerular mediante clearence de creatinina ajustado a superficie corporal identificó a tres sujetos con valores inferiores a 60 ml/min (rango 48,3-137,6 ml/min) (tabla 2).
En lo que refiere a los valores de PA, la media (±SD) en domicilio medida por médico fue de 127,0 / 77,5 (14,0) mmHg mientras que en consultorio fue de 123,9 (15,1) / 75,3 (11,3) mmHg. Para el MAPA, la media (±SD) fue de 122,8 (18,2) mmHg de presión sistólica y 77,3 (14,3) mmHg de presión diastólica. En el automonitoreo de PA, los promedios fueron de 123,5 (19,3) / 76,6 (12,1) mmHg, para la PA sistólica / diastólica, respectivamente.
Los promedios (±SD) de hemodinamia central obtenidos en reposo (SphygmoCor) fueron presión central (cPA) sistólica 116 ± 19,9 mmHg, cPA diastólica 81,6 ± 15,5 mmHg, cPP 34,6 ± 9,9 mmHg, VOP 9,1 ± 3,1 m/s y AIx: 26,1 ± 15,4. Los valores de PA central registrados de forma ambulatoria (Mobil-O-Graph) fueron cPA sistólica 111,6 ± 15,3 mmHg; cPA diastólica 77,5 ± 14,5; cPP 34,1 ± 10,6 mmHg, VOP; 7,4 ± 1,7 m/s y AIx: 24,9 ± 14,4.
No se presentan resultados de ecocardiografía, dado que al momento de este reporte solo se ha realizado esta técnica en menos de diez sujetos.
Discusión
En Uruguay existen varios reportes de datos transversales sobre HTA y otros factores de riesgo cardiovasculares(25-27) Sin embargo, los datos surgidos del seguimiento de cohortes son escasos, parciales, retrospectivos y/o discontinuos. Por este motivo existen algunas limitaciones para analizar la exposición a factores de riesgo y su relación con la aparición de eventos cardiovasculares y enfermedad renal con datos de nuestra población. El estudio GEFA-HT-UY se propone realizar un seguimiento longitudinal a largo plazo. Los datos presentados en este informe son una aproximación inicial a los resultados transversales que arrojará el estudio una vez que se complete el reclutamiento de la cohorte proyectado para el primer semestre de 2014. Adicionalmente, al finalizar el reclutamiento estaremos en condiciones de buscar asociaciones entre rasgos genotípicos y fenotípicos. Los datos del análisis de riesgo, donde relacionaremos los datos basales de fenotipo y genotipo con la ocurrencia de eventos cardiovasculares y renales, fatales y no fatales, podrán obtenerse a partir de los dos años de seguimiento de la cohorte. En este artículo reportamos un bajo número de sujetos; sin embargo, el objetivo de este trabajo es presentar nuestro protocolo de estudio en funcionamiento, donde apostamos a la generación de un registro de datos basales obtenidos siguiendo elevados estándares de calidad, con controles periódicos propios y externos, lo que sin duda se reflejará en la confiabilidad de la información surgida de su análisis.
Uno de los aspectos más originales de este proyecto es la posibilidad de conocer el perfil en 24 horas de los valores de hemodinamia central, que a la fecha no han sido descritos en ninguna población. Los estudios epidemiológicos que relacionan el incremento de las cifras de PA, tanto de consultorio(28) como ambulatoria(29), con el riesgo de sufrir eventos cardiovasculares, lo hacen utilizando mediciones de la PA a nivel braquial, es decir a nivel periférico. Recientemente, algunos trabajos han propuesto que la PA central refleja mejor la carga a la que está sometido el ventrículo izquierdo, y por lo tanto sería un mejor predictor de riesgo cardiovascular(30,31). A lo largo de la vida, debido al envejecimiento, la rigidez de la pared arterial aumenta y la onda de pulso viaja a mayor velocidad. El método considerado gold standard para la medición de rigidez arterial es la velocidad de la onda de pulso, mientras que el análisis de la onda de pulso (AOP) es también un enfoque alternativo(32).
Los avances tecnológicos han permitido la estimación no invasiva de la onda de presión central, contando actualmente con valores de referencia de PA central en diversas poblaciones(33-35). Sin embargo, aunque la PA central refleja mejor que la periférica la sobrecarga impuesta al corazón y a la circulación cerebral(36), aún no se ha difundido su uso en la práctica clínica, en parte debido a que se trata de una técnica que requiere equipos costosos y cierto entrenamiento. Recientemente fue validado un método que permite realizar el AOP y la medición de la VOP de forma ambulatoria(14), siendo este un aspecto aún no estudiado a nivel poblacional. La figura 1 muestra el resultado de un estudio que realizamos en Uruguay para evaluar la factibilidad de valorar las características ambulatorias de la PA central y la rigidez arterial. En este trabajo describimos, por primera vez, el perfil en 24 horas de la VOP, del índice de aumentación y de PA central(37). A diferencia de la tonometría de aplanamiento clásica, esta nueva metodología basada en el método oscilométrico tiene la ventaja de no requerir un operador entrenado y brinda información de los cambios en la rigidez arterial con el sujeto en movimiento, tanto durante la vigilia como durante el sueño. En este contexto, los valores de la PA ambulatoria central así como la VOP deben ser caracterizados y comparados con las mediciones de PA convencional y ambulatoria en la población general. Una vez obtenidos datos de eventos fatales y no fatales, analizaremos en base a datos poblacionales si esta novedosa manera de evaluar en forma no invasiva parámetros de la hemodinamia central aporta significativamente en la predicción de riesgo sobre las mediciones de PA periférica convencional y ambulatoria. La variada información de genotipo y fenotipo que se recoge con altos estándares de calidad así como el seguimiento longitudinal que realizaremos en el estudio GEFA-HT-UY constituyen la fortaleza de este trabajo que en un futuro próximo aportará información original y trascendente sobre aspectos novedosos como este y otros clásicos, pero con datos nacionales. Finalmente, destacamos la gran potencialidad que tiene este estudio para sumar y analizar nuevos aspectos del conocimiento que surjan durante el seguimiento de la cohorte.
Abstract
Introduction: essential high blood pressure results from complex interactions between genotype, phenotype and the environment. The GEFA-HT-UY study aims to analyse the role of different cardiovascular and renal phenotypic traits and their connection with genetic and environment factors in a random sample of the population in Montevideo.
Method: cohort observational and analytical study of the population. The study which was first designed and planned in 2011, being data collected in April 2012. The sample consists of 150 families (approximately 450 individuals), randomly chosen from the population in a certain geographical area in Montevideo. Basal determinations include recording relevant events in medical history, anthropometric measures, blood pressure measurements at home, at physician's office, self-monitoring of blood pressure and ambulatory monitoring of peripheral and central blood pressure. ECG, echocardiogram and arterial stiffness are recorded. Blood and urine samples are taken for biochemical tests, with a focus on risk factors for cardiovascular disease and chronic kidney disease, as well as evidence of target organ damage. During follow up the incidence of new cardiovascular and renal events will be evaluated.
Results: this publication aims to inform the protocol, and also to present the results for the first 36 individuals who have already completed it. Discussion: follow-up of the cohort will provide relevant and original data on hypertension and its association with the development of cardiovascular and kidney disease.
Resumo
Introdução: a hipertensão arterial essencial é o resultado de complexas interações entre o genótipo, o fenótipo e o ambiente. O estudo GEFA-HT-UY visa analisar o papel de diferentes características fenotípicas cardiovasculares e renais e sua relação com fatores genéticos e ambientais em uma amostra aleatória da população de Montevidéu.
Material e método: estudo de coorte populacional, observacional e analítico cuja planificação começou em 2011 e a coleta de dados em abril de 2012. A amostra está composta por 150 famílias (aproximadamente 450 pessoas), selecionadas de forma aleatória entre os habitantes de uma área geográfica delimitada de Montevidéu. As determinações basais incluiram registro de antecedentes médicos de relevância, medidas antropométricas, determinações de pressão arterial no domicilio, no consultório, auto-monitoramento de pressão arterial e monitoramento ambulatório de pressão arterial periférica e central. Foram realizados registros electrocardiográficos, ecocardiográficos e de rigidez arterial. Foram colhidas amostras de sangue e urina para determinações bioquímicas com especial ênfase nos fatores de risco cardiovascular e de doença renal crônica e a evidencia de dano de órgão alvo. Durante o seguimento se pesquisará a incidência de novos eventos cardiovasculares e renais.
Resultados: o objetivo desta publicação é comunicar o protocolo do estudo; no entanto se apresentam os resultados das primeiras 36 pessoas que completaram os estudos.
Discussão: o seguimento da coorte gerará dados relevantes e originais sobre a hipertensão arterial e sua relação com o desenvolvimento de patologias cardiovasculares e renais.
Bibliografía
1. Noboa O, Boggia J, Luzardo L, Márquez M. Hipertensión arterial y riñón. Rev Urug Cardiol 2012; 27(3):406-12.
2. Kuznetsova T, Staessen JA, Kawecka-Jaszcz K, Babeanu S, Casiglia E, Filipovsky J, et al. Quality control of the blood pressure phenotype in the European Project on Genes in Hypertension. Blood Press Monit 2002; 7(4):215-24.
3. European Project On Genes in Hypertension (EPOGH) Investigators, Stolarz K, Staessen JA, Kawecka-Jaszcz K, Brand E, Bianchi G, et al. Genetic variation in CYP11B2 and AT1R influences heart rate variability conditional on sodium excretion. Hypertension 2004; 44(2): 156-62.
4. European Project on Genes in Hypertension (EPOGH) Investigators, Wojciechowska W, Staessen JA, Stolarz K, Nawrot T, Filipovský J, Tichá M, et al. Association of peripheral and central arterial wave reflections with the CYP11B2 -344C allele and sodium excretion. J Hypertens 2004; 22(12):2311-9.
5. European Project On Genes in Hypertension (EPOGH) Investigators, Cwynar M, Staessen JA, Tichá M, Nawrot T, Citterio L, Kuznetsova T, et al. Epistatic interaction between alpha-and gamma-adducin influences peripheral and central pulse pressures in white Europeans. J Hypertens 2005; 23(5):961-9.
6. European Project On Genes in Hypertension (EPOGH) investigators, Tikhonoff V, Staessen JA, Kuznetsova T, Thijs L, Hasenkamp S, Bäumer V, et al. SAH gene variants revisited in the European Project On Genes in Hypertension. J Hypertens 2008; 26(2):244-50.
7. Society for Cardiological Science and Technology; British Cardiovascular Society. Clinical Guidelines by Consensus: recording a standard 12-lead electrocardiogram. An approved methodology, 2010. Disponible en: http://www.scst.org.uk/resources/consensus_guideline_for_recording_a_12_lead_ecg_Rev_072010b.pdf [Consulta: abril de 2013].
8. Council on High Blood Pressure Research Professional and Public Education Subcommittee, American Heart Association, Pickering TG, Hall JE, Appel LJ, Falkner BE, Graves JW, Hill MN, et al. Recommendations for blood pressure measurement in humans: an AHA scientific statement from the Council on High Blood Pressure Research Professional and Public Education Subcommittee. J Clin Hypertens (Greenwich) 2005; 7(2):102-9.
9. Subcommittee of Professional and Public Education of the American Heart Association Council on High Blood Pressure Research, Pickering TG, Hall JE, Appel LJ, Falkner BE, Graves J, Hill MN, et al. Recommendations for blood pressure measurement in humans and experimental animals: Part 1: blood pressure measurement in humans: a statement for professionals from the Subcommittee of Professional and Public Education of the American Heart Association Council on High Blood Pressure Research. Hypertension 2005; 45(1):142-61.
10. Chen CH, Ting CT, Nussbacher A, Nevo E, Kass DA, Pak P, et al. Validation of carotid artery tonometry as a means of estimating augmentation index of ascending aortic pressure. Hypertension 1996; 27(2):168-75.
11. Chen CH, Nevo E, Fetics B, Pak PH, Yin FC, Maughan WL, et al. Estimation of central aortic pressure waveform by mathematical transformation of radial tonometry pressure. Validation of generalized transfer function. Circulation 1997; 95(7):1827-36.
12. Pauca AL, O'Rourke MF, Kon ND. Prospective evaluation of a method for estimating ascending aortic pressure from the radial artery pressure waveform. Hypertension 2001; 38(4):932-7.
13. Wassertheurer S, Kropf J, Weber T, van der Giet M, Baulmann J, Ammer M, et al. A new oscillometric method for pulse wave analysis: comparison with a common tonometric method. J Hum Hypertens 2010; 24(8):498-504.
14. Weber T, Wassertheurer S, Rammer M, Maurer E, Hametner B, Mayer CC, et al. Validation of a brachial cuff-based method for estimating central systolic blood pressure. Hypertension 2011; 58(5):825-32.
15. Chirinos JA, Segers P. Noninvasive evaluation of left ventricular afterload: part 2: arterial pressure-flow and pressure-volume relations in humans. Hypertension 2010; 56(4):563-70.
16. Wassertheurer S, Mayer C, Breitenecker F. Modeling arterial and left ventricular coupling for non-invasive measurements. Simul Model Pract Theory 2008; 16(8):988-97.
17. American Society of Echocardiography, Gottdiener JS, Bednarz J, Devereux R, Gardin J, Klein A, Manning WJ, et al. American Society of Echocardiography recommendations for use of echocardiography in clinical trials. J Am Soc Echocardiogr 2004; 17(10):1086-119.
18. CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration),Levey AS, Stevens LA, Schmid CH, Zhang YL, Castro AF 3rd, Feldman HI, et al. A new equation to estimate glomerular filtration rate. Ann Intern Med 2009; 150(9):604-12.
19. Jaffe M. Über den Niederschlag, welchen Pikrinsäure in normalem Harn erzeugt und über eine neue Reaction des Kreatinins. Z Physiol Chem 1886; 10:391-400.
20. Bowers LD, Wong ET. Kinetic serum creatinine assays. II. A critical evaluation and review. Clin Chem 1980; 26(5):555-61.
21. Peake M, Whiting M. Measurement of serum creatinine-current status and future goals. Clin Biochem Rev 2006; 27(4):173-84.
22. Mosteller RD. Simplified calculation of body-surface area. N Engl J Med 1987; 317(17):1098.
23. Rule AD, Bergstralh EJ, Slezak JM, Bergert J, Larson TS. Glomerular filtration rate estimated by cystatin C among different clinical presentations. Kidney Int 2006; 69(2):399-405.
24. Tidman M, Sjöström P, Jones I. A Comparison of GFR estimating formulae based upon s-cystatin C and s-creatinine and a combination of the two. Nephrol Dial Transplant 2008; 23(1):154-60.
25. Sociedad Uruguaya de Cardiología, Comité de Hipertensión Arterial, Bianchi M, Fernández Cean JM, Carbonell ME, Bermúdez C, Manfredi JA, Folle LE. Encuesta epidemiológica de hipertensión arterial en Montevideo: prevalencia, factores de riesgo, plan de seguimiento. Rev Méd Urug 1994; 10(2):113-20.
26. Schettini C, Bianchi M, Nieto F, Sandoya E, Senra H. Ambulatory blood pressure: normality and comparison with other measurements. Hypertension Working Group. Hypertension 1999; 34(4 Pt 2):818-25.
27. Uruguay. Ministerio de Salud Pública. Dirección General de Salud. División Epidemiología. 1a Encuesta Nacional de Factores de Riesgo de Enfermedades Crónicas no Trasmisibles. Montevideo: MSP, 2006.
28. Kannel WB, Schwartz MJ, McNamara PM. Blood pressure and risk of coronary heart disease: the Framingham Study. 1969. Chest 2009; 136(5 Suppl):e23.
29. International Database on Ambulatory blood pressure monitoring in relation to Cardiovascular Outcomes (IDACO) investigators, Boggia J, Li Y, Thijs L, Hansen TW, Kikuya M, Björklund-Bodegård K, et al. Prognostic accuracy of day versus night ambulatory blood pressure: a cohort study. Lancet 2007; 370(9594):1219-29.
30. Willum-Hansen T, Staessen JA, Torp-Pedersen C, Rasmussen S, Thijs L, Ibsen H, et al. Prognostic value of aortic pulse wave velocity as index of arterial stiffness in the general population. Circulation 2006; 113(5):664-70.
31. CAFE Investigators; Anglo-Scandinavian Cardiac Outcomes Trial Investigators; CAFE Steering Committee and Writing Committee, Williams B, Lacy PS, Thom SM, Cruickshank K, Stanton A, Collier D, et al. Differential impact of blood pressure-lowering drugs on central aortic pressure and clinical outcomes: principal results of the Conduit Artery Function Evaluation (CAFE) study. Circulation 2006; 113(9):1213-25.
32. European Network for Non-invasive Investigation of Large Arteries, Laurent S, Cockcroft J, Van Bortel L, Boutouyrie P, Giannattasio C, Hayoz D, et al. Expert consensus document on arterial stiffness: methodological issues and clinical applications. Eur Heart J 2006; 27(21):2588-605.
33. European Project on Genes in Hypertension (EPOGH) Investigators, Wojciechowska W, Staessen JA, Nawrot T, Cwynar M, Seidlerová J, Stolarz K, et al. Reference values in white Europeans for the arterial pulse wave recorded by means of the SphygmoCor device. Hypertens Res 2006; 29(7):475-83.
34. Reference Values for Arterial Stiffness' Collaboration. Determinants of pulse wave velocity in healthy people and in the presence of cardiovascular risk factors: 'establishing normal and reference values'. Eur Heart J 2010; 31(19):2338-50.
35. Farro I, Bia D, Zócalo Y, Torrado J, Farro F, Florio L, et al. Pulse wave velocity as marker of preclinical arterial disease: reference levels in a uruguayan population considering wave detection algorithms, path lengths, aging, and blood pressure. Int J Hypertens 2012; 2012:169359.
36. O'Rourke MF, Adji A. Basis for use of central blood pressure measurement in office clinical practice. J Am Soc Hypertens 2008; 2(1):28-38.
37. Luzardo L, Lujambio I, Sottolano M, da Rosa A, Thijs L, Noboa O, et al. 24-h ambulatory recording of aortic pulse wave velocity and central systolic augmentation: a feasibility study. Hypertens Res 2012; 35(10):980-7.














