Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Médica del Uruguay
versión On-line ISSN 1688-0390
Rev. Méd. Urug. vol.28 no.2 Montevideo jul. 2012
Prevención de hepatitis A mediante vacunación en Uruguay (2005-2010)
Dras. Claudia Romero *, Virginia Perdomo †, Flavia Chamorro *, Elizabeth Assandri *, María Catalina Pírez ‡, Alicia Montano ‡
Facultad de Medicina. Universidad de la República. Centro Hospitalario Pereira Rossell. Uruguay
Resumen
Introducción: la hepatitis A es un problema sanitario en países en vías de desarrollo. Objetivos: describir estrategias para controlar hepatitis A mediante vacunación. Describir evolución de número de casos, tasas y brotes entre 2005-2010. Material y método: estudio descriptivo retrospectivo 2005-2010. Se analizan: -Estrategias utilizadas por Ministerio de Salud Pública (MSP) para controlar hepatitis A mediante vacunación: bloqueo de brotes; población de riesgo e inclusión universal de vacuna. -Descripción: número de casos de hepatitis A en Uruguay y Artigas; número de brotes en ciudades, barrios, familia y otros; número de casos/edad. Resultados: se registraron 21 brotes. Se aplicaron 16.715 primeras dosis y 11.354 segundas dosis. Entre el 10 de setiembre de 2007 y el 26 de noviembre de 2007, el MSP y el Ministerio de Desarrollo Social realizaron una campaña de vacunación dirigida a niños de entre 1 y 5 años del subsector público. Docentes y estudiantes de Medicina de la Universidad de la República apoyaron y difundieron la campaña. Se aplicaron 44.716 primeras dosis y 25.095 segundas dosis. En 2008 se incluye la vacuna en dos dosis en el esquema de vacunación, obligatoria y gratuita. La tasa país disminuyó de 69,6 a 2,7 entre 2005 y 2010 (p<0,05); en el departamento de Artigas de 780,57/100.000 en 2005 a 0,66 en 2010 (p<0,05). Durante 2005-2008 ocurrieron 22 brotes en ciudades; en 2010 se registraron escasos brotes intrafamiliares y en escuelas. El descenso de número de casos de 2005 a 2010 fue significativo en todas las edades. Comentario: del 2005 al 2010 se produjo una disminución significativa y sostenida del número de brotes y tasas de hepatitis A en Uruguay.
Palabras clave: HEPATITIS A - prevención y control VACUNAS CONTRA LA HEPATITIS A
Keywords: HEPATITIS A - prevention & control HEPATITIS A BACINES
* Prof. Adjunta de Clínica Pediátrica, Facultad de Medicina, Universidad de la República. Uruguay.
† Ex-Asistente de Clínica Pediátrica, Facultad de Medicina, Universidad de la República. Uruguay. ‡ Profesora Titular de Clínica Pediátrica, Facultad de Medicina, Universidad de la República. Uruguay.Correspondencia: Dra. Virginia Perdomo. Luis Melián Lafinur 1864/402. Montevideo, Uruguay. Correo electrónico: vnaranja5@hotmail.com
Recibido: 9/1/12. Aceptado: 22/6/12
Conflicto de intereses: las autoras declaran que no existen conflictos de intereses.
Introducción
La infección por el virus de hepatitis A (HVA) tiene distribución mundial, constituyendo un problema sanitario en países en vías de desarrollo(1).
Las regiones y los países se clasifican según la ocurrencia de número de casos por 100.000 habitantes. La endemicidad se relaciona fuertemente con las condiciones higiénico-sanitarias de los países(1).
Si bien la mayoría de los casos de hepatitis aguda a virus A presentan una evolución benigna autolimitada, existen formas clínicas prolongadas con recaídas y 0,1% a 0,2% de los casos evolucionan a fallo hepático agudo(1-3).
El número de casos sintomáticos aumenta con la edad. En niños menores de 5 años la enfermedad generalmente es asintomática. El 30% de los casos en niños mayores de 5 años y el 70% de los casos en adultos son sintomáticos, aumentando la morbilidad. En América Latina es la causa más frecuente de trasplante hepático en niños(4).
Se dispone de vacunas inactivadas, eficaces y seguras para prevenir la enfermedad(5-9). Los países que han mejorado las condiciones higiénico-sanitarias y han adoptado la utilización universal de la vacunación han logrado disminuir la incidencia de esta enfermedad no solo en la franja etaria de los niños vacunados, sino en todas las edades, demostrando la protección de rebaño conferida por la vacuna. Casos pioneros de esto son, por ejemplo, Estados Unidos e Israel(10-14).
Argentina es la primera nación de América Latina que desde el año 2005 incluye la vacuna en forma universal contra HVA, aplicando un esquema de dosis única a niños de 12 meses de edad. La protección contra la enfermedad obtenida con una sola dosis de vacuna es de 95% a 99%(5-7). En ese país, la incidencia de falla hepática aguda por HVA constituía un problema de salud, siendo la primera causa de trasplante hepático(15-18). Previo al 2005, en Argentina y en Chile se utilizó la vacuna de hepatitis A para bloqueo epidemiológico de brotes, obteniéndose buenos resultados(19,20).
En Uruguay, antes del año 2007, la HVA era una enfermedad endémica que presentaba brotes epidémicos en niños y adultos jóvenes. Antes del año 2004 se notificaban alrededor de 4.000 casos/año. En el año 2005 se notificaron 2.256 casos con una incidencia de 69,6/100.000 habitantes. Estas cifras pueden estar sesgadas por la subnotificación.
A fines del año 2004 y principios del 2005 ocurrieron brotes de hepatitis A en el departamento de Artigas. En la ciudad de Bella Unión de ese departamento, la tasa de ataque alcanzó en febrero a 2.987/100.000 habitantes. Esto determinó que el Ministerio de Salud Pública (MSP) indicara por primera vez la vacunación como estrategia de bloqueo de brotes en esa y otras ciudades del país. En los años siguientes se vacuna, además, a niños con riesgo de adquirir hepatitis A, asistidos en el subsector público de salud. Finalmente, en el año 2008 se inició la vacunación universal(21,22).
Objetivos de este trabajo:
- Describir las estrategias utilizadas por el MSP en Uruguay para el control de la infección por virus de hepatitis A mediante la utilización de la vacuna en el período 2005-2010.
- Describir la evolución del número de casos, tasas y brotes de hepatitis A en el período 2005-2010.
Material y método
Se realizó un estudio descriptivo retrospectivo que comprendió desde el año 2005 al 2010. Se analizaron:
- Estrategias utilizadas por el MSP para el control de hepatitis A mediante el uso de la vacuna: bloqueo de brotes (2005-2007); vacunación a población de riesgo (2007) e inclusión de la vacuna en forma universal (2008). La vacunación para todas las estrategias se realizó con un esquema de dos dosis separadas por seis meses.
- Evolución del número de casos de hepatitis A en el país, en el departamento de Artigas y en la ciudad de Bella Unión en el período 2005-2010. Se seleccionaron ese departamento y esa ciudad por presentar la mayor incidencia en Uruguay en dicho período.
- Evolución del número de brotes en ciudades, barrios, familias y otros, en el período 2005-2010.
- Evolución del número de casos por edad en el período 2005-2010.
Se utilizaron las denuncias de casos de hepatitis A realizadas en la División Epidemiología del MSP y los datos disponibles on line en el sector de Notificación obligatoria de enfermedades *. La Comisión Honoraria de la Lucha Antituberculosa y Enfermedades Prevalentes (CHLA-EP) proporcionó el número y la distribución geográfica de las dosis de vacuna de hepatitis A aplicadas.
Datos poblacionales. Para el cálculo de tasas se utilizaron los datos poblacionales aportados por el Instituto Nacional de Estadística (INE) del censo 2004**. Uruguay tiene una población de 3.241.003 habitantes. El departamento de Artigas cuenta con una población de 78.019 habitantes y la ciudad de Bella Unión de ese departamento, 13.187 habitantes.
Definición de caso de hepatitis. Se define como aquel paciente que tiene un test positivo para inmunoglobulina M específica o tiene clínica compatible con esta enfermedad y un nexo epidemiológico con un caso de hepatitis A.
Definición de brote. Se define como el aumento del número de casos o la presencia de dos o más casos relacionados epidemiológicamente, de aparición súbita y diseminación localizada en un espacio específico.
Análisis estadístico
Se aplicó análisis descriptivo. Se calculó incidencia anual de casos/100.000 habitantes con intervalos de
confianza de 95% (IC 95%) para Uruguay, el departamento de Artigas y la ciudad de Bella Unión. Se calculó
la incidencia anual del país para los grupos etarios utilizados: 0-3, 4-6, 7-14 y ? 15 años. El grado de
asociación univariado se examinó mediante el uso de la prueba exacta de Fisher o prueba de dos colas con corrección de Yates, o ambos, según fuera apropiado. Todos los valores de probabilidad informados fueron de dos colas y p<0,05 fue considerado estadísticamente significativo. El sistema de computación utilizado fue Epitable del programa Epi-info versión 6.0.
Resultados
- Estrategias utilizadas por el MSP para el control de hepatitis A mediante el uso de vacuna. Número de dosis aplicadas en cada estrategia:
- Bloqueo de brotes epidémicos. Entre el 2005 y el 2007 se notificaron 21 brotes de hepatitis A en Uruguay. Entre octubre de 2004 y febrero del 2005 ocurrió un importante número de brotes de hepatitis A en el departamento de Artigas. En la ciudad de Bella Unión de ese departamento la tasa de ataque alcanzó en febrero a 2.987,79/100.000 habitantes. En el año 2005 se inicia el bloqueo epidemiológico de brotes con la vacuna antihepatitis A en ese departamento, recomendándose la vacunación de niños entre 2 y 4 años. El MSP proporcionó en forma gratuita y no obligatoria las dosis de vacunas para el bloqueo de estos brotes. En ese departamento se administraron primeras dosis de vacuna a 4.769 niños y segundas dosis a 2.859 niños. El número de dosis de vacunas de hepatitis A aplicadas para el bloqueo de brotes epidémicos en el período 2005-2007 se muestra en la tabla 1.
- Vacunación a población de riesgo. En el año 2007, el MSP y el Ministerio de Desarrollo Social (MIDES) lanzan una campaña dirigida a aumentar las tasas de cobertura de las vacunas incluidas en el Programa Ampliado de Inmunizaciones (PAI). En esta campaña se recomendó la vacunación contra HVA de niños entre 12 y 59 meses incluidos en el Programa de Asistencia Nacional de Emergencia Social (PANES) y niños entre 12 y 23 meses, beneficiarios del subsector público de salud. Esta constituye una medida tendiente a promover la salud de la población. La campaña de vacunación se desarrolló entre el 10 de setiembre de 2007 y el 26 de noviembre de ese año. Los estudiantes y docentes del séptimo año de la carrera de Doctor en Medicina de la Universidad de la República se integraron a esta campaña de vacunación como actividad de extensión universitaria(23). Colaboraron en la promoción y ejecución de la misma mediante la coordinación de acciones con instituciones gubernamentales y no gubernamentales, instituciones de salud, medios de comunicación, empresas farmacéuticas y comerciales y mediante la realización de actividades lúdico-recreativas que promovieron la vacunación. La meta era vacunar a 30.000 niños dentro de esa población de riesgo. Durante los tres meses de campaña reciben la primera dosis 44.716 niños en todo el país. A los seis meses reciben la segunda dosis 25.095 niños, correspondiendo al 56% de los que recibieron la primera.
- Inclusión de la vacuna en forma universal. El 10 de marzo de 2008 se incluye en forma obligatoria y gratuita la vacuna de hepatitis A a nivel nacional, con dos dosis a los 15 y 21 meses. Se realiza "catch-up" para los niños nacidos en el año 2007. La cobertura con la primera dosis de los 48.243 niños nacidos en el 2007 fue de 74%.
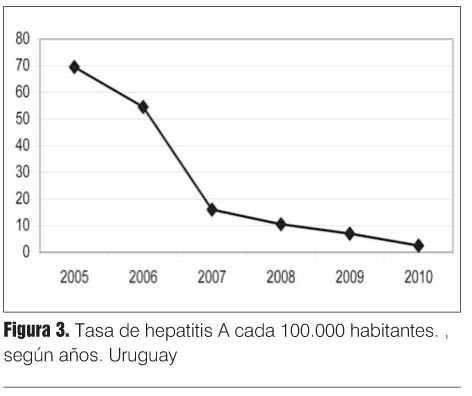
- Evolución del número de casos y tasas de hepatitis A en el país en el departamento de Artigas y en la ciudad de Bella Unión en el período 2005-2010. En el año 2005, la tasa de hepatitis A en Artigas alcanza la cifra de 780,57/100.000 (IC 95%, 717-841) habitantes y en la ciudad de Bella Unión 2.987,79/100.000 (IC 95%, 2.704-3.208). En las figuras1 y 2se muestra la evolución de las tasas de incidencia en el departamento de Artigas y en la ciudad de Bella Unión en el período 2005-2010. Con la intervención realizada para el control de la enfermedad en el año 2005 (bloqueo de brotes), la tasa disminuye significativamente en el año 2006 a 21,78/100.000 habitantes para el departamento de Artigas y 30,33/100.000 habitantes en la ciudad de Bella Unión (p < 0,05). En el 2010, las tasas fueron de 3,8/100.000 (IC 95%, 0,5 - 8,1) habitantes en Artigas y 0/100.000 en Bella Unión. En la tabla 2 se compara el número de casos y la incidencia (IC 95%) de hepatitis A a nivel nacional entre los años 2005-2010. En la figura 3 se muestra el descenso sostenido de las tasas de incidencia por 100.000 habitantes en el país en el período 2005-2010.
- Evolución del número de brotes en ciudades, barrios, familiares y otros brotes, en el período 2005-2010. Durante el período 2005-2007 se registran 21 brotes en ciudades del país. Posteriormente se observa un importante descenso en los brotes de ciudad, observándose solo brotes intrafamiliares, en escuelas y campamentos en los años 2009 y 2010. Estos datos se muestran en la tabla 3.
- Evolución del número de casos por edad. En la figura 4 se muestra el descenso sostenido de las tasas de incidencia por 100.000 habitantes según franjas etarias en el período 2005-2010.
Discusión
La prevención de las enfermedades por medio de vacunas es el gran reto del siglo XXI. Nuevas vacunas de probada eficacia y casi nulos efectos colaterales están disponibles en la actualidad(24). Por otra parte, las complejas tecnologías utilizadas para lograr varias de las vacunas hoy disponibles, han encarecido su inclusión en forma universal; esto ha dificultado la inmunización de niños que viven en condiciones económicas desfavorables, causando alta morbilidad e inaceptable mortalidad. Para la hepatitis A es claro que las medidas tendientes a mejorar las condiciones de vida (acceso al agua potable, mejoras en la eliminación de las excretas, adhesión a medidas de higiene ambiental y personal), causan impacto positivo en la disminución de la prevalencia de esta enfermedad en Uruguay, como en otros países de la región(1). Afrontar la enfermedad significa un costo importante para los gobiernos, la sociedad y las familias. La disponibilidad de vacunas seguras y eficaces que han probado casi erradicar la enfermedad en los países que las incluyeron en forma universal, transforma este problema en un dilema ético que todos las naciones deberían discutir(6-10). Para los países latinoamericanos el beneficio económico de la vacunación resulta igual o aun mayor que si se consideran los costos derivados de la pérdida de días laborables o las pérdidas económicas por expectativa de años perdidos cuando se mueren niños o adultos jóvenes(25,26). En Uruguay, el elevado costo en la atención directa de los casos y en la prevención de los contactos (que durante muchos años se realizó con gammaglobulina) y la necesidad, aunque excepcional, de trasplantes hepáticos costosos realizados fuera del país, justifican ampliamente el gasto en esta vacuna. Durante más de una década los pediatras en Uruguay realizaron gestiones para la inclusión de la vacuna de hepatitis A en el esquema nacional de vacunación. Este país, con tradición de incluir vacunas con cierta celeridad, incorpora la misma en forma obligatoria y gratuita en marzo de 2008.
Conclusión
Entre las estrategias utilizadas por el MSP para disminuir la aparición de casos de hepatitis A en Uruguay, la incorporación de la vacuna en el calendario nacional en niños en esquema de dos dosis produjo un descenso sostenido de las tasas de incidencia de hepatitis A, con desaparición de la existencia de brotes en ciudades y barrios.
Las otras dos estrategias (campaña de vacunación para el control de brotes y vacunación a población de riesgo, 2005-2007) se acompañaron de una disminución estadísticamente significativa del número de brotes y tasas de esa enfermedad aun considerando que solo recibieron la segunda dosis el 68% de los niños.
Agradecimientos
Dr. Fernando Arrieta. Comisión Honoraria de la Lucha Antituberculosa y Enfermedades Prevalentes.
Dra. Teresa Picón. Ministerio de Salud Pública. Directora del Programa Ampliado de Inmunizaciones.
Summary
Introduction: Hepatitis A is a health problem in developing countries.
Objectives: To describe strategies to control Hepatitis A through immunization. To describe the evolution of the number of cases, rates and outbreaks from 2005 through 2010.
Method: Retrospective descriptive study covering the 2005-2010 period of time. The following was analysed:
- Strategies used by the Ministry of Public Health to control Hepatitis A through immunization: blocking of outbreaks; population at risk; universal immunization.
- Description: Number of cases of Hepatitis A in Uruguay, and in the department of Artigas; number of outbreaks in cities, neighborhoods, families and other; number of cases/age.
Results: 21 outbreaks were recorded. 16.715 first doses and 11.354 second doses were applied. From 10 September, 2007 through 26 November, 2007 the Ministry of Public Health and the Ministry of Social Development conducted an immunization campaign aimed at children in the public sub-sector who were between 1 and 5 years old. Professors at the School of Medicine of the University of the Republic and medical students supported and contributed to the dissemination of the campaign. 44.716 first doses and 25.095 second doses were applied. In 2008 the two dose vaccine is included in the mandatory and free immunization plan.
The national rate dropped from 69.6 to 2.7 from 2005 through 2010 (p<0,05); and in the department of Artigas from 780.57/100.000 in 2005 to 0.66 in 2010 (p<0,05).
Between 2005 and 2008 there were 22 outbreaks in cities, in 2010 few intra-family outbreaks and in schools were registered.
The decrease in the number of cases from 2005 through 2010 was significant for all ages.
Comment: A significant and sustained decrease of Hepatitis A outbreaks and rates was evidenced in Uruguay from 2005 through 2010.
Resumo
Introdução: a hepatite A é um problema sanitário nos países em vias de desenvolvimento.
Objetivos: Descrever estratégias para controlar hepatite A por vacinação. Descrever a evolução do número de casos, taxas e surtos entre 2005-2010.
Material e método: estudo descritivo retrospectivo 2005-2010. Foram analisadas:
- Estratégias utilizadas pelo Ministério de Salud Pública (MSP) para controlar a hepatite A por vacinação: bloqueio de surtos; população de risco; inclusão universal da vacina.
- Descrição: número de casos de hepatite A no Uruguai e especificamente no departamento de Artigas; número de surtos en cidades, bairros, famílias e outros; número de casos/idade.
Resultados: foram registrados 21 surtos. Foram aplicadas 16.715 primeiras doses e 11.354 segundas doses. Entre o dia 10 de setembro de 2007 e o dia 26 de novembro de 2007, o MSP e o Ministério de Desenvolvimento Social realizaram una campanha de vacinação dirigida a crianças entre 1 e 5 anos do setor público. Docentes e estudantes de Medicina da Universidad de la República apoiaram e difundiram a campanha. Foram aplicadas 44.716 primeiras doses e 25.095 segundas doses. Em 2008 a vacina em duas doses foi incluída ao esquema de vacinação, obrigatória e gratuita.
La taxa país diminuiu de 69,6 a 2,7 entre 2005 y 2010 (p<0,05); no departamento de Artigas passou de 780,57/100.000 em 2005 a 0,66 em 2010 (p<0,05).
Durante 2005-2008 foram registrados 22 surtos em cidades; em 2010, foram registrados poucos surtos intrafamiliares e em escolas.
A redução do número de casos de 2005 a 2010 foi significativa em todas as idades.
Comentário: de 2005 a 2010 observou-se uma diminuição significativa e mantida do número de surtos e das taxas de hepatite A no Uruguai.
Referencias bibliográficas
1. Montano A, Barañano R, Lageard B, Moratorio G, Dibarboure H, García A, et al. Prevalencia de hepatitis A en niños de 2 a 14 años y en población laboral de 18 a 49 años en Montevideo, Uruguay. Rev Méd Urug 2001; 17(2): 84-98.
2. Quian J, Ruttiman R, Matrai L. Prevalencia de anticuerpos contra hepatitis A en una población de Montevideo. Arch Pediatr Urug 2005; 76(2): 100-5.
3. Ciocca M. Clinical course and consequences of hepatitis A infection. Vaccine 2000; 18(Suppl 1): S71-4.
4. Ciocca M, Moreira-Silva SF, Alegría S, Galoppo MC, Ruttiman R, Porta G, et al. Hepatitis A as an etiologic agent of acute liver failure in Latin America. Pediatr Infect Dis J 2007; 26(8): 711-5.
5. Van Der Wielen M, Vertruyen A, Froesner G, Ibáñez R, Hunt M, Herzog C, et al. Immunogenicity and safety of a pediatric dose of a virosome-adjuvanted hepatitis A vaccine: a controlled trial in children aged 1-16 years. Pediatr Infect Dis J 2007; 26(8): 705-10.
6. Dagan R, Amir J, Livni G, Greenberg D, Abu-Abed J, Guy L, et al. Concomitant administration of a virosome-adjuvanted hepatitis a vaccine with routine childhood vaccines at age twelve to fifteen months: a randomized controlled trial. Pediatr Infect Dis J 2007; 26(9): 787-93.
7. López EL, Del Carmen Xifró M, Torrado LE, De Rosa MF, Gómez R, Dumas R, et al. Safety and immunogenicity of a pediatric formulation of inactivated hepatitis A vaccine in Argentinean children. Pediatr Infect Dis J 2001; 20(1): 48-52.
8. Riedemann S, Reinhardt G, Ibarra H, Frösner GG. Immunogenicity and safety of a virosomal hepatitis A vaccine (Epaxal) in healthy toddlers and children in Chile. Acta Paediatr 2004; 93(3): 412-4.
9. Bovier PA, Bock J, Loutan L, Farinelli T, Glueck R, Herzog C. Long-term immunogenicity of an inactivated virosome hepatitis A vaccine. J Med Virol 2002; 68(4): 489-93.
10. Lieberman JM, Word BM, Jacobs RJ, Dagan R, Marchant CD. Universal hepatitis A vaccination in the United States: a call for action. Pediatr Infect Dis J 2008; 27(4): 287-91.
11. Wasley A, Samandari T, Bell BP. Incidence of hepatitis A in the United States in the era of vaccination. JAMA 2005; 294(2): 194-201.
12. Dagan R, Leventhal A, Anis E, Slater P, Ashur Y, Shouval D. Incidence of Hepatitis A in Israel following universal immunization of toddlers. JAMA 2005; 294(2): 202-10.
13. Centers for Disease Control and Prevention. Prevention of Hepatitis A through active or passive immunization: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR 2006; 55(RR 07): 1-30.
14. Belmaker I, Dukhan L, Yosef Y, Leventhal A, Dagan R. Elimination of Hepatitis A infection outbreaks in day care and school settings in southern Israel after introduction of the national universal toddler hepatitis A immunization program. Pediatr Infect Dis J 2007; 26(1): 36-40.
15. Argentina. Ministerio de Salud y Ambiente de la Nación. Dirección de Epidemiología. Hepatitis A: documento técnico especial. Bol Epidemiol Periódico 2005; 3: 3-15. Disponible en: http://msal.gov.ar/htm/site/sala_situacion/PANELES/boletines/boletin_especial_HAV2.pdf [Consulta: 12 de noviembre de 2010]
16. Argentina. Ministerio de Salud de la Nación. Dirección de Epidemiología. Enfermedades de declaración obligatoria en todo el país hasta la semana 40 de 2006. Bol Epidemiol Periódico 2006; p.20. Disponible en: http://msal.gov.ar/htm/site/sala_situacion/PANELES/boletines/boletin_BEP31.pdf [Consulta: 12 de noviembre 2010]
17. Argentina. Ministerio de Salud de la Nación. Calendario Nacional de Vacunación de la República Argentina. Disponible en: http://www.msal.gov.ar/htm/calendario vacunacion 2007.html [Consulta: 18 de diciembre 2009]
18. Cervio G, Trentadue J, D´Agostino D, Luque C, Saa G, Sánchez C, et al. Fulminant hepatic failure: the argentine experience over 10 years in four liver transplant center. Simposio Latinoamericano, Iberoamericano y Colombiano Gastroenterología, Hepatología y Nutrición Pediátrica, 2. Cartagena, Colombia, abril 19-21 de 2007.
19. Chile. Ministerio de Salud. Departamento de Epidemiología. Situación de las Enfermedades de notificación obligatoria: situación de la hepatitis A en Chile, enero a junio/julio 2003. Disponible en: http://epi.minsal.cl/evigant/Numero20/evigia/html/notific/hepa/hepa1.htm [Consulta: 20 de enero 2011]
20. Cofré J, Abarca K. Vacuna anti hepatitis A. Rev Chil Infect 2003; 20(4): 243-52. Disponible en: http://www.scielo.cl/pdf/rci/v20n4/art04.pdf [Consulta:20 de enero de 2011]
21. Uruguay. Ministerio de Salud Pública. Certificado esquema de vacunación año 2008: informe al cuerpo médico y personal de salud. Disponible en: http://www.msp.gub.uy/ucepidemiologia_1710_1.html [Consulta: 21 de enero de 2011 ]
22. Uruguay. Ministerio de Desarrollo Social. Más de la mitad de los niños del Panes fueron vacunados contra la hepatitis A. Disponible: http://www.mides.gub.uy/noticias/lr071107. html. Noviembre 17 [Consulta: 24 de junio 2009 ]
23. Romero C, Chamorro F, Perdomo V, Assandri E, Giachetto G, Montano A, et al. Uruguay: Faculty of Medicine plays mayor role in National Vaccination Campaign. Immun Newsl 2010; 32 (3): 1, 3-4.
24. Organización Panamericana de la Salud. El siglo de las vacunas. OPS Ahora 2004. Disponible en: http://www.paho.org/spanish/dd/pin/ahora11_jul04.htm [Consulta: 12 de noviembre de 2010]
25. Valenzuela MT, Jacobs RJ, Arteaga O, Navarrete MS, Meyerhoff AS, Innis BL. Cost-effectiveness of universal childhood hepatitis A vaccination in Chile. Vaccine 2005; 23(32): 4110-9.
26. López E, Debbag R, Coudeville L, Baron-Papillon F, Armoni J. The cost-effectiveness of universal vaccination of children against hepatitis A in Argentina: results of a dynamic health-economic analysis. J Gastroenterol 2007; 42(2): 152-60.














