Services on Demand
Journal
Article
Related links
Share
Revista Médica del Uruguay
On-line version ISSN 1688-0390
Rev. Méd. Urug. vol.25 no.2 Montevideo June 2009
Centro especializado primario en ataque cerebrovascular.
Primera experiencia en Uruguay - Informe preliminar
Dres. Eduardo J. Legnani*, Hugo Tarigo*, Cecilia Legnani†,
Patricia Braga†, Mónica Bagés‡
Departamento de Neurología de la Cooperativa Médica de Canelones (COMECA) de la Federación Médica del Interior (FEMI). Uruguay
Resumen
Introducción: los centros especializados en ataque cerebrovascular (ACV) o Stroke (CES) tienen por objetivo mejorar la prevención, asistencia y rehabilitación de pacientes afectados por un ACV.
Objetivos: exponemos nuestra experiencia, fortalezas y carencias en el primer Centro Especializado Primario en Stroke (CEPS) de Uruguay, desarrollado en la Cooperativa Médica de Canelones (COMECA) en el primer año de trabajo.
Material y método: es un centro de adultos, de fase aguda y de seguimiento intra y extrahospitalario. Criterios de inclusión: pacientes adultos, menos de tres días de instalación del cuadro, de cualquier gravedad e internados en el sanatorio 1 de COMECA. Incluye hemorragia subaracnoidea (HSA), hemorragia parenquimatosa (HP) e infarto cerebral (INF).
Es multidisciplinario, con actividad totalmente protocolizada y computarizado.
Resultados: se incluyeron 45 pacientes: INF 69%, HP 20% y HSA 11%. La mortalidad precoz fue 13%, asociada fundamentalmente a HP y a mayor severidad al inicio. La duración media de estadía fue de nueve días.
Conclusiones: las características poblacionales y cifras de mortalidad son comparables a otros centros. La duración de la estadía se acerca a los mejores resultados internacionales. Los actuales resultados no tienen valor epidemiológico, los que se darán con el paso del tiempo.
Palabras clave: ACCIDENTE CEREBROVASCULAR.
UNIDADES DE TERAPIA INTENSIVA.
Keywords: STROKE.
INTENSIVE CARE UNITS.
* Médico neurólogo. Uruguay.
† Profesora adjunta de neurología. Facultad de Medicina, Universidad de la República. Uruguay.
‡ Médico neurólogo. Ex Ayudante y Asistente del Departamento de
Histología y Embriología. Facultad de Medicina, Universidad de la República. Uruguay.
Correspondencia: Dr. Eduardo Legnani.
Treinta y Tres 459. Canelones, Uruguay
Correo electrónico: elegnani@montevideo.com.uy
Recibido: 20/10/08.
Aceptado: 20/4/09.
Introducción
El ataque cerebrovascular (ACV) o Stroke ocupa el tercer lugar en causas de muerte en la mayoría de los países desarrollados y determina, además, discapacidad en un alto porcentaje de los sobrevivientes. En nuestro país contamos con datos recabados en un reciente estudio retrospectivo realizado por el Instituto de Neurología, basado en los certificados de defunción por ACV(1). Resumiendo los resultados correspondientes a los diez últimos años del estudio (1997-2006), se observaron tasas de mortalidad que oscilaban entre 96,5 y 114 muertes por ACV cada 100.000 habitantes/año, constituyendo 11% de todas las defunciones en forma constante en dicho período. En forma más gráfica y utilizando los números crudos, podemos decir que un promedio de 3.500 personas fallecieron anualmente por ACV en Uruguay.
Los centros especializados en ACV o CES, también denominados unidades de Stroke (US), fueron creados en la década de 1960 con criterios similares a las unidades coronarias: optimizar racionalmente el diagnóstico, el tratamiento y la recuperación de los pacientes aquejados con esta patología(2), disminuir costos y hacer docencia(3). Esto es, contribuyen a mejorar el conocimiento para una mejor prevención, asistencia y rehabilitación de los pacientes afectados por un ACV(4-8). En particular, se ha demostrado que las US disminuyen la morbimortalidad a corto y largo plazo, mejoran la relación costo-efectividad y son beneficiosas para todo tipo de ACV, independientemente de la edad y la gravedad inicial(9).
Hay dos tipos de CES(7): 1) Centro especializado primario de Stroke (CEPS)(3) con la infraestructura, personal y programas necesarios para estabilizar y tratar la mayoría de los pacientes afectados de stroke. 2) Centros de gran alcance (Comprehensive Stroke Centers) en condiciones de realizar, por su diseño, las más complejas acciones y, por tanto, ser centros de referencia para centros primarios.
En este contexto, desde el 1º de abril de 2007, COMECA puso en funcionamiento su CEPS, para atender a los pacientes afectados por una patología prevalente y que tiene una elevada morbimortalidad en el adulto. Al cumplirse el primer año de actividad, y siendo el primer centro multidisciplinario para manejo exclusivo del paciente con ACV en funcionamiento en el país, presentamos los resultados de nuestro trabajo.
Objetivos
Los objetivos específicos al desarrollar nuestro CEPS fueron: 1) generar un equipo multidisciplinario trabajando en forma coordinada para la asistencia del paciente con ACV; 2) la optimización de las estrategias diagnósticas urgentes y racionalización de los estudios paraclínicos; 3) disminuir el tiempo desde el inicio del ACV hasta el inicio de la terapéutica; 4) proveer a los pacientes del mejor tratamiento específico disponible en forma homogénea, y 5) asegurar a todos los pacientes la rehabilitación precoz y sostenida.
Material y método
Definición y concepto
Nuestro CEPS es un centro de adultos, limitado a la población afiliada a la institución. Fue concebido en el concepto de una unidad de ACV de modelo mixto(9), ya que incluye a los pacientes en fase aguda y rehabilitación, contando con equipo multidisciplinario, personal de enfermería entrenado y rehabilitación. No se desarrolla en una planta física exclusiva para estos pacientes, ni cuenta con camas de internación especialmente destinadas, estableciéndose bajo el modelo de sistema abierto en el cual el centro es una unidad funcional, no necesariamente espacial.
Infraestructura material
La planta física está ubicada en el sanatorio N° 1 de la ciudad de Canelones, y cuenta con tomografía axial computarizada (TAC) (CRECENSUR), electroencefalograma, ecografía y Doppler vasculares, angiografía, radiología, centro de tratamiento intensivo, laboratorio, cuatro blocks quirúrgicos y servicio de emergencia. La institución cuenta con servicio de asistencia prehospitalaria coordinado con la emergencia, conformado por el Servicio Emergencia Móvil Integral de COMECA (SEMIC). En la misma planta física se desarrolla el Centro de Cuidados Intensivos (UMIC) y el Área de Cuidados Intermedios (UCIC).
La resonancia nuclear magnéticoa (RNM) y el Doppler transcraneano son las próximas incorporaciones previstas; actualmente se contratan fuera de la institución.
Infraestructura profesional
El equipo médico actuante durante el primer año de funcionamiento estuvo integrado por los neurólogos Dr. Eduardo J. Legnani, Dr. Hugo Tarigo, Dra. Cecilia Legnani, Dra. Patricia Braga y Dra. Mónica Bagés; los neurocirujanos Dr. Eduardo Wilson, Dr. Saúl Wajskopf, Dr. Pablo García, Dr. Daniel Scioscia y Dr. Carlos Aboal. Ambos equipos funcionan en régimen de retén cubriendo todos los días del año, con una policlínica de neurocirugía y tres de neurología semanales. Se trabaja coordinadamente con un centro de fisiatría totalmente equipado, psiquiatría, tratamiento con toxina botulínica, nutricionista, fonoaudiólogo, cardiólogo, internista y todas las especialidades que hacen a una asistencia integral(3,10,11).
Población
La inclusión de pacientes con ACV en el protocolo del CEPS se definió mediante los siguientes criterios de inclusión y exclusión: pacientes adultos, con menos de tres días de instalación del cuadro neurológico agudo, cualquier nivel de gravedad inicial e internados en sanatorio Nº 1 de la institución para asegurar el seguimiento diario por parte del equipo actuante. Este concepto comprende pacientes con hemorragia subaracnoidea (HSA), hemorragia parenquimatosa (HP) e infarto cerebral (INF). Se excluyeron los ataques isquémicos transitorios (AIT), que algunos autores y centros incorporan; se consideran dentro de los factores de riesgo(5,6). En la clasificación del subtipo de ACV isquémico se siguieron las definiciones del TOAST (Trial of Org 10172 in Acute Stroke Treatment)(12).
Funcionamiento
La planificación del centro fue realizada por el equipo neurológico actuante de acuerdo a la realidad institucional y a la experiencia internacional(4-6,8,10). La actividad está totalmente protocolizada(4,5,13-16) y se trabaja en forma computarizada, en red con todos los servicios institucionales. El trabajo específico del CEPS, si bien coordinado con la atención prehospitalaria de la institución, comienza en la sala de emergencias con la recepción por personal de enfermería y médicos entrenados, realización de electrocardiograma (ECG), exámenes de laboratorio, TAC de cráneo y consulta inmediata con el neurólogo de retén. La definición del nivel de cuidados de internación requeridos para cada paciente se realiza por equipo multidisciplinario, con seguimiento diario por neurólogo, además de internista o intensivista.
La consulta cardiológica y estudios cardiovasculares (ecocardiograma transtorácico y eco Doppler de vasos de cuello) se realizan en forma estándar, habitualmente en las primeras 24-48 horas del ingreso, así como la evaluación por fisiatra e inicio de medidas de rehabilitación acordes a cada caso. Durante la asistencia del paciente en sanatorio se completa la evaluación clínica con la aplicación protocolizada de escalas de valor ponóstico(17): National Institute of Health Stroke Scale (NIHSS)(18,19), escala de Rankin modificada(20,21), escala de Fisher, test de deglución, Glasgow Coma Scale (GCS), score de Hunt Hess, escala de hemorragia intracraneal. Si existe indicación, se solicita precozmente la arteriografía de vasos con destino encefálico o el ecodardiograma transesofágico. Asimismo, el equipo neuroquirúrgico participa activamente no sólo en el manejo y la resolución de los paciente con HSA, sino también en la decisión y ejecución de procedimientos invasivos en pacientes con otras formas de ACV: evacuación de hematomas parenquimatosos, craneotomías decompresivas o colocación de dispositivos para monitorización de la presión intracraneana (tornillo de PIC). En nuestro CEPS no se realiza aún ningún tratamiento con trombolíticos ni técnicas invasivas de reperfusión cerebral en agudo. Los pacientes al alta son controlados en policlínicas por el equipo neurológico, fisiátrico y eventualmente neuroquirúrgico. El seguimiento neurológico incluye el control periódico de estudios realizados y tratamiento de prevención secundaria, así como la aplicación en cada consulta de las escalas NIHSS y Rankin modificada, seguimiento que también se encuentra protocolizado.
Cada tres meses se realizan jornadas de actualización con el personal no médico y médico no especializado, así como reuniones mensuales del equipo médico actuante.
Análisis de los datos
Toda la información de los pacientes ingresados al CEPS y su seguimiento es ingresada prospectivamente a una base de datos computarizada por los neurólogos a cargo de la asistencia, en un sistema en red institucional, a partir del cual se obtienen los datos primarios de la serie de pacientes.
El análisis estadístico de los datos se realizó mediante el Statistical Package for Social Sciences (2006, SPSS inc). La incidencia de ACV asistidos en el CEPS se calculó como el número de eventos nuevos acaecidos en el transcurso de un año que generaron su ingreso a la unidad, ponderado por el total de población en riesgo, considerada en este caso como el número total de socios adultos (mayores a 15 años) a la fecha del análisis. La descripción de las variables se expresó a través de porcentajes para variables cualitativas y medias con su correspondiente desvío estándar para variables cuantitativas continuas. Para el análisis bivariado se utilizó chi cuadrado para variables cualitativas y test de T para variables continuas. La comparación de los puntajes de las escalas al ingreso y egreso se realizó mediante prueba T para datos apareados. La comparación de medias de más de dos grupos se efectuó mediante ANOVA de un factor. En todas las pruebas utilizadas se consideró un nivel de significación a=0,05.
Resultados
El período considerado en la oportunidad de este informe preliminar comprende el primer año de trabajo del CEPS, y se extiende desde el 1º de abril de 2007 al 31 de marzo de 2008.
Con fines estadísticos es importante conocer que COMECA contaba con 34.000 afiliados hasta el 1º de enero de 2008; en los tres últimos meses del período considerado la cifra aumentó a 39.800, casi exclusivamente por incorporación de población infantil. Actualmente, 31.840 (80%) son adultos, 17.131 de sexo masculino (54%) y 14.709 de sexo femenino (46%).
La incidencia de ACV fue de 142/100.000 socios adultos, esto es 45 pacientes en este primer año. No son estos todos los pacientes con ACV atendidos en la institución, sino sólo aquellos que cumplieron con los criterios de inclusión-exclusión establecidos.
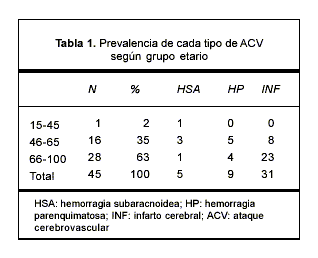
En este grupo de 45 pacientes, la distribución por sexos fue de 18 mujeres y 27 hombres (F: M, 0.67:1), con una media de edad de 69 ±11 años (rango 41-86). Se muestra la distribución por grupos etarios y naturaleza del ACV en la tabla 1: cinco fueron HSA, nueve HP y 31 INF.
Factores de riesgo modificables
Los factores de riesgo más frecuentes fueron la hipertensión arterial (HTA) (82%), cardiopatía (38%), ACV previo (27%), obesidad (24%) y tabaquismo (22%) (tabla 2). En esta población se encontró asociación entre cardiopatía y naturaleza isquémica (x2; p=0,06). La HTA fue igualmente prevalente en pacientes con infarto (26/31) y con HP (8/9) (x2; p=0,54).
Tipo de ACV
Hemorragia subaracnoidea: 5 pacientes
Se observaron tres sangrados de aneurismas del sector anterior del polígono de Willis, una disección espontánea de arteria vertebral y una HSA de etiología desconocida.
Hemorragia parenquimatosa: 9 pacientes.
En nuestra serie predominaron las hemorragias cerebrales (78%), y dentro de estas las ganglio-basales sobre las lobares. Se presentaron dos hematomas de tronco cerebral, en tanto no hubo ningún caso de hemorragia cerebelosa (figura 1).
Infarto: 31
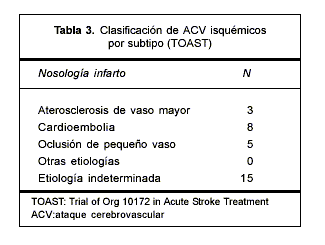
Del total de los infartos, 90% fueron supratentoriales, 10% infratentoriales. El territorio más frecuentemente infartado a nivel supratentorial fue el silviano (78%), seguido por el territorio de la arteria cerebral posterior en 22%; ningún infarto ocurrió en el territorio de la arteria cerebral anterior (figura 2). En cuanto a la nosología y siguiendo la clasificación propuesta en el TOAST, cinco infartos fueron secundarios a oclusión de pequeño vaso, tres por oclusión demostrada de vaso mayor, ocho infartos fueron cardioembólicos y en 15 no se pudo determinar la etiología con el algoritmo de estudio disponible (tabla 3).
Tratamiento
La demora en llegar al sanatorio de COMECA desde el inicio de los síntomas osciló entre menos de una hora y 69 horas; 38,6% de los pacientes fueron asistidos en las primeras tres horas del ACV, tiempo ventana potencial para trombolisis.
Dentro del tratamiento médico, todos los pacientes con infarto recibieron antiagregantes plaquetarios (ácido acetilsalicílico 325 mg/día) desde el diagnóstico. En todos los pacientes, la evaluación completa de los factores de riesgo vascular y el tratamiento de los mismos se realizó en forma individualizada en conjunto con internista del equipo.
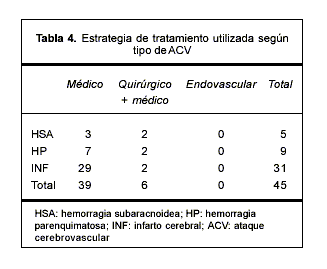
Se realizó tratamiento quirúrgico en seis pacientes, dos en cada tipo de patología: en los dos infartos operados se realizó craniectomía decompresiva, en tanto dos pacientes con HP requirieron evacuación quirúrgica y se efectuó clipado del aneurisma responsable de la HSA en dos de los cinco pacientes ingresados por este motivo. Treinta y nueve pacientes recibieron tratamiento exclusivamente médico (tabla 4).
Mortalidad
La mortalidad intrahospitalaria fue de 13% (seis pacientes) y todos ellos fallecieron por complicaciones neurológicas derivadas de su ACV. La distribución de mortalidad por tipo de ACV muestra una tendencia a asociar naturaleza hemorrágica y mortalidad: 26,7% de muertes en pacientes con ACV hemorrágico versus 6,7% en pacientes con INF (x2, p=0,063), sin alcanzar significación estadística, probablemente en relación con el pequeño tamaño poblacional. Dentro de los ACV hemorrágicos, se observó una mortalidad algo mayor de los pacientes con HP (33%) en comparación con aquellos con HSA (20%), pero los números son realmente pequeños para obtener conclusiones de valor (total de ACV hemorrágicos=15).
En cuanto a posibles predictores de mortalidad, los pacientes que fallecieron presentaban cuadros de extrema gravedad ya al ingreso, evidente clínicamente: una hemorragia de tronco, dos hematomas ganglio-basales totales, un hematoma lobar masivo; un infarto de tronco y una hemorragia meníngea grado 5 de Hunt-Hess. Esto es concordante con la evaluación por las escalas utilizadas al ingreso: el puntaje inicial en la escala NIHSS fue significativamente mayor en los pacientes que tuvieron una evolución fatal, con valores medios de 15 y 8,9 en pacientes que fallecieron y sobrevivieron respectivamente (test T; p=0,022). Asimismo, los pacientes que fallecieron presentaban menor GCS al ingreso: un score medio de 8 puntos versus 13,7 puntos en los pacientes sin evolución fatal (test T; p= 0,000).
En referencia al perfil temporal de la mortalidad, los datos se muestran en la tabla 5. Se observó una mediana de 8,5 días, destacándose como concepto que la mayoría de las muertes ocurren en los primeros diez días. El bajo número de pacientes no permite la evaluación de diferencias potenciales vinculables a la naturaleza del ACV.
Evolución medida por escalas
En la población total estudiada, sin diferenciar según la naturaleza del ACV, se observó un puntaje de déficit medido por la escala NIHSS promedio al ingreso de 8,44 y al egreso de 7,38, diferencia observada en plazo promedio muy breve, y no estadísticamente significativa (prueba T para datos apareados; p=0,11). Las evaluaciones por GCS y Rankin fueron aun menos sensibles para evidenciar diferencias en la situación clínica al egreso.
El puntaje inicial en la escala de NIHSS fue más bajo en pacientes con INF que en aquellos con HP: score medio de 8,6 puntos en INF versus 13,9 puntos en HP (test T; p=0,026).
Duración de la estadía
La duración media de la estadía en los sobrevivientes a su ACV fue de 9 ± 8 días (rango 2 a 41 días). Requirieron internación en CTI (UMIC) 11 pacientes (24%), y 9% adicional recibió internación en el área de cuidados intermedios (UCIC); 67% de los pacientes pudo ser manejado exclusivamente en sala general.
En los pacientes que sobrevivieron a su ACV, la duración media de la internación difirió significativamente en función de la naturaleza del mismo: 18 días en la HSA, 11 días en la HP y siete días en los INF (ANOVA; p=0,018).
Discusión
La literatura es concluyente acerca de los beneficios de los centros de Stroke(4-8,17,22,23,9). De la metodología desarrollada para cumplir con los objetivos específicos propuestos, destacamos que nuestro centro estableció criterios de inclusión y exclusión de pacientes que permitieron abarcar la compleja variedad de la patología, a la vez que aportaron la homogeneidad de infraestructura y abordaje necesarios para la coherencia asistencial. El desarrollo y la aplicación de un protocolo estandarizado y con el razonable margen de flexibilidad que hace a la buena práctica clínica, consideramos que fue un pilar para el cumplimiento de los objetivos de optimización diagnóstica y terapéutica. El funcionamiento sin planta física exclusiva, referido como modelo de menor eficacia(9), no ha perjudicado en nuestro caso la actividad del CEPS ni el resto de las actividades sanatoriales, dado el número de pacientes atendidos en un área de internación adecuada para los fines. En este sentido, es de destacar que el sanatorio N°1 de COMECA se desarrolla en una planta física con distribución horizontal de todos sus servicios. Es de particular importancia práctica la proximidad física entre las áreas de emergencia, cuidados especializados (UMIC, UCIC) y el servicio de tomografía computada, angiografía, ecografía y fisiatría, que se interconectan entre sí y con las salas de internación en un área total de 2.437 m2. La aceptación y participación del personal en las jornadas de actualización y en la protocolización asistencial ha sido masiva.
La incidencia de ACV observada es algo menor a la referida en la literatura internacional, de 200/100.000 habitantes(24), así como a la descripta a nivel nacional en el trabajo de Hochmann y colaboradores(25) en la ciudad de Rivera, de 181 casos/100.000 habitantes. Las características de la muestra: incidencia, edad, sexo; factores de riesgo, naturaleza y topografía más prevalentes de ACV, resultan en cifras similares a las de la literatura(8,11,26,27). Sólo el porcentaje de HSA está por encima de lo esperado, pero puede corresponder a una variación al azar dado el bajo número de casos hasta el momento. Consideramos de todas formas que el período de actividad no tiene una extensión suficiente para arribar a conclusiones epidemiológicas definitivas.
La mortalidad intrahospitalaria de 13% es similar a la descripta por Jorgensen y colaboradores(28), y es claramente inferior a la observada en un estudio previo en nuestro país (24,7%)(27) en un centro académico sin unidad de ACV en esa fecha; en ambos casos son estudios de poblaciones mixtas de ACV isquémico y hemorrágico. Nuestra cifra de mortalidad precoz es apenas superior a la observada en centros asistenciales no académicos en Argentina (10,6%)(29), de especial interés ya que ese estudio incluyó solamente infartos cerebrales. Al igual que en estos trabajos, la mortalidad intrahospitalaria está en clara relación con la gravedad inicial. De los parámetros de valor pronóstico en agudo, la naturaleza hemorrágica se asoció a mayor mortalidad, así como un menor puntaje de GCS y mayor puntuación de NIHSS, también en forma similar a lo descripto en la literatura(30,31). Paralelamente, los pacientes con hematoma tuvieron un puntaje de NIHSS al debut más alto que los infartos.
El hecho de no realizar trombolisis en nuestro centro simplifica el trabajo institucional y extrainstitucional (educación de la población, coordinación con los servicios de traslados y la emergencia dentro de la institución), habida cuenta que la aplicación de este tratamiento implica que el mismo se deba realizar dentro de las tres primeras horas y con criterios de indicación muy estrictos. Considerando únicamente el criterio temporal, 38% de los pacientes fue ingresado al centro en el plazo de esta ventana terapéutica, previo al desarrollo de cualquier tipo de campaña hacia la comunidad para una consulta precoz.
Considerando parámetros de valor evolutivo y para el seguimiento (outcome), las escalas NIHSS y Rankin mostraron valores similares ingreso/egreso. Esto no significa una falta de eficacia del CEPS en la recuperación del paciente, sino que estos valores están relacionados con que los datos que se presentan actualmente reflejan solamente la evolución intrahospitalaria y la evaluación funcional al término de la fase aguda, con un alta sanatorial precoz. Recordemos que la escala NIHSS es una escala de déficit, que consiste en una ponderación de los déficits observados en un examen neurológico protocolizado y resumido. Los hallazgos focales al examen clínico en el contexto de un ACV mejoran en forma gradual y parcial a medida que los mecanismos de compensación cerebral y rehabilitación fisiátrica hacen su labor, por lo cual los cambios significativos se evidencian en el seguimiento a mediano plazo. En concordancia con estos conceptos, la escala NIHSS fue en realidad originalmente diseñada y validada como predictor de evolución funcional a tres meses del ACV. Por otra parte, la escala de Rankin evalúa la reinserción funcional del paciente en actividades de vida diaria y eventualmente laborales, por lo que recién aporta datos en su real dimensión al ser aplicada en forma diferida. Es evidente, entonces, la necesidad de una evaluación funcional evolutiva con tiempos más prolongados y ya en la fase de seguimiento ambulatorio, que está incluida en el protocolo de seguimiento de los pacientes del CEPS y cuyos resultados podrán evaluarse más adelante.
Planteamos que la selección y el análisis de los parámetros de evaluación de los beneficios aportados por un CEPS(8) deben realizarse con cautela, dada la variabilidad de los pacientes y la complejidad de las interacciones entre los parámetros.
El parámetro más evidente y jerárquico sería la reducción en la tasa de mortalidad intrahospitalaria. En nuestro caso, lamentablemente no contamos con datos de mortalidad por ACV en la institución, previos a la creación del centro, debido a la reorganización del archivo institucional centralizado inmediatamente antes de nuestro trabajo. Tampoco contamos con datos disponibles de otros centros estrictamente comparables a esta etapa previa en nuestra institución, pero sí definimos que la mortalidad hallada es claramente inferior a la evidenciada en el Hospital de Clínicas en el período en que no contaba con un centro de Stroke, como fuera analizado previamente.
Un parámetro habitualmente utilizado es la duración de la estadía, pero en una revisión reciente(9) no se ha podido establecer un efecto homogéneo de la atención especializada en ACV sobre la misma. La duración de la estadía referida por cada centro dependerá también del modelo de unidad de ACV aplicado (fase aguda, rehabilitación). En este sentido, nuestra media de estadía de nueve días se aproxima a la mediana de estadía reportada en centros no académicos en la República Argentina (seis días) en un estudio multicéntrico reciente(29), en tanto que es francamente inferior a la verificada en el Hospital de Clínicas de nuestro país en 1998, previo al funcionamiento de un centro especializado en ACV(27). Más aún, si nos remitimos a los datos aportados en estudios que comparaban la performance de centros con y sin unidad de ACV, refiriendo una media de 8 a 162 días para grupos asistidos en unidad de ACV y 10 a 129 días en centros control, nuestra cifra se encuentra en el límite inferior de ambos rangos. Considerando que nuestro CEPS no se remite a la fase aguda, sino que inicia la rehabilitación y otorga el alta sólo una vez encaminada ésta y asegurada su continuidad, creemos que la duración de la estadía evidenciada en nuestro centro es una muestra de la eficacia del sistema, si bien su beneficio final para el paciente sólo podrá ser asegurado en seguimientos a seis y 12 meses como mínimo.
Dentro de los ítems cuantificables, otro punto clave es la optimización de costos. Hasta el momento sólo podríamos realizar una estimación parcial en base a los días de internación requeridos(32) y la necesidad de acceso a CTI. Por otra parte, se acepta que la duración de la estadía es el ítem que mayor incidencia tiene en los costos globales; es la que hace que en enfermos con igual patología, métodos de estudio y tratamiento se establezca la diferencia. Probablemente tenga relación con la gestión (que depende de varios factores) y no con la calidad asistencial.
Consideramos que los parámetros manejados en el CEPS no tienen el mismo valor en los beneficios generados por el mismo(8). En este sentido la inclusión de los infartos originados en pequeño vaso seguramente tienen un menor peso en el momento de evaluar los beneficios del CEPS, por lo menos en el corto plazo. A su vez, hay parámetros que son cuantificables (por ejemplo, días de estadía) mientras que otros son sobre todo de evaluación cualitativa (por ejemplo, la capacidad técnica del equipo actuante).
Conclusiones
Luego del primer año de funcionamiento del CEPS podemos concluir que las características de nuestra población encuadran dentro de las cifras internacionales. La mortalidad intrahospitalaria de 13%, aun dentro de cánones internacionales, es un claro marcador de la importancia de mejorar todavía más el abordaje y fundamentalmente la prevención de esta patología. La HTA y la cardiopatía fueron los factores de riesgo más frecuentes, denotando una vez más la importancia de las campañas de salud cardiovascular y el tratamiento precoz y óptimo de los mismos. Por otra parte, la duración de la internación promedio de nueve días marca la factibilidad de optimizar los tiempos de asistencia e internación de estos pacientes en nuestro medio.
Consideramos que estos centros constituyen un elemento de suma importancia para la prevención, tratamiento y recuperación de los pacientes afectados por un Stroke, reducen los días de internación, los costos y promueven la tecnificación del personal actuante. Son necesarios para un buen funcionamiento un equipo homogéneo neurológico y neuroquirúrgico con actividad diaria sin interrupciones, una estructura asistencial multidisciplinaria médica y no médica, un servicio de fisiatría con actividad permanente, una planta física con estructuras médicas y quirúrgicas adecuadas, paraclínica desarrollada, computarización y protocolización de toda la actividad.
Un análisis profundo de la problemática que implica el ACV debería abarcar no sólo la fase intrahospitalaria sino también la evolución a mediano y largo plazo. Un año de trabajo, con número acotado de pacientes, permite conclusiones parciales y limitadas. La introducción de la trombolisis y eventualmente otras técnicas planteará nuevos problemas organizativos y estructurales, incluso extrainstitucionales. Esta presentación es el paso inicial para un estudio más completo que se dará exclusivamente con el paso del tiempo.
Agradecimientos
El equipo actuante agradece al centro de cómputos y al archivo de COMECA la invalorable colaboración prestada para la elaboración de este informe.
Summary
Introduction: health care centers specialized in cerebrovascular accidents (CVA) or strokes (CES) aim to improve prevention, health care assistance and rehabilitation of patients affected by CVA.
Objetives: we present our experience along with the strengths and weaknesses found at the First Primary Care Center Specialized in Stroke (CEPS) in Uruguay, developed at the Canelones Medical Cooperative (COMECA) during the first year of work.
Methods: the center provides health care services to adult patients, both in acute phases and during intra-hospital and extra-hospital follow-up. Inclusion criteria: adult patient who were hospitalized at COMECA’s Sanatorio , under three days after the presentation of symptoms, all severity severity levels. It includes subarachnoid hemorrhage (SAH), parenchymatous hemorrhage (PH) and cerebral infarction (INF).
The center is multidisciplinary; activities are completely protocolized and computerized.
Results: 45 patients were included: INF 69%, PH 20% and SAH 11%. Early mortality was 13%, mainly associated to PH and greater severity at stroke onset. Average length of hospital stay was nine days.
Conclusions: the population characteristics and mortality figures are comparable to those of other centers. Length of stay is similar to the best international results. Current results lack epidemiological value, which will be achieved after a certain time.
Résumé
Introduction: les centres spécialisés en accidents cérébro-vasculaires (ACV) ou Stroke (CES), ont comme but d’améliorer le prévention, l’assistance et la réhabilitation des patients qui subissent un ACV.
Objectifs: on expose ici nos expériences, nos réussites et nos faiblesses au Premier Centre Spécialisé Primaire en Stroke (CEPS) de l’Uruguay, mis en place au sein de la Coopérative Médicale de Canelones (COMECA) lors de sa première année de travail.
Matériel et méthode: c’est un centre pour adultes en phase aigue et de suivi intra et extra hospitalier. Les critères d’inclusion: patients adultes, moins de trois jours d’apparition du trouble, degré de gravité varié et hospitalisés à la clinique 1 de COMECA. On inclut hémorragie sous arachnoïde (HSA), hémorragie parenchymateuse (HP) et infarctus cérébral (INF).
Il est multidisciplinaire aux actions absolument protocolaires et informatisées.
Résultats: on a inclus 45 patients: INF 69%, HP 20% et HSA 11%. La mortalité précoce a été de 13%, associée surtout à HP et à une plus haute gravité depuis le début. Durée moyenne de séjour, neuf jours.
Conclusions: les caractéristiques de la population et les chiffres de mortalité sont comparables à ceux d’autres centres. La durée du séjour est proche des meilleurs résultats internationaux. Les résultats actuels n’ont pas encore de valeur épidémiologique.
Resumo
Introdução: os centros especializados em acidente vascular cerebral (AVC) ou Stroke (CES) têm como objetivo melhorar a prevenção, assistência e reabilitação de pacientes afetados por um AVC.
Objetivos: descrevemos nossa experiência, fortalezas e carências no primeiro ano de trabalho no primeiro Centro Especializado Primário em Stroke (CEPS) do Uruguai, criado na Cooperativa Médica de Canelones (COMECA).
Material e método: é um centro de adultos, de fase aguda e de seguimento intra e extra-hospitalar. É multiprofissional, com atividades totalmente protocolizadas e computadorizadas.
Critérios de inclusão: pacientes adultos,com menos de três dias de instalação do quadro, de qualquer gravidade e internados no hospital 1 de COMECA. Inclui hemorragia subaracnóidea (HSA), hemorragia parenquimatosa (HP) e infarto cerebral (INF).
Resultados: 45 pacientes foram incluídos no estudo: INF 69%, HP 20% e HSA 11%. A mortalidade precoce foi de 13%, associada fundamentalmente a HP e a uma maior gravidade no início. A duração media da permanência foi de nove dias.
Conclusões: as características populacionais e os dados de mortalidade são comparáveis a outros centros. Os valores de duração da permanência são próximos aos melhores resultados internacionais. Os resultados atuais no têm valor epidemiológico, o que acontecerá com o passar do tempo.
Bibliografía
1. Hackembruch HJ, Perna A, Vázquez C, Ketzoian C. Sección Neuroepidemiología del Instituto de Neurología del Hospital de Clínicas (datos no publicados, presentados en Congreso Panamericano de Neurología, 2008). Montevideo, 2008.
2. Riggs JE. Changing demographics and neurologic disease in the elderly. Neurol Clin 1996; 14(2): 477-86.
3. Alberts MJ, Hademenos G, Latchaw RE, Jagoda A, Marler JR, Mayberg MR, et al. Recommendations for the establishment of primary stroke centers. JAMA 2000; 283(23): 3102-9.
4. Rønning OM, Guldvog B. Stroke units versus general medical wards I: twelve and eighteen-month survival: a randomized, controlled trial. Stroke 1998; 29(1): 58-62.
5. Flemming KD, Brown RD Jr, Petty GW, Huston J 3rd, Kallmes DF, Piepgras DG. Evaluation and management of transient ischemic attack and minor cerebral infarction. Mayo Clin Proc 2004; 79(8): 1071-86.
6. Goldstein LB, Bian J, Samsa GP, Bonito AJ, Lux LJ, Matchar DB. New transient ischemic attack and stroke. Arch Intern Med 2000; 160(19): 2941-6.
7. Alberts MJ, Latchaw RE, Selman WR, Shephard T, Hadley MN, Brass LM, et al. Recommendations for comprehensive stroke centers. Stroke 2005; 36(7): 1597-616.
8. Faggi A. Definiendo las variables de eficiencia y eficacia de una Unidad de Stroke. Anuario Fundación Dr. J. R. Villavicencio 2006; 14: 081-8.
9. Organised inpatient (stroke unit) care for stroke (Cochrane Review). In: The Cochrane Library, Issue 1, 2009. Oxford: Update Software.
10. Hospital Ramos Mejía. Unidad de Stroke. Disponible en: www.ramosmejia.org.ar/stroke.html.
11. Phillips SJ, Eskes GA, Gubitz GJ; Queen Elizabeth II Health Sciences Centre Acute Stroke Team. Description and evaluation of an acute stroke unit. CMAJ 2002; 167(6): 655-60.
12. Adams HP Jr, Bendixen BH, Kappelle LJ, Biller J, Love BB, Gordon DL, et al. Classification of subtype of acute ischemic stroke. Definitions for use in a multicenter clinical trial- TOAST. Trial of Org 10172 in Acute Stroke Treatment. Stroke 1993; 24(1): 35-41.
13. Broderick J, Connolly S, Feldmann E, Hanley D, Kase C, Krieger D, et al. Guidelines for the management of spotaneous intracerebral hemorrhage in adults. Stroke 2007; 38(6): 2001-23.
14. Johnston SC, Nguyen-Huynh MN, Schwarz ME, Fuller K, Williams CE, Josephson SA, et al. National Stroke Association guidelines for the management of transient ischemic attacks. Ann Neurol 2006; 60(3): 301-13.
15. Adams HP Jr, del Zoppo G, Alberts MJ, Bhatt DL, Brass L, Furlan A, et al. Guidelines for the early management of adults with ischemic stroke: a guideline from the American Heart Association/American Stroke Association Stroke Council, Clinical Cardiology Council, Cardiovascular Radiology and Intervention Council, and the Atherosclerotic Peripheral Vascular Disease and Quality of Care Outcomes in Research Interdisciplinary Working Groups: the American Academy of Neurology affirms the value of this guideline as an educational tool for neurologists. Stroke 2007; 38(5): 1655-711.
16. Sacco RL, Adams R, Albers G, Alberts MJ, Benavente O, Furie K, et al. Guidelines for prevention of stroke in patients with ischemic stroke or transient ischemic attack: a statement for healthcare professionals from the American Heart Association/American Stroke Association Council on Stroke: co-sponsored by the Council on Cardiovascular Radiology and Intervention: the American Academy of Neurology affirms the value of this guideline. Circulation 2006; 113(10): e409-e449.
17. Indredavik B, Bakke F, Slordahl SA, Rokseth R, Hâheim LL. Treatment in a combined acute and rehabilitation stroke unit. Stroke 1999; 30(5): 917-923.
18. Brott T, Adams HP Jr, Olinger CP, Marler JR, Barsan WG, Biller J, et al. Measurements of acute cerebral infarction: A clinical examination scale. Stroke 1989; 20(7): 864-70.
19. Wiebers DO, Feigin VL, Brown RD Jr. Appendixes: functional status scales. In: Handbook of Stroke. Philadelphia: Lippincott-Raven, 1997: 354-7.
20. Rankin J. Cerebral vascular accidents in patients over the age of 60: II. Prognosis. Scott Med J 1957; 2(5): 200-15.
21. Wiebers DO, Feigin VL, Brown RD Jr. Appendixes: Functional Status Scales. In: Handbook of Stroke. Philadelphia: Lippincott-Raven, 1997: 357.
22. Brainin M, Bornstein N, Boysen G, Demarin V. Acute neurological stroke care in Europe: results of the European Stroke Care Inventory. Eur J Neurol 2000; 7(1): 5-10.
23. Fuentes B, Diez-Tejedor E. Unidades de ictus: una necesidad asistencial coste-efectiva. Neurología 2007; 22(7): 456-66.
24. Indredavik B, Bakke F, Slordahl SA, Rokseth R, Hâheim LL. Stroke unit treatment: 10 year follow-up. Stroke 1999; 30(8): 1524-7.
25. Hochmann B, Coelho J, Segura J, Galli M, Ketzoian C, Pebet M. Incidencia de accidentes cerebrovasculares en la ciudad de Rivera, Uruguay. Rev Neurol 2006; 43(2): 78-83.
26. Favat J, Pebet M, Dalmas F. Enfermedad cerebrovascular isquémica: epidemiología y factores de riesgo. Montevideo: Instituto de Neurología, 1995: 9-12.
27. Braga P, Ibarra A, Rega I, Ketzoian C, Pebet M, Servente L, et al. Prediction of early mortality after acute stroke. J Stroke Cerebrovasc Dis 2002; 11(1): 15-22.
28. Jørgensen HS, Nakayama H, Raaschou HO, Olsen TS. Intracerebral hemorrhage versus infarction: stroke severity, risk factors and prognosis. Ann Neurol 1995; 38(1): 45-50.
29. Sposato LA, Esnaola MM, Zamora R, Zurrú MC, Fustinoni O, Saposnik G; ReNACer Investigators; Argentinian Neurological Society. Quality of ischemic stroke care in emerging countries: the Argentinian National Stroke Registry (ReNACer). Stroke 2008; 39(11): 3036-41.
30. Braga P, Botti B, Ibarra A, Rega I, Servente L, Benzano D, et al. Ataque cerebrovascular: un estudio epidemiológico prospectivo en el Hospital de Clínicas de Montevideo. Rev Méd Urug 2001; 17(1): 42-54.
31. Baptista MV, van Melle G, Bogousslavsky J. Prediction of in-hospital mortality after first-ever stroke: the Lausanne Stroke Registry. J Neurol Sci 1999; 166(2): 107-14.
32. Jørgensen HS, Nakayama H, Raaschou HO, Larsen K, Hübbe P, Olsen TS. The effect of a stroke unit: reductions in mortality, discharge rate to nursing home, length of hospital stay and cost. A community-based study. Stroke 1995; 26(7): 1178-82.