Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Médica del Uruguay
versión On-line ISSN 1688-0390
Rev. Méd. Urug. vol.24 no.1 Montevideo mar. 2008
Monitoreo de anticuerpos HLA en insuficientes renales crónicos en lista de espera uruguaya para trasplante renal 2005
Dres. Nelson Toledo*, Adriana Tiscornia†, Milka Bengochea*,
Elena Carretto‡, Lic. Lab. Ely Silva§, Adriana Cabrera§, Doris Abilleira§, Tec.Transf. Martha Sosa¶, Prof. Dra. Inés Alvarez††
Laboratorio de Inmunogenética e Histocompatibilidad, Instituto Nacional de Donación y Trasplante de Células, Tejidos y Órganos (INDT), Facultad de Medicina y Ministerio de Salud Pública. Montevideo, Uruguay
Resumen
Introducción: en el trasplante renal, la investigación en los pacientes en lista de espera de anticuerpos (Ac) contra Human Leucocyte Antigen (HLA) resulta necesaria para adjudicar el órgano y para adecuar el tratamiento inmunomodulador que promueva mayor sobrevida al trasplante.
Material y método: realizamos búsqueda de anticuerpos HLA en 488 pacientes en lista de espera nacional de trasplante renal (2005). Definimos como inmunizados a aquellos con reactividad > 20% (41 pacientes), y altamente inmunizados con > 80% (6 pacientes), por técnica de microlinfocitotoxicidad enfrentados a un panel linfocitario, detectando especificidad por ELISA y citometría de flujo.
Resultados y conclusiones: detectamos anticuerpos HLA clase I y II por ELISA, e identificamos especificidades HLA por citometría de flujo: 41 (8,4%) pacientes inmunizados presentaron anticuerpos HLA clase I y 22 (4,5%) asocian clase II. Las especificidades de estos anticuerpos más frecuentemente encontradas fueron: A24, A23, BW6, B44, CW6, CW2, DR8, DR7, DQ2, DQ7. Comparamos distribución por edad, sexo, retrasplante, grupo sanguíneo, transfusiones previas, tiempo en lista de espera y diagnóstico en población inmunizada respecto a no inmunizada. Constatamos que en el grupo de inmunizados predominan los candidatos a un segundo trasplante (X2=130,47), quienes han recibido transfusiones previas (X2=119,2) y aquellos con mayor tiempo en lista de espera (p<0,0001). No hay diferencias en la distribución por edad, sexo ni diagnóstico etiológico de insuficiencia renal crónica, predominando la nefropatía indeterminada y glomerulopatías. La distribución por grupo sanguíneo mostró diferencias significativas: en el grupo de inmunizados hay más pacientes del grupo 0 (X2 =7,9) y menos del grupo A (X2 =3,94).
Palabras clave: INSUFICIENCIA RENAL CRÓNICA - inmunología.
TRASPLANTE RENAL - inmunología.
ANTÍGENOS HLA.
Keywords: RENAL INSUFFICIENCY, CHRONIC - immunology.
KIDNEY TRANSPLANTATION - immunology.
HLA ANTIGENS.
* Prof. Agregado del Laboratorio de Inmunogenética e Histocompatibilidad, INDT, Facultad de Medicina y Ministerio de Salud Pública. Uruguay.
† Asistente del Laboratorio de Inmunogenética e Histocompatibilidad, INDT, Facultad de Medicina y Ministerio de Salud Pública. Uruguay.
‡ Ex Asistente del Laboratorio de Inmunogenética e Histocompatibilidad, INDT, Facultad de Medicina y Ministerio de Salud Pública. Uruguay.
§ Lic. Laboratorio Clínico del Laboratorio de Inmunogenética e Histocompatibilidad, INDT, Facultad de Medicina y Ministerio de Salud Pública. Uruguay.
¶ Téc. Transfusionista del Laboratorio de Inmunogenética e Histocompatibilidad, INDT, Facultad de Medicina y Ministerio de Salud Pública. Uruguay.
†† Prof. Director del Laboratorio de Inmunogenética e Histocompatibilidad, INDT, Facultad de Medicina y Ministerio de Salud Pública. Uruguay.
Correspondencias: Dr. Nelson Toledo Lumillo.
INDT Hospital de Clínicas. Av. Italia s/n, 4º piso.
Correo electrónico: ntoledo@adinet.com.uy
Recibido: 9/8/07.
Aceptado: 10/3/08.
Introducción
El sistema HLA cumple fisiológicamente un importante rol en los fenómenos de presentación y reconocimiento antigénico(1). Desde hace décadas se conoce su papel en los trasplantes, por lo que ha sido identificado en el hombre como complejo mayor de histocompatibilidad. Las moléculas del sistema HLA y sus anticuerpos se clasifican en clase I y clase II.
El reconocimiento inmunológico del órgano trasplantado está vinculado a la distancia genética existente entre donante y receptor. Las diferencias en la dotación de antígenos HLA y la presencia de anticuerpos contra ellos incide en la evolución del trasplante(2). Existen diversos eventos inmunizantes como la transfusión sanguínea, el embarazo y el propio trasplante, que pueden promover la aparición de anticuerpos HLA.
La presencia de anticuerpos (Ac) HLA en candidatos a trasplante renal limita las posibilidades de trasplante, dado que es menor la probabilidad de encontrar un donante con antígenos HLA para los cuales el receptor no tenga anticuerpos. La ausencia de Ac HLA donante específicos se constata por una prueba cruzada (cross match) negativa. Por otro lado, la presencia de Ac HLA compromete la sobrevida del injerto a largo plazo(3,4). En este contexto, resulta fundamental estudiar Ac HLA en todos los pacientes con insuficiencia renal crónica en lista de espera para trasplante renal. Los resultados de este análisis deben ser considerados en la adjudicación del órgano y en la adecuación del tratamiento para poder disminuir la frecuencia de rechazos y prolongar la sobrevida del injerto, hechos trascendentes para promover la mejor calidad de vida del paciente.
En los programas de trasplante renal es necesario contar con datos seriados de anticuerpos HLA. En el Instituto Nacional de Donación y Trasplante (INDT) realizamos tres estudios anuales para definir el grupo de receptores sensibilizados contra sistema HLA.
Evaluamos el porcentaje de reactividad del suero de cada paciente en lista de espera contra un panel celular linfocitario representativo de los antígenos HLA de la población general. Este porcentaje de anticuerpos reactivos contra panel (panel reactivity antibody = % PRA), permite predecir el porcentaje de donantes que pueden dar prueba cruzada positiva al ser enfrentados contra el suero del receptor. En función de este resultado definimos grupos de receptores, inmunizados y no inmunizados. En este trabajo planteamos un estudio descriptivo de las características principales de la población de receptores renales en lista de espera en función de su sensibilización HLA.
Objetivos
1) Determinar la presencia de Ac HLA clase I y II en la población de pacientes en lista de espera para trasplante renal.
2) Identificar la población de pacientes inmunizados HLA y comparar distribución por edad, sexo, número de trasplantes, transfusiones previas, tiempo en lista de espera, diagnóstico y grupo sanguíneo, respecto a la población de no inmunizados.
Material y método
A) Población de estudio: incluimos todos los pacientes en lista de espera nacional de trasplante renal con suero vigente al año 2005, N = 488.
En todos los casos se recabó consentimiento informado para su ingreso a lista de espera y extracción de sangre para estudios correspondientes, de acuerdo con el protocolo del INDT.
B) El monitoreo inmunológico que se realiza en el INDT consiste en enfrentar los sueros de todos los pacientes en lista de espera contra paneles celulares linfocitarios de 50 células cada uno (con una distribución antigénica representativa de la población general uruguaya) por técnica de microlinfocitotoxicidad (MLCT), en tres cortes anuales. Se estudiaron 488 sueros, correspondiente a la seroteca del año 2005. Se define al grupo de pacientes inmunizados HLA como integrado por aquellos con reactividad contra panel ³ 20%.
Se realizó test de ELISA (LAT M ONE LAMBDA MR) para determinar especificidad de clase (Ac HLA clase I y clase II).
Posteriormente identificamos la especificidad antigénica de los anticuerpos HLA por técnica de citometría de flujo (Flow PRA specific FL1 SP y FL2 SP ONE LAMBDA MR).
C) Técnicas utilizadas
C1) Técnica de MLCT. Utilizada para la determinación de PRA.
Se efectuó de acuerdo con el protocolo estándar de NIH (5).
Para lectura de viabilidad en microscopio invertido de inmunofluorescencia (Zeiss MR) se utilizó tinción con reactivo fijador celular y fluorogénico con bromuro de etidio y naranja de acridina (Fluoroquench-One Lambda).
La viabilidad celular o el grado de mortalidad (células vivas-verde y muertas-rojo), se evaluó de acuerdo al escore internacional. Para cada paciente se calculó el porcentaje de PRA de acuerdo con el número de veces que su suero provocó mortalidad celular (reacción positiva) en el total del panel.
C2) Prueba de ELISA. Utilizada para la determinación de especificidad de clase.
Se trabajó con el kit comercial Lambda Antigen Tray LATM (One Lambda), que determina especificidades genéricas de anticuepos HLA clase I o II de tipo IgG, o ambos(6,7).
C3) Citometría de flujo. Utilizada para la determinación de especificidad HLA antigénica.
Se usó kit Flow PRA FL1SP y FL2SP (ONE LAMBDA MR) que permite determinar especificidades privadas de Ac HLA I y II, tipo IgG. Trabajamos con citómetro Coulter, modelo Epic XL, de cuatro colores y el software de interpretación correspondiente al kit(8).
Análisis estadísticos
Para la comparación de medidas de resumen de tendencia central (promedio o mediana) se utilizó test no paramétrico, para muestras no pareadas test de Mann-Whitney. Para evaluar la asociación entre las variables cualitativas y el estado de sensibilización HLA se utilizaron tablas de contingencia de dos por dos, test de chi cuadrado o test exacto de Fisher.
Resultados
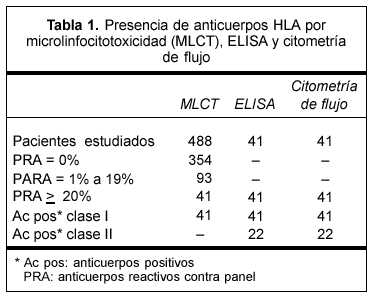
En el período correspondiente a enero-diciembre 2005 estudiamos 488 pacientes candidatos a trasplante renal. En la tabla 1 se resumen los resultados de presencia de Ac por las tres técnicas (MLCT, ELISA y citometría de flujo).
Por técnica de MLCT detectamos 41 personas inmunizadas (8,4%), confirmando en todos los casos este resultado por ELISA y citometría de flujo. Estas dos últimas técnicas tienen mayor sensibilidad que las de citotoxicidad e incluyen la detección de anticuerpos no fijadores de complemento. Todos los casos positivos para clase I o II, o ambas, por técnica de ELISA, también lo son por citometría.
Los 41 pacientes sensibilizados tienen Ac HLA clase I (100%) y 22 de ellos tienen además Ac HLA clase II (54%).
El análisis de especificidad privada detecta un total de 149 anticuerpos: 102 clase I y 47 clase II y revela que estos Ac son mayoritariamente poliespecíficos.
Los Ac detectados reconocen especificidades correspondientes a diferentes loci HLA clase I, locus A (n=57), locus B (n=33) y locus C (n=12), o loci HLA clase II, locus DR (n=30) y DQ (n=17).
Los resultados del estudio de especificidad de clase y antigénica son resumidos en la tabla 2.
El rango de edades en los inmunizados osciló entre 23 y 67 con una mediana de 42 años y en los no inmunizados entre 12 y 76 con una mediana de 46 años.
La comparación de perfiles etarios entre ambos grupos no mostró diferencias significativas (p=0,1641) de acuerdo con el test de Mann-Whitney.
Representamos gráficamente la distribución por sexo en la figura 1. En el grupo de inmunizados hay 19 hombres (46%) y 22 mujeres (54%), y en el de no inmunizados 262 hombres (59%) y 185 mujeres (41%), diferencia no significativa (p=0,139) de acuerdo con el test exacto de Fisher.
En la población estudiada existen 55 candidatos a retrasplante, 26 inmunizados y 29 no inmunizados.
El porcentaje de pacientes candidatos a retrasplante en ambos grupos es estadísticamente diferente (63% versus 6,4%), x2=130,47, p< 0,0001 (figura 2).
En 30% de los inmunizados candidatos a retrasplante (n=8), las especificidades estaban dirigidas contra antígenos presentes en el primer donante: cinco clase I (locus A) y tres de clase II (DR). En 70% no se detectaron anticuerpos dirigidos contra especificidades HLA privadas de los respectivos donantes.
En la figura 3 representamos la distribución de acuerdo con el antecedente transfusional. En el grupo de inmunizados todos los pacientes habían recibido al menos una transfusión (100%), mientras que en el grupo de no inmunizados sólo 89 pacientes (19,9%) fueron transfundidos. Esta diferencia resultó significativa (X2 con corrección de Yates=119,2). Este resultado confirma la fuerte relación del antecedente transfusional como evento inmunizante.
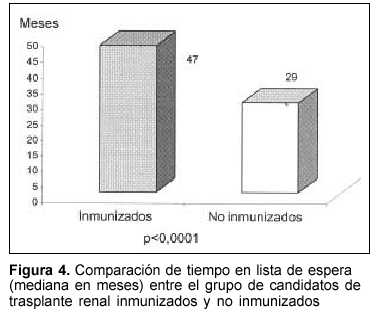
En la figura 4 representamos las medianas de tiempo en lista de espera para ambos grupos: 47 meses en los inmunizados y 29 meses en los no inmunizados, diferencia estadísticamente significativa de acuerdo con el test de Mann-Whitney (p<0,0001).
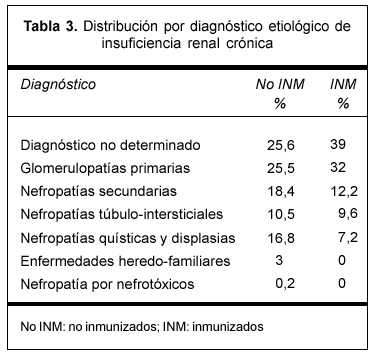
Los diagnósticos etiológicos de la insuficiencia renal crónica presentados en la tabla 3 fueron proporcionados por los equipos de trasplante en el momento de solicitar la inclusión del paciente en lista de espera. Destacamos que en ambos grupos predominan la nefropatía indeterminada y las glomerulopatías primarias.
En la tabla 4 se muestra la distribución en sistema ABO de ambos grupos, respecto a los datos correspondientes de población general, obtenidos en un trabajo previo del servicio(9). El grupo de no inmunizados no presenta diferencias significativas en la distribución de frecuencias respecto a la población general. Sin embargo, se aprecia que 73% de los inmunizados pertenece al grupo O contra 49% de la población general. Esta diferencia resultó estadísticamente significativa (X2 con corrección de yates =7,9).
La frecuencia de grupo A en el grupo de inmunizados (22%) es menor que en la población general (39%), diferencia que también resultó tener significación estadística (X2 con corrección Yates=3,94).
Discusión
En un total de 488 pacientes en lista de espera para trasplante renal identificamos por técnica de MLCT 41 pacientes inmunizados (8,4%) con PRA > 20%, y confirmamos este resultado por técnicas de ELISA y citometría de flujo.
La concordancia en todos los casos de los resultados de las tres técnicas revela la presencia de anticuerpos de clase IgG. La MLCT también detecta Ac HLA IgM fijadores de complemento, por lo que no queda descartada la posibilidad de asociación de ambas clases de inmunoglobulina. La presencia de IgG es esperable, debido en particular a que el grupo de inmunizados estudiados tiene mayor tiempo en lista de espera y los eventos inmunógenos son temporalmente lejanos.
Tomando en cuenta que hasta 17% de los pacientes pueden presentar resultados discordantes cuando se comparan las tres técnicas(10) y considerando recursos económicos limitados para implementar estudios citométricos en aproximadamente 500 pacientes, nuestro servicio efectúa estudio de PRA en tres cortes anuales por MLCT que nos brinda un historial inmunológico y define población de riesgo.
En todos los casos en el operativo de trasplante cadavérico realizamos cross match final por MLCT, y en aquellos receptores que presentan factores de alto riesgo inmunológico, complementamos los estudios pretrasplante con cross match final por citometría del flujo. La especificidad de anticuerpos en los receptores PRA positivos se realiza por citometría de flujo y ELISA. Este algoritmo es técnicamente factible y económicamente viable en nuestro país.
Todos los inmunizados poseen Ac HLA clase I, confirmados por MLCT, ELISA y citometría, y 22 de ellos poseen Ac HLA clase II (54%), detectados por ELISA y citometría. La técnica de MLCT utilizada incluye linfocitos totales (con mayor porcentaje de linfocitos T), por lo que detecta anticuerpos HLA clase I, mientras que las técnicas de ELISA y citometría utilizadas están diseñadas para la detección de anticuerpos HLA clase I y II.
Los anticuerpos hallados son generalmente poliespecíficos y están dirigidos en frecuencia decreciente contra los loci HLA- A, B y DR. El grupo de inmunizados tiene un alto porcentaje de candidatos a retrasplante. Como en su primer trasplante se priorizó la compatibilidad en el orden DR, B y A, la formación de anticuerpos contra lo no compatible podría resultar en frecuencia en orden inverso: A, B y DR. Esta sería una explicación plausible para nuestros hallazgos.
Cuando comparamos al grupo de inmunizados respecto al de no inmunizados observamos que no hay diferencias estadísticas significativas en la distribución por edad y sexo. En cambio, existen diferencias entre ambos grupos cuando se consideran las transfusiones, el número de candidatos a retrasplante, el tiempo en lista de espera y la distribución por grupo sanguíneo. De acuerdo con estudios realizados en nuestro servicio, la población de inmunizados en nuestra lista ha descendido progresivamente desde 20% en 1987 a porcentajes cercanos al actual en los últimos ocho años(11). Este hecho puede explicarse por el menor número de transfusiones que reciben estos pacientes desde el advenimiento de la terapia con eritropoyetina y por un cambio de la indicación de la terapia transfusional. La presencia de transfusiones es un factor capital en la aparición y en el mantenimiento de la inmunización contra sistema HLA, dada la presencia de leucocitos en las unidades de sangre desplasmatizada sin proceso de leucorreducción por filtros(12). Asimismo, constatamos un aumento en la proporción de candidatos a retrasplante en los últimos dos años.
Los inmunizados son pacientes que han recibido transfusiones (100%), han sido transplantados previamente (63%) y esperan más tiempo en lista (47 meses).
Los candidatos a retrasplante predominan ampliamente en la población de inmunizados (63%), y entre ellos 30% asocian la presencia de anticuerpos HLA donante específicos. El porcentaje de pacientes con anticuerpos específicos contra el primer donante depende de muchas variables, entre ellas del grado de compatibilidad con que se realicen los trasplantes. Existen reportes en los que se refiere que hasta 72% de pacientes trasplantados desarrollan anticuerpos donante específico luego de un primer trasplante(13). Para evaluar posibles causas de esta diferencia sería necesario un estudio complementario que analice la compatibilidad de los trasplantes.
Un grupo de ocho pacientes, actualmente en lista de espera, tuvieron un injerto funcionante y generaron anticuerpos contra el primer donante. Existen actualmente trabajos multicéntricos destinados a evaluar el rol de la inmunidad humoral en el rechazo crónico. En este contexto el estudio de anticuerpos HLA en el postrasplante tendría valor predictivo en el rechazo de injerto.
El programa de trasplante renal vigente en nuestro país lleva varias décadas de funcionamiento. Toma en cuenta compatibilidad en sistemas ABO, HLA y nivel de PRA, el cual se define por MLCT. Se seleccionan los receptores con pruebas cruzadas donante específicas (PCDE) negativas por MLCT. Cuando los pacientes con PRA superior a 80% o candidatos al retrasplante quedan seleccionados en la lista de asignación se realiza, además, prueba cruzada por citometría de flujo. Esta técnica aumenta la sensibilidad de la prueba cruzada y brinda mayor información para el manejo terapéutico del postrasplante.
El tiempo en lista de espera más prolongado (47 meses) en los inmunizados indica la dificultad para este grupo de encontrar donante. Es frecuente la selección preliminar de pacientes inmunizados en la adjudicación de órganos. A pesar de que comparten especificidades HLA con los donantes, la presencia de anticuerpos en su suero resulta en frecuentes cross match positivos, contraindicando la realización del trasplante. El PRA refleja las posibilidades de encontrar un donante, los porcentajes más altos indican menores chances de ser trasplantado. A pesar de que existen planes terapéuticos alternativos para bajar los títulos de anticuerpo y permitir la realización del trasplante que podrían discutirse para su implementación(14,15), su indicación no está extendida.
La distribución de grupos sanguíneos ABO mostró en el grupo de inmunizados frecuencia mayor de individuos del grupo O y menor del grupo A respecto a la población general. Es difícil explicar este hecho, pero podría pensarse que existe una selección de pacientes del grupo O, por motivos no evaluados en este trabajo. Pensamos que en el futuro sería conveniente evaluar la persistencia de esta distribución y analizar qué parámetros podrían influir en ella.
Finalmente, en el análisis de diagnósticos interesa destacar que los casos con etiología vinculados a patología inmune no alcanzaron un número suficiente como para analizar estadísticamente su influencia.
Dentro de las soluciones propuestas para poder trasplantar al grupo de pacientes hiperinmunizados, existen a nivel mundial argumentos como el esgrimido por Gebel, o la utilización del HLA Matchmaker por parte del grupo de Cambridge(16). Hay dos aproximaciones para poder trasplantar a este tipo de pacientes, una es la aproximación farmacológica y otra la biológica. La farmacológica utiliza inmunoglobulina asociada o no a plasmaféresis, la cual se utiliza básicamente con donante vivo y con bajos títulos de anticuerpos, ya que su alto costo y la lógica de su aplicación lo desaconseja en trasplante cadavérico.
La aproximación biológica puede ser de utilidad y consiste básicamente en estudiar exhaustivamente al receptor hipersensibilizado mediante ensayos citométricos en fase sólida, primero de screening y luego altamente específicos (single antigen bead) para conocer la totalidad de anticuerpos HLA existentes en el suero. De aquí como paso primario se elabora una lista de antígenos HLA ina-ceptables para trasplante. Ante un potencial donante, se realiza cross match por citometría de flujo y de ser éste negativo, el paciente puede trasplantarse con mayores posibilidades de éxito y menores riesgos de rechazo hiper-agudo y acelerado. El programa europeo (Eurotrasplant) recientemente combina este algoritmo con el programa computarizado de HLA match maker, el cual predice computarizadamente la compatibilidad donante-receptor comparando las secuencias aminoacídicas lineales de sus antígenos/anticuerpos HLA(16,17).
De cualquier manera, todas las soluciones propuestas sólo pueden ser instrumentadas si se cumplen premisas importantes, entre ellas: la existencia de buen número de donantes, adecuados estudios del paciente, representativos de su situación inmunológica actual, de un país con buenas posibilidades terapéuticas (financiación de planes de inmunosupresión y plasmaféresis personalizados), y de un receptor que cumpla correctamente con la terapéutica planteada.
En resumen, realizamos un trabajo descriptivo de las características de la población en lista de espera nacional para trasplante renal del año 2005, destacamos que ha disminuido el porcentaje de pacientes inmunizados y que este grupo se caracteriza por haber recibido transfusiones, perdurar más tiempo en lista de espera e incluir un alto porcentaje de pacientes candidatos a segundo trasplante. Este análisis contribuye a definir las características de un grupo de riesgo y el estatus inmunológico del paciente previo al trasplante, ambas de interés para la adjudicación del órgano (programa de trasplante) y para el manejo terapéutico del mismo.
Agradecimientos
Agradecemos la colaboración de las administrativas del laboratorio: Laura Dávila y María Laura Moreira, quienes contribuyeron en la recopilación de datos.
Summary
Introduction: tests of Human Leucocyte Antigen (HLA), antibodies for patients on the waiting list for renal transplant, are necessary to allocate organs and to define the appropriate immunomodulator treatment that result in the best tranplant survival rates.
Methods: we looked for HLA antobodies in 488 patients on the national waiting list for renal transplant. We defined patients with reactivity > 20% (41 pacients) as immunized, and those with reactivity > 80% (6 patients) as highly immunized, by using the microlymphocitotoxicity technique against a lymphicyte test panel, detecting specificity by ELISA and flow cytometry
Results and conclusions: we found HLA antibodies class I and class II by ELISA ,and identified HLA specificities by flow cytometry: 41 (8.4%) of immunized patients showed HLA antibodies class I and 22 (4.5%) evidenced class II. The most frequently found specificities for these antibodies were : A24, A23, BW6, B44, CW6, CW2, DR8, DR7, DQ2, DQ7.We compared the distribution by age, sex, retransplantation, blood type, previous blood transfusions, time on the waiting list and diagnosis of the immunized population with those non-immunized. We found that in the immunized group most of them are candidates for a second transplant (X2=130,47), have received previous transfusions (X2=119,2) and have been on the waiting list longer(p<0,0001). NO differences were found in the distribution by age, sex or etiological diagnosis of chronic renal failure (CRF), being the non-determined nephropaty and glomerulopathies, the most frequent types. Distribution by blood type showed significant differences: in the immunized group there were more patients belonging to group 0 (X2 =7,9) and less of them belonging to group A (X2 =3,94).
Résumé
Introduction: dans la greffe rénale, les recherches chez les patients sur liste d’attente d’anticorps (Ac) contre Human Leucocyte Antigen (HLA) s’avère nécessaire dans le choix du receveur et pour adapter le traitement immunomodu-lateur qui assure une meilleure survie du greffon.
Matériel et méthode: recherche d’anticorps HLA chez 488 patients sur liste d’attente nationale de transplantation rénale (2005). On définit comme immunisés ceux à réactivité = 20% (41 patients), et hautement immunisés ceux ayant = 80% (6 patients), par technique de microlymphocytotoxicité (LCT) face à un panel lymphocytaire repérant spécificité par ELISA et cytométrie de fluxe.
Résultats et conclusion: on a repéré des anticorps HLA type I et II par ELISA et spécificité HLA par cytométrie de fluxe: 41 (8,4%) patients immunisés ont présenté des anticorps HLA type I et 22 (4,5%) type II. Les spécificités de ces anticorps repérés plus fréquemment ont été: A24,A23,BW6,B44,CW6,CW2,DR8,DR7,DQ2,DQ7. On compare la distribution selon l’âge, le sexe, la greffe, le groupe sanguin, les transfusions préalables, le temps sur liste d’attente et le diagnostic dans la population immunisée par rapport à la non immunisée. On constate que dans le premier de ces groupes, les candidats à un deuxième greffon sont prédominants (X2= 130,47), ainsi que ceux ayant été transfusés préalablement (X2= 119,2) et ceux inscrits plus longtemps sur liste d’attente (p< 0,0001). Il n’y a pas de différence à la distribution selon l’âge, le sexe ni selon le diagnostic étiologique d’insuffisance rénale chronique, repérant une prédominance de la néphropathie indéter-minée et des glomérulopathies. La distribution selon le groupe sanguin a montré des différences significatives : chez les immunisés, il y plus grand nombre de patients du groupe O (X2= 7,9) et sont moins nombreux ceux appartenant au groupe A (X2= 3,94).
Resumo
Introdução: no transplante renal, a pesquisa de anticorpos (Ac) contra Human Leucocyte Antigen (HLA) em pacientes em lista de espera é necessária para alocar o órgão e para a adequar o tratamento imunomodulador visando uma sobrevivência mais longa do transplante.
Material e método: realizamos pesquisa de anticorpos HLA em 488 pacientes em lista de espera nacional de transplante renal (2005). Definimos como imunizados os pacientes com reatividade > 20% (41 pacientes), e altamente imunizados com > 80% (6 pacientes),empregando a técnica de microlinfocitotoxicidade contra painel de linfocitos, detectando especificidade por ELISA e citometria de fluxo.
Resultados e conclusões: detectamos anticorpos HLA classe I e II por ELISA, e identificamos especificidade HLA por citometria de fluxo: 41 (8,4%) pacientes imunizados tinham anticorpos HLA classe I e 22 (4,5%) classe II. As especificidades desses anticorpos más freqüentes foram: A24, A23, BW6, B44, CW6, CW2, DR8, DR7, DQ2, DQ7. Comparamos a distribuição por idade, sexo, retransplante, grupo sanguíneo, transfusões anteriores, tempo na lista de espera e diagnóstico na população imunizada com relação a não imunizada. Constatamos que no grupo de imunizados predominam os candidatos a um segundo transplante (X2=130,47), os que receberam transfusões previas (X2=119,2) e os que estavam a mais tempo na lista de espera (p<0,0001). Não observamos diferenças na distribuição por idade, sexo nem pelo diagnóstico etiológico da insuficiência renal crônica, predominando a nefropatia indeterminada e as glomerulopatias. A distribuição por grupo sanguíneo mostrou diferenças significativas: o grupo de imunizados tinha mais pacientes do grupo 0 (X2 =7,9) e menos do grupo A (X2 =3,94).
Bibliografía
1. García-Lora A, Algarra I, Garrido F. MHC class I antigens, immune surveillance, and tumor immune escape. J Cell Physiol 2003; 195(3): 346-55.
2. Kozma L, Bohaty I. HLA class I antibody screening and typing in the sera of dialized patients with CDC and ELISA techniques: association with graft survival. Orv Hetil 2007; 148(12): 553-8.3. Terasaki P, Ozawa M. Predicting kidney graft failure by HLA antibodies: a prospective trial. Am J Transplant 2004; 4(3), 438-43.
4. Terasaki P, Ozawa M. Predictive value of HLA antibodies and serum creatinine in chronic rejection: results of a 2-year prospective trial. Transplantation 2005; 80(9): 1194-7.
5. Terasaki P, McClelland J. Microdroplet assay of human assay serum cytotoxins. Nature 1964; 204: 998-1000.
6. 12th International Histocompatibility Conference. Genetic diversity of HLA: functional and medical implications. Paris, France, June 9-12, 1996. Abstracts. Hum Immunol 1996; 47(1-2); 1-184.
7. Uboldi de Capei M, Praticó L, Curtoni ES. Comparison of different techniques for detection of anti-HLA antibodies in sera from patients awaiting kidney transplantation. Eur J Immunogenet 2002; 29(5): 379-82.
8. Pei R, Lee J, Chen T, Rojo S, Terasaki P. Flow cytometric detection of HLA antibodies using a spectrum of microbeads. Hum Immunol 1999; 60(12): 1293-302.
9. Sans M, Sosa M, Álvarez I ,Toledo R, Bengochea M, Salzano F. Blood group frequencies and the question of race admixture in Uruguay. Interciencia 1993; 18(1): 29-32.
10. Toledo R, Tiscornia A, Álvarez I, Bengochea M, Carretto E, Silva E, et al. Investigación de anticuerpos HLA en 10 poblaciones de insuficientes renales cronicos en lista de espera para trasplante renal. Rev Urug Patol Clin 2005; 38: 43.
11. Soosay A, 0’Neill D, Counihan A, Hickey D, Keogan M. Causes of sensitisation in patients awaiting renal transplantation in Ireland. Ir Med J 2003; 96(4): 109-12.
12. Díaz I, Sánchez P, Acuso C, Valdéz F. Immunological profile of patients awaiting renal transplant. Clin Transplant 2004; 18(5): 529-35.
13. Mancilla-Urrea E. The highly sensitized patient. Therapeutic alternatives for kidney transplantation. Rev Invest Clin 2005; 57(2): 206-12.
14. Jordan S, Vo A, Penq A, Toyoda M, Tyan D. Intravenous gamaglobulin (IVIG): a novel approach to improve transplant rates and outcomes in highly HLA-sensitized patients. Am J Transplant 2006; 6(3): 459-66.
15. Gebel H, Bray R. Sensitization and sensitivity: defining the unsensitized patient. Transplantation 2000; 69(7): 1370-4.
16. Bray R, Nolen J. Transplanting the highly sensitized patient: the emory algorithm. Am J Transplant 2006: 6(10):2307-15.
17. Goodman R, Taylor C, O’Rourke C, Lynch A, Bradley J, Key T. Utility of HLAMatchmaker and single-antigen HLA-antibody detection beads for Identification of acceptable mismatches in highly sensitized patients awaiting kidney transplantation. Transplantation 2006; 81(9): 1331-6.