Services on Demand
Journal
Article
Related links
Share
Revista Médica del Uruguay
On-line version ISSN 1688-0390
Rev. Méd. Urug. vol.21 no.4 Montevideo Dec. 2005
Trasplante heterotópico de corteza ovárica en paciente joven con cáncer de cuello uterino
Dres. Francisco Cóppola*, Jorge Martínez†, Álvaro Domínguez‡,
Héctor Pérez Campos§, Elías Regules¶, Fernanda Nozar††,
Sara Parada‡‡, Rafael Aguirre§§
Clínica Ginecotocológica "C". Hospital de la Mujer. Centro Hospitalario Pereira Rossell. Facultad de Medicina. Universidad de la República. Montevideo, Uruguay
Resumen
El pronóstico y los índices de curación del cáncer de cuello uterino han mejorado en los últimos años producto de su diagnóstico precoz y los avances en su tratamiento. Sin embargo, el diagnóstico precoz implica un mayor número de pacientes jóvenes con esta enfermedad, expuestas a la afección iatrogénica de sus ovarios secundaria al tratamiento del cáncer. La preservación de la función endocrina ovárica en las mismas reviste una gran importancia y busca evitar las consecuencias de una menopausia prematura o los potenciales riesgos de la terapia de sustitución hormonal. El presente artículo muestra el resultado del primer caso clínico en nuestro país, donde se aplicó una de las posibles estrategias de conservación ovárica: el autotrasplante de tejido ovárico en fresco a un sitio heterotópico (bíceps). Se expone el caso de una paciente de 33 años afectada por un cáncer de cuello uterino en estadio 1B en la cual, en el curso de la cirugía oncológica, se traslocó un ovario a una situación extrapelviana y se autotrasplantó el otro al brazo de forma de evitar su exposición a una eventual radioterapia complementaria. El seguimiento posoperatorio mostró un nivel mantenido de esteroides sexuales y una rápida revascularización de los fragmentos trasplantados a nivel bicipital. Este procedimiento se muestra como una de las opciones útiles para preservar la función endocrina en las pacientes jóvenes con cáncer cervical.
Palabras clave: NEOPLASMAS DEL CUELLO UTERINO - cirugía.
TRASPLANTE HETEROTÓPICO - utilización.
* Endocrinólogo y Ginecotocólogo. Prof. Adj. Clínica Ginecotocológica "C". Ex asistente de Endocrinología. Facultad de Medicina, Universidad de la República. Presidente de la Sociedad de Endocrinología Ginecológica del Uruguay.
† Ginecólogo Oncólogo. Prof. Agdo. Clínica Ginecotocológica "C". Encargado de Ginecología de Clínica Ginecotocológica "C". Facultad de Medicina, Universidad de la República.
‡ Ginecólogo especialista en Reproducción Humana. Ex Asistente Clínica Ginecotocológica "C". Facultad de Medicina, Universidad de la República.
§ Médico coordinador del área criopreservados del Banco Nacional de Órganos y Tejidos. Ministerio de Salud Pública.
¶ Prof. Agdo. del Departamento de Anatomía Normal. Ex Asistente Clínica Ginecotocológica "C". Facultad de Medicina, Universidad de la República.
†† Residente Clínica Ginecotocológica "C". Facultad de Medicina, Universidad de la República.
‡‡ Médico ecografista. Unidad de Ecografía Ginecológica, Centro Hospitalario Pereira Rossell.
§§ Ex Asistente Clínica Ginecotocológica "C". Facultad de Medicina, Universidad de la República.
Correspondencia: Dr. Francisco Cóppola.
Cuareim 2131 Apto. 1108. Montevideo, Uruguay.
E-mail: fracopp@adinet.com.uy.
Dr. Rafael Aguirre.
Santiago Gadea 3056. Apto 601. Montevideo, Uruguay.
E-mail: raguirre@chasque.apc.org.
Recibido: 14/3/05.
Aceptado: 27/9/05.
Introducción
Los adelantos en el diagnóstico y tratamiento del cáncer de cuello uterino ha mejorado el pronóstico y aumentado la esperanza de vida de mujeres premenopáusicas portadoras de este cáncer. Hay una población creciente de mujeres jóvenes que se han curado luego del tratamiento oncológico del cáncer de cérvix. Sin embargo, el tratamiento no está exento de efectos secundarios, siendo uno de los más comunes la afección iatrogénica de la función ovárica. La quimioterapia o la radioterapia pelviana, o ambas, necesarias en algunos casos, frecuentemente llevan a la falla ovárica prematura (FOP) con una máxima repercusión en las pacientes jóvenes, sobre todo en aquellas que no han tenido hijos(1). Se trata de una repercusión en lo reproductivo y lo hormonal exponiendo fundamentalmente a la paciente a las consecuencias del hipoestrogenismo (osteoporosis, atrofia urogenital, sintomatología climatérica). Evitar el mismo implica iniciar un plan de hormonoterapia de reemplazo hormonal, no siempre posible (por los factores de riesgo de la paciente) y no exento de efectos secundarios (trombosis). Es por ello que aquellas estrategias que buscan preservar la función ovárica de las pacientes jóvenes con cáncer de cuello uterino tienen una gran importancia desde el punto de vista médico.
Nos ocupa el caso de pacientes con cáncer de cuello uterino de tipo epidermoide, en estadios iniciales (estadios I, confinados al cuello uterino con exclusión de los microinfiltrantes). Estos casos tienen en común cuatro características que hacen planteables estrategias de preservación ovárica:
1. Se observan en un alto porcentaje en pacientes premenopáusicas(2).
2. No presentan metástasis ováricas(3-5).
3. No requieren quimioterapia.
4. Requieren, eventualmente, radioterapia abdómino-pélvica (luego de conocer la invasión ganglionar).
Desde hace varios años se ha establecido la conveniencia de preservar al menos un ovario, de forma de mantener el nivel hormonal en estas pacientes premenopáusicas(6). Se debe destacar que la terapia de sustitución hormonal en pacientes jóvenes ooforectomizadas no reproduce el funcionamiento fisiológico de la gónada y nunca es ideal. Sin embargo, algunas de las pacientes requerirán radioterapia ya sea luego de la cirugía (en función de la invasión regional linfática) o de inicio (por contraindicación de la cirugía). Los ovarios son particularmente sensibles a la radioterapia(7). Se conoce que una dosis de entre 5 a 20 Gy administrada al ovario es suficiente para dañar completamente la gónada, independientemente de la edad de la paciente(8).
Para preservar la función ovárica se propone la transposición ovárica a un sitio alejado de la pelvis (por ejemplo en el sector subdiafragmático) buscando evitar los efectos de la radioterapia pélvica Sin embargo, esta técnica es dificultosa (pediculización del ovario hasta el espacio subfrénico), con una alta tasa de fallas (por trombosis, elongación o irradiación del pedículo y compromiso vascular consiguiente) y con potenciales complicaciones (necrosis y quistes difíciles de resolver), todo lo cual limita su efectividad(9). La falla de ovarios transpuestos fuera de la pelvis (subdiafragmáticos) en pacientes que luego requieren radioterapia oscila entre 22% a 50% en diferentes series(10-12), y cuando se realiza seguimiento a más largo plazo llega a 88%(13).
Una nueva opción propuesta es el autotrasplante del ovario a una zona externa a la cavidad abdómino-pélvica (trasplante heterotópico), que en un número limitado de casos en el mundo se ha realizado conservando su pedículo (ovario entero)(14), o más frecuentemente de corteza ovárica, ambas de tejido en fresco, obteniendo una buena respuesta endocrina y en algunos casos crecimiento y maduración ovocitaria(15,16).
Dada esta problemática y el desarrollo de nuevas opciones, en el año 2004 en la Clínica Ginecotocológica "C" de la Facultad de Medicina, Universidad de la República, se constituyó un Grupo de Trabajo para la Preservación de la Función Ovárica después del Cáncer, siendo una de las estrategias puestas a punto el autotrasplante heterotópico de corteza ovárica. El caso que describimos es el primero de este protocolo y la primera experiencia en Uruguay.
Caso clínico
Paciente de 33 años, previamente sana, nuligesta, portadora de un carcinoma escamo-celular de cuello uterino con estadificación clínica IB1. Se programó para realizar una histerectomía radical, más eventual linfadenectomía abdómino-pélvica. De acuerdo con el protocolo de nuestro servicio se planteó realizar el estudio previo del ganglio centinela, que es la marcación radioisotópica del principal linfático tributario de la lesión. De identificarse se reseca para su estudio por biopsia extemporánea. De mostrar ésta la infiltración se realiza la linfadenectomía, de ser negativa no se procede a la misma. La paciente fue informada de la repercusión sobre la función ovárica del tratamiento oncológico, las características del protocolo que se estaba iniciando y los potenciales riesgos y beneficios del mismo. Se acordó con la paciente y su familia un plazo prudencial para que los mismos reflexionaran sobre lo informado, realizando en dicho período interconsultas a nivel local y en el exterior. La paciente optó por el autotrasplante heterotópico firmando el correspondiente consentimiento informado.
Preparación y cirugía
El día previo a la cirugía se inyectó el cuello uterino con una dosis total de 148-185 MBq de tecnesio 99 (99mTc - Nanocis, CIS Bio International, Francia). La dosis fue dividida en cuatro jeringas, conteniendo cada una un volumen de 0,2-0,3 ml, que se administraron por punción en cada uno de los cuadrantes cervicales. La intervención se realizó el 24 de enero de 2004, conformándose dos equipos.
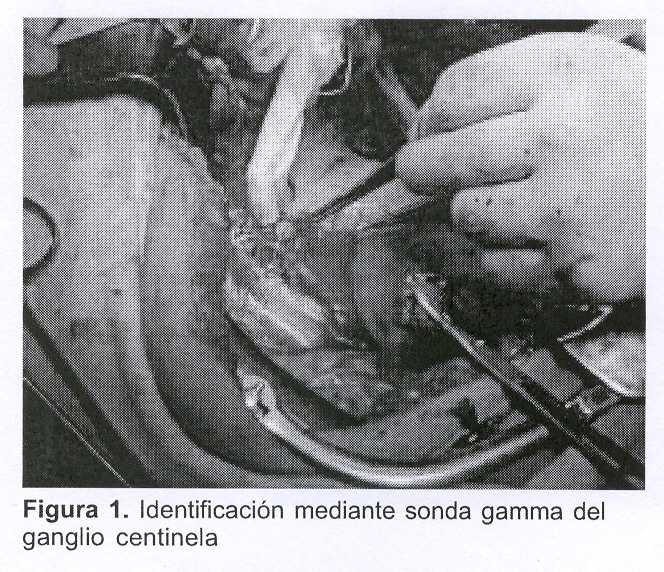
Equipo 1: se abordó la cavidad abdominal por una incisión mediana suprainfraumbilical, se procedió a identificar mediante sonda gamma los nodos linfáticos radioactivos en los espacios célulo-vasculares de la pelvis y retroperitoneo. El ganglio satélite principal tributario de la zona tumoral se identificó en la zona inter-ilíaca derecha (figura 1).
Se extrajo quirúrgicamente el ganglio centinela y se envió a estudio anatomopatólogo mediante estudio extemporáneo. En virtud que del análisis anatomopatológico no se puede descartar su infiltración (dudoso), se procede a la realización de la linfadenectomía abdómino-pélvica bilateral, seguida de histerectomía radical con colpectomía superior. En este procedimiento se diseca el pedículo lumbo-ovárico derecho y se conserva el ovario derecho que se aplica en el sector superior de la gotera parieto-cólica derecha, fuera de la pelvis. Se realiza la ooforectomía izquierda total que se entrega al equipo 2. Se dejó un drenaje aspirativo a través de la cúpula vaginal. La técnica quirúrgica (operación de Wertheim - Meigs) no prestó ningún tipo de complicaciones.
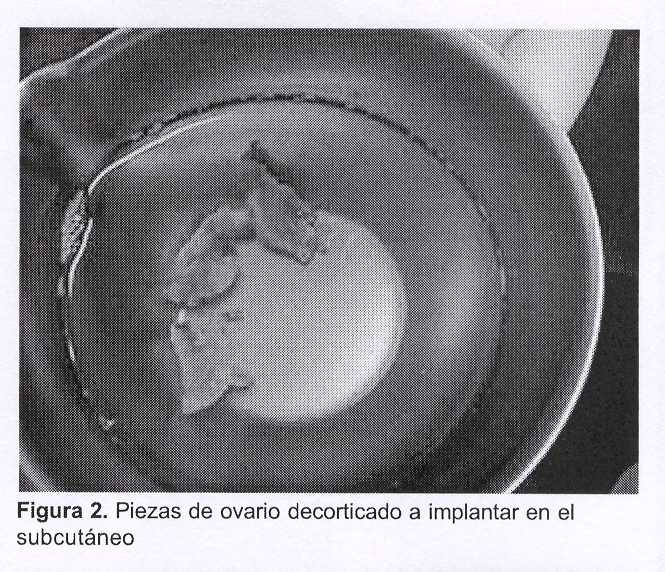
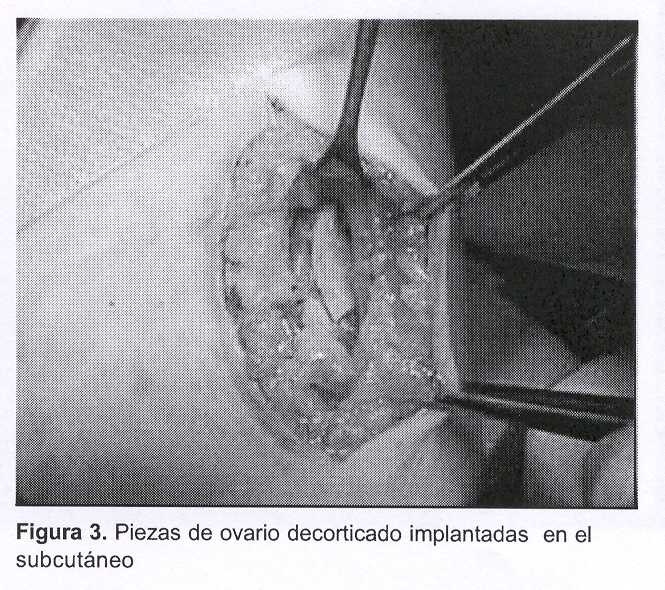
Equipo 2: simultáneamente a la cirugía oncológica, este equipo talló un bolsillo subcutáneo mediante una incisión longitudinal de 2 centímetros en la cara interna del tercio superior del brazo. Recibido el ovario izquierdo se procede a la decorticación, que se realizara bajo líquido de transporte RPMI 16-40 más albúmina humana a 10%, a efectos de preservar al máximo las condiciones de nutrición del tejido. El procedimiento que dura unos minutos se realiza a temperatura ambiente y se preparan fragmentos (ocho) de aproximadamente 5 mm x 3 mm. Estos son ubicados entre el celular y la aponeurosis, sin sutura. La pared se cierra por planos con Vicryl® (figuras 2 y 3).
Evolución. En la evolución posoperatoria no se presentaron complicaciones, se retiró el drenaje aspirativo por escasa colección a las 24 horas, retomó la vía oral a las 24 horas y el tránsito intestinal a las 72 horas. En la zona bicipital se palpaba un endurecimiento subcutáneo que remitió a los 30 días, un pequeño hematoma superficial se desarrolló en la zona del brazo, remitiendo espontáneamente.
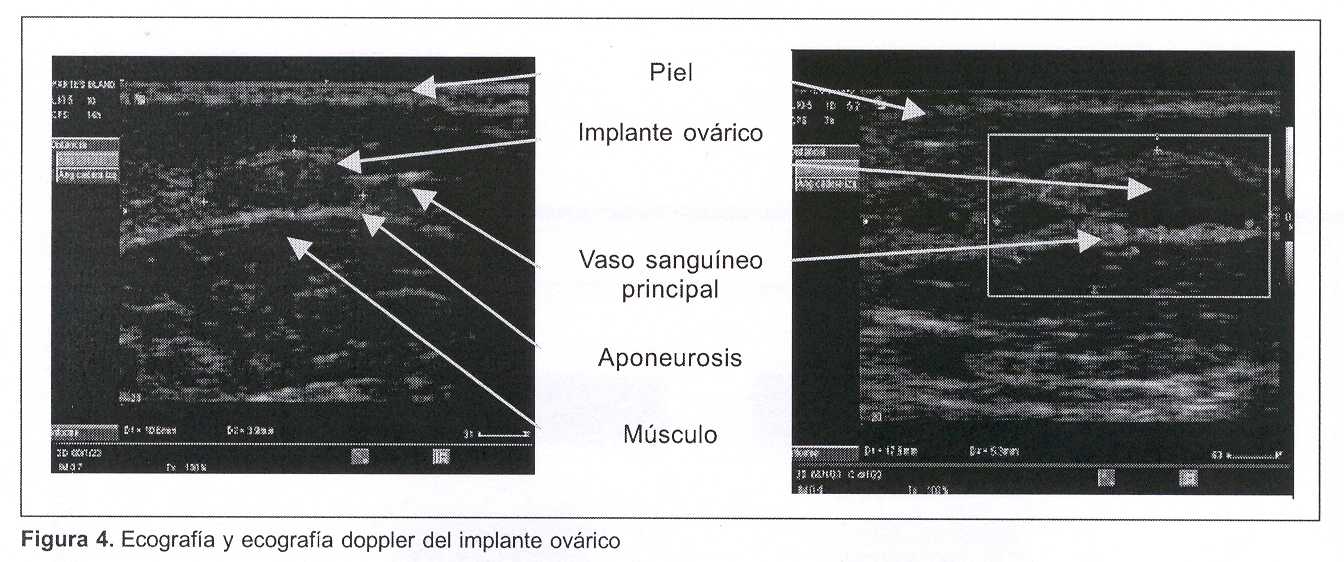
Seguimiento. El protocolo de seguimiento prevé un seguimiento estructural por medio de ecografía doppler (cabezal de 7,5 MHz) y un seguimiento funcional con dosificación de hormona folículo estimulante (FSH), a partir de los 60 días y luego en forma mensual.
(figura 4)
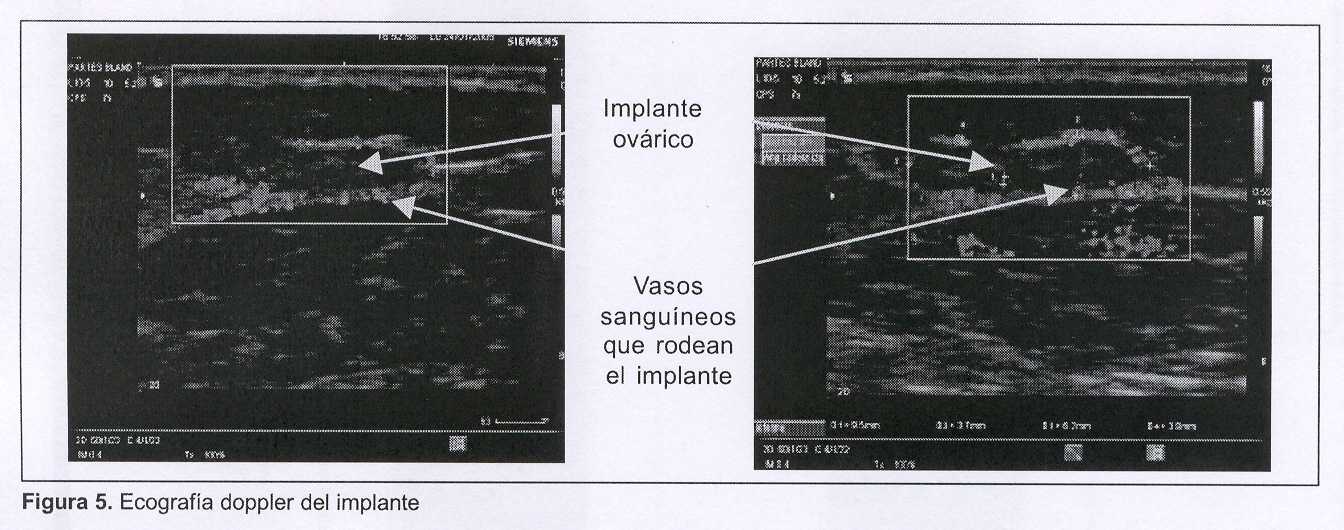
(Figura 5)
Ecografía y ecografía doppler. Se estudió mediante ecografía doppler a los 60 días de la cirugía, identificándose vascularización periférica al implante con un vaso dominante. Además, se visualizan imágenes compatibles con desarrollo folicular incipiente.
( Tabla 1)
Curvas de FSH y estradiol. Se realiza un seguimiento de la función ovárica mediante dosificaciones mensuales de FSH y estradiol tomando como punto de partida la dosificación preoperatoria. Se observa una rápida recuperación de la función endocrina ovárica luego de una afectación inmediata posoperatoria. Se debe aclarar que, dado que a la paciente se le traslocó el ovario izquierdo a nivel subhepático, además de realizar el injerto heterotópico, no se pudo identificar cuál de los dos ovarios es el predominante en la secreción de estradiol.
Discusión
Las pacientes con cáncer de cérvix de tipo epidermoide en sus estadios iniciales no presentan metástasis ováricas, por lo cual no estaría indicada su resección. Sin embargo, hasta que se realiza la cirugía y se estudia la invasión ganglionar no es posible saber si requerirán o no radioterapia complementaria. Los ovarios son particularmente sensibles a la misma, de tal forma que si es necesaria la radioterapia, la FOP es el resultado final esperable. La FOP implica la anulación total del futuro reproductivo, y desde el punto de vista endocrino presenta una enorme repercusión en la calidad de vida, exponiendo a la paciente a un mayor riesgo de osteoporosis, atrofia urogenital y sintomatología climatérica. La terapia de sustitución hormonal en estos casos simula pero no reproduce la situación endocrina de la paciente, siendo además una terapia no exenta de riesgos (trombosis). El dejar los ovarios en una posición pelviana, de ser necesaria la radioterapia, implica habitualmente la anulación de su función. Una forma de preservar la función es la translocación ovárica al espacio subfrénico, de forma de alejarlos del campo de radioterapia. Sin embargo, esto también se asocia con una alta frecuencia de falla ovárica y en ocasiones agrega complicaciones adicionales. La elongación del pedículo y la radioterapia complementaria suelen afectar la nutrición y con ello la función.
El caso que nos ocupa es el primero a nivel nacional de autotrasplante heterotópico en fresco de corteza ovárica al tejido celular del espacio bicipital. Esto busca alejar los ovarios del campo de radiación y un mejor resultado funcional a largo plazo. En este caso, dado que se trata de la primera experiencia nacional de trasplante ovárico, el equipo tratante decidió una estrategia mixta (translocación de un ovario y trasplante del otro). Esto busca aumentar las posibilidades de preservación de la función, manteniendo una estrategia "clásica" como la translocación, pero con un alto índice potencial de falla ovárica (más aun ante la eventualidad de recibir radioterapia complementaria) y una estrategia nueva con importantes ventajas teóricas.
En este caso la investigación del ganglio centinela fue dudosa, lo que obligó a realizar una linfaadenectomía abdómino-pélvica. Los estudios de los ganglios extraídos en la linfaadenectomía fueron todos negativos, por lo cual no requirió radioterapia complementaria. Se comprobó una caída de la función en el posoperatorio con una rápida recuperación, hecho que ocurre frecuentemente en este tipo de cirugía. Aunque, en este caso, no fue posible diferenciar la contribución en la secreción endocrina de cada ovario, pudo verificarse una rápida neovascularización de los implantes mediante eco-doppler y signos indirectos de desarrollo folicular. El tiempo que demora la recuperación de la función endocrina en los ovarios trasplantados es variable según los estudios. En los casos publicados por Callejo(15) (dos pacientes en las que sólo se realizaron implantes bicipitales) la síntesis hormonal se restableció a los tres y cuatro meses, siendo la duración de esta recuperación muy breve. Sin embargo, se destaca que estas pacientes son diferentes a nuestro caso, ya que ambas tenían una edad significativamente mayor (46 y 49 años respectivamente) por lo cual de hecho estaban en período premenopáusico. El caso publicado por Oktay es más similar al nuestro(16), con una paciente de 35 años en la cual se realizó sólo el implante braquial. En ella la recuperación de la función endocrina fue mucho más precoz: diez semanas. Esto permite plantear que, dada la recuperación hormonal y los elementos de neovascularización, los implantes puedan estar contribuyendo en parte a los niveles hormonales en nuestra paciente.
El lapso transcurrido entre la cirugía de implante y la neovascularización es crítico para la pérdida folicular, pudiéndose perder hasta 50% del capital folicular. Por ello, cuanto más joven es la paciente y mayor la densidad folicular, existe una mayor capacidad de soportar este proceso y una mayor chance de recuperación funcional. Una estrategia a explorar es la aceleración del proceso de angiogénesis, ya sea actuando sobre los factores angiogénicos en el implante o sobre el lecho receptor, de forma de reducir el tiempo hasta que se establece la neovascularización, y con ello tener una mayor chance de preservación de la función ovárica.
El tamaño de los implantes es otra variable a tener en cuenta. Como se observa en el doppler, la neoangiogénesis comienza en la superficie ovárica, por lo cual cuanto más fraccionado esté el implante (menor tamaño) mayor será la superficie expuesta a la neoangiogénesis. En nuestro caso se implantaron fragmentos algo mayores (ocho implantes de 5 mm x 2 mm) que en los casos de Callejo (40 implantes de 2 mm x 1mm). En un nuevo caso incluido recientemente en este protocolo, el equipo aumentó el número y redujo el tamaño de los implantes. Otra estrategia plausible es la inserción de los implantes subcutáneos por vía laparoscópica, buscando reducir el tamaño de la incisión cutánea y con ello el riesgo de infecciones.
En conclusión, los estudios muestran que los implantes heterotópicos de corteza ovárica en fresco son capaces de vascularizarse a través de un proceso de neoangiogénesis y con ello restituir la función endocrina. Se trata de una opción para mejorar las chances de preservar la función ovárica en pacientes con cáncer que eventualmente podrán ser sometidas a irradiación abdómino-pélvica.
Summary
Prognosis and cure rates of cervical cancer have increased during the last years due to early diagnosis and improved treatment. However, early diagnosis implies that a greater number of young women carriers of this disease are exposed to a iatrogenic affection of the wombs, as a consequence of cancer treatment. Preservation of ovarian endocrine function aims to prevent consequences of premature menopause and potential risks of hormonal replacement therapy. The purpose of this paper is to show the results of an auto-transplant of ovarian tissue to a heterotopic site (biceps).
A 33-year-old woman with a stage 1B cervical cancer underwent a surgery. One ovary was transferred to an extra-pelvic site and the other was auto-transplanted to the arm to prevent it from radiotherapy exposure. Post-surgical follow up showed a constant level of sexual steroids and fast revascularization of transplanted fragments at a biceps level. This procedure is seen as an adequate option to preserve endocrine function in young women with cervical cancer.
Résumé
Le pronostic et la guérison du cancer de col de l’utérus sont actuellement plus avancés grâce à un diagnostic précoce et à un meilleur traitement. Cependant, le diagnostic précoce fournit un nombre plus large de patientes ayant cette maladie, exposées à une atteinte iatrogénique ovarienne secondaire au traitement du cancer. Il s’avère donc très important de préserver la fonction endocrinienne ovarienne et d’éviter une ménopause prématurée ou les risques d’une thérapie de substitution hormonale.
On présente le premier cas dans notre pays d’autogreffe de tissu dans un site hétérotopique (biceps). Une patiente de 33 ans ayant un cancer de col de l’utérus en stade 1B qui au cours d’une chirurgie oncologique a subi une transposition d’un ovaire dans un site extra-pelvien et on fit une autogreffe de l’autre dans le bras, afin d’éviter l’exposition à une éventuelle irradiation complémentaire. Le suivi post-opératoire a révélé un niveau soutenu de stéroïdes sexuels et une rapide revascularisation des fragments greffés.
Cette procédure est envisagée comme un des choix utiles pour préserver la fonction endocrinienne chez des patientes jeunes à cancer cervical.
Bibliografía
1. Larsen EC, Muller J, Schmiegelow K, Rechnitzer C, Andersen AN. Reduced ovarian function in long-term survivors of radiation- and chemotherapy-treated childhood cancer. J Clin Endocrinol Metab 2003; 88(11): 5307-14.
2. Coppleson M, Monaghan JM, Morrow CP, Tattersall MH. Cervical cancer. In: Coppelson M, ed. Gynecologic oncology. 2nd ed. New York: Churchill Livingstone, 1992: 457-523.
3. Sutton GP, Bundy BN, Delgado G, Sevin BU, Creasman WT, Major FJ, et al. Ovarian metastases in stage IB carcinoma of the cervix: a Gyneacologic Oncology Group Study. Am J Obstet Gynecol 1992; 166(1 Pt 1): 50-3.
4. Parente JT, Silberblatt W, Stone M. Infrequency of metastasis to ovaries in stage I carcinoma of the cervix. Am J Obstet Gynecol 1964; 90: 1362.
5. Wu HS, Yen MS, Lai CR, Ng HT. Ovarian metastasis from cervical carcinoma. Int J Gynaecol Obstet 1997; 57(2): 173-8.
6. McCall ML, Keaty EC, Thompson JD. Conservation of ovarian tissue in the treatment of carcinoma of the cervix with radical surgery. Am J Obstet Gynecol 1958; 75(3): 590-600.
7. Meirow D, Nugent D. The effects of radiotherapy and chemotherapy on female reproduction. Hum Reprod Update 2001; 7(6): 535-43.
8. Lushbaugh CC, Casarett GW. The effect of gonadal irradiation in clinical radiation therapy: a review. Cancer 1976; 37(2 Suppl): 1111-25.
9. Morice P, Junker L, Rey A, El-Hassan J, Haide-Meder C, Castaigne D. Ovarian transposition for patients with cervical carcinoma treated by radiosurgical combination. Fertil Steril 2000; 74(4): 743-8.
10. Hodel K, Rich WM, Austin P, DiSaia PJ. The role of ovarian transposition in conservation of ovarian function in radical hysterectomy followed by pelvic radiation. Gynecol Oncol 1982; 13(2): 195-202.
11. Chambers SK, Chambers JT, Kier R, Peschel RE. Sequelae of lateral ovarian transposition in irradiated cervical cancer patients. Int J Radiat Oncol Biol Phys 1991; 20(6): 1305-8.
12. Feeney DD, Moore DH, Look KY, Stehman FB, Sutton GP. The fate of the ovaries after radical hysterectomy and ovarian transposition. Gynecol Oncol 1995; 56(1): 3-7.
13. Anderson B, LaPolla J, Turner D, Chapman G, Buller R. Ovarian transposition in cervical cancer. Gynecol Oncol 1993; 49(2): 206-14.
14. Hilders CG, Baransky AG, Peters L, Ramkhelawan A, Trimbos JB. Susccessful human auto-transplantation to the upper arm. Cancer 2004; 101(12): 2771-8.
15. Callejo J, Salvador C, Miralles A, Vilaseca S, Lailla JM, Balasch J. Long-term ovarian function evaluation after autografting by implantation with fresh and frozen-thawed human ovarian tissue. J Clin Endocrinol Metab 2001; 86(9): 4489-94.
16. Oktay K, Economos K, Kan M, Rucinski J, Veeck L, Rosenwaks Z. Endocrine function and oocyte retrieval after autologous transplantation of ovarian cortical strips to the forearm. JAMA 2001; 286(12): 1490-3.