Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Médica del Uruguay
versión On-line ISSN 1688-0390
Rev. Méd. Urug. vol.21 no.2 Montevideo jun. 2005
Análisis de sobrevida de una población con cáncer de mama y su relación con factores pronósticos: estudio de 1.311 pacientes seguidas durante 230 meses. Trabajo de equipo multidisciplinario
Dres. Tabaré Vázquez*, Gabriel Krygier†, Enrique Barrios‡, Sandra Cataldi§, Álvaro Vázquez¶, Ing. Rafael Alonso††, Dres. Fernando Estellano‡‡, Enrique Folle§§, Raúl Laviña§§, Fernando Delgado¶¶, Carlos Pressa†††
CENDIMA (Centro de Diagnóstico Mamario)
AEPSM (Asociación Española Primera de Socorros Mutuos)
Laboratorio de Bioestadística. Departamento de Biofísica de la Facultad de Medicina
Resumen
A partir de una población de 1.311 mujeres con cáncer de mama diagnosticadas, tratadas y seguidas en un mismo centro de patología mamaria, el Centro de Diagnóstico Mamario (CENDIMA), durante un lapso de 230 meses, se realiza el análisis descriptivo, el análisis de sobrevida y el de sobrevida libre de enfermedad correlacionándolo con factores pronósticos conocidos para dicha enfermedad.
Los dos parámetros de mayor peso pronóstico con valor estadístico para esta población en relación con el intervalo libre de enfermedad fueron el estatus ganglionar y el estadio; el estatus ganglionar y el score histológico final se constituyeron, asimismo, en las variables principales en lo que hace a la sobreviva global.
Los datos finales obtenidos son comparables a los encontrados en la literatura internacional.
Palabras clave: NEOPLASMAS DE LA MAMA.
ANÁLISIS DE SUPERVIVENCIA.
* director del CENDIMA. Ex Prof. del Servicio de Radioterapia de la Facultad de Medicina.
† Profesor Adjunto de Oncología Médica, Facultad de Medicina.
‡ Profesor Agregado de Biofísica, Laboratorio de Bioestadística, Facultad de Medicina.
§ Asistente de Oncología Médica, Facultad de Medicina.
¶ Residente de Oncología Médica.
†† Profesor Adjunto de Métodos Cuantitativos, Asistente de Bioestadística de la Escuela de Nutrición y Dietética, Facultad de Medicina.
‡‡ Ex Residente de Cirugía.
§§ Ex Profesor Adjunto de Clínica Quirúrgica, Facultad de Medicina.
¶¶ Ex Profesor Agregado de Clínica Quirúrgica, Facultad de Medicina.
††† Profesor Agregado de Clínica Quirúrgica, Facultad de Medicina.
Correspondencia: Dr. Gabriel Krygier
Br. Artigas 1438. CENDIMA - AEPSM. Montevideo. Uruguay
E-mail: hrygier@mednet.org.uy
Recibido: 10/12/04.
Aceptado: 13/03/05.
Introducción
El cáncer de mama constituye un enorme problema sanitario a nivel mundial, siendo el más frecuente en la mujer del mundo occidental y, en particular, en los países desarrollados.
A nivel mundial es responsable de unas 300.000 muertes al año; tiene una incidencia ascendente y representa 21% del total de los tumores femeninos(1).
Nuestro país presenta un perfil epidemiológico en todo similar, representando esta enfermedad el cáncer con mayor incidencia en la mujer uruguaya y constituyendo la primera causa de muerte por cáncer en la mujer(2). Según datos de la Comisión Honoraria de Lucha contra el Cáncer (CHLCC) anualmente se registran 1.800 nuevos casos y aproximadamente 630 mujeres mueren por año; estas cifras ilustran claramente la magnitud del problema en nuestro medio(3).
En el pasado, la enfermedad se diagnosticaba con mayor frecuencia en etapas avanzadas; afortunadamente y gracias a la amplia difusión del screening mamográfico, cada vez se llega al diagnóstico en etapas más precoces, con lo cual ha aumentado en forma significativa la detección del carcinoma ductal in situ (DCIS). Al momento actual, 20% a 30% de todos los cánceres diagnosticados por mamografía corresponden a DCIS. De éstos, aproximadamente 80% son detectados mamográficamente y 20% se presentan como masa palpable. Esto, sumado a la mejoría de las herramientas terapéuticas, ha contribuido a la mejora sustantiva en el pronóstico de la enfermedad, siendo posible en el momento actual lograr sobrevidas globales superiores a 70% a cinco años(4).
Varios factores de riesgo han sido asociados con el cáncer de mama; el sexo femenino es el principal ya que más de 99% de los cánceres de mama ocurren en la mujer.
La edad mayor a 50 años, el diagnóstico previo de cáncer de mama, la historia familiar de cáncer de mama u ovario y la hiperplasia ductal atípica, histológicamente comprobada, constituyen otros factores de riesgo alto.
Otros factores de riesgo significativo pero de menor peso que los anteriores son: menarca precoz, menopausia tardía, nuliparidad, primer parto a término luego de los 30 años, lactancia pobre, hormonoterapia de reemplazo, muchos de ellos vinculados a la exposición más prolongada de las células mamarias a los efectos estimuladores de los estrógenos y progestágenos(5).
La obesidad, la dieta rica en grasas y el alcohol tienen una influencia menor.
Es bien conocido el impacto que distintos factores pronósticos tienen en la sobrevida, siendo importante su identificación con vistas a elaborar la más adecuada estrategia terapéutica. El estatus axilar es indudablemente el de mayor valor; así las pacientes sin compromiso metastásico a nivel axilar tienen hasta 30% de recaídas a los cinco años, mientras que aquellas con axila positiva recaen globalmente entre 50% y 75% en ese lapso. También es de valor el número de ganglios comprometidos, aumentando la tasa de recurrencia en concordancia con el número de ganglios afectados(6). El tamaño tumoral es otro factor pronóstico que cobra mayor jerarquía cuando los ganglios axilares están indemnes. El grado histológico, determinado fundamentalmente por la túbulo formación, el grado nuclear y el índice mitótico en forma combinada determinan el score histológico final, cuyo rango va de 3 a 9, empeorando el pronóstico a medida que aumenta el score. La presencia de receptores hormonales (RH), de estrógeno y progesterona en el tumor no sólo es un factor predictivo de respuesta a la endocrinoterapia, sino que también constituye un factor pronóstico independiente para la sobrevida, siendo esta mejor cuando están presentes(7).
Otros factores pronósticos aunque menores son la invasión linfovascular intratumoral y el compromiso perineural.
Una activa investigación ha postulado el valor que otros factores podrían tener, tales como la sobreexpresión tumoral de HER-2-neu (asociada a un peor pronóstico), mutación del gen p53, expresión del receptor de factor de crecimiento epidérmico, catepsina D, presencia de micrometástasis en médula ósea, pero su aplicabilidad clínica aún es limitada(8).
La mayoría de los cánceres son ductales, representando aproximadamente 80% del total, 10% lobulares, 5% medulares y el 5% restante integrado por tumores bien diferenciados (tubulares, papilares, coloides, adenoide quísticos) con mejor pronóstico. El cáncer inflamatorio, independientemente del tipo histológico subyacente, es de pronóstico más pobre(9).
El presente trabajo intenta realizar un análisis descriptivo, de evolución clínica y de sobrevida libre de enfermedad y global de una población numerosa de más de 1.300 pacientes con cáncer de mama y su correlación con los citados factores pronósticos.
Objetivos
Objetivo principal
El objetivo principal de este trabajo es analizar la sobrevida de una población mutual con cáncer de mama homogéneamente tratada en un centro para el diagnóstico y tratamiento de dicha enfermedad.
Asimismo, se intentará relacionar la sobrevida de dicha población con factores pronósticos ya conocidos internacionalmente pero aún no documentados en nuestro medio (edad, tamaño tumoral, balance ganglionar axilar, hallazgos histopatológicos y receptores hormonales).
Objetivo secundario
Los objetivos secundarios son:
– Analizar el intervalo libre de enfermedad de esta población evaluando la importancia pronóstica de las mismas variables definidas en el objetivo principal.
– Definir las características de la población estudiada en relación con otras variables (antecedentes ginecoobstétricos, tratamientos recibidos, etcétera).
Material y método
Desde el 1º de julio de 2002 hasta el 1º de marzo de 2004 se revisaron 1.542 historias de pacientes portadoras de cáncer de mama del archivo del CENDIMA (Centro de Diagnóstico Mamario) de la Asociación Española Primera de Socorros Mutuos (AEPSM).
Se correlacionaron los datos obtenidos con los de la historia central de la AEPSM, es decir que para cada paciente se revisaron ambas historias (CENDIMA y AEPSM).
Se desarrolló y confeccionó previamente una base de datos específicamente diseñada para almacenar y procesar informáticamente los datos recogidos.
La misma incluía datos referentes a la ficha patronímica (edad, sexo, antecedentes ginecoobstétricos, antecedentes familiares de cáncer de mama u ovario), motivo de consulta (cuando era sintomática) o nódulo subclínico (cuando era un hallazgo mamográfico), fecha de la cirugía y características de la misma (conservadora, radical, si hubo más de un acto quirúrgico, etcétera), informe detallado de la anatomía patológica (con histología principal y accesoria, mayor tamaño tumoral, grado histológico, grado nuclear, índice mitótico, score final, número de ganglios colonizados, macrometástasis, ruptura capsular y embolias linfovasculares, multifocalidad y multicentricidad, margen de resección, compromiso de piel y pezón, tumor inflamatorio), bilateralidad (sincrónica o metacrónica) y estadificación (TNM).
En otro sector de la planilla se detallaba el tratamiento asociado recibido: radioterapia (que incluía dosis total y fracción, campos, complicaciones), quimioterapia (adyuvante, neoadyuvante y complementaria; esquema, número de ciclos, complicaciones) y hormonoterapia (neoadyuvante, adyuvante o sistémica con sus características).
Asimismo se constataban las recaídas (primera, segunda, tercera) documentando la(s) fecha(s), sitio y tratamiento recibido.
En caso de debutar como enfermedad diseminada se llenaba directamente la columna correspondiente y el tratamiento recibido.
En caso de haber sido controlada exclusivamente se llenaba una columna específica, habiendo tres columnas para la rehabilitación: física, preventiva del linfedema, quirúrgica (prótesis) y psicológica.
Finalmente se constataba el estatus (viva, fallecida, pérdida de seguimiento), la fecha del último control en la institución, la causa del fallecimiento (oncológica o no), fecha de revisada, qué colega la había revisado y un espacio para observaciones varias.
Los datos recabados en la planilla fueron doblemente chequeados por distintos revisores para minimizar los errores de transcripción de la historia clínica a la correspondiente base de datos.
Una vez corroborados los datos extraídos se pasaron del papel a la planilla electrónica.
Del 1º de marzo de 2004 al 10 de marzo de 2004 se actualizaron para todos los pacientes el estatus de vivo o fallecido dado que entre el comienzo del trabajo (julio de 2002) y el fin del mismo (marzo de 2004) pudieron ocurrir eventos que alteraran el estatus final (recaída, fallecimiento, etcétera).
Para dicha tarea se contó con el apoyo del sector administrativo del CENDIMA y del área de informática de la AEPSM.
Para la incorporación de los datos de la planilla escrita a la planilla electrónica se utilizó un programa de Excel correspondiente a un sistema operativo Windows 2000.
Para los análisis estadísticos se utilizaron los siguientes softwares específicos: SPSS (versión 11.0) y SAS (versión 6.0).
Los análisis de la distribución estadística de los tiempos de "fallo" (sobrevida e intervalo libre de enfermedad) se llevaron a cabo usando el método de Kaplan-Meier(10), para el contraste univariado se utilizó el Logrank test(11) y para el análisis multivariado se apeló al modelo de riesgos proporcionales de Cox(12). Las hipótesis de proporcionalidad de riesgo fueron verificadas por métodos analíticos y gráficos.
Resultados
De las 1.542 historias revisadas y con el fin de homogeneizar la muestra quedaron finalmente 1.311 para el análisis de sobrevida, descartándose para este análisis las historias de pacientes cuyo primer tratamiento fuera realizado previo al año 1985 (136 casos), pacientes del sexo masculino (4 casos), los tumores bilaterales (57 casos), dado que para el cálculo de la sobrevida se tomó como un solo paciente con dos tumores (tomando el primer tumor para el cálculo de sobrevida), las pacientes que no recibieron cirugía como parte del tratamiento inicial (20 pacientes), dado que constituían un número muy pequeño de pacientes añosas que por motivos médicos no pudieron operarse, y los que tuvieron sobrevidas menores a dos meses (4) donde pudieron influir claramente otros factores.
Análisis descriptivo
– Variables demográficas
Ya comentamos que de la muestra inicial se descartaron cuatro casos del sexo masculino, por lo que toda la muestra analizada (1.311 pacientes) fue del sexo femenino.
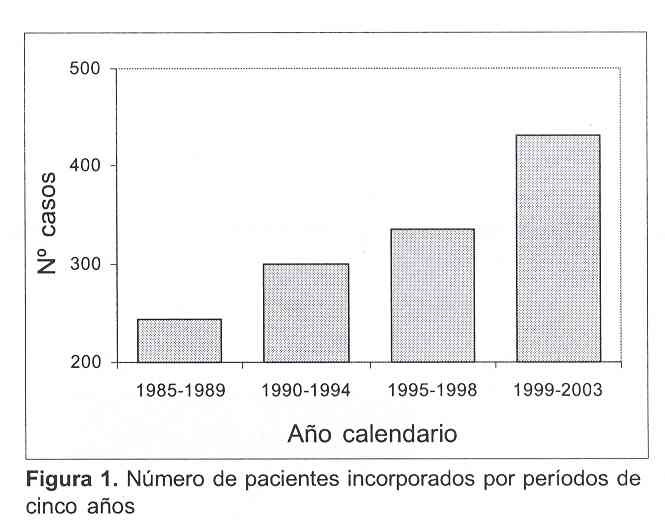
La incorporación de pacientes fue progresivamente creciente con los años; si se divide en períodos de cinco años, se observa claramente que el período 1999-2003 fue el que incorporó más pacientes (más de 400, figura 1).
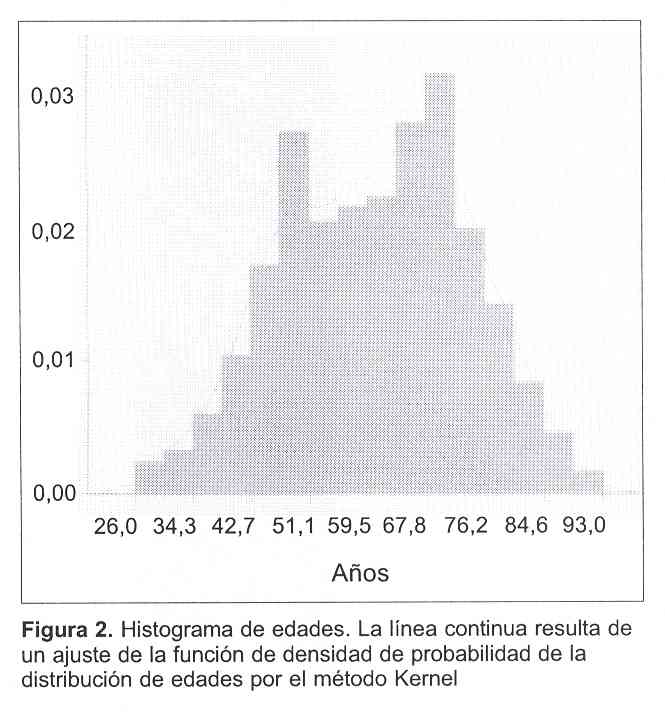
En cuanto a la edad al diagnóstico de tumor, en 1.310 pacientes se pudo extraer el dato de la historia y se observó una clara curva bimodal de presentación con un pico inicial a los 52 años y otro a los 67 años (figura 2). La media fue de 60,59 (desvío estándar 13,33) con una mediana de 61 años (rango 26 a 93 años).
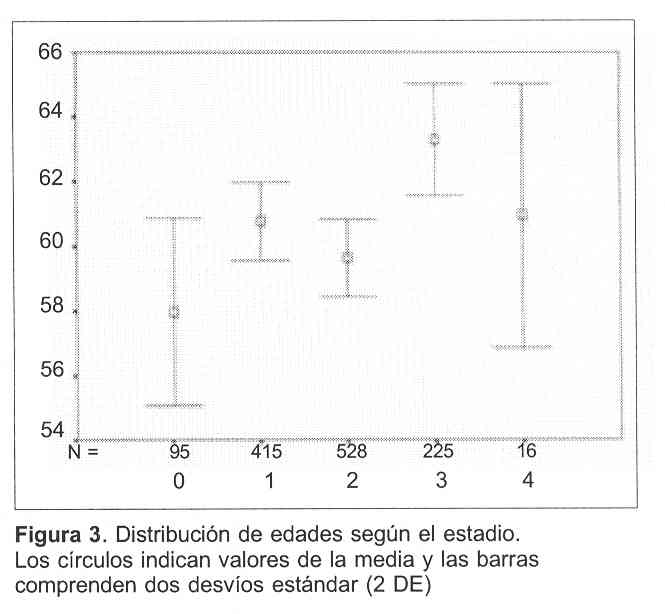
En la figura 3 se observa la distribución de las edades para cada estadio (permite distinguir la media y dos desvíos estándar para cada estadio).
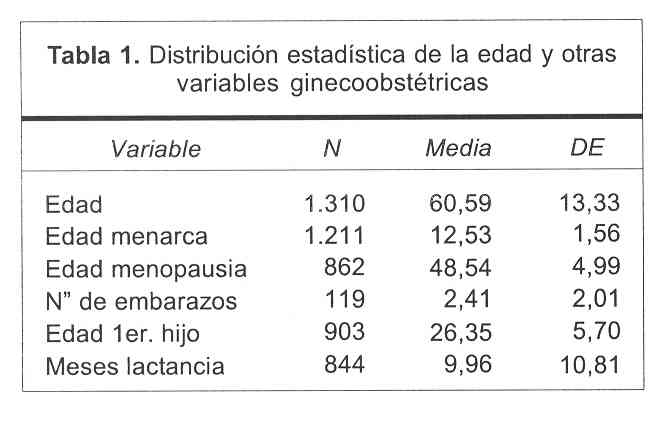
– Variables ginecoobstétricas (tabla 1)
La media para la edad de la menarca fue de 12,53 (desvío estándar 1,56) con una mediana de 12 años (rango 8 a 19 años) en las 1.211 pacientes en que este dato constaba en la historia.
La toma de anticonceptivos orales lamentablemente no pudo evaluarse correctamente en esta población ya que sólo en 45 historias figuraba este dato (elemento que luego analizaremos en la discusión).
En 1.119 pacientes figuraba el número de embarazos, donde se obtiene que 140 no tuvieron embarazos, y de las 979 que sí tuvieron embarazos, la media fue de 2,41 (desvío estándar 2,01) con una mediana de 2 (rango 0 a 17); en 192 casos no se obtuvo este dato.
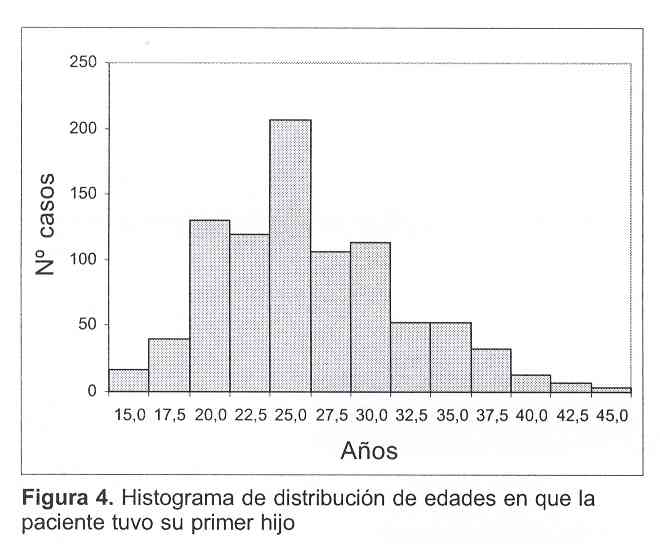
En 903 pacientes figuraba la edad del primer hijo, con una media de 26,35 años (desvío estándar 5,70) y una mediana de 26 años (rango 14-45) (figura 4).
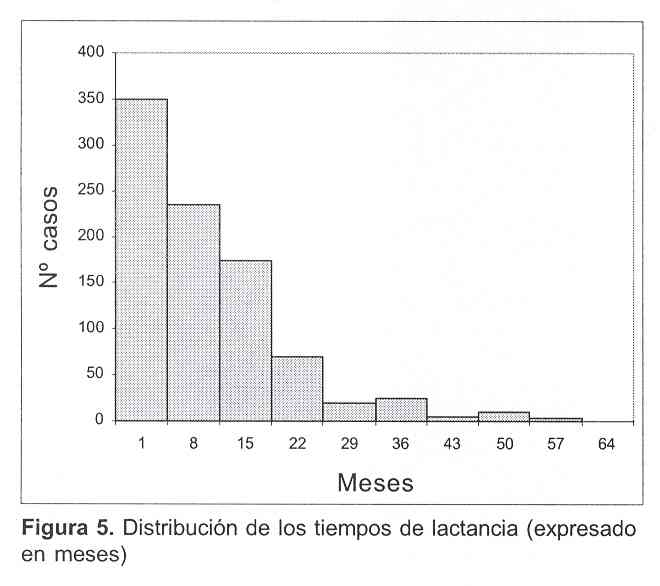
La duración de la lactancia medida en meses se obtuvo en 844 casos con una media de 9,96 (desvío estándar 10,81) y una mediana de 6 meses (figura 5).
Para la variable menopausia, este dato se extrajo de 862 pacientes, destacándose una media de 48,54 (desvío estándar 4,99), con una mediana de 50 años (rango 37 a 68).
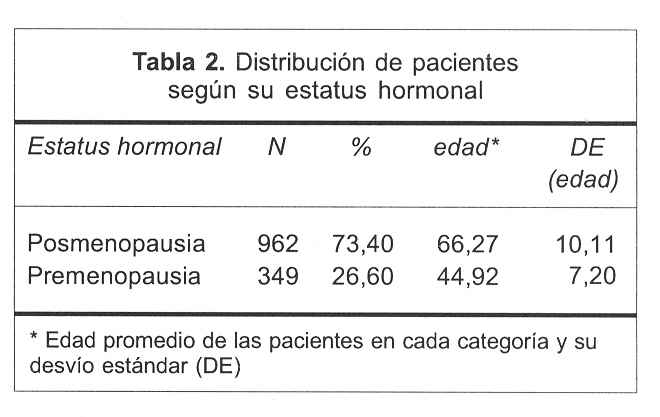
En la tabla 2 se muestra la distribución de las pacientes según el estatus hormonal; como se puede ver, 349 pacientes fueron premenopáusicas (26,6%) con una media de edad al diagnóstico de 44 años (desvío estándar 7,20); 962 pacientes eran posmenopáusicas (73,4%) con una media de 66,27 años al diagnóstico (desvío estándar 10,11). Como se desprende de estos datos, en el grupo de las posmenopáusicas existen 100 pacientes en las cuales no constaba el dato de la edad en que se alcanzó la menopausia pero sí su condición de posmenopáusica.
– Motivo de consulta
Para analizar esta variable se codificaron previo al ingreso de los datos en siete items: tumor, signos inflamatorios, secreción por el pezón, dolor sin inflamación, hundimiento del pezón, ganglio axilar al debut y sin datos. Se encontraron 150 casos que concurrieron asintomáticas a control, hallándose en la mamografía un tumor; todas ellas fueron reportadas como nódulos subclínicos y agrupan más de 30% de los carcinomas in situ de esta muestra (31,58%). De todos los nódulos subclínicos, 75% correspondió a estadios 0 y 1 (30 pacientes en estadio 0 y 82 pacientes en estadio I).
En 163 pacientes este dato no estaba reportado en la historia del CENDIMA ni en la historia central de la AEPSM (la gran mayoría correspondió a historias previas al año 1990).
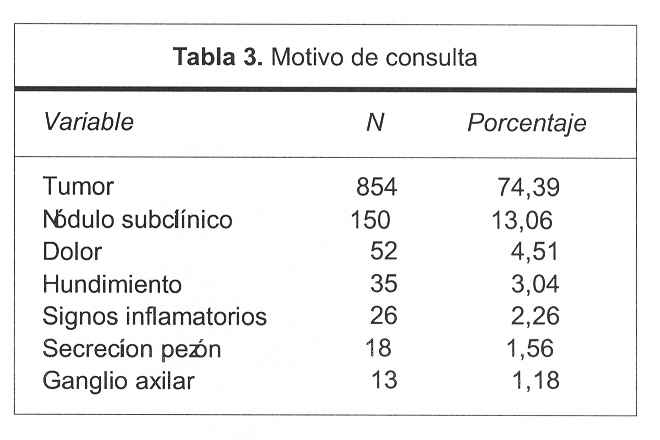
Del resto de las historias, la tumoración mamaria fue el motivo de consulta en 854 casos (85,6%), seguido de dolor como síntoma aislado en 52 casos (5,2%), destacándose la presentación como axila positiva en tumor mamario inicialmente oculto en 13 casos (1,3%) (tabla 3).
– Cirugía
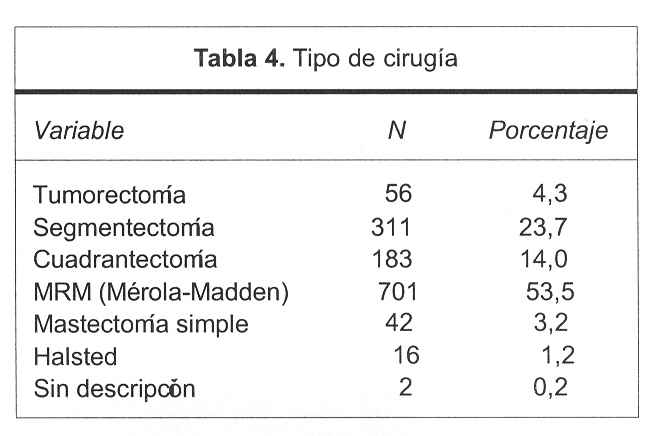
Las 1.311 pacientes analizadas fueron sometidas a cirugía como parte del esquema de tratamiento inicial codificándose la misma en cirugía conservadora (tumorectomía, segmentectomía y cuadrantectomía) y cirugía radical (mastectomía radical modificada tipo Mérola-Madden, mastectomía simple y mastectomía radical tipo Halsted). Hubo sólo dos pacientes donde no constaba en la historia el tipo de cirugía realizada ni el protocolo operatorio y 20 pacientes descartadas previamente por no haber sido sometidas a cirugía como parte del tratamiento inicial.
En caso de haber sido sometidas a más de un acto quirúrgico inicial se tomó para el análisis final la cirugía mayor.
Los resultados obtenidos muestran que 550 pacientes (41,9%) fueron sometidas a cirugía conservadora como tratamiento quirúrgico principal y 759 (57,9%) recibieron cirugía radical, ya sea de inicio o como complemento de la cirugía conservadora inicial; como ya mencionamos, en dos casos no se obtuvo el dato de la cirugía, si bien fueron operadas inicialmente.
El porcentaje de distribución de las cirugías por tipo fue el siguiente: la segmentectomía se utilizó como único acto quirúrgico en 311 casos (23,7%), la cuadrantectomía en 183 (14%) y la tumorectomía aislada en 56 casos (4,3%).
En cuanto a las cirugías más radicales, la gran mayoría correspondió a mastectomía radical modificada (Mérola o Madden) en 701 pacientes (53,5%), en 42 casos (3,2%) se realizaron mastectomías simples (generalmente en pacientes añosas) y sólo 16 casos correspondieron a la técnica de Halsted (tabla 4).
– Anatomía patológica
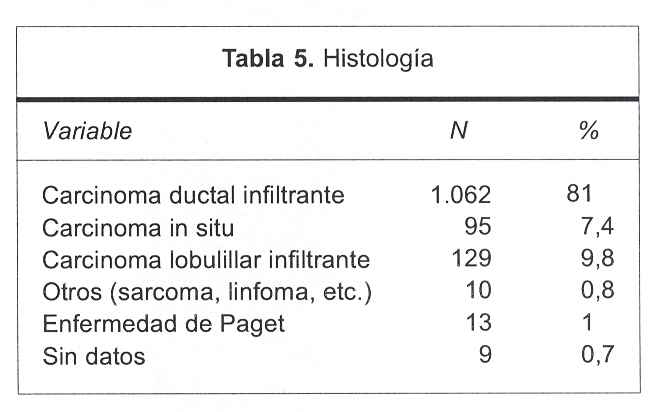
La variable histología se codificó en 17 columnas donde se incluyeron los carcinomas in situ (ductal comedónico, ductal no comedónico, lobulillar y papilar), los carcinomas ductales infiltrantes (NOS, tubular, papilar, mucinoso, medular, apócrino y metaplásico), el carcinoma lobulillar infiltrante, la enfermedad de Paget y otros (sarcomas, linfomas, carcinomas escamosos).
La enorme mayoría de los casos (1.062 pacientes) correspondió al carcinoma ductal infiltrante (81%); dentro de este grupo predominó la variante NOS (non otherwise specified) en 964 casos (73,5%), la tubular (3,5%), mucinoso (1,6%), medular (1,5%) correspondiendo 0,9% al resto de las variantes (tabla 5).
En 129 pacientes (9,8%) la histología carcinoma lobulillar infiltrante fue la predominante.
Es de destacar en el análisis de esta población que el carcinoma in situ (con todas sus variables) fue el único hallazgo histológico en 95 casos (7,4%), siendo en su mayoría ductales comedónicos (3,3%) y no comedónicos (3,1%).
La enfermedad de Paget se observó sólo en 13 pacientes (1%).
En diez casos (0,8%) la histología final integró el grupo otros (sarcomas, linfomas, carcinomas escamosos, etcétera), siendo este grupo excluido del análisis final de sobrevida.
No se obtuvieron datos específicos de la histología neoplásica en nueve historias (0,7%) si bien todas ellas fueron tratadas como carcinomas mamarios infiltrantes.
– Factores pronósticos primarios
En lo que respecta al tamaño tumoral (T), tomando el mayor diámetro, se pudo obtener en 1.207 pacientes con una media de 22,96 mm (desvío estándar 15,30), y una mediana de 20 mm (rango 1 a 140); no pudo obtenerse el T en la mayoría de los carcinomas in situ, que de cualquier forma se estadificaron como Tis.
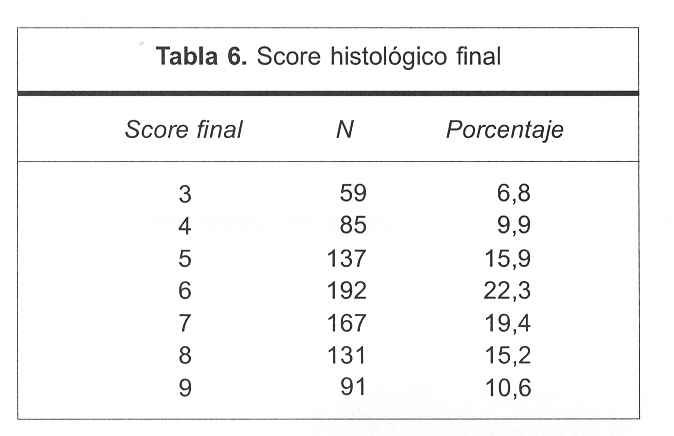
En 862 pacientes contamos con datos relativos al grado histológico, grado nuclear e índice mitótico, cuya suma constituye el score histológico final. La gran mayoría de los tumores (57,6%) correspondieron a un score final intermedio (5 a 7), habiendo 16,7% de casos de bajo grado final (3 y 4) y 25,8% de alto grado (score final 8 y 9) (tabla 6).
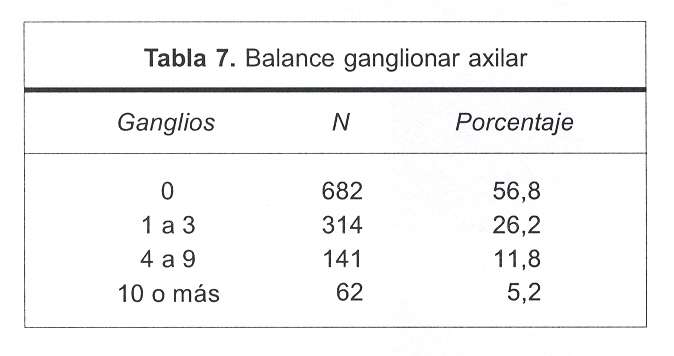
En cuanto al balance ganglionar, 1.199 historias aportaron dicho dato, observándose que 682 pacientes no tenían ganglios afectados (56,8%), mientras que los restantes 517 pacientes tenían balance ganglionar positivo distribuido de la siguiente forma: menor o igual a 3 ganglios en 314 casos, 4 a 9 ganglios en 141 casos y los restantes 62 pacientes tuvieron 10 o más ganglios afectados (tabla 7).
La media de afectación ganglionar fue de 2,00 (desvío estándar 4,30) y la mediana fue cero ganglio afectado; en 112 pacientes analizados faltaba ese dato (entre ellos, los carcinomas in situ en cuya mayoría no fue realizado el balance ganglionar tomándose estos casos como no clínicos). De los pacientes con balance ganglionar positivo la mitad (50,4%) tenía macrometástasis y 42,9% de ellos tenía ruptura capsular (113 pacientes), coincidiendo en su mayoría con compromiso ganglionar masivo.
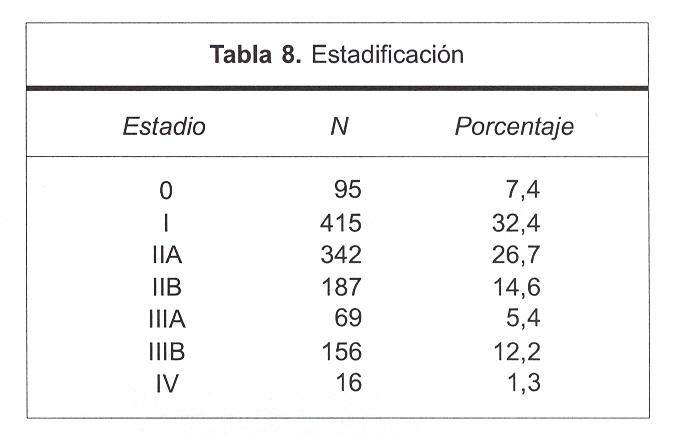
Estos elementos (tamaño tumoral, balance ganglionar) junto a los datos obtenidos de la historia sobre estadificación (que también fueron constatados en la planilla de Excel original), nos permitieron estadificar a 1.281 pacientes (tabla 8).
Si bien desde julio de 2003 los pacientes nuevos ingresados al CENDIMA son clasificados siguiendo la última versión (sexta) del TNM, dado que la mayoría de los pacientes incorporados en este análisis son de fechas anteriores, se tomó en cuenta para la estadificación final la quinta versión del TNM, reestadificando los últimos pacientes para homogeneizar la muestra final.
El estadio 0 (carcinoma in situ, Tis) abarcó a 95 pacientes (7,4%).
El estadio I (que en nuestro caso, como ya fue explicado, incluyó a los T1mic), comprendió a 415 pacientes (32,4%).
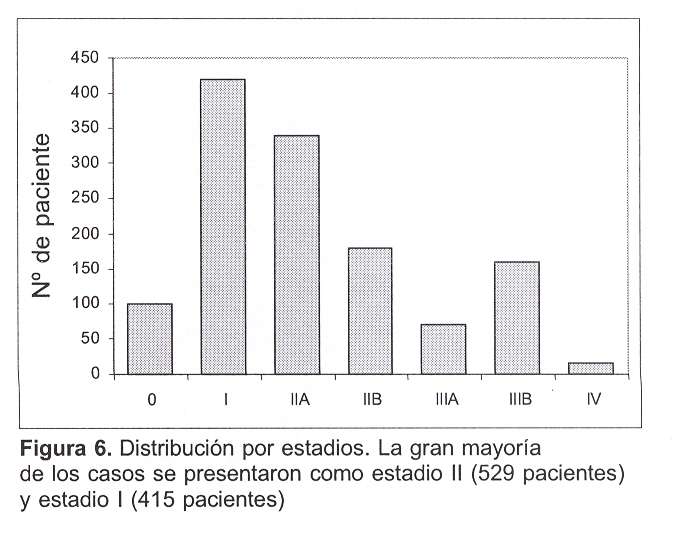
La gran mayoría de los pacientes fue agrupada en el estadio II, 529 casos (41,3%); en el estadio IIA fueron ubicados 342 casos (26,7%) y en el estadio IIB, 187 casos (14,6%) (figura 6).
El estadio III agrupó a 225 pacientes (17,6%), que se subdividieron en IIIA (5,4%) y IIIB (12,2%).
Por último, sólo 16 pacientes (1,3%) fueron diagnosticadas en estadio IV.
Sólo 31 pacientes de la muestra inicial no lograron estadificarse por falta de datos concluyentes.
La dosificación de receptores hormonales, dato de alto valor pronóstico, fue evaluable en sólo 552 casos (42,1%), hecho comprensible tomando en cuenta que hasta 1995 no era exigible en forma obligatoria en las instituciones de asistencia médica colectiva(13).
Los valores obtenidos provienen en su enorme mayoría (82,6%) de la inmunohistoquímica; hay un porcentaje (14,1%) en que no consta en la historia el método de obtención y sólo en 3,3% de los casos se obtuvo por método bioquímico.
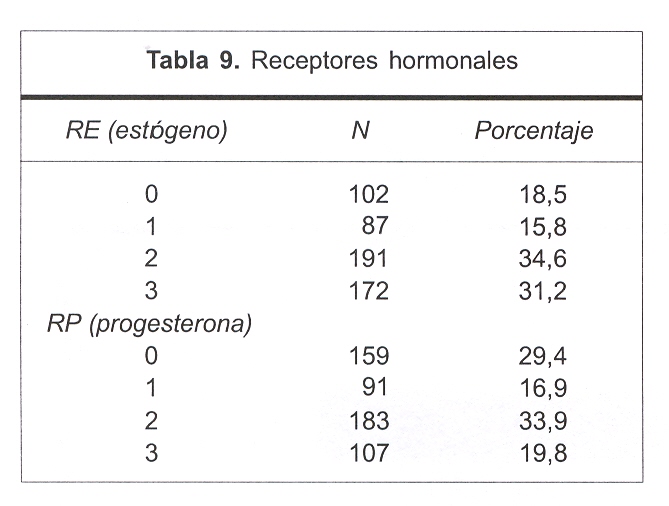
Para homogeneizar la muestra se categorizó en 0 (receptor negativo), 1 (receptor débilmente positivo), 2 (receptor moderadamente positivo) y 3 (receptor intensamente positivo) (tabla 9).
Para el receptor de estrógeno, 18,5% fue negativo, 15,8% débilmente positivo, 34,6% moderadamente positivo y 31,2% intensamente positivo.
Para el receptor de progesterona, 29,4% fue negativo, 16,9% débilmente positivo, 33,9% moderadamente positivo y 19,8% intensamente positivo.
– Tratamiento
Los datos de la(s) cirugía(s) recibida(s) ya fueron oportunamente comentados.
Dado que la intención de este trabajo no incluye un análisis de los tratamientos recibidos sólo comentaremos los resultados hallados como dato descriptivo.
Un total de 899 pacientes (68,6%) recibieron radioterapia como tratamiento complementario (la gran mayoría asociada a cirugía conservadora), en su casi totalidad bajo un mismo esquema de fraccionamiento y dosis total recibida.
Sólo 270 pacientes (20,5%) recibieron quimioterapia de inicio, ya sea como complementaria al tratamiento local, de inducción en los casos en que se utilizó la neoadyuvancia o como tratamiento sistémico en estadios avanzados.
Los planes utilizados fueron los habituales e internacionalmente aceptados para esta enfermedad, según edad, estado menopáusico, tamaño tumoral, balance ganglionar, estado general del paciente, etcétera.
La hormonoterapia como parte del tratamiento inicial del cáncer de mama (adyuvante, neoadyuvante, sistémica o como preventiva en caso de carcinoma in situ) se empleó en 733 pacientes (55,9%) e incluyó en su casi totalidad tamoxifeno; en sólo tres pacientes con alto riesgo tromboembólico se utilizaron de inicio los inhibidores de la aromatasa.
Tampoco haremos mención en este trabajo de los tratamientos recibidos en caso de recaídas ni las complicaciones de los mismos, lo que será motivo de otro análisis.
– Seguimiento
El período de seguimiento de las 1.311 pacientes incluidas en este análisis abarcó 230 meses (19,16 años) con fecha de inicio en enero de 1985 y fecha de corte en marzo de 2004.
Todas las pacientes fueron doblemente chequeadas para corroborar su estado (estatus), tanto por personal del CENDIMA como por el sector de informática de la AEPSM.
Para todas las pacientes se obtuvo el estado (estatus) de viva, fallecida o pérdida de seguimiento y la fecha correspondiente.
Se tomó marzo de 2004 para todas aquellas pacientes chequeadas vivas a dicha fecha, si bien el último control pudo realizarse con anterioridad (este nuevo dato se obtuvo ya que muchas historias habían sido revisadas inicialmente hasta 20 meses previos y pudieron cambiar su estatus a la fecha de corte; no olvidar que el período de reclutamiento de datos comenzó en julio de 2002).
Para las fallecidas se tomó la fecha de fallecimiento que figuraba en la historia del CENDIMA o en la historia central de la institución (AEPSM) siempre y cuando hubiese sido reconfirmado en el último control informático (marzo de 2004) por personal administrativo entrenado en dicha tarea.
Las pacientes dadas de baja de la institución por distintas razones (cambio de institución de asistencia, pase al sistema público, radicación fuera del país, etcétera) fueron tomadas como perdidas vivas, salvo en aquellas que hubieran fallecido sin pertenecer más a la AEPSM, pero cuyo dato fuera obtenido en el último control realizado por personal administrativo del CENDIMA, fuera de la institución; en esta última eventualidad se tomó como fallecida y se documentó la fecha. Para todas las demás pacientes perdidas vivas se tomó como fecha de corte el último control en la institución.
Tomando en cuenta estas consideraciones se analizaron finalmente 1.311 pacientes con una media de seguimiento de 86,53 meses (desvío estándar 58,44), y una mediana de 72,2 meses, es decir que para 50% de las pacientes se obtuvo un seguimiento de al menos 72 meses.
Discusión
En cuanto al análisis descriptivo de los datos queremos destacar algunos hechos.
Está claramente establecido en nuestra población que la mayoría de los tumores de mama (75%) se presentaron por encima de los 50 años, adquiriendo una característica curva de presentación bimodal según se observa en el histograma de edades (figura 2), con un primer pico a los 52 años (coincidiendo con la perimenopausia) y un segundo pico más pronunciado a los 67 años (coincidiendo con la media de edad para las pacientes posmenopáusicas) (tabla 2). Esta peculiar curva bimodal estaría fuertemente relacionada con los efectos hormonales estrogénicos y progestágenos(14).
El resto de las variables ginecoobstétricas está en concordancia con los datos ya conocidos por lo cual no serán analizadas en este trabajo.
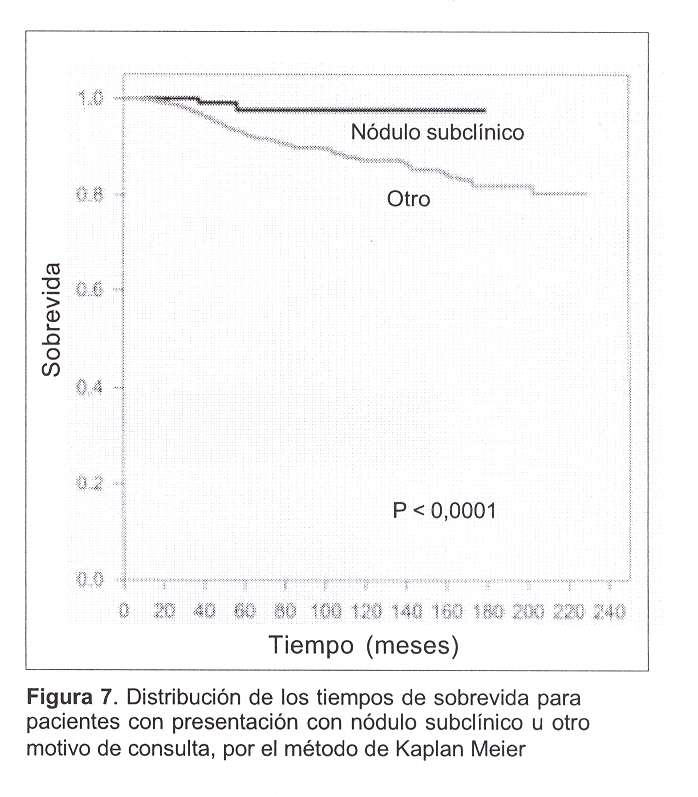
Como era de esperar, la proporción de nódulo subclínico decrece con los estadios; analizando por estadio no se puede ver bien el efecto pues no hay fallos (decesos) en el estadio 0, en los otros no hay diferencias significativas. No obstante, cuando se reúnen los estadios 0, 1 y 2 se notan diferencias significativas (Logrank test p<0,0001) (figura 7).
Esas diferencias desaparecen cuando se efectúa el análisis multivariado (modelo de Cox).
Se han encontrado en este trabajo 57 pacientes con tumores bilaterales de mama, en su mayoría metacrónicos, que dada su peculiariedad no serán motivo de este análisis. La bilateralidad por sí misma no denota un peor pronóstico y evoluciona en función del tumor de mayor agresividad(15).
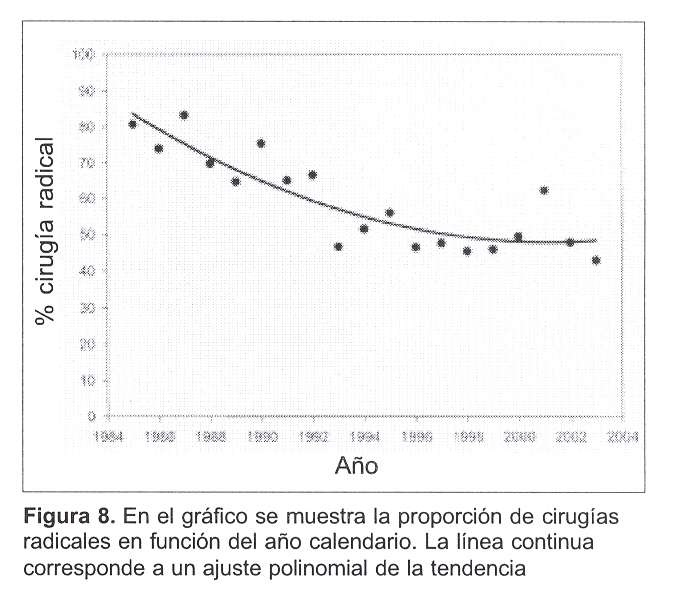
En lo que refiere a la cirugía, los datos obtenidos muestran que si bien las cirugías más radicales comprendieron casi 58% del total de los actos quirúrgicos, en ellas se incluyeron también aquellas pacientes inicialmente sometidas a cirugías conservadoras y que por márgenes muy próximos o comprometidos fueron finalmente reoperadas, totalizando este grupo 105 pacientes (8% del total de las cirugías). Un dato interesante que se desprende de este trabajo es que el porcentaje de cirugías consideradas como radicales disminuyó claramente con el correr de los años, abarcando más de 80% de las cirugías totales realizadas en el año 1985, descendiendo a 48% actual (año 2003), aun incluyendo en las cirugías radicales aquellas realizadas en dos tiempos (conservadora de inicio y radical posterior). La tendencia en los últimos años, según se desprende del trabajo, fue a realizar menos cirugías radicales de inicio (figura 8).
El alto porcentaje de carcinomas in situ encontrados como único componente histológico (6,7%), en su mayoría en los últimos años y muchos de ellos de hallazgo mamográfico (31,58% en pacientes asintomáticas) refuerza el valor de la mamografía como método de screening poblacional (prevención secundaria).
Análisis de sobrevida
De las 1.311 pacientes finalmente incluidas para el análisis de sobrevida, han fallecido 279 (21,3%); 166 pacientes (59,5% de los fallecimientos) murieron por causa oncológica, lo que comprende a 12,67% del total de la muestra.
Un porcentaje muy pequeño de 48 casos (3,7%) fue pérdida de seguimiento incluyéndose para el análisis final como perdidas vivas.
A la fecha de corte del trabajo estaban vivas 1.032 pacientes (78,7%).
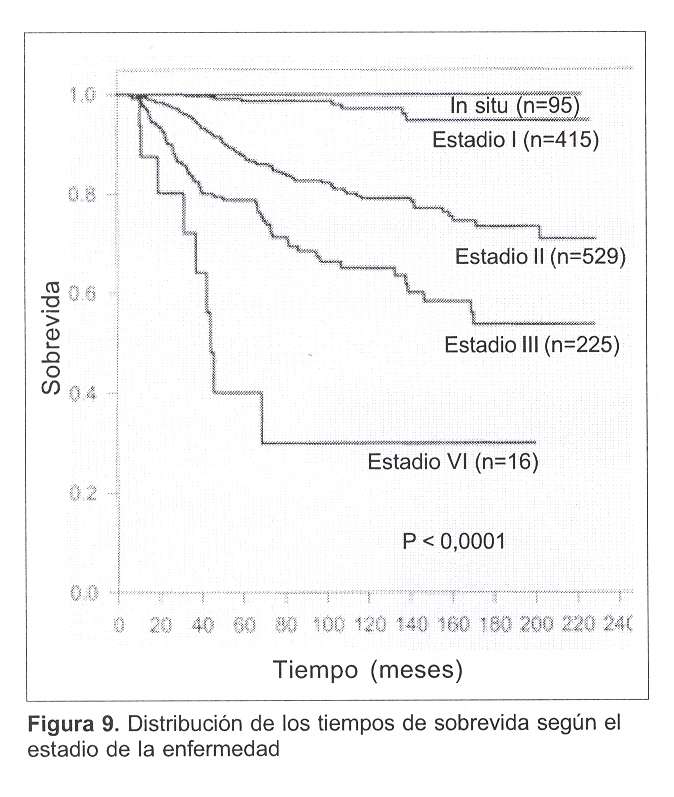
En la figura 9, se muestra la distribución de tiempos de sobrevida en función de los estadios. Puede observarse una nítida diferencia, estadísticamente significativa (p<0,0001), en la distribución de tales curvas. Es interesante que en el caso del estadio 0 (cáncer in situ) no se observaron muertes, en presencia de casi 100 casos con una media de seguimiento de 86 meses.
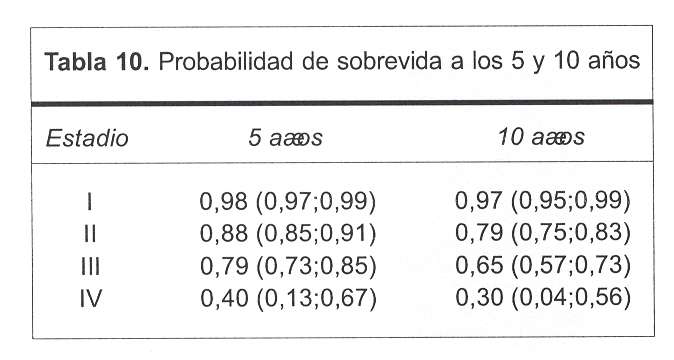
De acuerdo con tales estimaciones en la tabla 10 se muestran las probabilidades de sobrevivir al cabo de cinco y diez años por estadio, exceptuando el cáncer in situ, caso en el cual, como fue referido antes, no se registraron fallos.
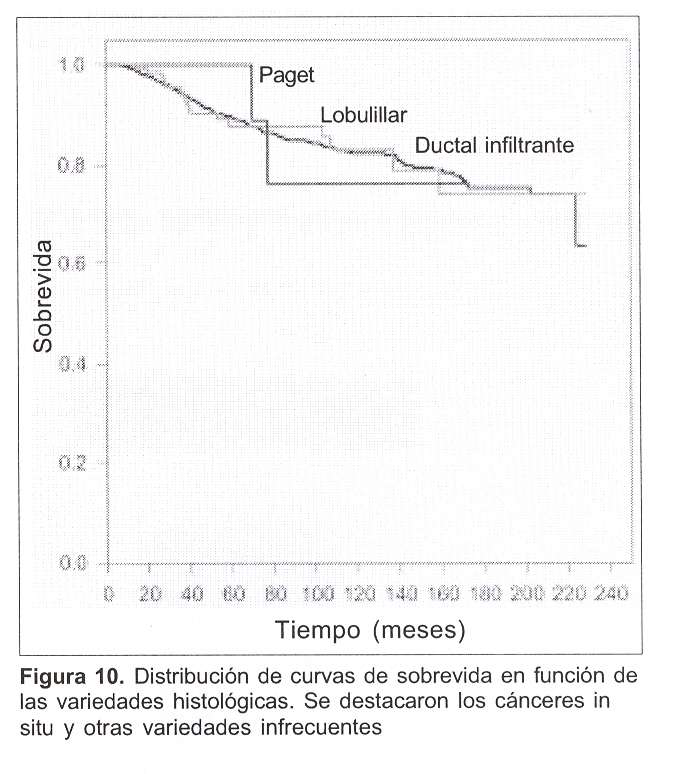
En la figura 10 se muestra la distribución de los tiempos de sobrevida en las distintas variedades histológicas de los tumores; se han omitido del análisis los carcinomas in situ (por no haber presentado fallos) y las variedades histopatológicas infrecuentes (otros: sarcomas, linfomas, etcétera).
A pesar de la enorme desproporción en los números de pacientes involucrados en los distintos tipos histológicos, con más de 80% de carcinomas ductales infiltrantes (tabla 5), puede observarse que no existen diferencias significativas en la distribución de los tiempos de sobrevida.
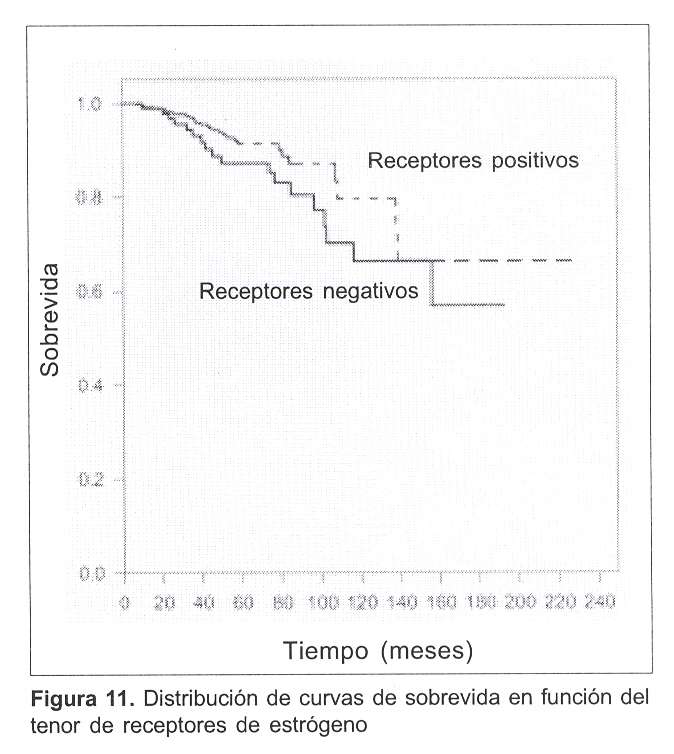
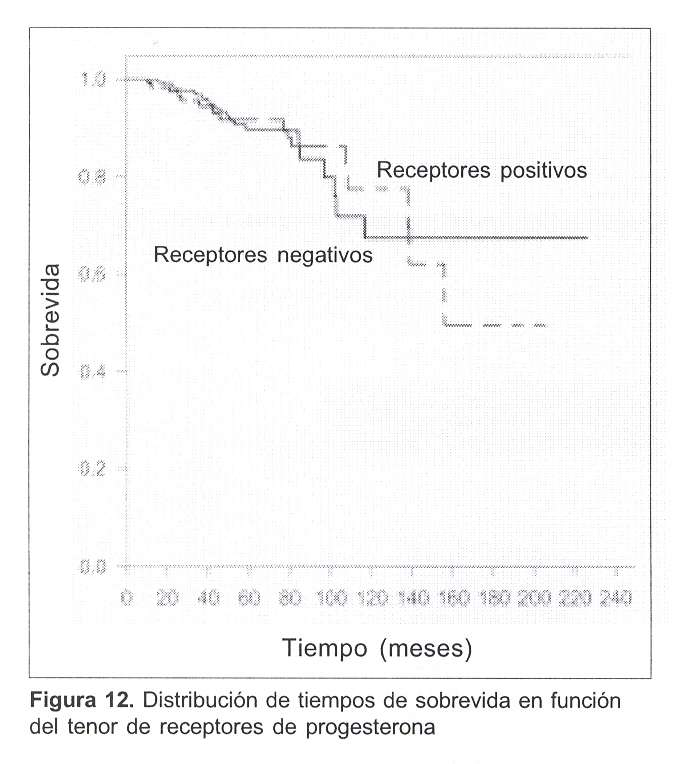
En las figuras 11 y 12 se muestran las distribuciones de sobrevida según la positividad o negatividad de los receptores hormonales.
La figura 11 muestra esa distribución para los receptores de estrógenos y en ella se observa que la sobrevida en función del tiempo es levemente mejor para los pacientes con receptores de estrógeno positivos, al menos entre los 40 y 120 meses (si bien estas diferencias no resultaron estadísticamente significativas).
En el caso de los receptores de progesterona (figura 12), las curvas de sobrevida no mostraron diferencias.
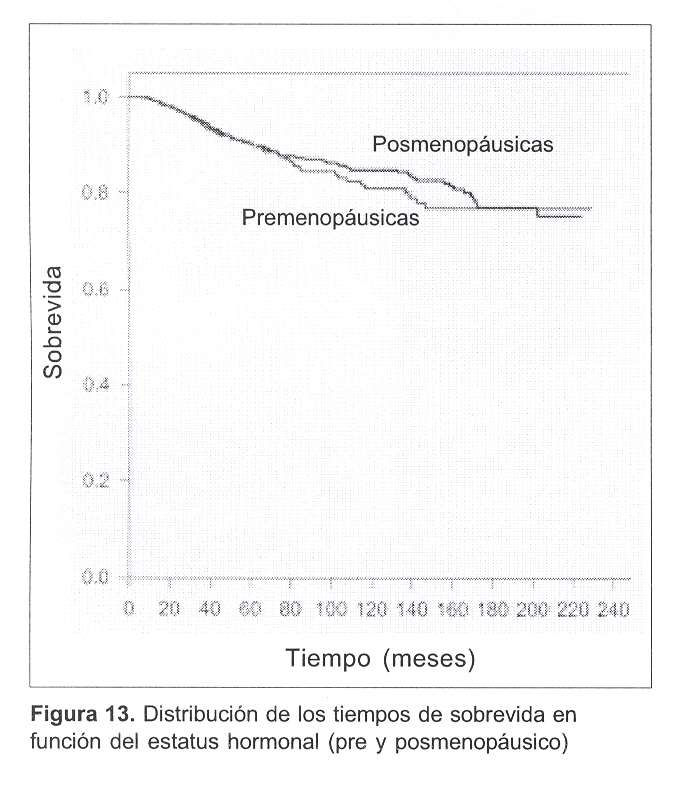
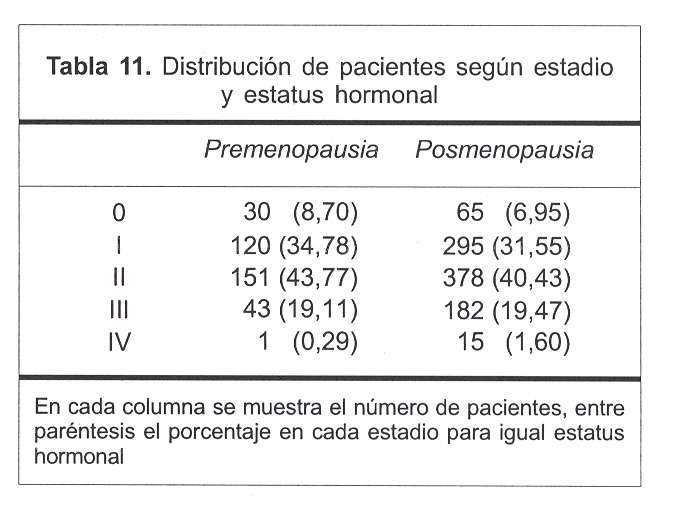
En la figura 13 se ilustra la distribución de los tiempos de sobrevida para las pacientes pre y posmenopáusicas; allí se puede observar que no existen diferencias significativas entre ambos grupos. La presentación por estadio fue correctamente balanceada para cada estadio tanto en las pre como en las posmenopáusicas (las proporciones de pacientes para cada estadio es muy similar (tabla 11).
Aunque se necesitan análisis más detallados del rol pronóstico del tamaño tumoral considerado como variable continua, no resultó significativa en el análisis multivariado.
Diversas variables exploradas resultaron influir significativamente en la distribución de los tiempos de sobrevida.
En el análisis multivariado se exploraron diferentes modelos apelando a distintas combinaciones de las covariables disponibles. Los resultados del mejor modelo obtenido para el caso de los tiempos de sobrevida se muestra en la tabla 12.
Las variables que resultaron finalmente significativas en la determinación de los riesgos de morir (debido al cáncer), esto es, variables pronósticas fueron: el estadio, el número de ganglios determinado por el patólogo, el score histológico final y la edad. Para este análisis el estadio fue considerado en los cinco estadios definidos más arriba, el número de ganglios fue estratificado según las clases establecidas por la clasificación TNM (N0, N1, N2, N3), y el score histológico fue recodificado en tres clases, a saber, un primer nivel incluyendo hasta el score 4, un segundo nivel incluyendo los scores 5, 6 y 7, y un último nivel que incluye los scores iguales o superiores a 8. La edad fue incluida como variable continua en el modelo.
Puede verse que exceptuando la edad, el resto de las variables inciden negativamente en el pronóstico de la sobrevida, exhibiendo distintos rate ratios (RR). Este indicador establece el riesgo de fallo en función del tiempo para la variable en cuestión. El valor más alto de RR que exhibe el modelo corresponde al estatus ganglionar (2,49), seguido por el score histológico (2,40) y el estadio (1,92). Los datos del score histológico final como valor pronóstico independiente que surgen de este análisis fueron recientemente confirmados en la literatura internacional(16).
La edad muestra un coeficiente negativo con un RR muy próximo a 1 (0,98), pero significativo estadísticamente, indicando que si bien el efecto es muy leve, el pronóstico empeora cuanto más joven es el debut de la enfermedad ajustando por las variables anteriormente mencionadas incluidas en el modelo.
Algunas variables cuyos análisis univariados arrojaron resultados significativos (receptores de estrógenos), no resultaron significativas en el modelo multivariado, revelando tal vez información redundante con las variables remanentes.
De estos datos resulta interesante remarcar que si bien el estadio constituye un sólido indicador pronóstico, el estatus ganglionar y el score histológico final también se consolidan como informaciones complementarias de elevado valor pronóstico.
En cuanto a la edad este estudio estaría apoyando la hipótesis sugerida desde hace años de que las mujeres más jóvenes con cáncer de mama tendrían un comportamiento más agresivo que sus pares mayores.
Diversas variables en relación con el tratamiento recibido (cirugía, radioterapia, quimioterapia y hormonoterapia) fueron también exploradas en relación con la distribución de los tiempos de fallo; para ello fueron definidas sendas variables dicotómicas (haber recibido o no el tratamiento). Si bien constituyen una aproximación preliminar y dadas las connotaciones ya señaladas en el análisis descriptivo para estas variables, ninguna de ellas resultó ser de significación en los análisis uni o multivariados.
Esta ausencia de diferencias significativas en la sobrevida en función de los tratamientos recibidos podría estar indicando que el tipo de tratamiento está ligado al estadio de la enfermedad (máxime en el CENDIMA donde los tratamientos son básicamente homogéneos en función de los factores pronósticos ya comentados).
Intervalo libre de enfermedad
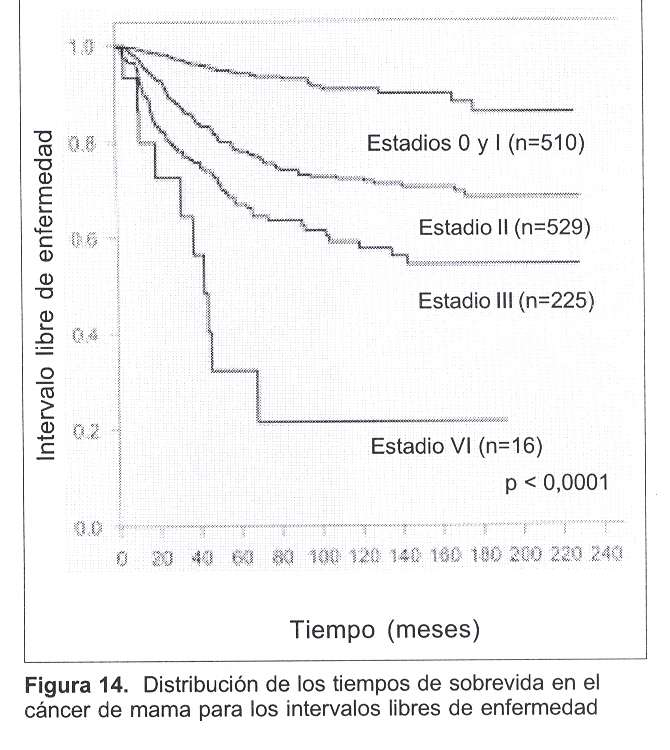
En la figura 14 se muestran las distribuciones de los intervalos libres de enfermedad. Puede verse que existen, al igual que en el caso de los tiempos de sobrevida, diferencias significativas entre las distribuciones de los distintos estadios. No obstante, y a diferencia de los intervalos de sobrevida, en este caso no se verifican diferencias significativas entre los estadios 0 y I. Por esta razón, en la figura se representan estos dos primeros estadios integrando una sola categoría.
Esta ausencia de diferencias en los ILE, para los estadios 0 y I, cuando existe significación estadística en las diferencias verificadas para las sobrevidas, podría estar indicando que la probabilidad de recaer es similar en esos estadios, pero, no obstante, la gravedad de éstas sería cualitativamente menor en tanto su impacto diferencial en las sobrevida; en otras palabras, las recaídas del estadio 0 tienen menor impacto en la sobrevida que las recaídas del estadio I.
En la tabla 13 se muestran los resultados del análisis multivariado (modelo de Cox) para los intervalos libres de enfermedad. Puede verse que el mejor modelo obtenido, no difiere de aquel seleccionado para los tiempos de sobrevida. También puede verse que el impacto pronóstico de las variables seleccionadas es también comparable a juzgar por los valores de los RR.
Si bien se sostiene el estatus ganglionar como la variable de mayor RR (2,22), a diferencia de lo que sucedía para la sobrevida, le sigue en importancia el estadio (1,55); en tercer lugar figura el score histológico cuyo RR es de 1,35.
La edad exhibe valores similares al modelo correspondiente a la sobrevida (RR 0,98).
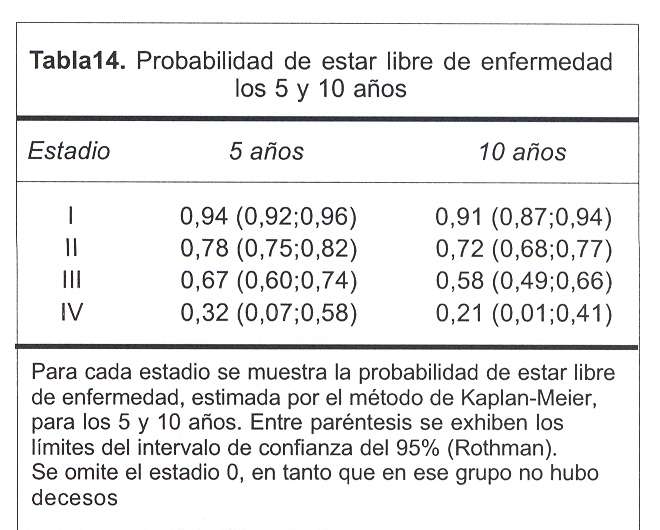
Por último, en la tabla 14 se observa la probabilidad de estar libre de enfermedad a los cinco y diez años, estimada por el método de Kaplan-Meier (junto a sus respectivos intervalos de confianza de 95%), destacando los altos valores para estadios precoces.
Conclusiones
Creemos que esta investigación constituye un importante aporte a la medicina nacional dado que se trata del primer trabajo nacional a gran escala que analiza una población mutual con cáncer de mama con más de 19 años de seguimiento que incluyó a más de 1.300 pacientes analizadas.
Siendo el cáncer de mama la primera causa de muerte por cáncer en la mujer, y con una incidencia en ascenso a nivel mundial, pensamos que los datos extraídos de este análisis puedan servir para tener una primera evaluación del comportamiento de dicha enfermedad en nuestro país.
En Uruguay ocupa el primer lugar en incidencia y mortalidad por cáncer en la mujer con 1.800 nuevos casos (tasa ajustada por edad, TAE 76,11) y 630 muertes al año (TAE 24,72)(2,3).
Estas elevadas cifras obligan a profundizar acciones preventivas y a identificar mujeres de alto riesgo para incluirlas en programas de screening adecuados.
Después de este minucioso análisis destacamos como elementos positivos:
- Trabajo en equipo, pudiendo acceder fácilmente a los distintos especialistas (cirujano, oncólogo médico, oncólogo radioterapeuta, enfermería especializada, radiólogo, citólogo, patólogo, fisiatra, ginecólogo, psicólogo) para compartir opiniones y tomar decisiones en pos del bien del paciente.
– Tener acceso a la tecnología (mamografía, ecografía mamaria, punciones citológicas, arponajes, etcétera) en forma rápida y efectiva, de ser posible en el mismo lugar de trabajo.
– Contar con la rapidez y calidad de obtención de los estudios paraclínicos (radiología, ecografía, tomografía, medicina nuclear, laboratorio de análisis clínicos y laboratorio de anatomía patológica) que permitan una adecuada estadificación del paciente, pudiendo comenzar con los tratamientos en tiempo y forma, confiando plenamente en las técnicas realizadas por profesionales de reconocida trayectoria en nuestro medio.
– El manejo de un archivo propio de historias clínicas de los pacientes en el centro paralelo al de las historias centrales de la institución permite tener mayor independencia, rapidez en la obtención de datos, seguridad de contar con ella en el momento que se requiera sin depender de factores exógenos que pueden retrasar este proceso.
– Poder acceder eficientemente a los tratamientos internacionalmente aceptados para esta enfermedad.
– Contar con una estructura administrativa fija en el centro, tanto en el archivo de historias como en la recepción y en el seguimiento del paciente, que mantenga el flujo de información requerida para asegurar la calidad de las historias clínicas.
– Por último, disponer de una planta física adecuada que permita atender confortablemente al paciente, contando con la infraestructura necesaria para llevar a cabo esta tarea.
Como aporte constructivo (dada la falta de numerosos datos de interés epidemiológico), destacamos la necesidad de mejorar el llenado de las historias clínicas de los pacientes, lo que permitirá no sólo aplicarlo durante la atención de los mismos, sino que facilitará la recolección de datos para aplicar en futuros estudios a fin de conocer otras características de nuestra población.
Un dato adicional de gran importancia en este estudio lo constituye el hecho de que para todos los pacientes incluidos se pudo saber finalmente la causa de muerte (oncológica o no), lo que otorga al mismo mayor potencia y fiabilidad.
Remarcamos nuevamente la importancia de este doble análisis: descriptivo (en relación con variables ginecoobstétricas, anatomopatológicas y terapéuticas) y de sobrevida e intervalo libre de enfermedad.
Los datos finales obtenidos son comparables a los encontrados en la literatura con las peculiaridades que ya mencionamos(16,17).
Los dos parámetros de más peso pronóstico con valor estadístico en esta población para el intervalo libre de enfermedad fueron el estatus ganglionar y el estadio, y para la sobrevida global lo constituyeron el estatus ganglionar y el score histológico final (tablas 12 y 13).
Estos hallazgos junto a los demás parámetros no analizados en este trabajo podrán en un futuro categorizar mejor a nuestra población con cáncer de mama, lo que redundará en beneficio directo para la paciente como así también para las autoridades sanitarias, las que con mayor información sobre el cáncer de mama en Uruguay podrán encarar medidas oportunas para combatir esta enfermedad.
Summary
A descriptive analysis was conducted in the Breast Diagnostic Center (Centro de Diagnóstico Mamaria, CENDIMA, Uruguay) during 230 months when description, survival and disease-free survival were analyzed in 1.311 treated women with breast cancer, in correlation to the prognostic factors for breast cancer.
For this population, ganglia status and stage were the parameters of highest prognostic value in relation to disease-free survival; ganglia status and final histologic score were the main variables considering global survival.
Final data was comparable to international literature.
Résumé
Pour une population de 1.311 femmes avec cancer du sein diagnostiquées, traitées et contrôleés dans le même centre de pathologie du sein, le Centre Diagnostique du Sein (CENDIMA) pendant une période de 230 mois, on fait une analyse descriptive, l’analyse de survie et celle de survie libre de maladie, tout en les mettant en rapport avec des facteurs pronostiques connus pour cette maladie.
Les deux paramètres ayant le plus grand poids pronostique à valeur statistique pour cette population par rapport à l’intervale libre de maladie sont le status ganglionnaire et le stade; le status ganglionnaire et le score histologique final ont été les principales variables en ce qui concerne la survie globale.
Les données finales obtenues sont comparables à celles qu’on trouve dans la littérature internationale.
Bibliografía
1. De-Vita VT, Hellman S, Rosenberg S. Cancer: principles and practice of oncology. 6th ed. Philadelphia: Lippincott, 2001: 3235 p.
2. Vasallo JA, Barrios E. II Atlas de Mortalidad por Cáncer en el Uruguay- Comparación de 2 quinquenios 1989-1993 y 1994-1998. Montevideo: Comisión Honoraria de Lucha contra el Cáncer, 1999.
3. Vasallo JA, Barrios E, De-Stefani E, Ronco A. II Atlas de Incidencia del Cáncer en Uruguay 1996-1997. Montevideo: Comisión Honoraria de Lucha contra el Cáncer, 2001.
4. Sabini G, Delgado L, Suárez L, Musé IM. Cáncer de mama localizado. In: Musé I, Viola A, Sabini G, eds. Aspectos Prácticos de la Clínica Oncológica. Montevideo: Sudamericana, 2004: 235-50.
5. Fisher B, Osborne K, Margolese R, Bloomer W. Neoplasms of the breast. In: Holland J, Frei E, Bast R, Kufe D, Morton D, Weichselbaum R, Cancer Medicine (3rd ed) Philadelphia: Lea & Febiger, 1993: 1706-74.
6. Musé I, Viola-Alles A. Cáncer de Mama. Montevideo: U.R. 2 vol. 1981.
7. Artagaveytia N, Raymondo S, Román E, Delgado L, Alonso I, Alonso O, et al. Receptores hormonales en el CM y su relación con algunos parámetros de la enfermedad. Arch Med Interna (Montevideo) 1997; 20(suppl.): 53.
8. Bonadonna G, Hortobagyi G, Gianni M. Textbook of breast cancer: a clinical guide to therapy. London: Dunitz, 1997.
9. Nabholtz J, Tonkin K, Aapro M, Buzdar A. Breast cancer management: application of evidence to patient care. London: Dunitz, 2000.
10. Kaplan EL, Meier P. Nonparametric estimation from incomplete observations. J Am Stat Assoc 1958; 53: 457-81.
11. Savage IR. Contributions to the theory of rank order statistics - the two sample case. Ann Math Stat 1956 27: 590-615.
12. Cox DR. Regression models and life tables (with discussion). J.R. Stat Soc B 1972; 34: 187-220.
13. Ministerio de Salud Pública. Ordenanza Nº 752; ref: 1439/96. Montevideo: MSP, 1996.
14. Henderson B, Ross R, Bernstein L. Estrogens as a cause of human cancer. The Richard and Hinda Rosenthal Foundation Award Lecture. Cancer Res 1988; 48: 246-53.
15. Krygier G. Tratamiento sistémico del cáncer de mama. In: Vázquez T, Santini A, editores: Los cánceres más frecuentes. Tomo 2. Montevideo: Oficina del Libro AEM, 2000: 103-19.
16. Schneeweiss A, Katretchko J, Sinn H, Unnebrink K, Rudlowski C, Geberth M, et al. Only grading has independent impact on breast cancer survival after adjustment for pathological response to preoperative chemotherapy. Anticancer Drugs 2004:15(2): 127-35.
17. Viola A, Musé I, Vasallo J, Pees G, Pacheco H, Sabini G, et al. Sobrevida del cáncer de mama en poblaciones mutuales y hospitalarias. Cir Urug 1987; 57(1): 1-5.