Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Revista Médica del Uruguay
versión On-line ISSN 1688-0390
Rev. Méd. Urug. vol.18 no.3 Montevideo dic. 2002
Transmisión madre-hijo del VIH según quimioprofilaxis recibida, vía de nacimiento y amamantamiento
Dres. Jorge Quian1, Stella Gutiérrez2, Teresa Picón3, Ana Visconti4,
Alicia González3, Margarita Nin3, Jaqueline Martín3, Ana Galli5, Virginia Galeano6
Resumen
Se estudiaron los binomios madre VIH positiva y sus hijos nacidos entre el 1º de enero de 1995 y el 30 de junio de 2000.
Objetivo: analizar el porcentaje de transmisión materno-infantil del VIH según quimioprofilaxis recibida, vía de nacimiento y amamantamiento.
Material y método: se clasificaron los niños como infectados, serorrevertidos o expuestos.
Se establecieron tres grupos: A) sin quimioprofilaxis, B) zidovudina (AZT) en el embarazo, trabajo de parto o cesárea y recién nacido durante 42 días, C) más de un antirretroviral durante el embarazo y AZT en el parto o cesárea y recién nacido durante 42 días. Se tipificaron como amamantados aquellos que recibieron leche materna durante más de una semana. Se analizó la vía de nacimiento según fuera parto, cesárea de elección o cesárea de urgencia.
Se analizó peso al nacer, edad gestacional, edad materna y número de embarazos.
Resultados: 82 binomios integraron el grupo A con 41 niños infectados (50%). Fueron amamantados 34 (42%). La vía de nacimiento fue vaginal en 58 (70%) y cesárea de elección en siete. El grupo B estuvo integrado por 101 binomios con cinco niños infectados (5%). Dos fueron amamantados. Nacieron por vía vaginal 62 (61%) y por cesárea de elección 29 (29%). El grupo C estuvo integrado por 34 binomios. Los 34 niños fueron serorrevertidos; 33 no fueron amamantados y en uno se desconoce el dato. Nacieron por cesárea de elección 26,5%.
No hubo diferencias en los tres grupos en cuanto peso al nacer, prematurez, edad gestacional, edad materna o número de embarazos.
Conclusiones: la transmisión del VIH madre-hijo disminuye en forma marcada con el uso de antirretrovirales. El aumento de la cesárea programada y la ausencia de amamantamiento se asocian a esta disminución.
Palabras clave:
TRANSMISIÓN VERTICAL DE ENFERMEDAD - prevención y control.
INFECCIONES POR VIH - transmisión.
INFECCIONES POR VIH - quimioterapia.
QUIMIOPREVENCIÓN.
AGENTES ANTI VIH - uso terapéutico.
1. Profesor Agregado de Pediatría.
2. Profesora Adjunta de Pediatría. Profesora Adjunta de Farmacología.
3. Médica Pediatra.
4. Asistente de Clínica Ginecoobstétrica.
5. Residente de Pediatría.
6. Asistente Social.
Centro Hospitalario Pereira Rossell.
Policlínica Obstétrico - Pediátrica de Seguimiento VIH.
Correspondencia: Dr. Jorge Quian.
Verdi 4630, CP 11600. Montevideo-Uruguay.
E-mail: jorgeq@internet.com.uy
Presentado: 18/4/02.
Aceptado: 11/10/02.
Introducción
En 1994 se publicó el trabajo de Connors y colaboradores(1) donde se confirma la reducción del riesgo de transmisión materno-infantil del virus de la inmunodeficiencia humana (VIH) en 66% utilizando zidovudina (AZT) durante el embarazo, el trabajo de parto y en el recién nacido. A partir de esa publicación y de las recomendaciones de los Center of Disease Control (CDC)(2) se ha difundido el uso de esta quimioprofilaxis, y los porcentajes de transmisión han descendido en todos los lugares donde se aplica esta conducta(3-5).
Posteriormente se comienza a discutir la conveniencia de que la mujer embarazada reciba la medicación necesaria a su condición clínica, independientemente de su condición obstétrica, con información adecuada a la gestante de los posibles efectos teratogénicos de los fármacos utilizados(6-8).
Las mujeres embarazadas infectadas con VIH pueden así recibir múltiples esquemas terapéuticos. Pueden recibir un esquema necesario para su condición VIH, que en el momento actual es una triterapia, variable de acuerdo al infectólogo tratante y a la historia previa con antirretrovirales (ARV) que tenga.
Puede recibir monoterapia, en general siguiendo el protocolo PACTG076(1), en cuyo caso el ARV es AZT. Pero hay autores que recomiendan como profilaxis más de un ARV y, por otro lado, un grupo de madres tratadas como quimioprofilaxis (QP) de la transmisión vertical con biterapia(9).
El amamantamiento es responsable de un porcentaje importante de los niños infectados(10). Es aconsejable evitarlo y sustituirlo en lo posible por leches modificadas. Los hijos de madres que no controlan su embarazo y que desconocen su condición de seropositivas, además de no recibir QP, no se benefician tampoco de evitar la lactancia natural.
Por último, se ha insistido en la importancia de la cesárea electiva, antes del inicio del trabajo de parto, como otro mecanismo para evitar la transmisión vertical(11). Para ello es prioritario también el control del embarazo.
En Uruguay, país en vías de desarrollo, se ha intentado difundir el uso de la quimioprofilaxis en la mujer embarazada(12), pero existe una parte de la población de bajos recursos, que no controla su embarazo adecuadamente, y concurre al centro de salud solamente para el nacimiento de su hijo.
En la policlínica de seguimiento obstétrico-pediátrica del Centro Hospitalario Pereira Rossell se controla más de 90% de los hijos de madre VIH positiva de todo el país, que provienen de los diversos estratos sociales. Se reciben niños hijos de madres que controlan bien su embarazo y reciben medicación, junto a los de madres que no lo han hecho, desconociendo su situación serológica para VIH.
El objetivo del presente trabajo fue describir el porcentaje de transmisión vertical de la madre embarazada VIH positiva a su hijo, en la población asistida a partir de 1995, según QP, vía de nacimiento y amamantamiento.
Material y método
Se analizó en forma retrospectiva los binomios madre-hijo con fecha de nacimiento a partir del 1° de enero de 1995 y hasta el 30 de junio de 2000.
Los embarazos gemelares se analizaron como dos o más binomios. Se excluyeron aquellos en los cuales la QP se realizó en forma incompleta (una o dos etapas en vez de tres), o en quienes no hubo datos confiables (niños institucionalizados o adoptados).
Los datos sobre el embarazo y el parto se obtuvieron de la anamnesis y del carné de control del niño, donde consta, entre otros, peso al nacer y edad gestacional.
Se consideró cesárea de elección a la realizada antes de entrar en trabajo de parto.
Se consideró que la madre había recibido ARV (uno o más) durante el embarazo, si la administración fue de un mes o más antes del nacimiento.
Se consideró amamantado a todo niño que lo fue por más de una semana.
Se analizó número de embarazos, edad materna y vía de nacimiento.
Los niños fueron clasificados según los criterios de los CDC(13) en: S o serorrevertidos, cuando tuvieron tres o más PCR negativos, o cuando tuvieron Elisa y Western-Blot negativos y sin clínica sugerente de infección; I o infectados cuando tuvieron dos o más PCR positivos, o cuando con más de 18 meses de edad tenían Elisa y Western-Blot positivos al menos en dos oportunidades, o si tenían clínica sugerente de infección; E o perinatalmente expuestos, cuando no pudo ser definida su condición y sin tener clínica sugerente.
Se establecieron tres grupos de binomios:
Grupo A: aquellos que no recibieron ningún tipo de QP.
Grupo B: aquellos que recibieron AZT durante el embarazo, el trabajo de parto o cesárea a la dosis de 2mg/kg/intravenosa a pasar en una hora y luego 1mg/kg/hora hasta el nacimiento y el recién nacido, 2mg/kg/dosis, cada seis horas durante 42 días.
Grupo C: aquellos en que la madre recibió más de un ARV durante el embarazo, recibió AZT endovenosa durante el trabajo de parto o la cesárea y también recibió AZT el recién nacido, en las mismas dosis del grupo anterior.
Estadística
Se utilizó Epi Info 6.04. Las proporciones se calcularon como porcentajes con sus respectivos intervalos de confianza (IC) de 95%. Para las variables continuas, se compararon los promedios por test de Student. Se determinó si existía o no asociación entre infección y amamantamiento (test de ?2).
Resultados
En el período estudiado se analizaron 308 binomios madre-hijo; se descartaron para el análisis 91 (29%) debido a que no cumplían con los criterios de inclusión (70 QP solo en uno o dos períodos, y 21 por desconocimiento de datos por ser niños institucionalizados, etcétera).
Se obtuvieron los siguientes resultados:
Grupo A, 82 binomios que no recibieron QP. De ellos, 41 niños fueron I (50%) (IC95%: 39%-61%), 37 fueron S (45%) y 4 permanecieron como E (5%).
Fueron amamantados 34 (42%) (IC95%: 31%-53%). De ellos, 24 (70,6%) fueron I y 10 (29,4%) S. (?2 = 9,85, p = 0,002).
El peso promedio al nacer fue de 3.142 gramos (DS ± 503,5) (rango: 2.000 a 4.450 g; 8 pesaron menos de 2.500 g) y su edad gestacional promedio fue de 39 semanas (DS ± 1,0) (rango: 33 a 42; 4 fueron menores de 37 semanas).
La vía de nacimiento fue vaginal en 58 casos (70%). De ellos, 28 niños fueron S (48,3%), 28 fueron I (48,3%) y dos E (3,4%); cesárea coordinada 7 (8%) (IC95%: 4%-17%), de los cuales hubo cinco niños S, uno I y uno E; cesárea de urgencia 8 (10%) y sin datos 9 pacientes.
El número de embarazo promedio fue 3 (rango: 1 a 11).
La edad promedio de la madre fue de 25 años (rango: 16 a 38).
Grupo B, 101 binomios que recibieron QP con AZT en los tres períodos. De ellos, fueron I cinco niños (5%) (IC95%: 2%-12%), 90 fueron S (89%) y 6 permanecieron como E (6%).
Fueron amamantados dos niños (2%) (IC95%: 0,3%-7,7%), ambos S y se desconoce el dato en uno.
El peso promedio al nacer fue de 3.086 gramos (DS ± 508,3) (rango: 1.060 a 4.300 g; 11 pesaron menos de 2.500 g) y su edad gestacional promedio fue de 39 semanas (DS ± 2,0) (rango: 30 a 42; 6 fueron menores de 37 semanas).
La vía de nacimiento fue vaginal en 62 casos (61%), cesárea coordinada 29 (29%) (IC95%: 20%-39%), de los cuales 26 fueron S y tres E; cesárea de urgencia 10 (10%).
El número de embarazo promedio fue 3 (rango: 1 a 9).
La edad promedio de la madre fue de 25 años (rango: 16 a 40).
Grupo C, 34 binomios cuyas madres recibieron dos o más ARV en el embarazo y AZT en el momento del parto y en el período neonatal. Los 34 niños resultaron S. (IC95%: 0%-12,6%).
No fueron amamantados 33 (0%) (IC95%: 0%-13%) y en uno se desconoce el dato.
El peso promedio al nacer fue de 3.156 gramos (DS ± 416,7) (rango: 2.370 a 3.920; dos pesaron menos de 2.500 gramos) y su edad gestacional promedio fue de 39 semanas (DS ± 1,0) (rango: 36 a 41; tres fueron de menos de 37 semanas).
La vía de nacimiento fue vaginal en 16 casos (47%), cesárea coordinada 9 (26,5%) (IC95%: 13,5%-44,6%), cesárea de urgencia 9 (26,5%).
El número de embarazo promedio fue 2 (rango: 1 a 6).
La edad promedio de la madre fue de 26 años (rango: 18 a 41).
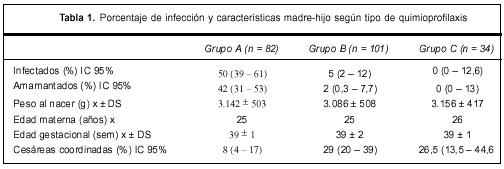
Los resultados de los diferentes grupos se muestran en la tabla 1.
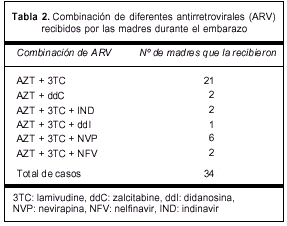
Las diversas combinaciones de ARV que recibieron las madres se muestran en la tabla 2. La biterapia más frecuente fue AZT más lamivudine (3TC) en 21 casos. La triterapia más frecuente fue AZT, 3TC y nevirapina (NVP) en seis casos. Hubo otras combinaciones de bi y triterapia, y en todas estuvo presente AZT.
No existieron diferencias significativas entre edad gestacional y peso de nacimiento entre los tres grupos; sí existieron entre cesárea programada y amamantamiento entre el grupo A por un lado y los grupos B y C, respectivamente.
Discusión
El grupo que no recibió ningún tipo de QP tiene porcentajes de transmisión vertical muy elevados: 50%, y es el que debe recibir atención prioritaria.
A partir de 1995, los autores pudieron demostrar que el número de mujeres embarazadas que recibía QP iba en aumento(12) y que el número de I disminuía. Sin embargo, aún existe un número importante de mujeres que no controla su embarazo y que no se beneficia de la medicación y del conjunto de medidas para disminuir la transmisión vertical(14-16).
En Uruguay, desde 1997, el equipo de salud está obligado por ley a ofrecer el test del VIH a toda mujer que concurra a controlar su embarazo.
La cifra de 50% de niños I es más elevada que las previamente descritas en Uruguay y se compara con las de otros países subdesarrollados(17-19). Seguramente, interviene en este porcentaje la transmisión a través de la leche materna, ya que 42% de los niños de este grupo fue amamantado.
En los 41 niños I, 24 (58,5%) recibieron pecho materno más de una semana y las diferencias entre amamantados y no en este grupo sin QP fueron estadísticamente significativas. Hasta la mitad de las transmisiones verticales se hace a través de la leche materna y desde hace años se aconseja evitar esta práctica(20,21).
No se discuten otros factores maternos que pueden haber influido en la transmisión vertical, como grado de enfermedad, número de linfocitos CD4, carga viral, tiempo de ruptura de membranas, etcétera, porque el trabajo no estaba diseñado en ese sentido. Esto también sucede para los otros grupos.
Esta decisión la toman varios autores al analizar la transmisión vertical del VIH; parece claro, al estado actual de los conocimientos, que recibir ARV durante el embarazo, elegir como vía de nacimiento la cesárea programada y evitar el amamantamiento, son los factores de mayor interés en prevenir la transmisión. La combinación de las dos primeras modalidades es quizá el punto clave en la toma de decisiones.
No hubo con respecto a las madres diferencias significativas en los tres grupos en la edad ni en el número de embarazos; sí las hubo en la medicación recibida y en la vía de nacimiento.
En los recién nacidos, en los tres grupos, no hubo diferencias en el peso ni en la edad gestacional, como ha sucedido en otras series(22,23).
En el grupo A hubo 8% de cesáreas coordinadas, en el grupo B hubo 29% y en el C 26,5%.
Las cesáreas del grupo A, probablemente se debieron a razones obstétricas (datos no investigados).
En los grupos B y C se debieron a la discusión con las mujeres embarazadas de la conveniencia de esta práctica para disminuir la transmisión vertical.
Son numerosas las publicaciones que se refieren a los beneficios de este modo de nacer en relación a la transmisión del VIH(24-28); queda por discernir el beneficio de la cesárea en quienes reciben más de un ARV durante el embarazo(29).
Fueron evidentes las diferencias en cuanto al porcentaje de I entre el primer grupo por un lado y los otros dos. Entre los grupos B y C las diferencias no fueron estadísticamente significativas entre ellos (p > 0,05). El hecho de que no exista ningún infectado en el grupo C es, de todas maneras, estimulante, al igual que lo que ha ocurrido en otras series(8,15), y se debe continuar analizando los datos obtenidos para ver cuáles son los mejores planes a utilizar durante la gestación con una triple finalidad: a) evitar la transmisión del VIH; b) evitar enfermedades por los ARV en el neonato y en el niño; c) evitar el desarrollo de resistencias en el VIH, que perjudiquen posteriormente para su tratamiento a la madre.
Las madres del grupo C recibieron diferentes tipos de ARV; las 34 recibieron AZT y 32 la combinación AZT + 3TC. Esta parece ser hasta el momento la más eficaz y segura, aunque hay publicaciones recientes que pondrían en duda esta afirmación(9).
El presente trabajo no fue diseñado para analizar las enfermedades del recién nacido, lo que será objeto de una revisión posterior.
Por último, el aumento en el porcentaje de las cesáreas de urgencia en el grupo C en comparación con los dos grupos anteriores queda sin explicación. Debiera determinarse si en este grupo que recibía más de un ARV, las complicaciones ginecoobstétricas fueron realmente mayores que en los otros dos grupos.
Conclusión
El tratamiento antirretroviral durante el embarazo es la piedra angular para la casi desaparición del VIH en pediatría.
En esta pequeña muestra, no hubo diferencias significativas en cuanto a edad gestacional y peso de nacimiento entre los tres grupos, ni diferencias en infección por VIH en los dos grupos que recibieron tratamiento. La ausencia de amamantamiento secundaria al diagnóstico materno de esta infección junto al aumento de cesárea programada constatado contribuyen también a disminuir la infección del recién nacido.
Agradecimientos
A Cecilia Murialdo por su paciencia en la transcripción de los manuscritos y en el ordenamiento de los originales.
Summary
HIV positive mothers and their children born between 1st January 1995 and 30th June 2000 were studied.
Objective. To analyze HIV mother-to-child transmission related to prophylactic therapy, delivery mode and breastfeeding.
Methods. Children were categorized as infected, serum-reverted or exposed.
Three groups were established: A) without prophylactic therapy, B) zidovudine (ZDV) during pregnancy, labor or cesarean and newborn of at least 42 days old, C) more than one antiretroviral drug during pregnancy and ZDV in labor or cesarean, and newborn of at least 42 days old.
Infants were considered as breastfed if they had been receiving mother-milk during more than one week. Delivery modes such as labor, elective cesarean or emergency cesarean were analyzed.
Birth weight, gestational age and quantity of pregnancies.
Results. In the group A eighty-two mother-child pairs were enrolled in the study, of which they were 41 infected infants (50%). Breastfed infants accounted for 42% (34 infants). In relation to delivery mode, vaginal was seen in 58 mothers (70%) and elective cesarean for 7. The group B was composed by 101 mother-child pairs with 5 infected infants (5%). Two infants were breastfed. Vaginal delivery was seen in 62 patients (61%) and there were 29 cesarean of choice (29%), and the group C by 34 pairs of whom 34 infants were serum-reverted, 33 were not breastfed, no data in the other case. Elective cesarean accounted for 26,5%.
There were no differences between the three groups on weight, pregnancy age, mother's age or quantity of pregnancies.
Conclusions. HIV mother-to-child transmission frankly decrease with antiretroviral treatment. Increase in elective cesarean and no breastfeeding are associated with this condition.
Résumé
On a étudié le binome mère VIH positive et enfants nés entre le 1er janvier 1995 et le 30 juin 2000.
But: analyser le pourcentage de transmission maternelle enfantine du VIH selon la chimioprophylaxie reçue, la voie de la naissance et l'allaitement.
Matériel et méthode: on a classé les enfants comme infectés, sérorévertis ou exposés. On a établi trois groupes: a) sans chimioprophylaxie, b) zidovudine (AZT) pendant la grossesse, accouchement ou césarienne et nouveau-né pendant 42 jours, c) plus d'un anti-rétroviral durant la grossesse et AZT à l'accouchement ou césarienne et nouveau-né pendant 42 jours. On a typifié comme allaités ceux qui ont reçu du lait maternel pendant plus d'une semaine au moins. On a analysé la voie de naissance soit accouchement, césarienne de choix ou césarienne d'urgence, ainsi que le poids au moment de la naissance, l'âge de gestation,âge maternel et nombre de grossesses.
Résultats: 82 binomes ont fait partie du groupe A avec 41 enfants infectés (50%). 34 ont été allaités (42%). La voie de naissance a été vaginale pour 58 (70%) et 7 césariennes de choix. Le groupe B a été intégré par 101 binomes avec cinq enfants infectés(5%) dont deux ont été allaités. 62 sont nés par voie vaginale(61%) et 29 par césarienne de choix (29%). Le groupe C a été intégré par 34 binomes dont tous ont été sérorévertis; 33 n'ont pas été allaités et on l'ignore pour un enfant. 26,5% sont nés par césarienne de choix.
Il n'y a pas eu de différences parmi les trois groupes en ce qui concerne le poids de naissance,la prématurité,l' âge de gestation, l'âge de la mère ou le nombre de grossesses.
Conclusions: la transmission du VIH mère-fils diminue remarquablement avec l'emploi d'anti-rétroviraux. L'augmentation de la césarienne programmée et l'absence d'allaitement sont associés à cette diminution.
Bibliografía
1. Connor EM, Sperling RS, Gelber R, Kiselev P, Scott G, O'Sullivan MJ, et al. Reduction of maternal-infant transmission of HIV type 1 with Zidovudine treatment. N Engl J Med 1994; 331(18): 1173-80.
2. Center of Disease Control (CDC). Recomendations of the U.S. Public Health Service Task Force on the use of Zidovudine to reduce perinatal transmission of HIV. MMWR (Mob Mortal Wkly Rep) 1994; 43, RR-11, 1-18.
3. Aleixo LF, Goodenow MM, Sleasman JW. Zidovudine administered to women infected with HIV type 1 and to their neonates reduces pediatric infection independent of an effect on levels of maternal virus. J Pediatr 1997; 130(6): 906-14.
4. Mayaux MJ, Dussaix E, Isopet J, Rekacewicz C, Mandelbrot L, Ciraru-Vigneron N, et al. Maternal virus load during pregnancy and mother-to-child transmission of HIV type 1: the French perinatal cohort studies. J Infect Dis 1997;175(1): 172-5.
5. Sperling RS, Shapiro DE, Coombs RW, Todd JA, Herman SA, McSherry GD, et al. Maternal viral load, zidovudine treatment, and risk of transmission of HIV type 1 from mother to infant. Pediatric AIDS Clinical Trial Group Protocol 076 Study Group. N Engl J Med 1996; 335(22): 1621-9.
6. Carpenter CC, Fischl MA, Hammer SM, Hirsch MS, Jacobsen DM, Katzenstein DA, et al. Antiretroviral therapy of HIV infection in 1997. Update recommendations of the International AIDS Society - USA panel. JAMA 1997; 277(24): 1962-9.
7. Center of Disease Control (CDC). Public Health Service Task Force recommendations for the use of antiretroviral drugs in pregnant women infected with HIV-1 for maternal health and for reducing perinatal HIV-1 transmmission in the United States. MMWR (Mob Mortal Wkly Rep) 1998; 47 (RR-2): 1-29.
8. Mc Gowan J, Crane M, Wiznia A, Blum S. Combination antiretroviral therapy in HIV-infected pregnant women. Obstet Gynecol 1999; 94(5 Pt 1): 641-6.
9. Mandelbrot L, Landreau-Mascaró A, Reckacewicz C, Berrebi A, Bénifla J, Burgard M, et al. Lamivudine-zidovudine combination for prevention of maternal-infant transmission of HIV-1. JAMA 2001; 285(16): 2083-93.
10. Nicoll A, Newell ML, Peckham C, Luo C, Savage F. Infant feeding and HIV-1 infection. AIDS 2000; 14(suppl.3): S57-S74.
11. European Collaborative Study. Caesarean section and risk of vertical transmission of HIV 1 infection. Lancet 1994; 343(8911): 1464-67.
12. Quian J, Picón T, Rodríguez I, Gutiérrez S, González A, Nin M, et al. Evaluación de la quimioprofilaxis con zidovudine a la mujer embarazada VIH+ y su hijo. Rev Enf Infec Ped 2000; 13(52): 377-82.
13. Center of Disease Control (CDC). 1994 Revised Classification System for HIV infection in children less than 13 years of age. MMWR 1994; RR- 12, 1-13.
14. Gibb D, Tess B. Interventions to reduce mother-to-child transmission of HIV infection: new developments and current controversies. AIDS 1999; 13(suppl. A): S93- S102.
15. European collaborative study. HIV infected pregnant women and vertical transmission in Europe since 1986. AIDS 2001; 15(6): 761-70.
16. Frenkel LM, Wagner LE 2nd, Demeter LM, Dewhurst S, Coombs R, Murante BL, et al. Effects of zidovudine use during pregnancy on resistance and vertical transmission of HIV Type 1. Clin Infect Dis 1995; 20(5): 1321-6.
17. Quian J, Picón T, Rodríguez I, Gutiérrez S, González A, Nin M, et al. Evaluación de la quimioprofilaxis con zidovudine a la mujer embarazada VIH (+) y su hijo. Arch Pediatr Uruguay 1999; 70(1): 5-10.
18. Ryder RW, Nsa W, Hassig SE, Behets F, Rayfield M, Ekungola B, et al. Perinatal transmission of the HIV type 1 to infants of seropositive women in Zaire. N Eng J Med 1989; 320(25): 1637-42.
19. Adjorlolo-Johnson G, De Cock KM, Ekpini E, Vetter KM, Sibailly T, Brattegaard K, et al. Prospective comparison of mother-to-child transmission of HIV-1 and HIV-2 in Abidjan, Ivory Coast. JAMA 1994; 272(6): 462-73.
20. Ruff A, Halsey N, Coberly J, Boulos R. Breast-feeding and maternal-infant transmission of HIV type 1. J Pediatr 1992; 121(2): 325-9.
21. Quian J, Picón T. VIH-SIDA en pediatría. Arch Pediatr Uruguay 1990; 61: 71-4.
22. Martin R, Boyer P, Hammill H, Peavy H, Platzker A, Settlage R, et al. Incidence of premature birth and neonatal respiratory disease in infants of HIV-positive mothers. The Pediatric Pulmonary and Cardiovascular Complications of Vertically Transmitted HIV Study Group. J Pediatr 1997; 131(6): 851-6.
23. Lambert JS, Watts DH, Mofenson L, Stiehm ER, Harris DR, Bethel J, et al. Risk factors for preterm birth, low birth weight, and intrauterine growth retardation in infants born to HIV-infected pregnant women receiving zidovudine. AIDS 2000:14(10): 1389-99.
24. Blanche S, Rouzioux C, Moscato ML, Veber F, Mayaux MJ, Jacomet C, et al. A prospective study of infants born to women seropositive for HIV type 1. N Engl J Med 1989; 320(5): 1643-8.
25. European Collaborative Study. Risk factors for mother-to-child transmission of HIV 1. Lancet 1992; 339(8800): 1007-12.
26. Duliege AM, Amos CI, Felton S, Biggar RJ, Goedert JJ. The International Registry of HIV-Exposed Twins. Birth order, delivery route, and concordance in the transmission of HIV type 1 from mothers to twins. J Pediatr 1995; 126(4): 625-32.
27. The International Perinatal HIV Group. The mode of delivery and the risk of vertical transmission of HIV type 1. A meta-analysis of 15 prospective cohort studies. N Engl J Med 1999; 340(13): 977-87.
28. The European collaborative study. Maternal viral load and vertical transmission of HIV-1: an important factor but not the only one. AIDS 1999; 13(11): 1377-85.
29. The European mode of delivery collaboration. Elective caesarean-section versus vaginal delivery in prevention of vertical HIV-1 transmission: a randomised clinical trial. Lancet 1999; 353(9158): 1035-9.