Introducción
La prevalencia actual de la Diabetes Mellitus (DM) a nivel mundial es de 10.5%, con una proyección de 643 millones de personas con DM para 2030. 1 En Uruguay en los últimos 20 años, tres encuestas con distintos niveles de representatividad reportan datos. En 2004 un estudio realizado en la 14ª sección censal de Montevideo, sobre un total de 610 personas de entre 20 y 79 años de edad a quienes se les efectuó glucemia en ayunas en plasma venoso, mostró una prevalencia de 6,4% de diabéticos conocidos y 1,6% de diabéticos no conocidos, totalizando una prevalencia real de 8,2%. 2 Dos años más tarde, la encuesta realizada con la metodología STEPS en una muestra de población de 25 a 64 años de todo el país halló que un 5,5% de la población era diabética en tratamiento o presentaba glucemia mayor a 110 mg/dL. 3 Más recientemente, la Segunda Encuesta Nacional de factores de riesgo de enfermedades no transmisibles reportó una prevalencia de DM del 7,6% en población entre 25 y 64 años. 4
La DM se clasifica convencionalmente en 4 subtipos: DM tipo 1 (DM 1), DM tipo 2 (DM 2), diabetes gestacional y otros tipos específicos de diabetes, siendo relevantes para este trabajo los dos primeros.
La DM1 abarca 5-10% de los pacientes con DM. Se caracteriza por una destrucción de la célula beta que conduce a déficit absoluto de insulina e hiperglucemia, siendo en su mayoría inmunomediada (con presencia de anticuerpos anti-islote, anti-glutamato decarboxilasa 65 -GAD 65, anti-insulina, anti-tirosina fosfatasa IA-2 y IA-2ɞ, anti-transportador de Zinc- ZnT8). La edad de presentación habitual es la niñez o juventud, sin embargo, puede ocurrir en cualquier grupo etario. La tendencia a la cetosis está presente y la terapia insulínica es determinante para la supervivencia. 5
La DM2 corresponde al 90-95% de los casos de DM. Asocia deficiencia relativa de insulina, respuesta disminuida a la misma e insulinorresistencia (IR). El descenso de la masa y funcionalidad de la célula beta conduce a hiperglucemia. Se asocia frecuentemente a sobrepeso/obesidad. La enfermedad puede pasar inadvertida por años y su diagnóstico suele ser tardío. La tendencia espontánea a la cetosis es infrecuente. 5
EL término Diabetes Doble (DD), introducido por primera vez en 1991 6, refiere a pacientes con características de DM1 con predisposición genética y fenotípica para DM2 (sobrepeso/obesidad), otros elementos de síndrome metabólico - dislipemia, hipertensión arterial (HTA) - y alto requerimiento insulínico (clásicamente se consideró el requerimiento de insulina > 1 U/kg/día como marcador clínico de IR 7). La IR asociada a DD define un estado proinflamatorio y procoagulante 7,8,9,10 asociado a complicaciones microangiopáticas de la DM 9,10,11, enfermedad cardiovascular (ECV) 12,13 y mayor mortalidad. 14,15
El patrón oro para diagnosticar IR es el clamp euglucémico hiperinsulinémico, técnica de laboratorio de alta complejidad 16, en la cual se infunde en forma intravenosa insulina y glucosa al organismo para mantener un nivel de glucemia estable de 90 mg/dL. A mayor tasa de infusión de glucosa necesaria para mantener la euglicemia, mayor captación de glucosa, mayor sensibilidad insulínica y menor IR (y viceversa). Se han desarrollado distintos índices para cuantificar de forma indirecta la IR; la tasa estimada de captación de glucosa (eGDR estimated Glucose Disposal Rate) es uno de ellos y se considera una herramienta validada útil y de fácil aplicación clínica 17,18. Admite variantes en la forma de cálculo (anexo).
En nuestro medio existe un estudio de prevalencia que evaluó la presencia de IR en DM119.
Con el objetivo general de evaluar la prevalencia de DD en una población con DM1 se diseñó el presente estudio, teniendo como objetivos secundarios: conocer la relación entre DD con la edad, sexo, tiempo de evolución de la DM, dosis diaria total (DDT) de insulina, antecedentes familiares de DM, presencia de HTA y dislipemia, índice albuminuria/creatininuria, presencia de retinopatía diabética (RD), índice de masa corporal (IMC) y control metabólico.
Metodología
b) Población
Criterios de inclusión: pacientes mayores de 15 años, que se asisten en servicios de policlínica especializados (Servicio de Endocrinología y Unidad de Diabetes) del Hospital Pasteur (Montevideo, Uruguay) con diagnóstico de DM1 consignado por el médico tratante en la historia clínica, (considerando aquellos pacientes que requieren múltiples dosis de insulina para sobrevivir, con debut en cetosis o tendencia a la misma) 1 No se cuenta con la determinación de anticuerpos.
Criterios exclusión: otros tipos de DM (DM2, diabetes gestacional y otros tipos de diabetes).
Se destaca que se recabó el consentimiento informado de los participantes o tutores (en caso de menores de 18 años).
c) Procedimiento
En la consulta médica se realizó un cuestionario al paciente. Las variables clínicas: como edad, sexo, tiempo de evolución de la DM, dosis diaria total (DDT) de insulina (incluyendo insulina basa y prandial), antecedentes familiares de DM, presencia de HTA y dislipemia conocidas previamente fueron respondidas por el paciente. Se realizó medida antropométrica de peso y talla en la consulta. Se pesquisó de la historia clínica electrónica del paciente el registro de Fondo de ojo compatible con Retinopatía diabética, la determinación del índice proteinuria/ creatininuria, perfil lipídico y HbA1c en los últimos 6 meses. Se calculó eGDR según fórmula matemática. Con los datos mencionados se completó una planilla prediseñada para el estudio.
d) Definiciones
HTA: cifras de presión arterial > 130/85 mmHg - de acuerdo al Adult Treatment Panel III 20.
Dislipemia: colesterol HDL en sangre < a 40 mg/dL en hombres o < 50 mg/dL en mujeres, o triglicéridos > 150 mg/dL, o el uso de medicación hipolipemiante (estatinas o fibratos) - de acuerdo al Adult Treatment Panel III 20. En cuanto al LDL, se cuantificó sin determinar un valor deseado dado que el mismo depende de la situación clínica del paciente.
Índice albuminuria /creatininuria: se consideró patológico si era > 30 mg/g.
Retinopatía diabética: se evaluó a través del antecedente referido por el paciente y con fondo de ojo compatible.
IMC: se calculó peso/talla2. Se consideró bajo peso IMC < 18.5; normopeso IMC entre 18.5 - 24.9, sobrepeso IMC entre 25 - 29.9 y obesidad IMC ≥ 30 kg/m2.
Control metabólico se evaluó a través de la determinación del porcentaje de hemoglobina glicosilada (HbA1c), determinada con técnica de laboratorio estandarizada, certificada por International Federation of Clinical Chemistry (IFCC) y National Glycohemoglobin Standardization Program (NGSP). Se consideró buen control metabólico si HbA1c ≤ 7%. 5
Dosis de insulina sugestivas de IR cuando la DDT era ≥ 1 U/kg/día. 7
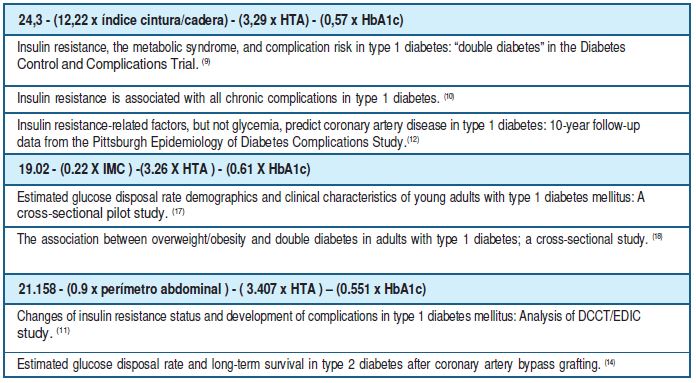
La fórmula utilizada para estimar la tasa de captación de glucosa fue:
eGDR= 19.02- (0.22 x IMC) - (3.26 x HTA) - (0.61 x HbA1c%)
donde la presencia de HTA se codifica 1 y la ausencia 0.
DD: si el eGDR < 8
e) Análisis estadístico
Las variables cualitativas se describieron mediante frecuencias absolutas y porcentajes. Las variables cuantitativas se resumieron mediante media y desvío estándar o mediana e intervalo intercuartílico. La normalidad de las distribuciones se investigó con el test de Shapiro Wilk. La asociación entre variables cualitativas se investigó usando test de chi cuadrado y las variables cuantitativas entre grupos se compararon con el test de Mann Whitney. Se investigó la correlación de variables cuantitativas usando el r de Spearman. Se consideraron significativos valores p < 0.05.
Resultados
Se incluyeron en el estudio 76 pacientes, sus características clínico -paraclínicas se muestran en tabla 1.
Tabla 1: Características antropométricas, clínicas y humorales Abreviaturas- IMC: Índice de masa corporal, HbA1c: hemoglobina glicosilada, eGDR: Tasa estimada de captación de glucosa, DDT: dosis diaria total de insulina, DM: diabetes mellitus
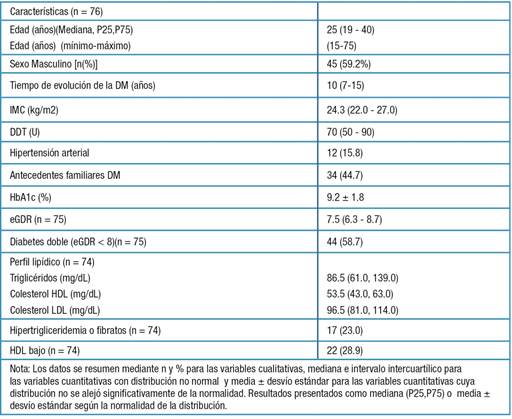
Se registró sobrepeso en 32.9% (25/76 pacientes), obesidad 11.8% (9/76 pacientes) y normopeso 55.3 % (42/76 pacientes).
La HbA1c se obtuvo en 75/76 pacientes; el valor mínimo fue de 5.9% y el máximo de 13.5%. Tenía HbA1c ≤ 7%, el 6.7% de la población.
Se encontró RD en 13/68 pacientes que contaban con fondo de ojo realizado (19.1%).
Se determinó la índice albuminuria/creatininuria en 68/76 pacientes, siendo patológico en 17/68 (25%). De los 64 pacientes que tenían ambos datos completos, 9 asociaban retinopatía y microalbuminuria (14%), en tanto que 46 no tenían ninguna de las dos (71 %).
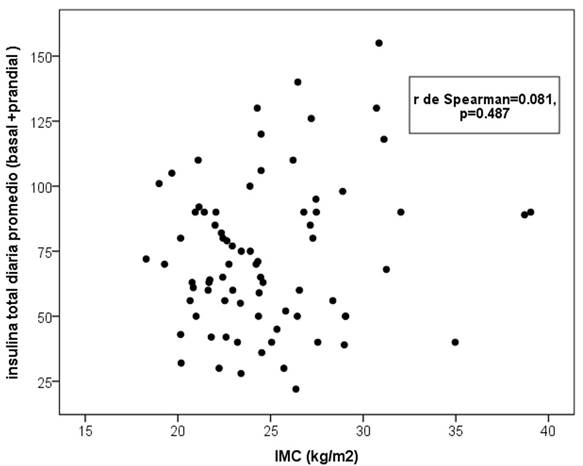
No se encontró correlación lineal entre la DDT y el IMC (p = 0.487). Gráfico 1
Según el valor del eGDR, 58.7% de los pacientes (44/75) se clasificarían como portadores de DD.
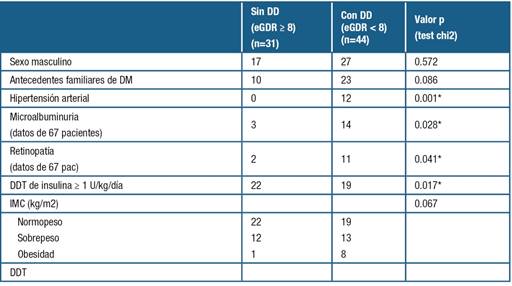
Estos tenían edad significativamente más elevada y presentaban frecuencia significativamente mayor de RD y microalbuminuria (valor p = 0.028 y 0.041 respectivamente).
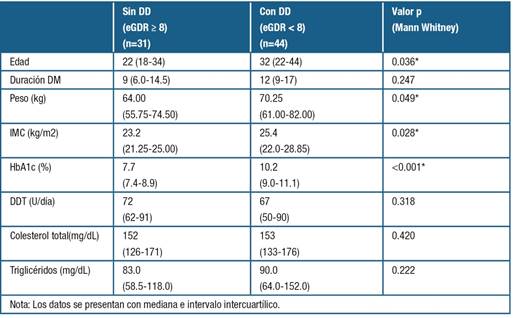
En las Tablas 2 y 3 se resume una comparación entre individuos con y sin DD.
Las variables HTA, HbA1c e IMC presentaron diferencias significativas en los dos grupos como era de esperar de acuerdo al modelo utilizado.
La mediana de DDT de insulina no registró diferencia significativa entre los dos grupos (p = 0.318)
La proporción de pacientes que reciben dosis ≥ 1 U/kg/día es mayor entre los pacientes sin DD vs los DD (71% vs 43%).
Tabla 2: Características de los pacientes con y sin diabetes doble (variables categóricas) Abreviaturas - DD: diabetes doble, DM: diabetes mellitus, IMC: Índice de masa corporal, eGDR: Tasa estimada de captación de glucosa, DDT: dosis diaria total de insulina.
Discusión
Se describe aquí una cohorte uruguaya de 76 pacientes con DM1, con predomino del sexo masculino, con una mediana de tiempo de evolución de la DM de 10 años y alto porcentaje de pacientes con antecedentes familiares de DM (44.7%).
Se han realizado estudios similares en el Reino Unido, incluyendo 107 y 175 pacientes con DM1 17,18 con los que es posible comparar nuestros resultados.
El control glucémico en esta cohorte fue deficiente, con bajo porcentaje (6,7%) de pacientes en objetivo meta de HbA1c (< 7%); sin embargo, debe tenerse en cuenta que este valor es relativo, y debe ajustarse según las comorbilidades y repercusiones presentes en cada individuo. La HbA1c promedio fue 9.2%, valor superior al de las cohortes similares (Cantley et al 8.6%, Nishtala et al 8.9%) 17,18 y aún al promedio de 8.1% observado en 17.050 pacientes suecos con DM1 estudiados por Nystrom et al 14. En esto podrían influir aspectos socioculturales y económicos de la población estudiada.
Se destaca un alto porcentaje de pacientes con sobrepeso/obesidad (44.7%), dato intermedio entre los de las cohortes con las que comparamos (Cantley et al 53.3 %, Nishtala et al 41,1%). 17,18
La prevalencia de HTA fue de 15.8 %, algo menor que en el estudio de Cantley et al (19%) y similar al estudio de Nishtala et al que reporta 13.9 % de HTA sistólica. (17,18
En cuanto a las repercusiones microangiopáticas estudiadas, se encontró una frecuencia de retinopatía diabética del 19%, algo superior a la reportada por Nishtala et al (15%). En el estudio de Nystrom et al, la prevalencia de RD fue mucho mayor, esto podría explicarse por estar dicha cohorte integrada por personas más añosas y con un tiempo mayor de evolución de la DM1. La microalbuminuria se presentó en el 25% de los pacientes, valor superior al de Cantley et al (16%) y aún al de la cohorte de Nystrom et al, en la que los pacientes con albuminuria (micro o macro) alcanzan el 22% de la cohorte. 14,17,18
En esta cohorte se encontró una prevalencia de DD del 58%, similar al estudio realizado en Reino Unido por Cantley et al y algo superior al valor obtenido por Nishtala et al, quien utilizó otra versión del proxy de RI que incluye perímetro de cintura en lugar de IMC. La mediana de eGDR en nuestro estudio fue de 7.5, similar al estudio de Cantley et al y la media 7.4, menor a la obtenida por Nishtala et al utilizando la fórmula con el perímetro de cintura. 14,18
Al igual que en los dos estudios mencionados, los pacientes con DD eran más añosos y tenían más repercusiones microangiopáticas; en cuanto al tiempo de evolución de la DM, aunque la diferencia no fue significativa, los pacientes con DD presentaron mayor tiempo de evolución de la misma. No se encontró asociación entre sexo y DD. No se encontraron diferencias significativas en la proporción de pacientes que presentaban antecedente familiar de DM ni el perfil lipídico, mientras que Cantley et al, encontraron diferencias significativas en triglicéridos y HDL. Nishtala et al, usando tres categorías definidas por terciles encontró diferencias entre el grupo de menor eGDR y los otros dos en los valores de triglicéridos y colesterol total. 14,18
En comparación con el estudio de Cantley et al, la mediana de DDT en esta cohorte es significativamente mayor (70U vs 43U). Si bien la mitad de los pacientes presenta DDT de insulina ≥1 U/kg/día, esta variable no mostró asociación con DD, incluso reflejó una asociación inversa, la cual podría explicarse por una subvaloración de las dosis de insulina rápida utilizada por parte del paciente.
A diferencia del trabajo de Cantley et al 18, no se registró asociación entre DDT de insulina e IMC. Planteamos que existe una subvaloración de dosis de insulina mencionada anteriormente.
Entre las limitaciones de este estudio está el tamaño pequeño de la muestra y su procedencia de un único centro de atención médica. Las mediciones antropométricas fueron realizadas por distintos miembros del equipo y están sujetas a la variabilidad interobservador. El diagnóstico de DM1 no se confirmó con determinación de anticuerpos. Por otra parte, la utilización de modelos debe hacerse siempre con precaución. En este caso, se utilizó el modelo que incorpora el IMC en vez de la razón cintura/cadera que formaba parte del modelo. Si bien cualquiera de éstos son formas de evaluar la adiposidad, recientemente se ha difundido que la relación cintura-cadera es una mejor forma para estimar la misma y puede ser un indicador más preciso del riesgo de mortalidad por todas las causas. 21 Otro hecho que es discutible y puede ser revisado a futuro, es el punto de corte para el diagnóstico de DD (eGDR < 8).
Conclusiones
Se evaluó una cohorte uruguaya con alta prevalencia de DD, en población joven, con control glucémico fuera del objetivo y presencia de repercusiones microangiopáticas.
Es fundamental identificar a esta población, dado que por su mayor morbimortalidad requiere tomar conductas más agresivas en el control de los factores de riesgo cardiovascular así como intervenciones para mejorar el control glucémico, incluyendo educación, planes nutricionales y ejercicio individualizados, y eventualmente el uso de fármacos con efecto sobre el descenso de peso y protección cardio-renal, sobre los cuales contamos con claras recomendaciones para DM2 , siendo necesarios estudios en DM1.












 Curriculum ScienTI
Curriculum ScienTI