Introducción
La viruela símica (mpox por sus siglas en inglés) es una infección viral zoonótica causada por un virus de ADN de doble cadena que pertenece a la familia Poxviridae, subfamilia Chordopoxvirinae y género Orthopoxvirus1 que produce una erupción similar a la de viruela 2. Mpox se detectó por primera vez en África en 1970 3, fue considerada endémica en varios países africanos, incluidos Benin, Camerún, República Centroafricana, la República Democrática del Congo, Gabón, Ghana (identificado únicamente en animales), Costa de Marfil, Liberia, Nigeria, Sierra Leona y Sudán del Sur 4.
En mayo de 2022 varios países donde mpox no es endémica notificaron casos, incluyendo algunos países de Las Américas. El 23 de julio de 2022, el Director General de la Organización Mundial de la Salud (OMS) declaró el brote de mpox como una emergencia de salud pública 5. Aunque posteriormente dejó de ser una alarma epidemiológica, recientemente, en 2024 fue declarada nuevamente como una emergencia. Hasta el 5 de marzo de 2024 se reportaron 94,274 casos confirmados de mpox a nivel global, de los cuales 32,125 casos y 58 muertes asociadas fueron reportados en Estados Unidos; en Guatemala se reportaron 405 casos y una muerte 6.
Se ha descrito entre 20 al 50% la coexistencia de mpox con otras entidades, principalmente con infecciones de transmisión sexual (ITS). El 60% a 100% de casos se han reportado entre hombres que tienen sexo con hombres (HSH) y personas que viven con virus de inmunodeficiencia humana (VIH) 7. En la serie de casos evaluada por Romo y cols., 31.5% de los casos de mpox tuvo alguna ITS diagnosticada durante la evaluación, con Neisseria gonorrhoeae en 21%, Chlamydia trachomatis con 11.2%, herpes simple 7% y Treponema pallidum con 3.7% 8.
En julio del 2022 fue reportado el primer caso de mpox en Guatemala, tratándose de un hombre que acudió voluntariamente a la Unidad de Atención Integral del VIH e Infecciones Crónicas “Dr. Carlos Rodolfo Mejía Villatoro” del Hospital Roosevelt para una evaluación por presentar lesiones en piel. El diagnóstico fue confirmado por el Laboratorio Nacional de Salud (LNS) de Guatemala; a partir de ese momento dio inicio la evaluación de casos y referencia de muestras sospechosas de mpox desde la Unidad al LNS para la confirmación; eventualmente la prueba molecular para detección de mpox fue implementada en la Unidad.
Todos los estudios complementarios en casos con sospecha de mpox fueron realizados en la Unidad, incluyendo pruebas para detección de VIH e ITS; así como tamizaje para virus de hepatitis B y virus de hepatitis C en caso de positividad de VIH. El objetivo del presente estudio es determinar positividad de infecciones de transmisión sexual en pacientes con sospecha de mpox atendidos en la Unidad de Atención Integral del VIH e Infecciones Crónicas “Dr. Carlos Rodolfo Mejía Villatoro” del Hospital Roosevelt, así como conocer el seguimiento de las mismas.
Metodología
a) Población
Se realizó un estudio descriptivo, longitudinal, retrospectivo. La población fue conformada por un total de 78 registros de adultos con sospecha de mpox atendidos en la Unidad de Atención Integral del VIH e Infecciones Crónicas “Dr. Carlos Rodolfo Mejía Villatoro” del Hospital Roosevelt, durante el período de julio del 2022 a marzo del 2023, de quienes se registró el seguimiento durante los siguientes 18 meses en caso de presentar alguna ITS. El diseño de muestreo fue no probabilístico de casos consecutivos.
b) Definiciones y métodos diagnósticos
Definición de caso de mpox
Prueba molecular para detección de mpox
Para la detección de mpox se utilizaron las pruebas moleculares LightMix Modular Orthopox/Monkeypox y U-Card Dx™ Monkeypox Virus Test, según disponibilidad, las cuales fueron procesadas en las en las plataformas automatizadas Cobas® 4800.
Diagnóstico de Virus Inmunodeficiencia Humana (VIH)
Se reportaron como positivos para VIH los casos reactivos para Determine™ HIV-1/2 y Anaquick® HIV 1/2 Ac, empleando el criterio diagnóstico basado en dos pruebas rápidas, indicado en la Guía de uso de los Antirretrovirales en personas con VIH y su aplicación profiláctica, del Ministerio de Salud Pública y Asistencia Social 9.
Recuento de linfocitos T CD4+
El recuento de linfocitos T CD4+ se realizó en el equipo BD FACSVia™ Flow Cytometry System, basado en la fluorescencia emitida teniendo en cuenta el tamaño y granularidad celular.
Determinación de carga viral de VIH
La medición de la carga viral del VIH se realizó con la técnica de reacción en cadena de la polimerasa (PCR) en tiempo real, en las plataformas automatizadas Cobas® 4800 y GeneXpert® Infinity, según disponibilidad de recursos.
Diagnóstico y monitoreo de sífilis
Para la detección de sífilis se utilizó la prueba no treponémica Reagina Plasmática Rápida (RPR), la cual fue titulada en caso de reactividad, y confirmada con la prueba treponémica Treponema Pallidum Haemagglutination (TPHA). Se registró como positivo los casos de RPR y TPHA positivos, independientemente del título de la primera prueba. El seguimiento se realizó únicamente con RPR.
Detección de Chlamydia trachomatis y Neisseria gonorrhoeae
C. trachomatis (CT) y/o N. gonorrhoeae (NG) fueron detectados con la prueba Xpert® CT/NG, en el Sistema GeneXpert® Infinity.
Detección de ITS
Se utilizó el panel NamuPlex™ STD12 Real-time PCR Kit para la detección molecular de agentes etiológicos de ITS.
Todos los resultados de las pruebas realizadas fueron registrados en el sistema de información 4DLab versión 3.11.0.280.
c) Procedimiento
La base de datos fue generada en una hoja electrónica de Excel Office 2019. La información fue tabulada en el orden preestablecido de los campos. Las variables demográficas sexo, edad y la variable de riesgo orientación sexual, fueron transcritas desde la base de datos “Sospecha de Mpox” del área de Consejería; los resultados de la prueba de mpox, así como de VIH, ITS, hepatitis B, hepatitis C, recuento de linfocitos T CD4+ y carga viral de VIH, fueron transcritos desde el sistema de información 4DLab versión 3.11.0.280.
d) Análisis de datos
Se utilizó el software estadístico Jamovi versión 2.3.28, de distribución libre. La descripción de las características demográficas se presenta a través de frecuencias y porcentajes. Las variables cuantitativas se muestran en rangos. La positividad de las ITS se calculó utilizando un intervalo de confianza del 95%.
f) Consideraciones éticas
El protocolo de investigación fue sometido a revisión de las autoridades de la Unidad de Atención Integral del VIH e Infecciones Crónicas “Dr. Carlos Rodolfo Mejía Villatoro” del Hospital Roosevelt, el Departamento de Medicina Interna y del Departamento de Docencia e Investigación del mismo hospital. Aprobación registrada en acta No. 753, punto 3ero., de fecha 25 de junio de 2024.
Resultados
Se analizó un total de 78 casos con sospecha de mpox. El 52.9% de los pacientes se encontraba en el rango de edad de 20-29 (36/78), con una media de 25 años. Todos los casos fueron sexo masculino, el 76.9% (60/78) indicó orientación HSH, 16.7% (13/78) bisexual y 6.4% (5/78) heterosexual. Tabla 1.
Tabla 1: Coinfección mpox / VIH. Abreviatura: mpox -viruela símica, VIH - virus inmunodeficiencia humana, f - frecuencia absoluta
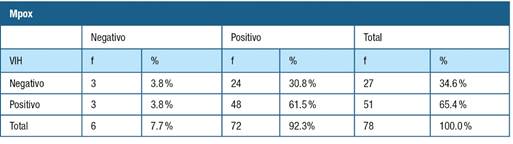
El 92.3% (IC 95% 95.0% - 100%) de los casos sospechosos para mpox fue positivo. La positividad para el Virus de Inmunodeficiencia Humana (VIH) fue de 65.4% (IC 95% 93.0% - 100%), de los cuales el 56.4% (44/78) tenía diagnóstico previo de VIH y el 9.0% (7/78) fue de reciente diagnóstico. Todos los casos ya conocidos por VIH se encontraban en terapia antirretroviral (TAR). Hubo 61.5% (48/78) de coinfección de VIH y mpox.
El 33.3% (2/6) de los pacientes a quienes se les detectó VIH al momento de la consulta por sospecha de mpox y el 7.31% (3/41) de los pacientes con diagnóstico previo de VIH tuvo recuento de linfocitos T CD4+ menor a 200 cél/µL, respectivamente; mientras el 51.2% (21/41) de los pacientes con diagnóstico previo de VIH tenía un recuento > 500 cél/µL. Todos los pacientes de reciente diagnóstico de VIH fueron positivos también para mpox. Tabla 2.
El 40.0% (2/5) de los pacientes de reciente diagnóstico y el 8.1% (3/37) de los pacientes en seguimiento de VIH tuvo una carga viral en el rango 50,001-100,000 cp/mL, respectivamente; en tanto que el 78.4% (29/37) de los pacientes en seguimiento de VIH tenía carga viral indetectable. Un paciente de reciente diagnóstico presentó una carga viral >100.000 cp/mL. Únicamente 4 pacientes VIH positivo conocidos fueron negativos para mpox, con carga viral indetectable y recuentos de linfocitos T CD4+ mayor a 500 cél/µL.
De los 78 pacientes incluidos en el análisis, el 33.3% (IC 95% 23.1% - 44.9%) presentó al menos una ITS. Se encontró 26.9% de coinfección de mpox con alguna ITS, se tuvo el mismo porcentaje para la coinfección de VIH e ITS. Figura 1.
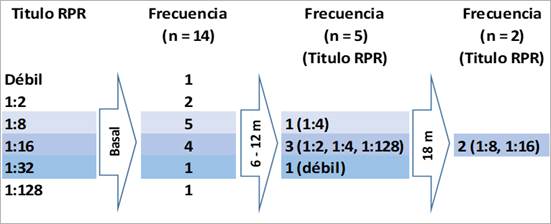
La positividad para sífilis fue de 17.9% (IC 95% 10.2% - 28.3%). El 15.4% presentó coinfección sífilis / mpox. De los pacientes detectados con sífilis, el 64.3% (9/14) fue identificado con coinfección VIH / mpox; únicamente dos pacientes tenían diagnóstico previo de sífilis. El 14.3% (2/14) fue negativo para mpox, con titulos de reagina plasmática rápida (RPR) en 1:8 y 1:128, respectivamente, el primero conocido por VIH y el segundo con diagnóstico reciente debido a la consulta por sospecha de mpox; ninguno asistió a la consulta de seguimiento por sífilis. Hubo 21.4% (3/14) de pacientes positivos para mpox y negativos para VIH, con titulos de RPR débil, 1:2 y 1:8, respectivamente, ninguno de ellos acudió a la cita de seguimiento para síflis.
El 35.7% (5/14) de los pacientes detectados con sífilis se presentó para su seguimiento entre los 6 y 12 meses siguientes y de ellos el 40.0% (2/5) acudió a su segumiento de 18 meses. De los 4 pacientes que durante la primera consulta tuvieron título inicial de RPR 1:16, 3 se presentaron al seguimiento de 6 - 12 meses, uno de ellos aumentó los títulos a 1:128 pero no se presentó al seguimiento de 18 meses; en los otros 2 pacientes, durante la primera consulta de seguimiento se observó una disminución de 8 y 4 veces en los títulos de RPR y en la segunda consulta se documentó un aumento de los mismos, en ambos pacientes, no mayor al titulo inicial.
Se identificó la presencia de C. trachomatis y/o N. gonorrhoeae en el 15.4% (IC 95% 8.2% - 25.3%) de los 78 pacientes analizados. La positividad de C. trachomatis fue de 10.3% (IC 95% 4.5% - 19.2%) y de 9.0% (IC 95% 3.7% - 17.6%) para N. gonorrhoeae. En pacientes confirmados para mpox, la positividad fue de 10.3% (7/68) para cada microorganismo. Figura 2.
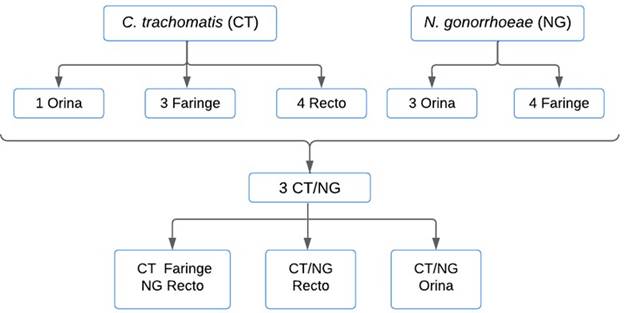
Figura 2: Seguimiento de infección de C. trachomatis y N. gonorrhoeae (n = 12) Abreviatura: CT-C.trachomatis, NG-N.gonorrhoeae. Fuente: Elaboración propia
De los pacientes en quienes se identificó C. trachomatis y/o N. gonorrhoeae, el 75% (9/12) presentó coinfección VIH / mpox; el 8.3% (1/12) fue negativo para mpox y positivo para VIH, identificando C. trachomatis en recto, y del 16.7% (2/12) de los pacientes detectados con mpox pero negativos para VIH, uno tuvo presencia de N. gonorrhoeae en orina y en otro se detectaron ambos microorganismos en recto.
Adicionalmente, se realizó a todos los pacientes el panel para detección de ITS, en el que se detectó Mycoplama hominis en 9.0% (IC 95% 3.7% - 17.6%), Ureaplasma urealyticum 9.0% (IC 95% 3.7% - 17.6%), Candida albicans 7.7% (IC 95% 2.9% - 16.0%), Mycoplasma genitalium 5.1% (IC 95% 1.4% - 12.6), herpes simple 2 en 5.1% (IC 95% 1.4% - 12.6) y 1.3% (IC 95% 0.0% - 6.9%) de herpes simple 1. Todos los casos fueron positivos para mpox y eran conocidos por ser portadores de VIH.
Se realizaron pruebas para detección del virus de hepatitis B (VHB) y virus de hepatitis C (VHC) como parte del tamizaje a todo paciente VIH positivo. La positividad para VHB fue de 2.6% (IC 95% 0.3% - 9.0%) y para el VHC fue de 5.1% (IC 95% 1.4% - 12.6%). Sobre el VHB, los dos pacientes tenian coinfección VIH/VHB conocida, recibían TDF (Tenofovir disoproxil fumarato) como parte del esquema de terapia antirretroviral (TAR) y refirieron ser HSH. Ambos tenían problemas de adherencia al TAR. Uno fue positivo para mpox. Para el momento del presente análisis, ambos estaban en abandono de TAR. Figura 3.
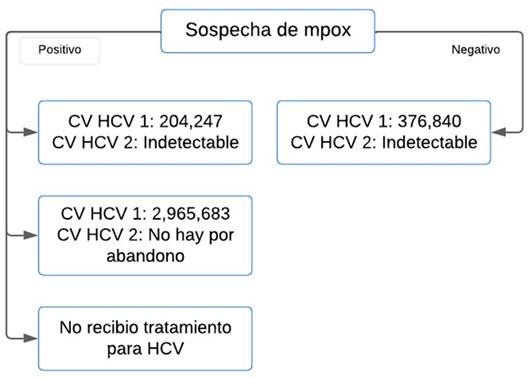
Figura 3: Seguimiento de infección el virus de hepatitis C Abreviatura: mpox-viruela símica, CV- carga viral, HCV- virus de hepatitis C. Fuente: Elaboración
Los cuatro pacientes detectados con el VHC durante la consulta por sospecha de mpox eran conocidos por VIH, dos indicaron ser HSH y dos bisexuales; a tres se les detectó mpox. Un paciente era tratado en otra Unidad de Atención del VIH, por lo que se le realizó la detección de mpox y se refirió nuevamente a su Unidad para el seguimiento del VHC. Se brindó tratamiento con Sofosbuvir/Velpatasvir a tres pacientes, dos de ellos con coinfección VIH / mpox y uno negativo para mpox.
Discusión
El brote de mpox ocurrido durante los años 2022 y 2023 fue motivo de preocupación en salud pública en Guatemala al igual que en otros países, a la vez que evidenció el riesgo de contagio de ITS, principalmente en los grupos de HSH y personas viviendo con VIH.
Un estudio de 528 casos de cuatro regiones de la OMS (Europa, América, Pacífico Occidental y Mediterráneo oriental) y 16 países, reportó la edad entre 18 a 68 años con una mediana de 38 años 10. Otros estudios reportaron casos en adultos con mayor edad 11,12,13 en comparación con lo identificado en este estudio, en que 52.9% de los casos tenían entre 20 y 29 años, con una mediana de 25 años. Esta diferencia podría deberse a las pirámides de población y la distribución por edades. El grupo de edad más afectado fue el sexualmente activo, principalmente el grupo HSH.
Todos los casos incluidos en este estudio fueron de sexo masculino, el 76.9% indicó orientación HSH y el 16.7% bisexual. Los resultados son similares a estudios conducidos en el Reino Unido y Australia 12,14. La conducta sexual entre HSH es un factor de riesgo, incluidos encuentros con parejas desconocidas, parejas múltiples o relaciones sexuales sin protección 13).
Según el informe de la Organización Panamericana de la Salud (OPS) sobre la Situación de Respuesta al Brote de mpox en varios países de la Región de las Américas, hasta marzo de 2023 fueron confirmados 58,578 casos en 31 países y territorios, y 76 muertes 15. Los seis países de América Latina con mayor número de casos hasta diciembre de 2023 fueron Brasil, Colombia, México, Perú, Chile y Argentina 16. En el presente análisis el 92.3% de los casos sospechosos para mpox tuvo diagnóstico confirmado.
Todos los casos de mpox sospechosos y confirmados de este análisis, fueron sometidos a pruebas de detección de VIH, otras ITS, así como hepatitis B y C, como parte de los protocolos de abordaje de mpox. La revisión sistemática realizada por Sharif y cols. 7 documentó una prevalencia del 30% - 50% de VIH antes del mpox en los casos notificados, y el VIH fue identificado como la principal enfermedad preexistente por los Centros para el Control y la Prevención de Enfermedades (CDC por sus siglas en inglés), la Organización Mundial de la Salud (OMS) y el Centro Europeo para la Prevención y el Control de Enfermedades (ECDC por sus siglas en inglés) 7,11,14, levemente menor al 56.4% de positividad de VIH previo a mpox encontrado en la presente investigación. Además, se han reportado casos de detección paralela de mpox y VIH 11, lo que fue identificado en el 9.0% de los pacientes de este estudio, para un total de 65.4% de casos positivos para VIH (tabla 1).
El análisis conducido por Mitjà et. al. mostró que durante el brote de mpox, se observó mayor gravedad de la enfermedad en pacientes VIH con recuentos de linfocitos T CD4+ menor de 200 cél/uL 2, a diferencia de aquellos con cargas virales indetectables. En este estudio, el 50.0% (3/6) de los pacientes con diagnóstico reciente de VIH y el 9.8% (4/41) de los pacientes con VIH previo, tuvo un recuento de linfocitos T CD4+ inferior a 200 cél/µL (tabla 2). Ninguno requirió hospitalización y tampoco se observaron complicaciones relacionadas con el mpox; por lo que los pacientes continuaron su esquema de TAR y mpox fue tratado en base a la sintomatología.
El 16.7 % (1/6) de los pacientes de reciente diagnóstico de VIH y el 51.2% (21/41) de los pacientes con diagnóstico previo tuvo un recuento mayor a 500 cél/µL. Recuentos elevados de linfocitos T CD4+ en pacientes que no han sido expuestos al TAR sugieren un diagnóstico temprano 17 en tanto que, estos recuentos son los esperados en pacientes en TAR, como se reportó en un análisis de seis estudios 18 ya que evidencia el éxito de la terapia y una favorable recuperación inmunológica.
En cuanto a la carga viral, en pacientes de reciente diagnóstico de VIH se espera encontrar cargas virales elevadas, debido a que el virus está en constante replicación 19. En la tabla 2 se observa que el 20.0% (1/5) de estos casos tenía una carga viral en el rango de 41 - 1000 cp/mL.
Es inusual encontrar una carga viral menor a 1000 cp/mL durante una infección reciente de VIH, lo que puede explicarse por diferentes posibilidades: 1) el paciente ya conocía su diagnóstico de VIH y llevaba su seguimiento en otra Unidad de Atención Integral, 2) probablemente tomaba PrEP, el cual se toma como profiláctico y es de uso frecuente entre el grupo de HSH, y no fue adherente. 3) que fuera progresor lento.
El 78.4% (29/37) tuvo carga viral indetectable, que es lo esperado en una población tratada. Por otra parte, la principal razón de cargas virales detectables en pacientes en TAR son la falta de adherencia y la resistencia a los antirretrovirales 17; lo cual a su vez deriva en recuentos bajos de células CD4+ y que en el contexto de mpox podrían agravar la infección 2, además de las complicaciones propias del VIH.
En relación a la detección de otras infecciones, la positividad general para sífilis en este estudio fue de 17.9% y de 15.4% en pacientes con mpox. Català et al. reportaron 14.3% y 3.7% de esta infección, respectivamente 20, en tanto que, en análisis realizados por otros autores se reportó entre 7% y 41.5% de positividad para sífilis en pacientes positivos para mpox 10,13,21. La sífilis es una de las ITS más prevalentes, de importancia en salud pública por su morbimortalidad; en los últimos años ha aumentado su incidencia en grupos de riesgo, principalmente en HSH y personas viviendo con VIH. La sífilis incrementa de 2 a 3 veces el riesgo de contraer VIH u otras ITS; y el VIH, a la vez, puede alterar el curso clásico de la sífilis 5.
El 64.3% (9/14) de los pacientes con síflis fue identificado con coinfección VIH / mpox; debido a que tienen en comun la vía de contagio sexual, es frecuente encontrar coinfecciones con esta u otras ITS, las cuales pueden ser adquiridas de manera simultánea o una precedida de otra. Una vez realizado el diagnóstico de sífilis, a todos los pacientes del estudio se les prescribió el tratamiento de elección, penicilina G benzatínica, independientemente de los títulos de sífilis (la prueba no treponémica: RPR), como se indica en la literatura 22.
En cuanto al tiempo de monitoreo de la infección después del tratamiento, se recomienda repetir la prueba no treponémica a los 6 y 12 meses en personas de población general, y a los 3, 6, 9, 12 y 24 meses en personas VIH positivo 22,23. El 35.7% (5/14) de los pacientes detectados con sífilis en este estudio se presentó para su seguimiento entre los 6 y 12 meses siguientes y de ellos el 40.0% (2/5) acudió a su seguimiento de 18 meses (figura 1), lo cual puede ser un reflejo del desinterés de los pacientes, derivado de la falsa percepción de seguridad al recibir el tratamiento antibiótico, o a otros factores como la dificultad de asistir a la cita médica por el trabajo, situación económica, entre otros.
La disminución de los titulos es variable, depende de factores como la fase de la enfermedad, su duración y el título inicial, en general se espera una caída de 4 veces del título inicial a los 6 meses en la sífilis temprana 23. De los cuatro pacientes que inicalmente tuvieron un titulo de RPR 1:16, en la primera cita de seguimiento uno de ellos presentó un incremento de 1:128 y en los otros dos se evidenció una disminución del título, posteriormente esos dos pacientes tuvieron un aumento de 4 a 8 veces los títulos en la segunda cita de seguimiento. Las posibles casusas pueden ser no haber completado el tratamiento de tres dosis, o una reinfección.
De los 14 pacientes detectados, únicamente dos tenian diagnóstico previo por sífilis; en los 12 pacientes en quienes se detectó sífilis al momento de la consulta la infección se clasificó como sífilis latente. El período de incubación de mpox fue de 4 - 7 días en los pacientes de este estudio quienes acudieron a consulta una vez que aparecieron las lesiones. Por otra parte, el tiempo de incubación de sífilis es de 21 días (rango de 9 - 90 días), lo que sugiere que los pacientes pudieron haber estado infectados con sífilis al momento de contraer la infección por mpox 23. Por lo que es importante realizar controles de síflis periódicamente a todo paciente con VIH para identificar nuevas infecciones; asimismo reforzar la educación sobre medidas de prevención para evitar coinfecciones en la persona que acude a la atención médica, asi como el contagio a otros.
Se identificó la presencia de C. trachomatis y/o N. gonorrhoeae en 15.4% del total del grupo de estudio y hubo 10.3% de positividad para cada una de las ITS en pacientes con mpox. La detección se realizó utilizando un método molecular en orina para todos los pacientes como parte del protocolo de atención por sospecha de mpox, a través de la cual se identificó un caso; en tanto que la prueba en recto y faringe se realizó por sintomatología, identificando casos individuales y de coinfección en estos sitios (figura 2). El tamizaje para C. trachomatis y N. gonorrhoeae esta indicado en pacientes asintomáticos que pertenecen a grupos de riesgo (HSH y hombres o mujeres que han sido diagnosticados recientemente o con pareja sexual diagnosticada con ITS), y el diagnóstico de infección por estos microorganismos está indicado en pacientes sintomáticos y sexualmente activos 24.
Se ha reportado entre 20% y 50% de coinfección de mpox con otras ITS, presentándose de 60% a 100% en HSH y personas que viven con VIH 7, datos comparables con el 26.9% de coinfección mpox e ITS en portadores de VIH identificado en el presente estudio, en su mayoría HSH. Al tener en común la vía sexual de infección, es importante realizar el tamizaje en pacientes asintomáticos y sintomáticos, dirigido especialmente a grupos de riesgo; ya que las ITS pueden ocasionar daños que usualmente tienen consecuencias en la salud sexual y reproductiva. Además, debido a las prácticas sexuales, algunos microorganismos comúnmente asociados a una forma específica de transmisión, pueden encontrarse en un sitio diferente del conocido, como el caso de los herpes 1 y 2 25. Todos los pacientes positivos para alguna ITS fueron tratados con doxiciclina, azitromicina, fluconazol o aciclovir, según correspondió a cada caso.
Otros virus como los agentes causantes de las hepatitis virales, aunque pueden transmitirse sexualmente, no son genuinamente ITS 26. El VIH, VHB y VHC comparten vías de transmisión, lo que crea un traslape de los grupos de población en riesgo; las tasas de infección por el VHC y el VHB en las personas con infección por el VIH son más altas que en la población general 27. El 2.6% de los pacientes de este análisis era conocido por hepatitis B crónica, y por tener coinfección con VIH, ambos HSH. La prevalencia de hepatitis B crónica entre las personas VIH positivo es reflejo de la vía de transmisión sexual, siendo los HSH y bisexuales los grupos más afectados 28. Para el momento del presente análisis, ambos pacientes recibian TDF (Tenofovir disoproxil fumarato) como parte del esquema de TAR.
El 5.1% de diagnósticos del VHC corresponde a cuatro pacientes conocidos por VIH, dos HSH y dos bisexuales. En los últimos años se ha observado un incremento de infecciones causadas por el VHC entre personas HSH VIH positivas, asociada con el sexo anal sin protección, un mayor número de parejas sexuales a lo largo de la vida e ITS recientes, entre otras. El VIH no es un requisito previo para la transmisión sexual de VHC, sin embargo, los HSH VIH negativo están menos expuestos a contagiarse 29. La presencia del ARN del VHC en el semen y su descarga durante la práctica de sexo anal en HSH coinfectados con VIH podría explicar la persistencia de la transmisión sexual del VHC limitada en gran medida a este grupo seropositivo de riesgo 29,30,31. Tres de los pacientes con el VHC se trataron con Sofosbuvir/Velpatasvir y dos resolvieron la infección (figura 3).
Dentro de los alcances del presente estudio se puede ver la importancia de como una enfermedad puede servir para detectar otras, estableciendo una sinergia de estrategias en cuanto a la identificación y tratamiento de otras ITS, También muestra como un modelo de atención integral es la forma idónea para el abordaje de estas enfermedades emergentes porque da una respuesta pronta al diagnóstico y tratamiento, todo en el mismo lugar.
Una limitante de los hallazgos derivados de este análisis, es que estos resultados no se pueden comparar con los obtenidos en otros centros de atención, ya que no siempre es factible replicar el modelo de Atención Integral en otras unidades porque no se tiene la misma infraestructura, disponibilidad y acceso a pruebas moleculares, ni un equipo multidisciplinario conformado.
Conclusiones
Los resultados de esta investigación muestran la importancia de realizar pruebas de detección de ITS en personas con sospecha de mpox, así como pruebas de infecciones no consideradas de transmisión sexual, pero que pueden ser adquiridas al tener la misma vía de transmisión, con la finalidad de realizar el abordaje oportuno para mejorar la salud a nivel individual y consecuentemente disminuir la probabilidad de transmisión.