Introducción
La cefalea postpunción dural(CPPD) es una de las complicaciones más frecuentes luego de la anestesia subaracnoidea. La primera CPPD documentada por el cirujano alemán August Bier en 1898, se produjo como complicación de una anestesia raquídea que el mismo se realizó inyectándose 10 a 15 mg de cocaína como anestésico local. A principio de 1900 ya existían múltiples reportes de esta complicación alcanzándose una incidencia de hasta 50 %. La introducción de agujas punta de lápiz por Whitacre y Hart en 1951 disminuyó notablemente la incidencia de CPPD 1. A pesar de los avances en su prevención y tratamiento, continúa siendo una causa importante de morbilidad y hospitalización, siendo la paciente embarazada particularmente vulnerable por los factores de riesgo que presenta y las limitaciones que esta complicación puede ocasionar en el vínculo madre hijo que se inicia.
La Clasificación Internacional de Cefaleas ICHD-III 2, clasifica a la CPPD como un subtipo de cefalea atribuida a hipotensión de líquido cefalorraquídeo (LCR) y la define como la cefalea ortostática, que se manifiesta dentro de los cinco días siguientes a una punción lumbar, causada por pérdida de LCR a través de la punción dural. Suele acompañarse de dolor cervical, acufenos, alteraciones auditivas, fotofobia y/o náuseas y se resuelve de manera espontánea en un plazo de dos semanas o después del sellado de la fuga con un parche epidural autólogo. Los criterios diagnósticos son:
(1) Se ha practicado una punción dural.
(2) La cefalea se desarrolla dentro de los cinco días siguientes a una punción dural.
(3) Sin mejor explicación por otro diagnóstico de la ICHD-III
La severidad puede ser evaluada a través de la escala verbal análoga como una forma de asignar un valor al dolor y poder cuantificarlo. Se considera dolor leve una puntuación entre 1-3, moderada entre 4-7 y severa de 8 a 10; también a través de la incapacidad funcional que provoca en la madre o la respuesta al tratamiento.
Los factores de riesgo se dividen en no modificables y modificables 3,4, 5. En el primer grupo, se encuentran la edad, siendo más frecuente en menores de 40 años, el sexo femenino y la historia previa de CPPD y de cefalea crónica; la relación entre el índice de masa corporal (IMC) y la CPPD es discutida 6,7,8, si bien recientes estudios no pudieron demostrar que la obesidad fuera un factor protector, lo que se sabe es que no incrementa el riesgo de CPPD. Entre los factores de riesgo del segundo grupo, el tipo y tamaño de la aguja es definida como una de las variables más importantes, siendo este punto analizado más adelante. Las punciones durales múltiples y la poca experiencia del operador incrementan la probabilidad de CPPD 3.
El mecanismo exacto de la CPPD no se conoce con certeza. La teoría más aceptada es que el orificio dural provoca una pérdida de LCR que produce hipotensión intracraneal y tironeamiento de estructuras encefálicas sensibles al dolor. Un segundo mecanismo sería por incremento del flujo sanguíneo cerebral y vasodilatación cerebral, secundaria al descenso del volumen y presión de LCR, como mecanismo compensador para mantener un volumen cerebral constante.
Para el tratamiento de la CPPD se recomienda reposo sintomático, no existiendo evidencias de que sea mejor que la movilización inmediata 9,10,11. No se ha demostrado que la administración de líquidos v/o o i/v sea beneficiosa 9,10,11,12. El uso de cafeína v/o ampliamente usada en el tratamiento conservador de la CPPD, es actualmente controvertido; aquellos estudios a favor de la misma 13,14, plantean que esta droga es un estimulante del sistema nervioso central, la cual produce vasoconstricción cerebral por bloqueo de los receptores de adenosina implicados en la CPPD, siendo la dosis oral efectiva de 300 a 500 mg/día, alcanzándose un pico de concentración plasmática a los 30 minutos, con una vida media de 3 a 8 horas. Aparece en pequeñas cantidades en la leche materna, aunque recientes estudios no han demostrado efectos adversos neonatales 3. Otros estudios no encontraron beneficio 15,16, por lo que recientes revisiones de la literatura sólo recomiendan cafeína i/v como prevención de la CPPD en la punción dural accidental, pero no como tratamiento 12,17. De igual forma las últimas revisiones recomiendan gabapentina y pregabalina en el tratamiento conservador 12. Nosotros incluimos la cafeína como tratamiento, dado que nuestro trabajo fue anterior a estas revisiones. Por la misma razón no incluimos pregabalina ni gabapentina.
Los análogos de la hormona adrenocorticotrópica como el Cosyntropin ® han mostrado reducción significativa de CPPD luego de una punción dural accidental, pero como tratamiento recientes estudios no han demostrado beneficios 12,18,19. Los corticoides como la hidrocortisona 100 mg cada 8 horas i/v en tres dosis ha mostrado beneficio como prevención y/o tratamiento de la CPPD en casos reportados20. Se plantea que el efecto beneficioso se debería al aumento de la retención de agua y sodio a nivel renal lo que favorecería la generación de LCR. Nuestro grupo lo adoptó como una medida más de tratamiento dado que si bien el grado de recomendación es débil presentan un amplio margen de seguridad. Se debe ser cuidadoso en pacientes diabéticas o hipertensas de difícil control o en pacientes infectadas.
El parche hemático epidural continúa siendo la terapia más efectiva para el tratamiento de la CPPD 12,21. Se plantean varios mecanismos para explicar su alta efectividad. En primer lugar, produce un efecto mecánico que taparía el orificio dural disminuyendo la pérdida de LCR. Su efecto más importante se debería al aumento de la presión del espacio epidural y subaracnoideo por desplazamiento del LCR a nivel cefálico, disminuyendo la tracción de estructuras encefálicas. Por último, la restitución de la presión intracerebral disminuye la vasodilatación cerebral compensadora produciendo vasoconstricción inmediata y alivio del dolor. No hay suficiente evidencia para justificar el uso rutinario de parche hemático profiláctico 8, si bien existen estudios que muestran algún grado de beneficio disminuyendo la duración y la severidad de la cefalea3,21,23. En cuanto al volumen de inyección de parche hemático si bien es discutido se recomienda 15-20 ml de sangre autóloga o limitado por dolor dorsal o disconfort de la paciente 22. No hay evidencia suficiente para recomendar un nivel de punción para el parche hemático. No encontramos literatura que apoye un tiempo mínimo de reposo luego del parche.
El objetivo primario fue conocer la incidencia de CPPD en las pacientes que recibieron raquianestesia para cesárea. Los objetivos específicos fueron conocer en qué proporción aparecen factores de riesgo reconocidos de CPPD en nuestra población, como son el tamaño y tipo de la aguja, el número de punciones¸ el índice de masa corporal, la escoliosis, la oportunidad de la cesárea, el antecedente de migraña o CPPD previa y la experiencia del operador; evaluar la efectividad del tratamiento médico en aquellas pacientes que presentaron CPPD y cuantificar la necesidad de parche hemático peridural
Material y método
Realizamos un estudio prospectivo, descriptivo, que implicó el seguimiento diario postoperatorio por 72 horas, a todo el universo de la población objetivo que incluyó las embarazadas que recibieron raquianestesia para su cesárea en el Hospital Pereira Rosell (HPR) por un período de 1 año. Fueron excluidas las pacientes que tenían algún déficit intelectual que no permitía evaluar adecuadamente la cefalea o las pacientes que recibieron anestesia general para la cesárea. El estudio fue realizado luego de aprobado por el Comité de Ética del Hospital. Las variables evaluadas se muestras en la Figura 1. La recolección de datos fue realizada por un residente de anestesiología. Se obtuvo consentimiento informado por escrito.
Una vez diagnosticada una CPPD se realizó tratamiento de acuerdo a protocolo de la Cátedra de Anestesiología que consistió en un tratamiento médico en base a reposo sintomático, ibuprofeno 400 mg v/o cada 8 horas, cafeína 100 mg cada 8 horas v/o e hidrocortisona 100 mg i/v cada 8 horas (3 dosis). Si a pesar de este tratamiento la cefalea persistió, agregamos rescates con tramadol 100 mg i/v. Si después de 48 horas de tratamiento médico la paciente presentaba una CPPD severa estaba indicado un parche hemático epidural con 20 ml de sangre autóloga o limitado por dolor.
El seguimiento de las pacientes con cefalea fue diario hasta la resolución de la misma y todas fueron dadas de alta sin cefalea. Se describen datos por tablas y gráficos de frecuencia, así como medidas de resumen para variables continuas. La incidencia de CPPD se calculó como el cociente entre el número de casos nuevos encontrados por el total de pacientes a las que se les realizó el procedimiento, con una constante k = 100. Para el estudio de diferencias entre variables continuas, se utilizó test t de Student para muestras independientes. Así como para el cálculo de asociación entre variables se utilizó test Chi cuadrado o exacto de Fisher en los casos en que su aplicación fuese necesaria. En aquellos casos en que se comprobó la existencia de asociación entre variables, formando parte de la comparación una variable de las nominadas como factor de riesgo, se estudió la medida de riesgo relativo correspondiente, en este caso el riesgo relativo, con su correspondiente IC 95%. En todos los casos se fijó un umbral de significación de alfa = 0.05.
Resultados
Se estudió un total de 914 pacientes. De los factores de riesgo estudiados encontramos los siguientes datos: en relación a la o portunidad de la cesárea , el 16.7% (153) fueron electivas y el 80.7% (738) de urgencia y emergencia. Se carece del dato para el 2.5% (23)de las pacientes. En relación al horario : 32.9% (301) fueron en horario nocturno (de 22 hs a 8 de la mañana) mientras que 65.2% (596) fueron durante el día. Se carece del dato para el 1,8% (17). En relación al operador : 10.3% (94) fue realizada por anestesiólogos con menos de 5 años de recibidos, 31.6% (289) con más de 5 años, 54.0% (494) residentes, careciéndose del dato para el 3.8% (37) del total de procedimientos. En relación a la deformidad de columna , el 96.3% (880) no la presentaba y sí se presentó en el 3.1% (28); se carece del dato para 6 de las pacientes. El tipo y tamaño de la aguja usados en este estudio se muestra en la (Tabla 1).
En relación al número de punciones : al 76.6% (700) de las pacientes se les realizó una única punción, al 15.2% (139) 2 punciones, al 7.0% (64) más de 2 punciones, careciéndose del dato para el 1.2% (11). En relación al IMC se obtuvo un promedio de 29.8 ± 0.2 Kg. /m2, con un mínimo y un máximo en 16.01 y 51.56 respectivamente. Si utilizamos la clasificación de la OMS observamos que 5(0,6%) presentaban bajo peso, 129(14,4) normopeso, 373(41,8) sobrepeso y 386(43,2) obesidad, careciéndose de dato para 21 pacientes. (Figura 1)
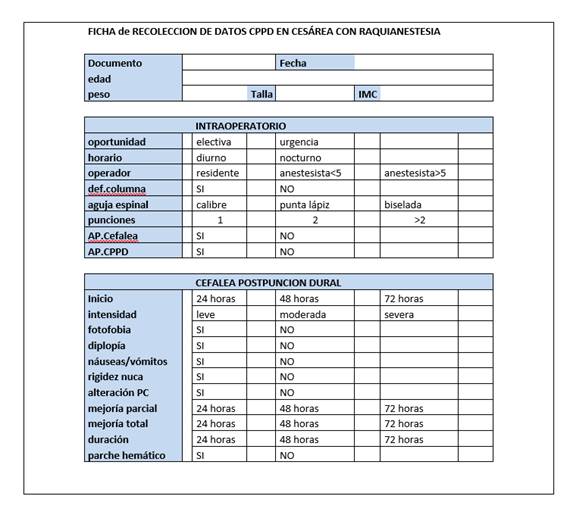
Figura 1 Ficha de recolección de datos. IMC (Índice de masa corporal), anestesista<5 años (anestesista de menos de 5 años de recibido), anestesista >5 (anestesista de más de 5 años de recibido), Alteración PC (alteración de pares craneanos), Def. columna (deformidad de columna, AP (antecedentes personales).
El 8,6% (79) de las pacientes presentaban antecedentes personales de cefalea , careciéndose del dato para el 2.1% (19), mientras que el 2,7% (25) tenía antecedentes de CPPD previa, careciéndose del dato para 18 mujeres, las que representan el 19.7% del total.
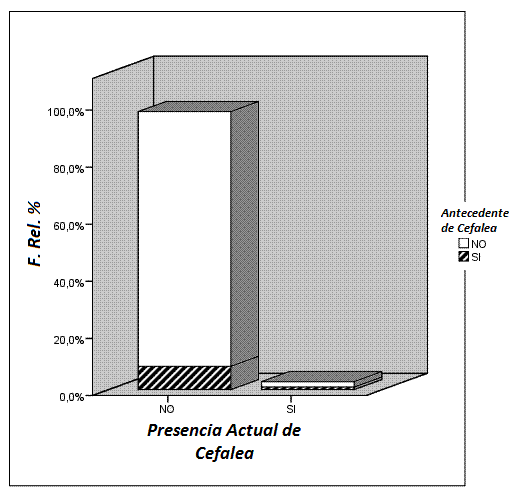
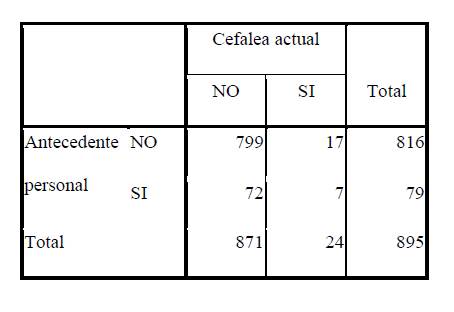
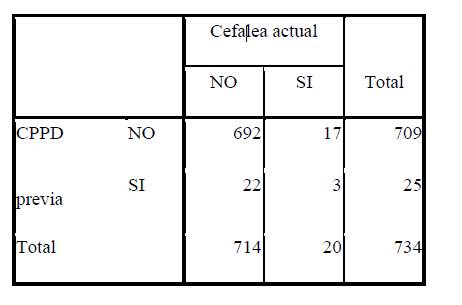
Se presentó una incidencia de cefaleas de 2.6 casos cada 100 pacientes. Un total de 24 casos en la población estudiada. La mayor parte se presentó en las primeras 24 horas post punción (66.7% - 16 casos). Tanto a las 48 horas como a las 72 horas se presentaron las mismas proporciones, 16.7% - 4 casos en cada rango horario. En relación a la intensidad de las cefaleas , 50.0% (12) fue leve, 29.2% (7) moderada, 4.2% (1) severa, careciéndose del dato para 4 pacientes. En relación a la duración , 54.2% (13) tuvieron una duración de 24 horas, 41.7% (10) tuvieron una duración de 48 horas y 4.2% (1) tuvo una duración de 72 horas. 13 de las pacientes obtuvieron una mejoría total a las 24 horas, en los 11 restantes la mejoría fue parcial. De dichas 11, 8 obtuvieron la mejoría total a las 48 horas, las 3 restantes presentaron mejoría parcial a las 48 horas. Finalmente, esas 3 pacientes presentaron una mejoría total a las 72 horas. La fotofobia se observó en 2 (8,3%) de las pacientes. 29.2% (7)presentaron náuseas y vómitos mientras que ninguna presentó irradiación a nuca, diplopía o alteración de pares craneales. Ninguna de las pacientes requirió parche hemático. Se encontró una asociación estadísticamente significativa entre la presencia de cefalea previa y la CPPD actual, valor p <0.001, con un valor de riesgo (RR) de 4.6 veces más en las pacientes con antecedentes personales que en las que no presentaron antecedentes. IC RR 95% de (1.8; 11.4). Se muestra en la (Figura 2) y en la (Tabla 2) correspondiente. También se encontró asociación entre el antecedente de CPPD y la presencia actual de CPPD, valor p = 0.004 con un valor de riesgo (RR) de 5.6 veces más en las pacientes que ya habían presentado cefalea que en las que no la habían presentado. IC RR 95% de (1.5; 20.3).
Ver (Figura 3) y (Tabla 3). No se encontró asociación estadísticamente significativa para las siguientes variables. Oportunidad y CPPD, valor p = 0.630. 19 casos fueron en cesáreas electivas y 5 en cesáreas de urgencia y emergencia. Horario de la cesárea y CPPD, valor p = 0.644. 17 casos se realizaron en horario diurno y 7 en horario nocturno. Experiencia del operador y CPPD, valor p = 0.585. De las pacientes que presentaron cefalea 2,3 % fueron realizadas por residentes (16/478), mientras que 2,1% fueron realizadas por anestesiólogos (2/92 con menos de 5 años de recibido y 6/283 con más de 5 años de recibidos). Deformidad de columna y CPPD, valor p = 0.722, (2 casos la presentaban y 22 no). Tipo y calibre de la aguja y CPPD. Valor p = 0.759. 23 casos con aguja 25 punta de lápiz y 1 caso con aguja 27 punta de lápiz. No se encontró asociación entre el número de punciones y la CPPD, valor p = 0.204. 22 casos para 1 punción, 2 casos para 2 punciones y ningún caso para más de 2 punciones. Por último tampoco se encontró asociación entre el IMC y la CPPD, valor p = 0.296. Ningún caso para bajo peso, 1 caso para normopeso, 3 casos para sobrepeso y 9 casos para obesidad.
Discusión
La incidencia de CPPD en obstetricia con agujas espinales reportada en la literatura va de 0 a 36% dependiendo del tipo y tamaño de la aguja 3 4 5. Para agujas espinales biseladas se reporta una incidencia de 36% para calibre 22 G, de 3 a 25 % para calibre 25 G y 1,5 a 5,6% para calibre 27 G, mientras que con agujas punta de lápiz, atraumáticas, la incidencia se reduce, siendo de 0 a 4,7 % con calibre 25G y de 0 a 1,6% con calibre 27G. Tomando en cuenta que en nuestro estudio el 98 % de las agujas que se usaron fueron punta de lápiz, planteamos que una incidencia de CPPD de 2,6 % (24) es comparable con los datos de la literatura. En contraposición con estos resultados no obtuvimos una diferencia estadísticamente significativa en la incidencia de CPPD entre el calibre 25 y 27. Una limitante de nuestro estudio que podría explicar este punto es el bajo número de pacientes en las que se usó calibre 27. (11,2%)
Con respecto a otros factores de riesgo reconocidos como son la experiencia del operador y el número de punciones no obtuvimos asociación estadística, así como tampoco con otros factores de menor importancia pero que podían influir en la dificultad de la punción y/o en el número de punciones como son la deformidad de columna, la obesidad, la cesárea de urgencia y el trabajo nocturno. Al igual que otros estudios, sí encontramos una fuerte asociación entre la CPPD actual y el antecedente de cefalea crónica y CPPD previa, con un RR 4,6 para la primera y 5,6 para la segunda.
De las 24 CPPD, solo una (4,2%) fue severa, 29.2% (7) moderadas, mientras que el 50.0% (12) fueron leves. De los síntomas y signos asociados, solo se observó fotofobia (2) y náuseas/vómitos (29), no evidenciándose signos más graves como compromiso de pares craneanos. Además, el 100 % se resolvió dentro de los plazos esperados, 24 horas para el 54.2%, 48 horas para el 41.7% y 72 horas en el 4.2%. De las características de la CPPD observadas en nuestro estudio destacó el bajo número de CPPD intensas, su rápida resolución y sobre todo la ausencia de necesidad de parche hemático epidural lo que motivo la búsqueda de estos datos en la literatura. Comparando con otros estudios similares al nuestro, en 2010 Gisore E. y col. estudiaron la incidencia de CPPD en pacientes sometidas a cesárea con anestesia espinal comparando agujas biseladas vs punta de lápiz de diferentes calibres, encontrando una incidencia de 24% vs 4,5 %, no siendo estudiadas otras variables como la necesidad de PHE 24.
En 2014 H. M. Ali y col. estudiaron 2736 pacientes sometidas a cesárea con anestesia espinal, pero en este caso las agujas usadas fueron biseladas y de mayor calibre (Quincke 22 y 20 G), obteniendo una incidencia de 32 % de CPPD. Ninguna paciente con cefalea persistente, la cual definieron como una cefalea de duración mayor a 7 días recibió PHE dado que se negaron a recibirlo 25. Por otro lado, a diferencia de nuestro estudio, Shaikh J.M. y col compararon la incidencia y severidad de CPPD en un total de 480 anestesias espinales para cesárea con agujas 25 (grupo I) y 27 G (grupo II) Quincke y 27 G punta de lápiz (grupo III); encontraron no sólo que la incidencia en el grupo III fue menor sino también la severidad; estos datos podrían reflejar que a menor tamaño del agujero dural, existiría menor pérdida de LCR pudiendo corresponderse con incidencias más bajas de CPPD (dato que no encontramos en nuestro estudio ) y con menor severidad 26 . Otros 2 estudios 27,28evaluaron la CPPD en cesárea con anestesia espinal realizados en Hospitales Obstétricos; los mismos fueron realizados en pequeño número de pacientes, usando agujas de mayor calibre y/o biseladas, obteniendo mayor incidencia de CPPD, no siendo evaluadas las características de la misma o la necesidad de PHE.
Por último, no encontramos datos concluyentes que reporten la incidencia de PHE para el tratamiento de la CPPD en anestesia espinal para cesárea, aunque algunos trabajos hacen referencia a esto. Por ejemplo; en 2016 J.L Booth y col. Realizaron un estudio retrospectivo de 466 PHE asociados a 84804 procedimientos neuraxiales obstétricos en un periodo de 15 años, no encontrando diferencias estadísticas en la incidencia de PHE entre las diferentes técnicas anestésicas: epidural (0,17%), combinada (0,22%) y espinal (0,18%)29.
Según nuestros resultados podemos concluir que la CPPD postanestesia espinal para cesárea, continúa siendo causa de morbilidad, aun con agujas punta de lápiz de pequeño calibre; sin embargo, la gran mayoría son de intensidad leve a moderada, responden al tratamiento médico, se resuelven rápido y no requieren parche hemático epidural. Creemos que se requieren más estudios de mayor N para definir cuál es la incidencia real de PHE en anestesia espinal para cesáre
Conclusiones
Obtuvimos una incidencia de CPPD de 2,6%, concordante con datos de la literatura; la mayoría apareció a las 24 horas y todas mejoraron con tratamiento médico. Las pacientes con cefalea y CPPD previa presentaron un RR 5,8 y 5,4 respectivamente (IC 95%), no encontrando asociación con otros factores de riesgo. En cesáreas de urgencia y emergencia, las agujas calibre 25 tipo punta de lápiz parecen ser una alternativa válida, asegurando fiabilidad en la técnica, con una incidencia aceptable de cefaleas postpunción dural.