Introducción
La hipofosfatemia aguda y grave en cuidados críticos puede asociarse a disfunción multiorgánica. Son pocas las notificaciones que informen su prevalencia, si bien se estima frecuente1.
En la Unidad de Cuidados Intensivos de Niños del Centro Hospitalario Pereira Rossell (UCIN-CHPR) se identificó una prevalencia de 33% en pacientes con riesgo de síndrome de realimentación, una de sus probables etiologías2. En una encuesta de prevalencia transversal realizada por la Sociedad Europea de Medicina de Cuidados Intensivos (ESICM) en 2020, en la que participaron 60 unidades de cuidados intensivos (UCI) de 22 países, la prevalencia fue de 15,4%. En ese trabajo se observó que 60% de las unidades participantes no contaban con protocolos de tratamiento1. Varios estudios informan que la hipofosfatemia se asocia con peor evolución, aumentando la estadía en UCI y una mayor duración de asistencia ventilatoria mecánica (AVM)1-4. Estas complicaciones son más prevalentes en pacientes desnutridos y asociándose la hipofosfatemia al uso de furosemide, dopamina, esteroides y agonistas beta dos adrenérgicos4. La ingesta baja de energía y la gravedad de la enfermedad se relacionan con la hipofosfatemia, siendo la inflamación del paciente crítico un pilar importante en su desarrollo. Particularmente, el paciente con factores de riesgo de síndrome de realimentación puede tener predisposición a desarrollarla5. A pesar de la asociación entre hipofosfatemia y peor evolución clínica, no se ha determinado el umbral óptimo a partir del cual la hipofosfatemia se vuelve crítica y requiere tratamiento, ni el tiempo en que debe ser corregida6. Se necesitan más estudios para conocer su impacto en la mortalidad, ya que lo publicado hasta el momento no es concluyente6. Existe mayor consenso en su corrección cuando es aguda, severa o sintomática7. El fósforo es un electrolito que representa el 1% del peso corporal total, su reserva está presente sobre todo a nivel óseo en un 85%. El resto se encuentra distribuido a nivel del músculo y de tejidos blandos, y menos del 1% está presente en el líquido extracelular8. El aporte principal se obtiene de la dieta, siendo más disponible en alimentos de origen animal, además en lácteos, sobre todo descremados, legumbres y cereales8.
El nivel de fósforo plasmático se mantiene en un rango estrecho vinculado a cambios en su absorción intestinal, reabsorción renal a nivel tubular y redistribución entre los compartimentos intra y extracelular, así como su reserva ósea8. La reabsorción tubular renal es su principal determinante8.
La (Tabla 1) se enumeran las principales causas de hipofosfatemia en las tres categorías que ya referimos.
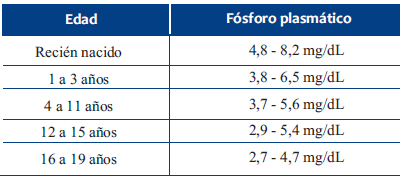
Los niveles plasmáticos de fósforo dependen de la edad, siendo mayores en niños pequeños y adolescentes. En adultos oscila entre 2,5 y 4,5 mg/dl (0,81 - 1,45 mmol/l)8. La hipoalbuminemia disminuye el nivel plasmático. En (Tabla 2) detalla referencia de rangos en pediatría, si bien se sugiere contar con tablas de referencia que se usen en el laboratorio de cada centro hospitalario9.
El fósforo es el principal anión intracelular y tiene una función estructural como componente de fosfolípidos, nucleoproteínas y ácidos nucleicos8.
Interviene en la fosforilación oxidativa, en la glucólisis y en procesos enzimáticos con fosforilación de proteínas10.
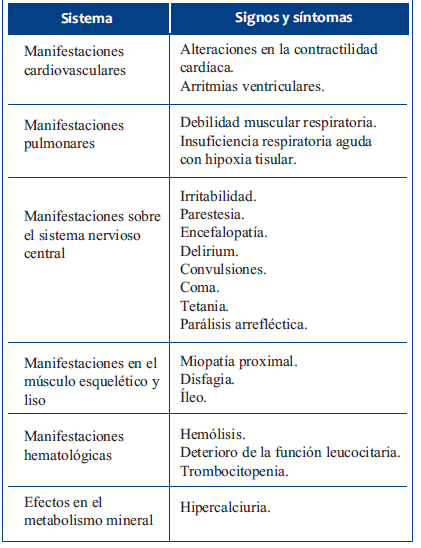
La deficiencia puede determinar disfunción cardiorrespiratoria, arritmias, así como disminución de difosfoglicerato, que aumenta la afinidad de la hemoglobina por el oxígeno, favoreciendo la hipoxia tisular10. La hipofosfatemia aguda sin agotamiento crónico previo de fosfato no suele ser sintomática8. En la (Tabla 3) se detallan los principales síntomas atribuibles a la hipofosfatemia severa por sistemas11.
Indicaciones de corrección de hipofosfatemia
A partir de la revisión realizada se sugiere corregir la hipofosfatemia cuando es aguda y severa o sintomática7-12.
Se considera severa cuando la misma es menor a 2 mg/dL12.
En la hipofosfatemia moderada puede valorarse la suplementación oral.
El aporte de fósforo puede realizarse de forma enteral o por enema, o intravenoso.
Suplementación de fósforo oral
La formulación que sugerimos para uso oral es utilizada en nuestro medio para pacientes con insuficiencia renal que requieran aporte externo de fósforo y se denomina solución de Jolie, es una solución magistral que se realiza a solicitud13.
Esta solución contiene por cada ml: 1 mmol de fosfato y 1 mEq de sodio13.
Su composición es:
• Ácido orto fosfórico 85% - 5,45 g.
• Fosfato disódico (12H2O) - 18,75 g.
• Agua conservante sin propilenglicol csp 100 ml.
Como efectos adversos de la administración oral de fósforo se han descrito diarrea, náuseas, vómitos y dolor abdominal13. En caso de sobredosis: hiperfosfatemia, hipocalcemia, hipopotasemia, hipernatremia y fallo renal agudo13.
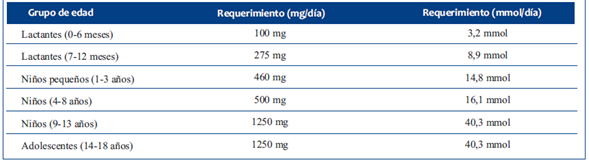
La suplementación oral sugerida es 2-3 veces la ingesta dietética normal según tolerancia, en 2-3 dosis14. Se adjunta tabla con la ingesta dietética sugerida para la edad acorde a la OMS (Organización Mundial de la Salud). La misma varía según la edad del niño/a15.
Puede considerarse también 2-3 mmol/kg/día, según otros autores.
En la (Tabla 4) se adjunta la ingesta dietética sugerida de fósforo acorde a la edad en mg y en mmol por día.
Hay que tener en cuenta que se requiere vitamina D activa para la absorción intestinal de fosfato14.
Se cuenta con formulaciones comerciales de fósforo que se utilizan como laxantes orales o vía enemas. Existen trabajos que mostraron un aumento de los niveles de fósforo en forma segura en la UCI16.
En nuestro medio esta solución oral contiene fosfato dibásico de sodio 900 mg/5 mL (180 mg/mL) + fosfato monobásico de sodio 2,4 g/5 mL (0,48 mg/mL). Al ser un laxante determina las complicaciones digestivas ya referidas previamente, por lo que sugerimos no administrar más de 5 ml de la solución para la corrección de hipofosfatemia y controlar la aparición de síntomas adversos.
Suplementación de fósforo intravenosa
Se cuenta con ampollas para uso intravenoso para cuando es severa y/o sintomática, o en casos particulares donde exista mala tolerancia del fósforo oral o entera(l).
La ampolla contiene 20 ml de glicerolfosfato de sodio (Glycophos), 1 ml de dicha ampolla contiene 1 mmol de fósforo y 2 mmol de sodio1. El glicerolfosfato requiere ser hidrolizado a nivel hepático y niveles de fosfatasa alcalina normales17.
Los solventes compatibles son suero fisiológico y dextrosa al 5% y debe diluirse hasta alcanzar la concentración máxima sugerida, que varía acorde al acceso venoso del cual dispongamos. Concentración máxima por vía central 0,12 mmol/ml y por vía periférica 0,05 mmol/ml12-18.
Se sugiere administrar en 6 horas no superando la velocidad de infusión de 0,6 mmol/kg/hora.
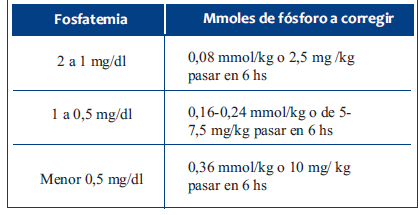
En la (Tabla 5) se muestran los aportes de mmoles sugeridos acorde a la depleción plasmática de fósforo en el niño12-19.
Tabla 5 Niveles de severidad de hipofosfatemia y mmoles sugeridos para corrección por vía intravenosa.
En el adulto la corrección aproximada es de 10 a 20 mmol/dosis (media ampolla o una ampolla), siendo esta la dosis máxima, independientemente del peso.
Hay autores que plantean realizar un mantenimiento intravenoso posterior cuando la hipofosfatemia es severa, las dosis de mantenimiento sugeridas son las siguientes12.
Tengamos en cuenta que la hipofosfatemia puede ocurrir con niveles de depósitos de fósforo bajos, moderados o altos, ya que el descenso del fósforo plasmático puede ser consecuencia de un movimiento transmembrana del mismo. Es por eso que la colocación de un mantenimiento de fósforo debe ser individualizada y podría, por ejemplo, considerarse en un paciente desnutrido grave con síndrome de realimentación, en quien presuponemos depósitos insuficientes, la misma podría realizarse dentro de la propia alimentación parenteral si la recibe.
Como un ejemplo práctico, entonces, si tenemos un niño de 1 año, 10 kilos de peso, que cursa una hipofosfatemia grave sintomática con un valor de fósforo plasmático de 1 mg/dl, como hemos referido en el texto, realizaremos una corrección de 0,16 mmol/kg, o sea que al multiplicarlo por el peso obtenemos la dosis de 1,6 mmol a administrar.
Como ya referimos, 1 ml de glicerolfosfato de sodio (Glycophos) contiene 1 mmol de fósforo y 2 mmol de sodio. Si tenemos que corregir 1,6 mmoles, tomaremos 1,6 cc de la ampolla y lo vamos a diluir acorde al acceso venoso disponible.
Si contamos con una vía venosa central (concentración máxima 0,12 mmol /ml) la dilución será la siguiente: 1,6 cc de glicerolfosfato de sodio, llevar a 15 cc de suero fisiológico y administrar en 6 hs a 2,5 cc/hora.
La dilución antes referida es la máxima concentración permitida por osmolaridad, podemos, si así lo consideramos pertinente, diluir en mayor volumen de suero.
Si contamos con una vía venosa periférica (concentración máxima 0,05 mmol/ml) la dilución será la siguiente: 1,6 cc de glicerolfosfato de sodio, llevar a 35 cc de suero fisiológico y administrar en 6 hs a 5,8 cc/hora.
Se realiza la misma apreciación de la dilución que en el caso previo.
Complicaciones
Como complicaciones de la infusión intravenosa recordemos que el fosfato puede precipitar con el calcio, son incompatibles.
Dosis altas de fosfato cuando no hay depleción real pueden provocar hiperfosfatemia, hipomagnesemia, hipocalcemia e hipotensión7,18.
Controles
Se sugiere controlar la presión arterial durante la infusión de fósforo y realizar control sérico cada 12 horas cuando el riesgo de hipofosfatemia es importante.
En caso de estar frente a un síndrome de realimentación, recordemos que no alcanza con realizar la corrección de fósforo, sino que es necesario disminuir el aporte energético del paciente a fin de no perpetuar la hipofosfatemia, así como agregar tiamina intravenosa11,12.











 texto en
texto en