Introducción
Los HI comprenden lesiones vasculares clasificados de acuerdo a la International Society for the Study of Vascular Anomalies (ISSVA) como tumores vasculares benignos y subclasificados según su patrón de afectación (focal, multifocal, segmentario, indeterminado) y según su profundidad (superficial, profundo, mixto, otros)1. Son los tumores benignos más frecuentes en la infancia y se estima que afectan aproximadamente al 4% de los lactantes2,3.
La decisión de iniciar el tratamiento y la elección de la mejor opción terapéutica (tópica o sistémica) debe individualizarse en función de varios factores: el tamaño de la lesión, la localización, la presencia de complicaciones como ulceración, el riesgo de cicatrización o desfiguración, la edad del paciente, la tasa de crecimiento o regresión al momento del diagnóstico, los riesgos y beneficios del tratamiento4.
Caso clínico
Sexo masculino, 1 año y 10 meses. Nacido a término, adecuado para la edad gestacional. Presenta HI focal mixto a nivel supraciliar derecho con compromiso de párpado superior sin alteración funcional del mismo ni afectación visual. Se realiza diagnóstico a los 3 meses de vida y se decide iniciar propanolol 2 mg/kg/día, durante ocho meses, con el cual presentó respuesta parcial debido a que se realizó de forma intermitente por causa de múltiples eventos de crisis bronco-obstructivas.
A los 18 meses de vida dada la persistencia de la lesión vascular (Figura 1. A), se realiza ecografía Doppler, se confirma persistencia de flujo por lo que se decide cambiar terapia a atenolol.
Se inicia con dosis de 1 mg/kg/día aumentando luego a 2 mg/kg/día, con buena tolerancia, sin presentar efectos adversos.
En los controles posteriores, luego de dos meses de tratamiento se evidencia clínicamente una franca mejoría de la lesión presentándose blanda con disminución de la intensidad del eritema y del tamaño (Figura 1. B); a los cuatro meses ya se observa mejoría en el compromiso de párpado (Figura 1. C).
Discusión
Los betabloqueantes se usan desde hace años en el tratamiento de los HI, especialmente el propranolol, considerado primera línea en el tratamiento de los HI de riesgo o complicados5.
El propanolol ha provocado en algunos casos efectos secundarios indeseados, lo que puede limitar su empleo y hace que investigadores busquen otras alternativas6.
La dosis inicial recomendada de propanolol es de 1 mg/kg/día, llegando hasta 3 mg/kg/día, administrada dos a tres veces al día7.
Los principales efectos secundarios del propanolol son alteraciones del sueño, hipotensión, bradicardia, hipoglucemia y broncoespasmo. La hipoglucemia sintomática y las convulsiones secundarias a hipoglucemia se han observado en pacientes con baja ingesta de alimentos o con una infección concomitante. El riesgo de hipoglucemia disminuye al alimentar de manera regular al paciente y evitar ayunos prolongados. Los pacientes con enfermedad de vías respiratorias con riesgo de broncoespasmo también deben suspender transitoriamente el tratamiento7,8.
En 2011, Raphael MF y colaboradores informaron por primera vez que dos pacientes con HI abandonaron la terapia con propranolol debido a hiperreactividad bronquial y trastornos del sueño y que al indicar atenolol obtuvieron resultados sobresalientes sin efectos adversos9-11. Estas observaciones fueron nuevamente demostradas en un reciente metaanálisis que evaluó la eficacia y seguridad comparativa de atenolol versus propranolol en HI en términos de respuesta a la terapia, actividad de hemangioma y efectos adversos y secundarios concluyendo con evidencia científica que el atenolol tiene una eficacia comparable con el propranolol con un mejor perfil de seguridad2.
El atenolol es un bloqueante selectivo beta-1 hidrofílico, no actúa sobre los receptores beta-2 y por lo tanto se evita la hiperreactividad bronquial como lo hace el propanolol, como ocurrió en nuestro paciente. Por otro lado, el atenolol no favorece la hipoglucemia y sus propiedades hidrofílicas restringen el paso a la barrera hematoencefálica disminuyendo el efecto indeseado de alteraciones en el sueño. Como beneficio adicional, el atenolol se administra una vez al día, por lo que proporciona una mejor adherencia al tratamiento9.
El atenolol se utiliza a una dosis de 1 a 3 mg/kg/día10. Puede iniciarse a una dosis de 1 mg/kg/día ajustándose mensualmente según la ganancia de peso y si se observa una respuesta insuficiente puede incrementarse la dosis hasta 3 mg/kg/día, es aconsejable realizar un control a las dos semanas de iniciado el tratamiento y luego un seguimiento con controles mensuales2.
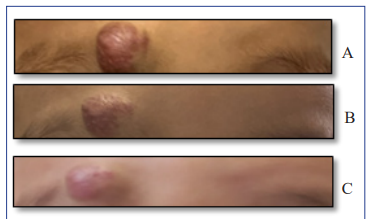
Figura 1: Hemangioma infantil con compromiso de párpado superior derecho (A), su evolución a los 2 y 4 meses de tratamiento con atenolol (B y C).
En el caso de nuestro paciente, recibió dosis de 2 mg/kg/día no siendo necesario el aumento, ya que los efectos terapéuticos fueron visibles con la dosis que se estaba utilizando.
Los efectos terapéuticos del atenolol parecen ser similares a los del propanolol, la respuesta en nuestro paciente fue objetivable a los dos meses de iniciado el tratamiento con disminución del tamaño y eritema del hemangioma, y luego de cuatro meses la mejoría fue notoria con cambios beneficiosos en el compromiso del párpado superior, destacamos que el tratamiento con atenolol en nuestro paciente se indicó a la edad de 18 meses debido a que mantenía flujo y actividad de la lesión. El atenolol además se asocia menos frecuentemente con efectos secundarios graves. En un estudio realizado en 2019 por Calderón-Castrat y colaboradores, en donde participaron 46 lactantes con HI tratados con atenolol se obtuvo que el 23,9% de los pacientes mostraron efectos secundarios moderados, siendo el principal efecto secundario notificado una diarrea transitoria leve. Únicamente un paciente presentó alteración moderada del sueño al inicio del tratamiento y no se obtuvieron efectos adversos como hipoglucemia, broncoespasmo, bradicardia o hipotensión3. Destacamos que nuestro paciente no ha presentado hasta el momento ningún efecto adverso. Igualmente son necesarios más ensayos clínicos controlados y aleatorizados para evaluar la eficacia y la seguridad del tratamiento con atenolol en HI10.
En cuanto a la duración del tratamiento aún no está estandarizado hasta cuándo indicar atenolol en el tratamiento de los HI. Un reciente ensayo clínico aleatorizado concluye que en la mayoría de los casos de HI tratados con atenolol se observaron mejoras significativas clínicamente después de los primeros seis meses de tratamiento. El tratamiento óptimo debe cubrir al menos toda la fase proliferativa y debe continuarse individualmente hasta que se logre la mejoría máxima. Para esto, hay que tener en cuenta que el 80% del crecimiento de los HI ocurre durante los primeros tres meses, y que los HI con un componente subcutáneo pueden continuar proliferando hasta por 6 a 12 meses, inclusive los HI segmentados continúan proliferando por más tiempo11. En nuestro paciente tenemos en cuenta que el tratamiento con atenolol no se realizó en los tiempos ideales (dado que se inició a los 18 meses), pero debido a que en el Doppler el HI aún mantenía flujo, se indicó el tratamiento con atenolol en esta etapa, logrando una mejoría de la lesión.
Conclusiones
Presentamos el caso clínico de un paciente con un HI con compromiso de párpado superior derecho tratado exitosamente con atenolol. Si bien el uso de este fármaco para esta patología no está aprobado por la Food and Drug Administration (FDA), existen múltiples ensayos clínicos aleatorizados que concluyen que el atenolol oral es una alternativa eficaz y segura para el tratamiento de los HI complicados. En este caso, ya que nuestro paciente había presentado efectos adversos con propanolol, el atenolol fue una buena opción terapéutica brindándonos un buen resultado clínico y sin efectos adversos hasta el momento.















