Introducción
La psoriasis es una enfermedad dermatológica inmunomediada con base genética que se manifiesta con empujes y remisiones1-4. Su prevalencia en la población global es de 2% a 3%2,5,6. En niños se estima una prevalencia de 0,5%-1%, que incrementa con la edad; suele manifestarse en forma más frecuente en la segunda década de la vida1,2,5,6. La psoriasis es una enfermedad compleja desencadenada por factores ambientales en sujetos genéticamente susceptibles2.
Se describen distintos tipos de psoriasis, con frecuencia diferencial según la edad1. La psoriasis en placa o vulgar es la forma de presentación más frecuente en todas las edades (40%-85%); se expresa en placas eritematosas y descamativas, focales o generalizadas. Otras formas de presentación son la psoriasis en gotas (con mayor frecuencia en adolescentes), psoriasis pustulosa, palmo-plantar, invertida (flexural), artropatía psoriásica, psoriasis del pañal, ungueal y del cuero cabelludo2,7-9.
La psoriasis pustulosa generalizada (PPG) puede presentarse de forma aguda o como una variante subaguda con fenotipo anular. Las tasas de prevalencia reportadas difieren ampliamente según la región, oscilando entre 1,76 y 198 casos por millón de personas10.
Las lesiones características son las pústulas acompañadas de eritema en la piel. La afectación sistémica apoya el diagnóstico, pero no es mandatoria. Se puede manifestar en grado variable con mal estado general, fiebre, dolor a nivel de la piel, astenia, leucocitosis con neutrofilia acompañada de reactantes de fase aguda elevados. Su diagnóstico es clínico. Según el Primer Consenso de Criterios Diagnósticos de PPG de la International Psoriasis Council (IPC) del año 2024, la biopsia de piel no es obligatoria, pero es útil para confirmar el diagnóstico y descartar diferenciales10.
Se postula que en la etiopatogenia de la PPG hay una alteración del sistema inmunitario innato. Las mutaciones del gen que codifica el antagonista del receptor de IL-36 (IL36RN) son la anomalía genética más frecuentemente observada6. El deterioro estructural y funcional de su proteína codificada provoca un aumento de la respuesta inflamatoria innata con liberación masiva de mediadores inflamatorios por los queratinocitos, macrófagos y células dendríticas, resultante de interacciones no reprimidas de los agonistas de la vía de IL36α, β y γ9. Otros genes que se han vinculado a la PPG son CARD14, AP1S3, MPO y SERPINA311,12. La infiltración periódica de neutrófilos en la piel que caracteriza a la PPG y el desarrollo de pústulas estériles puede relacionarse con una expresión fuertemente mejorada de las quimiocinas de neutrófilos CXCL1, CXCL2 y CXCL8 (IL8) que se observa en pacientes con esta afección13.
La PPG requiere de un abordaje terapéutico interdisciplinario e individualizado, planificado en conjunto con el dermatólogo pediatra. Existen pocos estudios del manejo terapéutico dada su baja frecuencia11-14.
El objetivo de esta comunicación es describir el abordaje diagnóstico y terapéutico de una escolar con PPG y compartir las interrogantes respecto a la etiología de la afectación hepática identificada.
Caso clínico
Escolar de 8 años, sexo femenino. Procedente del medio rural de Uruguay. Sin antecedentes personales patológicos. Buen crecimiento y desarrollo, con esquema de inmunizaciones vigente. Ambos padres presentaban antecedente de psoriasis vulgar. Un mes antes de su ingreso hospitalario, consultó por lesiones cutáneas. Se encontraba en apirexia y sin síntomas sistémicos. Se observaron placas descamativas y pruriginosas en la cara, cuello y tronco, que inicialmente se interpretaron como dermatitis atópica sobreinfectada. Se le indicó tratamiento con emolientes y antibióticos orales, sin mejoría clínica.
A los 20 días, reconsultó debido a la extensión de las lesiones. En el examen físico se hallaron placas eritematosas extensas que comprometían cuello, tórax, abdomen, miembros superiores e inferiores, con disposición anular, algunas con costras y pústulas en su interior (Figura 1). Ante la sospecha diagnóstica de PPG, se solicitaron estudios complementarios de laboratorio y se realizó una biopsia de piel. El hemograma no presentó alteraciones significativas. La proteína C reactiva (PCR) fue menor a 0,1 mg/L y la velocidad de eritrosedimentación (VES) estaba elevada (28 mm/hr). El hepatograma era normal.
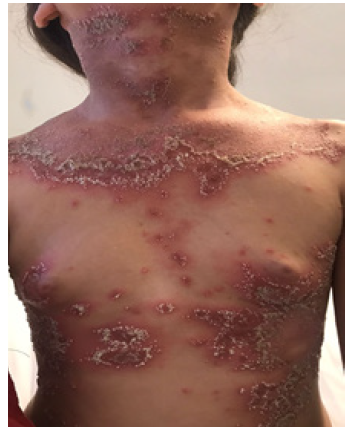
Figura 1 Placas eritematosas extensas que comprome ten cuello, tórax, abdomen con disposición anular con costras en el interior y pústulas en periferia (en oleadas).
Debido a la extensión de las lesiones, se decidió el ingreso a una sala de cuidados moderados, para realizar un abordaje y seguimiento interdisciplinario guiado por pediatra y dermatólogo. La anatomía patológica reveló una dermatitis pustular subcorneal formada por acúmulo de neutrófilos (pústulas espongiformes de Kogoj) y vasos tortuosos en la dermis con exudado inflamatorio perivascular, confirmando la sospecha clínica de PPG (Figura 2).
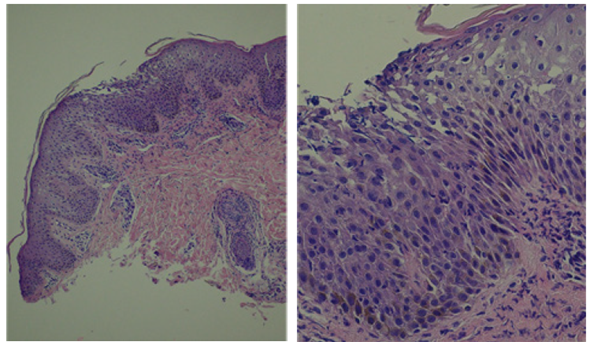
Figura 2 Microscopía óptica de las lesiones. Tinción hematoxilina-eosina, (A) x10; (B) x40. Pústula subcorneal, techo estrato córneo roto, cuerpo mucoso. Leve hiperplasia y espongiosis. Vasos tortuosos en la dermis con infiltrado inflamatorio perivascular.
El tratamiento inicial consistió en terapia tópica con emolientes, antibioticoterapia intravenosa con clindamicina y prednisolona oral, ya que el retinoide (acitretina) no estaba disponible en la institución. A los 9 días de hospitalización, se observó peoría clínica de las lesiones, con exantema eritrodérmico generalizado que se extendía desde el cuello a los miembros inferiores, asociado a fiebre de hasta 39,4 ºC, decaimiento, artralgias y astenia (Figura 3). Estas manifestaciones se interpretaron como la forma aguda de la PPG.
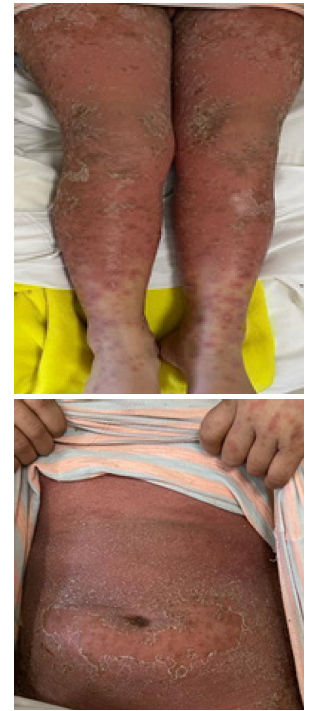
Figura 3 Empeoramiento de las lesiones. Eritrodermia, descamación generalizada extendida desde cuello a miembros inferiores.
Los resultados analíticos mostraron una hemoglobina de 11,7 g/dL, glóbulos blancos 33.500 cel/mm³ (neutrófilos 31.500 cel/mm³) y plaquetas 347 x 10^9/L. PCR y VES estaban normales. Se asoció ceftriaxona intravenosa al plan antibiótico. La medición de anticuerpos antiestreptococo beta hemolítico tipo A (AELO) fue 52 UI/ml (rango normal: 0-200 UI/ml). Los cultivos de piel y hemocultivos no identificaron patógenos. Se realizó una interconsulta con reumatólogo y oftalmólogo, descartando compromiso articular y ocular.
El día 11 de internación, se inició tratamiento con acitretina 25 mg/día (dosis de 0,7 mg/kg/día), lo que condujo a una mejoría progresiva de las lesiones. Sin embargo, a las 72 horas del inicio del retinoide, se evidenciaron elementos de lesión hepática en los exámenes de laboratorio, con aumento de transaminasa glutámico-oxalacética (TGO) 373 U/L (rango 3-38 U/L), transaminasa glutámico-pirúvica (TGP) 756 U/L (rango 2-65 U/L), gamma glutamil transferasa (GGT) 473 U/L (rango 6-28 U/L), sin afectación de los niveles de fosfatasa alcalina (FA) a 391 U/L (rango 20-630 U/L). La coagulación sanguínea, glucemia, albúmina y función renal se mantuvieron normales. Ante la sospecha de hepatitis tóxica por acitretina, se suspendió el retinoide y se continuó con prednisolona a 1 mg/kg/día, con posterior mejoría clínica y normalización progresiva de las enzimas hepáticas, sin elementos de falla hepática.
A los 20 días de hospitalización, se otorgó el alta a domicilio con corticoides sistémicos en descenso (prednisolona a 0,6 mg/kg/día). Un mes después del alta, presentó un nuevo empuje de la enfermedad, sin afectación paraclínica hematológica ni hepática. Se decidió reiniciar acitretina a 25 mg/día y continuar el descenso de prednisolona hasta su suspensión. Completó seis meses de tratamiento con el retinoide, mostrando una franca mejoría de las lesiones, sin alteraciones analíticas.
Discusión
La PPG es una enfermedad dermatológica inflamatoria crónica rara, multisistémica e inmunomediada. Dadas las complicaciones potencialmente graves que caracterizan a su presentación aguda, a diferencia de otras formas de psoriasis, requiere de un abordaje interdisciplinario y hospitalario en la mayoría de los casos3,9-14.
Frente a un primer episodio de PPG es necesario descartar otras dermatosis que comparten características clínicas, laboratoriales e histopatológicas. Al inicio predominaban las placas descamantes, lo que llevó a los clínicos a plantear una patología frecuente como es la dermatitis atópica complicada con impétigo. En la evolución tomaron mayor relevancia las pústulas en zonas no acrales. Dentro de las patologías imitadoras de la PPG la pustulosis exantemática generalizada aguda, toxicodermia grave, no fue planteable en este caso por la ausencia de exposición a fármacos; la dermatosis pustular subcorneal (conocida como enfermedad de Sneddon-Wilkinson) se alejó por la ausencia de pústulas de hipopión y por las regiones comprometidas; el planteo de pénfigo IgA se alejó dada la ausencia de ampollas o lesiones vesiculosas, a su vez, el antecedente familiar de psoriasis en placas de ambos progenitores apoyó la sospecha diagnóstica de PPG8-12. Hasta el 50% de los casos de PPG pueden tener en forma concomitante manifestaciones de psoriasis en placas; sin embargo, si las pústulas están exclusivamente en las placas no se considera PPG10,11. Los síntomas acompañantes pueden estar o no al momento del diagnóstico; incluyendo fiebre, fatiga y dolor, algunos de ellos presentes en este caso10.
Junto a la presentación clínica característica, el estudio histopatológico contribuye a descartar diferenciales10. La anatomía patológica informó la presencia de lesiones pustulosas con leucocitos polimorfonucleares neutrófilos adyacentes al estrato córneo en acúmulos característicos de la PGG2. También puede observarse paraqueratosis, acantosis, hiperqueratosis, disminución del grosor del estrato granuloso, edema y dilatación de los capilares de la dermis11. En este caso, dados los hallazgos anatomopatológicos característicos y la evolución clínica, no se realizó la técnica de inmunofluorescencia directa para descartar o confirmar otros diagnósticos diferenciales como el pénfigo IgA.
En casos donde persisten las dudas diagnósticas se puede solicitar el estudio genético con búsqueda de mutaciones asociadas a la PPG, no siendo mandatorio para el diagnóstico10-13. En el caso presentado el estudio genético no fue solicitado, ya que no existían dudas diagnósticas.
Además de las características clínicas e histopatológicas, tanto el European Consensus Statement (2017)15, las Japanese Guidelines (2018)16 y el Consenso de la International Psoriasis Council (2024)10 establecen criterios de laboratorio que son orientadores a la PPG.
Se describe la elevación de reactantes de fase aguda (aumento de la leucocitosis con neutrofilia y elevación de la VES y PCR) que en ocasiones puede acompañarse del ascenso en los niveles de las enzimas hepáticas, hipoalbuminemia, hipocalcemia e hiperlipidemia, algunos de estos hallazgos presentes en este caso2,3,4,11,14,17.
Los reactantes de fase aguda elevados, junto con la afectación extensa de la barrera cutánea, dificultan la distinción entre las manifestaciones propias de la PPG y la presencia de una infección activa por patógenos bacterianos. En este contexto, se optó por iniciar un tratamiento antibiótico empírico, a pesar de no haber logrado identificar ningún agente infeccioso específico.
En lo referente a la extensión del compromiso de la piel, no existe un área de superficie corporal mínima definida para el diagnóstico de PPG10. Para evaluar la severidad clínica se pueden utilizar dos escalas validadas: la escala GPPGA, por su sigla en inglés (Physician Global Assessment) y la escala GPPASI (Area Severity Index). GPPGA evalúa la severidad del eritema, pústulas y la descamación, utilizando una escala de 5 puntos; la piel sana se corresponde con un puntaje de 0 y la afectación extensa y severa de estos ítems otorga un puntaje de 518. La paciente presentó un puntaje de 4 aplicando la escala GPPGA, lo que implicaba la presencia de eritema rojo intenso, extensa cantidad de pústulas y lagunas con descamación severa y costras extensas.
El abordaje terapéutico constituye un desafío y requiere de una terapia multimodal (farmacológica y no farmacológica) que plantee objetivos terapéuticos acordes a la etapa en la que se encuentre la PPG. En la etapa aguda se deberá priorizar la eliminación rápida de las pústulas y el eritema inflamatorio, con particular énfasis en el abordaje de la sintomatología inflamatoria sistémica. A largo plazo, se intentará evitar recidivas de la enfermedad, con plazos más prolongados de piel sana, y monitorizar de forma continua la calidad de vida del paciente11-13,19-21. La alteración de la imagen corporal en las formas extensas se asocia a repercusiones en la salud mental, con síntomas de ansiedad y depresión, por este motivo es prioritario el seguimiento por psicología, como se realizó en este caso4,11,12,19.
En el año 2021, el Consenso Mundial Delphi de la Academia Europea de Dermatología destacó la importancia del tratamiento con retinoides orales (acitretina) en monoterapia o en combinación con corticoides orales (prednisona) en pacientes con enfermedad grave como tratamiento de primera línea(12, 14, 19-22). En algunos casos, es necesario utilizar fármacos con mayor poder antiinflamatorio sistémico como inmunosupresores (ciclosporina, metotrexato) o anticuerpos monoclonales (infliximab) y como segunda línea terapéutica biológicos anti-TNF alfa (etanercept o adalimumab)3,12,14,19-25. En los últimos años se han comunicado como opciones terapéuticas la efectividad de otros anticuerpos monoclonales como anakinra (antagonistas de receptor IL 1) y spesolimab (antagonistas del receptor IL 36)19,20-28.
El tratamiento inicial en este caso se realizó con prednisona a 1 mg/kg; si bien no es el tratamiento de elección para cualquier psoriasis y debería evitarse, debido a la extensión de las lesiones, su severidad y la imposibilidad de contar con retinoides en el primer momento se justifica su indicación, asociando a los 11 días de internación la terapia con retinoide (acitretina 25 mg/día). Al tercer día de iniciado el retinoide, se observó la elevación de las enzimas hepáticas. Son conocidos como efectos adversos de la acitretina la alteración de la función hepática en diversos grados. Suelen observarse hasta en un tercio de los pacientes la elevación de las transaminasas y la fosfatasa alcalina. Estas alteraciones analíticas son generalmente transitorias y reversibles luego de la reducción o suspensión del fármaco. La hepatotoxicidad está vinculada a dosis altas por un tiempo prolongado. Se puede sospechar una hepatitis tóxica aguda vinculada a acitretina en casos con valores altos de transaminasas, sobre todo de TGP. Se trata de un efecto adverso raro y grave17,22. Se discutió si la afectación hepática se debió a un efecto adverso de los retinoides o constituía una presentación grave de la PPG. El hecho de que se presentó al tercer día del inicio del fármaco, a dosis bajas, acompañado de síntomas sistémicos, apoyó el planteo de que se tratara de un efecto del empuje de la PPG que se presentó con inflamación hepática, más que a un efecto adverso de la acitretina. De todas maneras, se suspendió el fármaco de manera transitoria. La paciente presentó una rápida mejoría clínica y paraclínica, por lo que no justificó la realización de una biopsia hepática para determinar la etiología de esta alteración. Posteriormente se reinstaló el tratamiento con el retinoide en el siguiente empuje, sin objetivar afectación hepática, lo que alejó el planteo de que esta alteración se debiera a la acitretina18,24.
La evolución de la enfermedad es heterogénea, presentando brotes recurrentes o intermitentes. Aunque existen escasos estudios sobre las recurrencias, se estima que aproximadamente el 55,3% de los pacientes experimentan al menos un brote o empuje anual, 31,6% dos brotes y 13,2% más de dos. En general, los brotes de PPG tienden a resolverse con síntomas residuales como descamación, eritema y/o prurito29.
Conclusiones
La PPG es una forma grave e infrecuente de psoriasis de presentación sistémica en la infancia. Este caso se presentó con afectación cutánea moderada a severa y afectación sistémica con compromiso hepático transitorio. La duda de si la afectación hepática se debía a un efecto adverso grave al retinoide obligó a los clínicos a realizar cambios terapéuticos. El conocimiento por parte de pediatras y dermatólogos de esta enfermedad rara es clave para realizar un diagnóstico precoz e iniciar un tratamiento oportuno.















