Introducción
La fiebre chikungunya es una infección viral reemergente transmitida por picadura de mosquitos infectados (Aedes aegypti y A. albopictus). Es causada por un arbovirus (género Alfavirus, familia Togaviridae, especie Chikungunya), clínicamente se caracteriza por inicio brusco sin ningún pródromo, de fiebre elevada con escalofríos (la fiebre puede ser bifásica con intervalos de 2 a 6 días), dolores articulares severos y rash (erupción máculo-papular) con marcados síntomas generales1.
El primer aislamiento del virus chikunguya (CHIKV) fue realizado durante una epidemia en Tanzania (1952-1953)1, inicialmente causó pequeños brotes en regiones restringidas dentro de África y Asia. Esta situación cambió drásticamente a finales de 2004 cuando se inició el primer gran brote de CHIKV. Desde entonces, el virus se ha extendido globalmente con millones de personas infectadas. Actualmente, el CHIKV es epidémico en gran parte de África, Asia y regiones tropicales de las Américas. Ha sido identificado en 80 países, en cinco continentes y ha causado más de 6 millones de casos confirmados2.
Hay cuatro linajes, genotipos o subtipos de CHIKV, el de África Occidental (WA), el linaje Asiático, el linaje del África Este Sur Central (ECSA) y el linaje Océano Índico (IOL). Este último emergió del linaje ECSA en 20043. El linaje Asiático y ECSA son fundamentalmente los responsables de los brotes actuales en las Américas3. Los análisis de secuencia realizados han revelado que el virus circulante en el Caribe está filogenéticamente relacionado con cepas del genotipo Asiático que circulan en Indonesia, China y Filipinas4-6.
El primer caso de CHIKV en Venezuela se documentó el 5 de junio de 2014, desde entonces se ha presentado en forma endémica y se han descrito casos atípicos, severos y letales de la infección6,7.
Las manifestaciones clínicas asociadas con infección por CHIKV son muy variables y pueden ser de diferente severidad que las reportadas previamente, particularmente dentro de las poblaciones susceptibles. Estudios clínicos reportan que los síntomas de los pacientes con CHIKV Asiático-Caribe pueden ser quizás diferentes que aquellos infectados con la cepa ECSA, difieren de su capacidad de inducir respuesta proinflamatoria Th1 y de células NK8.
Recientes estudios informan los efectos de los fenotiacínicos en el tratamiento para mitigar la severidad de la infección, así como el descubrimiento del potente efecto para neutralizar el virus (SOFOSBUVIR) por un antiviral usado en el tratamiento de la hepatitis C3,9. Justifican los esfuerzos por dar a conocer e identificar formas graves, atípicas de la enfermedad.
Entre las manifestaciones cutáneas en los pacientes con fiebre chikungunya, que han sido poco documentadas, se ha reportado una gran variedad de lesiones en piel y en membranas mucosas, incluidas algunas que no se han descrito en otros exantemas virales.
Se incluyen entre las manifestaciones atípicas de la infección y son relativamente frecuentes, han sido reportadas durante la primera semana en 77% de los pacientes con la enfermedad en estudios provenientes de la India10, de esa variedad de manifestaciones cutáneas se han descrito lesiones en fase aguda, incluidas algunas únicas, asociadas a casos fatales (signo de chik)5 y otras que pueden aparecer semanas después de que los otros signos hayan desaparecido. La aparición secuencial es poco conocida.
Las manifestaciones cutáneas en niños difieren de las de adultos. Se presenta en este informe un escolar de 6 años de edad con infección por el virus chikungunya, que en su evolución presentó lesiones vesículo-ampollosas y máculo-purpúricas extensas y graves, se discuten diagnósticos diferenciales y otras lesiones mucocutáneas que secuencialmente se observaron durante el curso de la infección. La enfermedad fue confirmada por serología, anticuerpos IgM e IgG, positiva contra virus chikungunya.
Presentación del caso clínico
Escolar de 6 años de edad, quien inició cuadro clínico 6 días antes de su ingreso al hospital con fiebre elevada de 39 ºC - 40 ºC, acompañado de rash generalizado máculo-papular, eritematoso, que apareció en las primeras 24 horas del inicio de la fiebre y artralgias severas que dificultaban la marcha, vómitos, hiporexia, edema en manos y pies de tres días de evolución.
Niega antecedentes de alergia, atopia o asma.
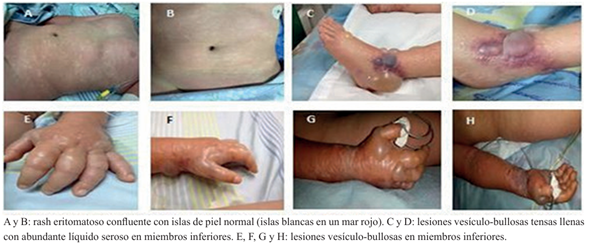
Al examen físico de ingreso se encontró taquicárdico (FC: 100/pm), febril, frecuencia respiratoria de 20/pm y tensión arterial normal (99/68 mmHg), regulares condiciones generales y como hallazgos positivos hipoactivo, en manos y pies edema difuso, doloroso a la palpación que deja fóvea. Vesículas de 0,5 cm aproximadamente en cara dorsal de ambas manos, un rash intenso eritematoso, generalizado en tórax, abdomen, miembros superiores e inferiores, respeta cara, pruriginoso, con islas de piel normal, similar al observado en la infección por virus dengue durante la etapa de convalecencia, denominado “islas blancas en un mar rojo”. (Figura 1).
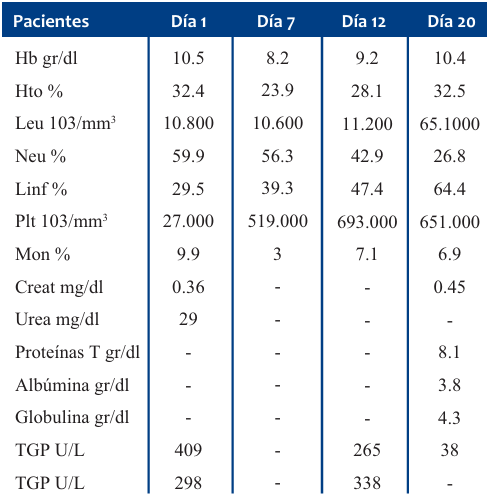
Resultados de laboratorio revelaron marcada leucocitosis de 16.300/ mm3 con 87% de neutrófilos y recuento de plaquetas 261.000/mm3, proteína C reactiva (PCR) de 72 mg/L y velocidad de sedimentación globular (VSG) 40 mm/L hora, procalcitonina positiva. El resumen de exámenes de laboratorio se presenta en la (Tabla 1). El niño fue ingresado con la presunción diagnóstica de probable fiebre chikungunya.
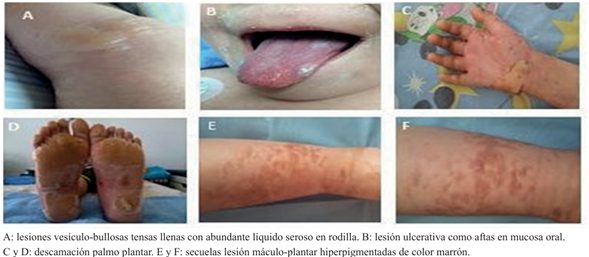
En el segundo día de evolución intrahospitalaria (séptimo día de evolución de la enfermedad): persiste febril, con alzas térmicas de 40 °C, se evidenciaron lesiones ampollosas, que contenían un líquido claro, a nivel de articulación de ambas rodillas, además se observaron lesiones vesículo-bullosas grandes llenas con abundante líquido seroso en el dorso de ambas manos (Figura 2), lesiones purpúricas y vesículo-bullosas en cara externa e interna de tercio inferior de pierna derecha (maléolo externo derecho). Exámenes paraclínicos reportaron glucosa, sodio y potasio sin alteraciones. No ameritó correcciones hidroelectrolíticas. Transaminasas elevadas: TGO: 359 U/l, TGP 94 U/l. Ecografía abdominal: hígado ecogenicidad levemente aumentada, hepatomegalia a 11,8 cm del reborde costal derecho. Valoración por cardiología: corazón estructuralmente normal, derrame pericárdico trivial.
El día 3 de admisión: el niño persistió febril con descamación superficial perioral y lesiones ulcerativas, como aftas en lengua. Descamación en pabellones auriculares, flictenas en articulación tibio-tarsiana derecha con fondo violáceo.
Se investigó coinfección incluyendo malaria, hepatitis, infección del tracto urinario, tuberculosis y otros patógenos virales y bacterianos: virus de Epstein-Barr, citomegalovirus, Ehrlichia, Leptospira y Rickettsia, salmonellas fueron excluidos por serología.
Serología en laboratorio de salud pública del Estado Mérida: prueba de Elisa negativo para dengue. IgM chikungunya: positivo.
El día 4 de admisión: por las características de las lesiones en piel se plantea la posibilidad de bulas penfigoides. Se indica inmunoglobulina 400 mg/kg/día por 5 días y metilprednisolona 30 mg/kg/peso dosis única, el siguiente día se inicia dexametasona 2 mg/kg/d. Se desbridan las ampollas y se cubren con vendaje. Urocultivo y hemocultivo negativos, Rx de tórax normal. Valoración oftalmológica normal.
El día 10 de admisión: se omite dexametasona. Valoración hematológica: anemia, leucocitosis con neutrofilia. Serie plaquetaria: aumentada (trombocitosis), anisotrombia, macroplaquetas. Se observa descamación palmo-plantar acentuada. Se practica biopsia de piel de lesión en pierna derecha que reporta a nivel de la dermis subyacente formación quística tapizada por epitelio plano estratificado, queratinizado, con luz ocupada por abundante queratina laminillar. En estroma circundante se observa discreto infiltrado inflamatorio mononuclear focal. Entre los días 10-23 intrahospitalarios evoluciona hemodinamente estable, el día 15 de evolución las lesiones en piel cicatrizan totalmente dejando lesiones pápulo-vesicular de diferente tamaño, hiperpigmentadas de color marrón en miembros inferiores, los signos de inflamación activa habían desaparecido. El día 23 de estancia hospitalaria se egresa por mejoría.
Discusión
El paciente presentó fiebre, exantema, asociado con artralgia. Nosotros teníamos razones, además de la fiebre, para sospechar chikungunya en el caso en estudio. Estas incluyen presencia de un rash característico el primer día de inicio del cuadro, con brotes cambiantes secuenciales, evidencia de artralgias, leucocitosis con neutrofilia. Sin embargo, estas características no son específicas de chikungunya, pueden observarse con varios otros virus, infecciones bacterianas, reacciones cutáneas adversas y enfermedades bullosas autoinmunes11.
Las infecciones por virus chikungunya y dengue son probablemente las más difíciles de diferenciar. Estos virus se transmiten por las mismas especies de mosquitos, las zonas endémicas son las mismas y los síntomas clínicos son similares. Además, ha sido reportada la infección simultánea de virus chikungunya con dengue10,12. En los estudios publicados comparando las manifestaciones clínicas de virus chikungunya y dengue, se ha observado que el inicio de la fiebre es más abrupto, las erupciones cutáneas máculo-papulares, la inyección conjuntival y las artralgias fueron significativamente más frecuentes en fiebre chikungunya que en dengue, en quienes la poliserositis y hemorragia gastrointestinal se presentaron solo en pacientes con dengue, la prueba del torniquete no ayudó a diferenciar chikungunya de dengue13. Las manifestaciones en piel, observadas en nuestro paciente al momento de su ingreso, son similares a las descritas para el dengue clásico, que se caracterizan por prurito y una erupción máculo-papular con áreas pequeñas de piel sana (“islas blancas en un mar rojo”), pero en dengue estas lesiones han sido observadas 6 días después del inicio de la fiebre y se asocian al período de recuperación14. Kumar A y colaboradores, en su estudio durante la primera epidemia de chikungunya en el Caribe15, estimaron que el riesgo relativo de presentar chikungunya en niños febriles con rash fue de 1,8 (IC95% 1,0 - 3,1) y la diferencia en riesgo de aquellos que tenían y no habían tenido rahs fue significativa (p=0,0240), cuando asoció fiebre, artralgia y rahs fue observado en 32 (46,4%) positivos y 3 (6,5%) negativos (RR 7,1; IC 2,3 - 21,9).
La etiología en este paciente fue confirmada por serología positiva para chikungunya y negativa para dengue.
Las ulceraciones en piel y úlceras parecidas a aftas en mucosa oral (lengua, paladar) se han observado como manifestaciones muco-cutáneas en fiebre chikungunya. Las observadas en la lengua de nuestro paciente coinciden con las informadas en reportes previos16, son muy raras y similares a las observadas en eritema multiforme y linfedema.
Por otra parte, brotes recurrentes de erupción máculo-papular, como lo observado en este paciente, han sido informados aun después de varios días de evolución de la enfermedad, probablemente como resultado de brotes sucesivos de viremia17. Inamadar AC18 reportó que uno de sus pacientes con artritis persistente, sin fiebre, desarrolló brotes recurrentes de erupción máculo-papular durante un período de ocho semanas. Valamparampil JJ19 reveló que por lo menos una manifestación en piel estuvo presente en todos sus pacientes y dos o más manifestaciones en 44% de los niños.
Así mismo, la descamación palmo plantar marcada, similar a la observada en este paciente, es una manifestación cutánea extremadamente rara en fiebre chikungunya20, debe distinguirse de la observada en enfermedad de Kawasaki21. Pero la lesión cutánea fundamental grave, de manejo complejo y clínicamente un verdadero reto diagnóstico por lo difícil de asociar con fiebre chikungunya, son las lesiones vesículo-ampollosas con máculas purpúricas en miembros superiores e inferiores.
Las lesiones vesícula-ampollosas han sido observadas principalmente en lactantes menores y son raras en adultos22,23.
Las manifestaciones cutáneas en chikungunya han sido vistas en 40% a 75% de los pacientes. Ellas pueden tener variadas presentaciones, tales como máculo-papular, rash, lesiones vesículo-bullosas, cambios pigmentarios, papular, urticarial, vasculítico, acrocianótico, purpúrico o lesiones parecidas a síndrome de Stevens-Johnson, necrolisis epidérmica tóxica, estas últimas son raras en niños mayores24,25. En la literatura asiática se han reportado 96 casos. Los 21 pacientes informados recientemente por Garg T y colaboradores (Nueva Delhi, India, 2018)11 son niños entre 1-36 meses. Presentaron múltiples vesículas o bulas, acompañadas por áreas de púrpura, necrosis y descamación parecidas a las observadas en síndrome de Stevens-Johnson, necrolisis epidérmica tóxica. En el hemisferio occidental, en niños, se ha informados en Cúcuta, Colombia, neonatos y lactantes menores con lesiones vesículo-bullosas26, y en Brasil, en niños con infección severa por virus chikungunya, encontraron exantema vesículo-bulloso en 8/14 (57,1%), fundamentalmente en niños menores de 6 meses (6/8 pacientes) y dos en niños mayores: uno de 2 años y otro de 13 años27.
Se describen comúnmente en extremidades, más frecuentemente en extremidades inferiores, incluidos glúteos y muslos. Estas lesiones se desarrollan 2-3 días después de la fiebre y desaparecen entre los 6 y 10 días22. En este caso se iniciaron a los 6 días y se resolvieron 15 días después, quedó con lesiones máculo-papulares hiperpigmentadas como secuelas que desaparecieron a los seis meses.
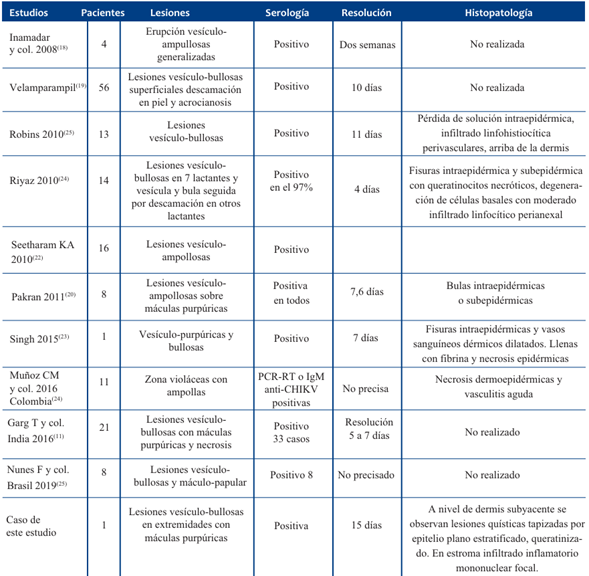
La incidencia de lesiones vesículo-ampollosas en fiebre chikungunya no se conoce exactamente. En la (Tabla 2) se presenta un resumen de los casos encontrados en la literatura.
Tabla 2 Series de casos previamente reportados en niños con fiebre chikungunya presentando lesiones vesículo-bullosas que simulan síndrome de Steven-Johnson y necrolisis epidérmica tóxica.
El amplio rango de lesiones cutáneas inducidas por CHIKV parecen reflejar un espectro de cambios vasculares, desde vasodilatación a daño severo del endotelio vascular, el cual puede ser debido a una combinación del efecto citopático directo de la replicación viral en el endotelio capilar que causaría un daño vascular severo o por una reacción inmune tipo III18.
El cuadro clínico clásico de fiebre chikungunya no incluye la observación de lesiones vesículo-bullosas extensas con máculas purpúricas en miembros superiores e inferiores en niños de este grupo etario. En consecuencia, para nosotros esta rara presentación de enfermedad vesículo-bullosa nos indujo a considerar como diagnóstico diferencial una amplia variedad de cuadros patogénicamente no relacionados, entre ellos: síndrome de Stevens-Jonhson, necrolisis epidérmica tóxica, eritema multiforme y enfermedades bullosas autoinmunes que pueden ser desencadenadas por infecciones virales o fármacos, como el penfigus inducido por drogas. Este paciente no tenía antecedentes de ingestión de medicamentos, así mismo, consideramos la posibilidad de bulas penfigoides que pueden acompañarse de lesiones orales secundaria a infecciones virales28 y asociamos el tratamiento con gammaglobulina y esteroides sugerido en esta entidad clínica.
Evidentemente, similar que en la sepsis, estos cuadros se tratan de una respuesta inflamatoria no controlada del huésped a la infección causante de una disfunción orgánica que compromete la vida y, como Kawasaki, se sugiere el uso de gammaglobulina y esteroides. Nosotros pensamos que esta terapia influyó en la evolución satisfactoria de este paciente.
En adultos un cuadro grave de infección por virus chikungunya, con necrosis y lesiones purpúricas en nariz y vesículo-bullosas en extremidades, se asoció a alta mortalidad29,30.
Conclusiones
Recientes informes apoyan la conclusión de que los síntomas en pacientes con infección por diferentes genotipos de este virus o sus mutaciones pueden variar en frecuencia y gravedad30. Desafortunadamente, en nuestro caso no se realizó estudio del genoma. Geográficamente, Mérida está más cerca y tiene un intercambio socioeconómico muy alto con la ciudad de Cúcuta, donde para la misma fecha de presentación de este caso clínico (diciembre 2014 y enero 2015) se reportaron lesiones vesículo-bullosas en neonatos y lactantes menores por la cepa Asian-WH24, diferente del hallazgo de Torres J y colaboradores en Caracas, Venezuela, de casos graves producidos por el genotipo Asiático que no mostró evidencias de mutación5.
Nosotros hipotetizamos que probablemente la cepa descrita en Cúcuta, Colombia, pudiera ser similar por su cercanía e intercambio socioeconómico permanente a la cepa que circula en Mérida, Venezuela.
El clínico debe familiarizarse con estos casos atípicos y severos.
Se necesita una mejor caracterización de la historia natural de la infección por virus chikungunya. El amplio espectro de la enfermedad requiere una investigación y documentación detallada de las diferentes manifestaciones clínicas que mejorarían nuestro conocimiento.