Introducción
La infección por SARS-CoV-2 puede afectar a las embarazadas de forma similar a la afectación en la población general1-3. El embarazo se asocia con enfermedad grave y mayor riesgo de resultados adversos obstétricos-neonatales4-6. Algunos estudios evidenciaron un mayor riesgo de complicaciones durante el embarazo, incluyendo parto prematuro, eclampsia o necesidad de practicar una cesárea3,6. Una revisión sistemática publicada en 2021, que incluyó más de 400.000 embarazadas, reportó que las mujeres embarazadas con infección por SARS-CoV-2 tienen un mayor riesgo de parto prematuro y bajo peso al nacer (BPN)7. Un estudio nacional realizado entre marzo de 2020 y junio de 2021, sobre los resultados obstétricos-neonatales en madres COVID-19 positivas al momento del nacimiento, mostró una prevalencia de prematurez de 10% y de BPN de 7%8.
La vacunación durante el embarazo es común para prevenir la morbilidad materna e infantil por otras enfermedades infecciosas. Se recomienda específicamente la vacunación para prevenir tanto la gripe como la tos ferina. Si bien algunas de las plataformas de las vacunas contra la COVID-19 disponibles son distintas de las vacunas contra la influenza y la dpaT que se usan actualmente durante el embarazo, como plataforma inmunogénica pero no infecciosa ni integradora, las vacunas de ARNm tienen beneficios potenciales sobre las vacunas de virus vivos atenuados, las vacunas inactivadas o de subunidades y las vacunas basadas en ADN9. En un principio, no se incluyeron mujeres embarazadas ni en lactancia en los estudios sobre vacunas contra COVID-19. Investigaciones posteriores demostraron que las vacunas de ARNm eran muy eficaces para prevenir la COVID-19 grave en el embarazo. Un estudio de cohorte prospectivo encontró que las mujeres embarazadas y en lactancia vacunadas producían respuestas inmunes comparables a las de los controles de no embarazadas y generaban títulos de anticuerpos más altos que los observados después de la infección por SARS-CoV-2 durante el embarazo10. Además, los anticuerpos generados por la vacuna están presentes en la sangre del cordón umbilical y en la leche materna después de la vacunación materna11. Las vacunas existentes contra el SARS-CoV-2 incluyen vacunas inactivadas, vivas atenuadas, de vectores virales, de subunidades proteicas, de ARN, de ADN y de partículas similares a virus (VLP).
En Uruguay se comenzó con la vacunación contra COVID-19 el 1 de marzo de 2021 con la plataforma CoronaVac®. El 28 de abril de 2021, el Ministerio de Salud Pública (MSP) comunica el inicio de vacunación en embarazadas, principalmente en aquellas que presenten riesgo alto de exposición o de infección severa. Si bien las embarazadas no fueron una población especialmente incluida en los estudios clínicos de fase III de las vacunas contra COVID-19, la evidencia hasta ese momento no planteaba contraindicaciones para vacunarse, pudiendo hacerlo con CoronaVac® o Pfizer®(12. Por su parte, la Sociedad Ginecotológica del Uruguay apoyó esta recomendación13.
Si bien la Academia Americana de Pediatría (AAP) y los Centros para el Control y la Prevención de Enfermedades (CDC, por sus siglas en inglés) recomiendan las vacunas contra COVID-19 para todas las personas mayores de 6 meses de edad14, en nuestro país se mantiene la recomendación de vacunación a partir de los 5 años15. Es por esto que la vacunación en el embarazo adquiere mayor relevancia, ya que brinda protección a las gestantes y puede proporcionar un beneficio adicional de protección a los lactantes que no son elegibles para la vacunación.
Objetivos
1 - Estimar la tasa de vacunación COVID y la incidencia de infección por SARS-CoV-2 en las embarazadas de un prestador de salud privado del interior del país.
2 - Describir los resultados obstétricos-neonatales y la incidencia de infección por SARS-CoV-2 y hospitalización en los primeros 6 meses de vida.
3 - Identificar diferencias entre las gestantes bien vacunadas (2 o más dosis) y no o mal vacunadas (0 - 1 dosis) en la infección materna, los resultados obstétricos-neonatales y la hospitalización en los primeros 6 meses de vida.
Metodología
Se realizó un estudio observacional, descriptivo, retrospectivo del seguimiento longitudinal de la cohorte de binomios constituidos por las gestantes que finalizaron su embarazo entre el 1/1/2022 y el 31/12/2022 y sus bebés hasta los 6 meses de vida. Se incluyeron todas las gestantes usuarias de un prestador de salud privado del interior del país que culminaron su embarazo con un recién nacido vivo (RNV) en el período de estudio. Se excluyeron los binomios que cambiaron de institución en los primeros 6 meses de vida del lactante. Las fuentes de información fueron los registros administrativos sistemáticos solicitados al departamento de informática del prestador de salud en forma anonimizada. Se recabaron datos del Sistema Informático Perinatal (SIP), Sistema Informático de Vacunas (SIV) y de la historia clínica electrónica. Las variables estudiadas fueron: 1. De la madre y el embarazo: edad al momento del primer control obstétrico, número de controles obstétricos, vacunación COVID (número de dosis previas o durante el embarazo), infección por SARS-CoV-2 durante el embarazo. 2. Del nacimiento: vía de finalización del embarazo, edad gestacional, peso al nacer, test de Apgar. 3. De los primeros 6 meses de vida del lactante: infección por SARS-CoV-2, hospitalización (edad y diagnóstico al egreso).
El análisis estadístico se realizó mediante el software EpiInfo versión 7.2. Se analizó mediante estadística descriptiva utilizando para las variables categóricas distribución de frecuencia absoluta y relativa porcentual; para las variables continuas, medidas de tendencia central, media y mediana, y dispersión, DE. Se calculó la cobertura vacunal, la tasa de incidencia de infección por SARS-CoV-2 y de hospitalización. Se determinó si existían diferencias entre las gestantes bien vacunadas (2 o más dosis en el embarazo) y mal vacunadas (0 o 1 dosis en el embarazo) en los resultados obstétricos, del recién nacido y la infección u hospitalización en los primeros 6 meses de vida utilizando chi cuadrado o test exacto de Fisher, según correspondiera, considerando una diferencia estadísticamente significativa un valor de p <0,05.
Resultados
Entre el 1 de enero de 2022 y el 31 de diciembre de 2022, en CRAMI IAMPP, prestador integral del Departamento de Canelones, finalizaron su embarazo 311 gestantes con 314 RNV (tres embarazos gemelares). Se excluyeron 13 binomios por cambio de institución en los primeros 6 meses de vida, por lo que participaron del estudio 298 gestantes y 301 recién nacidos.
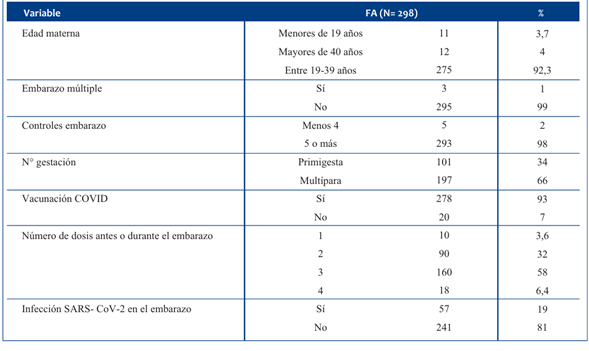
La edad materna al momento del primer control obstétrico tuvo una media de 28,6 años, con un DE de 5,9 años y un rango entre 15 y 43 años; 11 embarazadas adolescentes (3,7%). El 66% de las embarazadas era multípara. El embarazo fue bien controlado (cinco o más controles) en el 98% de los casos, con un promedio de 11 controles (DE 2,3).
La vacunación COVID en el embarazo se constató en 278 gestantes (92%). Se diagnosticó infección por SARS-CoV-2 (PCR o test antigénico) en 57 embarazadas, de las cuales 11 fue en los 14 días previos al parto. La tasa de infección por SARS-CoV-2 en el embarazo fue de 19 cada 100 embarazos. En el puerperio se diagnosticaron 19 casos de infección por SARS-CoV-2. En la (Tabla 1) se muestran las características del embarazo.
Resultados obstétricos
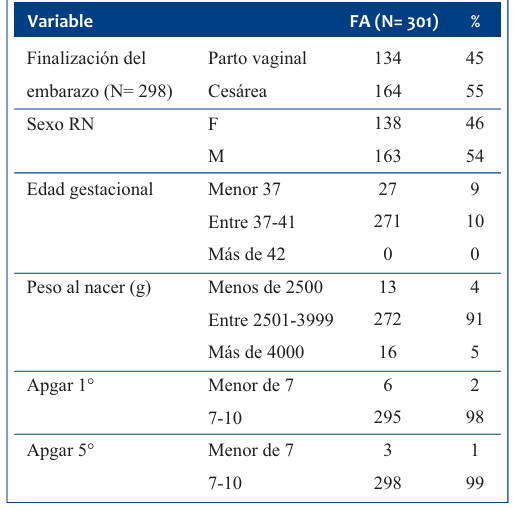
La finalización del embarazo se realizó por cesárea en el 55% de los casos (164/298).
De los 301 RNV, 138 fueron niñas (46%). La edad gestacional al nacer fue en promedio de 38 semanas (DE 1,7 semanas). El 9% de los recién nacidos tuvo menos de 37 semanas de edad gestacional al nacer (promedio 34 semanas, rango 29-36 semanas). En las madres que tuvieron infección por SARS-CoV-2 en el embarazo, la tasa de prematurez ascendió a 12% (p 0,28). El peso al nacer promedio fue de 3265 g, con un DE de 524, y un rango de 1090-5050 g. El 4% de los recién nacidos tuvo un peso inferior a 2500 g, en el caso de madres con COVID en el embarazo fue el 6% (p 0,24). En la (Tabla 2) se resumen los resultados obstétricos-neonatales.
La infección por SARS-CoV-2 en el embarazo no se relacionó con prematurez o BPN. En la (Tabla 3) se muestra la relación entre la infección por SARS-CoV-2 en el embarazo y los resultados neonatales.
Tabla 3 Relación entre infección por SARS-CoV-2 en el embarazo y resultados neonatales. CRAMI IAMPP, 2022.
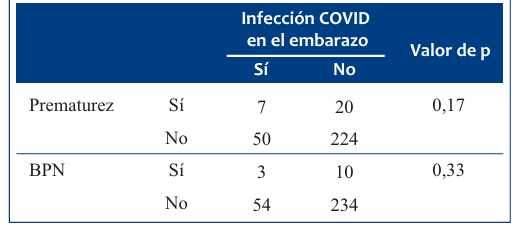
Se diagnosticó infección por SARS-CoV-2 por reacción en cadena de polimerasa (PCR) o test antigénico en cuatro lactantes menores de 6 meses. La tasa de incidencia de infección por SARS-CoV-2 fue de 1,3 por cada 100 lactantes menores de 6 meses. No se constató ninguna infección en el período neonatal. Se estudiaron el 100% de los recién nacidos hijos de madres que cursaron infección por SARS-CoV-2 en los últimos 14 días previos al parto.
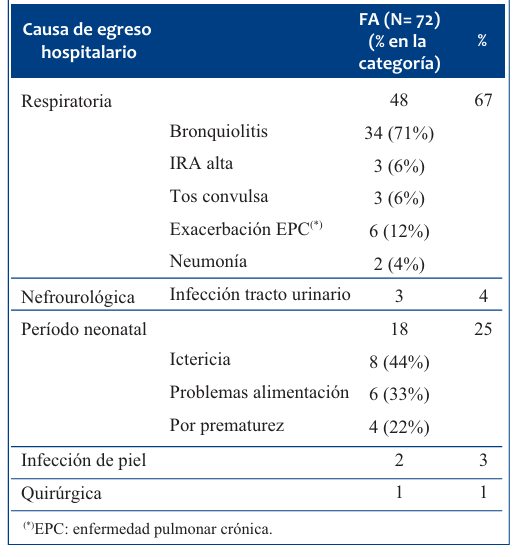
Se registraron 72 ingresos hospitalarios en 50 lactantes menores de 6 meses (15 lactantes con más de un ingreso). La tasa de hospitalización global en menores de 6 meses fue de 24%. La principal causa de egreso hospitalario fue la respiratoria en 67%; ningún ingreso por SARS-CoV- 2. La bronquiolitis fue la patología más frecuente (71% de los ingresos por causa respiratoria), siendo el virus sincicial respiratorio el agente causal más frecuente aislado (24/34). En la (Tabla 4) se muestran los egresos hospitalarios en los primeros 6 meses de vida.
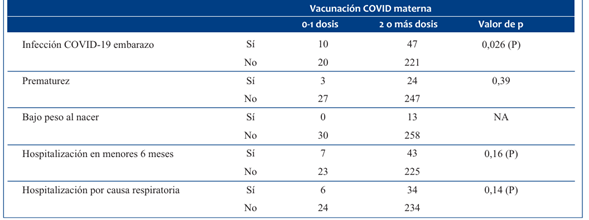
La vacunación COVID en el embarazo, considerada adecuada (dos o más dosis), mostró ser protectora para la infección por SARS-CoV-2 en el embarazo con significancia estadística (p 0,026) y para la hospitalización por todas las causas y por causa respiratoria en menores de 6 meses, pero en este caso con p >0,05. La infección por el virus SARS-CoV 2 en el embarazo no se asoció a prematurez o BPN. En la (Tabla 5) se muestra la relación entre la vacunación COVID en el embarazo (adecuada o no) y la infección por SARS-CoV-2 en el embarazo, los resultados obstétricos-neonatales y la hospitalización en menores de 6 meses.
Discusión
Los efectos de la vacunación en el embarazo en términos de efectividad y seguridad a nivel del feto, de los resultados obstétricos y neonatales, y los beneficios en los primeros meses de vida de los lactantes son siempre motivo de investigación, máxime ante el desarrollo de vacunas contra una enfermedad nueva, con plataformas innovadoras y en plazos extraordinarios.
En este estudio se investigó el impacto de la vacunación contra el COVID-19 en el embarazo, con las vacunas disponibles en nuestro país, sobre la infección materna, los resultados obstétricos y neonatales y sobre la infección y hospitalización en los primeros 6 meses de vida.
Lo primero a destacar es la alta cobertura vacunal de las embarazadas. El 93% presentaba al menos una dosis, y el 90% tenía dos o más dosis al momento del parto. Según datos del MSP, a agosto de 2023, el 81% de la población uruguaya tenía al menos dos dosis de vacunación COVID de cualquiera de las plataformas disponibles16. No existen datos públicos sobre la cobertura vacunal en embarazadas.
Las tasas de COVID-19 en el embarazo son variables en los diferentes estudios con prevalencias que oscilan entre 9% y 18%1,2,17 dependiendo de la región, el momento de la pandemia, la variante de virus circulante, la prueba diagnóstica, la cobertura de vacunación, etc. En nuestro trabajo, la tasa de infección por SARS-CoV-2 en el embarazo fue de 19%. La vacunación COVID en el embarazo se asoció en forma positiva (protectora) con la infección materna, siendo la única variable que mostró diferencias estadísticamente significativas entre las embarazadas vacunadas y no vacunadas.
La transmisión intrauterina del SARS-CoV-2 está respaldada por informes de casos que describieron el virus en recién nacidos, líquido amniótico e IgM placentaria o sangre del cordón umbilical18, aunque investigaciones posteriores determinaron que la transmisión vertical del SARS-CoV-2 es muy poco común19. En nuestro estudio, la incidencia de infección por SARS-CoV-2 en el embarazo fue de 19% y no se constató ningún caso de transmisión vertical, aun habiendo estudiado con PCR a todos los recién nacidos hijos de madres que cursaron la infección en los 14 días previos al parto.
La transferencia transplacentaria de anticuerpos de una madre embarazada previamente infectada por SARS-CoV-2 a su feto se ha demostrado repetidamente. Los anticuerpos anti-SARS-CoV-2, proteína Spike (anti-S) e IgG del dominio de unión al receptor (anti-RBD), se han detectado en la sangre del cordón umbilical en 87%-90% de los recién nacidos de una madre previamente infectada con serología positiva en el momento del parto20. No obstante, el efecto protector de la vacuna parece ser aún mayor que el producido por la infección natural10. El alto porcentaje de vacunación en nuestro estudio podría contribuir a explicar la ausencia de transmisión vertical de la infección.
Existe evidencia contundente sobre el riesgo de la infección por SARS- CoV-2 en el embarazo. Desde un mayor riesgo de enfermedad grave en la embarazada hasta un mayor riesgo de parto prematuro, muerte fetal, preeclampsia y restricción del crecimiento intrauterino (RCIU)3,6,7,21. En nuestro estudio, las tasas de prematurez y de BPN fueron levemente superiores en los hijos de madres con infección por SARS-CoV-2, pero no se encontró asociación de estos resultados con la infección materna en el embarazo (p<0,05). Ambas tasas son similares a las reportadas por Sobrero y colaboradores en un estudio realizado en las dos maternidades más grandes del país8.
El efecto de la vacunación COVID-19 en el embarazo en las hospitalizaciones por SARS-CoV-2 en los menores de 6 meses ha sido evidenciado en diversas investigaciones. En un estudio reciente de casos y controles que incluyó más de 1000 lactantes menores de 6 meses hospitalizados, se evidenció que la vacunación materna con dos dosis de la vacuna de ARNm contra COVID-19 durante el embarazo reducía el riesgo de hospitalización por COVID-19 en 61%, lo que sugiere que la vacunación contra la COVID-19 durante el embarazo podría ayudar a proteger a los lactantes22. La efectividad de la vacunación materna contra la hospitalización asociada a COVID-19 entre lactantes menores de 6 meses fue de 52% (IC95% 33-65)22. En nuestro estudio, si bien la vacunación COVID en el embarazo mostró un efecto protector para la hospitalización en los primeros 6 meses de vida, tanto por todas las causas como por causas respiratorias, en ninguno de los casos tuvo significancia estadística.
Entre los puntos destacables del estudio se encuentra la inclusión de todas las mujeres embarazadas de la institución y la posibilidad del seguimiento longitudinal de los binomios hasta los 6 meses de vida del lactante a través de registros administrativos confiables, en comparación con estudios transversales.
Dentro de las debilidades destacamos la falta de datos sobre el estado vacunal de las embarazadas en relación con las otras vacunas recomendadas en el embarazo (dpaT y antigripal), que también pueden tener impacto en la hospitalización de los lactantes, sobre todo por causas respiratorias.
Como vimos, es evidente el beneficio de la vacunación en el embarazo contra COVID-19 en la infección materna, en los resultados obstétricos y en las hospitalizaciones en los primeros 6 meses de vida, pero es preciso continuar investigando otros beneficios teniendo en cuenta los efectos a largo plazo de la infección en el embarazo por SARS-CoV-2, que advierten estudios recientes, al demostrar que lactantes expuestos a la infección durante el tercer trimestre experimentaron anomalías sustanciales en el desarrollo neurológico relacionadas con la función motora, el habla y el lenguaje21-26.
Conclusiones
La tasa de vacunación COVID en el embarazo es alta en nuestro estudio. No hubo diferencias en los resultados obstétrico-neonatales en vacunadas y no vacunadas.
La infección por SARS-CoV-2 en menores de 6 meses fue muy baja, no se detectó transmisión vertical. La vacunación COVID en el embarazo parece tener un impacto positivo en la infección materna y en la hospitalización de los menores de 6 meses.