Introducción
En nuestro país, el cáncer de próstata (CP) es el cáncer más frecuente en la población masculina, siendo diagnosticados 1.413 casos por año. Se ubica en el tercer lugar, luego del cáncer de pulmón y del cáncer colorectal como causa de muerte por cáncer en el hombre, con un promedio de 585 casos por año1.
Aproximadamente 10-20% de los pacientes presenta enfermedad avanzada al momento del diagnóstico y más del 40% eventualmente progresará a un cáncer de próstata metastásico hormono resistente (CPMHR), definido como la progresión de la enfermedad a pesar del tratamiento farmacológico o la castración quirúrgica2. Los pacientes con enfermedad localmente avanzada o metastásica que no pueden ser curados con tratamientos locales y reciben castración médica o quirúrgica a menudo presentan remisiones completas de su enfermedad por un periodo variable de tiempo (14–30 meses)3,4.
En pacientes con enfermedad avanzada, el tratamiento sistémico constituye el pilar del tratamiento, siendo la terapia de deprivación androgénica un componente fundamental, seguida de quimioterapia si la enfermedad progresa5. Para estos casos se encuentran aprobados antiandrógenos como la enzalutamida y la abiraterona, y los taxanos (docetaxel, cabazitaxel)6. Sin embargo, la respuesta a estos tratamientos es a menudo transitoria, dejando a muchos pacientes con enfermedad avanzada sintomática y pocas opciones terapéuticas.
Recientes estudios clínicos han mostrado resultados prometedores utilizando la terapia con radioisótopos en pacientes con CPMHR, basada en la sobreexpresión tumoral del antígeno prostático específico de membrana (PSMA), una glicoproteína transmembrana tipo II constituida por 750 aminoácidos. Se ha postulado que tendría múltiples funciones celulares, actuando como una enzima involucrada en la captación de nutrientes (folato). Asimismo, juega un rol en los procesos de migración, supervivencia y proliferación celulares7–9.
Mientras que es expresado a niveles bajos en el epitelio prostático humano normal, se encuentra sobreexpresado (superior a 1.000 veces respecto a las células prostáticas normales) en la mayoría de los pacientes con cáncer de próstata (solo el 5–10% de los casos parecen no expresar la glicoproteína PSMA)10.
El campo de la medicina nuclear ha centrado sus esfuerzos en la investigación de nuevas terapias dirigidas, que puedan modificar la historia natural de este estadio, caracterizado por una mortalidad neta a los pocos meses, pese al intento de múltiples terapias secuenciadas. Es así que se han desarrollado varios ligandos que se unen al PSMA con alta especificidad. En nuestro país contamos con el PSMA-11, que puede marcarse con 68GA o 18F para obtener imágenes diagnósticas mediante tomografía por emisión de positrones fusionada con tomografía computarizada (PET/CT). También contamos con el PSMA-617, que es marcado con 177Lutecio para terapia (Theragnostics).
Luego de producida la unión entre ligando y receptor, el PSMA sufre un proceso de internalización que permite la endocitosis de las proteínas unidas a la superficie celular, lo cual favorece su concentración dentro de las células tumorales que sobreexpresan PSMA11.
La densidad de expresión de este receptor transmembrana sobre las células del CP se incrementa en función del score de Gleason y es especialmente elevada en el CP resistente a la castración, lo que lo convierte en un blanco terapéutico ideal para el tratamiento con radioisótopos10.
El PSMA también es expresado en otras células, incluidas el intestino delgado, los túbulos renales proximales, las glándulas salivales y las lacrimales. Esto significa que, a pesar de que la expresión de PSMA en estas células es significativamente inferior a la de las células del cáncer de próstata, existe una dosis de radiación entregada a estos órganos cuando el PSMA es utilizado como blanco molecular en la terapia con radioisótopos. Esto tiene impacto en el perfil de efectos adversos de la terapia con 177Lu-PSMA-617 y en la dosis de radiación que puede ser administrada a un paciente sin causar un daño significativo a tejidos no blanco. En distintos ensayos clínicos, los tejidos con mayor riesgo de irradiación son las glándulas salivales y lacrimales12.
Terapia con 177Lutecio-PSMA
El lutecio 177 (177Lu) es un radioisótopo producto de reactor nuclear y utilizado para terapia, que actúa siendo un emisor de partículas beta de medianas energías (0,5 MeV) y con un rango de penetración en tejido <0,2 mm. Este rango corto proporciona una mayor irradiación de tumores pequeños. Emite además rayos gamma de baja energía (208 y 113 keV, con una abundancia del 10 y 6%, respectivamente). Esta emisión gamma permite obtener imágenes centellográficas, que son utilizadas para la localización tumoral y para estudios de dosimetría interna. El 177Lu tiene una vida media física de 6,73 días, lo que permite administrar actividades altas de 177Lu-PSMA-617 a las células del CP.
Evidencia clínica del uso de 177Lu-PSMA-617
Existe un número limitado de ensayos clínicos publicados acerca del uso de 177Lu-PSMA-617 en el tratamiento de pacientes con CPMHR. Principalmente, se trata de ensayos retrospectivos que de forma uniforme han mostrado, en una gran proporción de los pacientes tratados, una respuesta significativa al tratamiento y un bajo grado de toxicidad, con una aparente buena tolerancia al mismo.
Desde la introducción de la terapia con 177Lu-PSMA-617 en la práctica clínica en Alemania en 2013, varios grupos han publicado resultados prometedores en cohortes de pacientes que han agotado todas las opciones terapéuticas convencionales7–9. Hasta el momento, estos tratamientos son utilizados en la práctica clínica sin contar con información proveniente de ensayos clínicos controlados, y los radiofármacos como el 177Lu-PSMA-617 constituyen tratamientos de alto costo.
El 23 de marzo de 2022, la FDA aprobó Pluvicto® ([Lu-177]lutetium-vipivotide tetraxetan, Advanced Accelerator Applications, Novartis) para el tratamiento de pacientes adultos con antígeno de membrana específico de próstata (PSMA) metastásico positivo con CPMHR. La eficacia se evaluó en VISION (NCT03511664), un ensayo aleatorizado (2:1), multicéntrico y abierto, que evaluó Pluvicto® más el mejor estándar de atención (BSoC) (n=551) frente a BSoC solo (n=280) en hombres con CPMHR PSMA-positivo progresivo13.
El ensayo demostró una mejora estadísticamente significativa en los criterios de valoración primarios de supervivencia general (SG) y supervivencia libre de progresión radiográfica (rPFS). Las reacciones adversas más comunes (≥20 %) que ocurrieron con mayor incidencia en pacientes que recibieron Pluvicto® fueron fatiga, sequedad de boca, náuseas, anemia, disminución del apetito y estreñimiento. Las anormalidades de laboratorio más comunes que empeoraron desde el inicio en ≥30 % de los pacientes fueron disminución de linfocitos, disminución de hemoglobina, disminución de leucocitos, disminución de plaquetas, disminución de calcio y disminución de sodio.
En nuestro país se introdujo la terapia con 177Lu-PSMA-617 como opción terapéutica en octubre de 2017, con el apoyo del Organismo Internacional de Energía Atómica y el trabajo interdisciplinario de varias instituciones (CUDIM, INCA, Hospital de Clínicas y Facultad de Química).
Posteriormente, y luego de la publicación del estudio VISIÓN, pasó a formar parte de la rutina asistencial, en la que el paciente o la institución de origen realizan la cobertura financiera, o incluso pueden acceder a la misma mediante recurso de amparo.
En el presente estudio describimos nuestra experiencia desde la introducción de la terapia con 177Lu-PSMA-617 en pacientes con CPMHR, evaluando la factibilidad, la respuesta al tratamiento, eficacia y el perfil de seguridad/toxicidad observado en nuestros pacientes.
Materiales y métodos
Preparación de los trazadores 68Ga-PSMA-11
El radiofármaco se produce empleando 68GaCl3 eluido de un generador ITG, obteniéndose un producto final formulado en etanol al 6%, que contiene 2,6 nmol de HBEDCC-Ahx-(Lys-OH)-CO-(Glu-OH), estéril, libre de pirógenos y con un pH de 4,0 – 8,0. La pureza radioquímica debe ser superior al 90%, al igual que en la mayoría de los radiofármacos de diagnóstico. La actividad específica será superior a 100 GBq/μmol.
Preparación del 177Lu-PSMA-617
El radiofármaco 177Lu-PSMA-617 es preparado el mismo día de su administración al paciente, a partir de 177LuCl3 recibido de ITG (Alemania) y el precursor inactivo PSMA-617 recibido de ABX (Alemania). La preparación del 177Lu-PSMA-617 se realiza en un sistema de flujo laminar blindado, ubicado en un área limpia, que opera bajo la responsabilidad del responsable del área.
Reclutamiento de pacientes
Los pacientes referidos por su médico tratante (oncólogo médico, radioterapeuta o urólogo) fueron evaluados por el equipo de Oncología Médica del Instituto Nacional del Cáncer para su inclusión en el protocolo de terapia con 177Lu-PSMA-617, de acuerdo con los criterios de inclusión, exclusión y retiro del protocolo que a continuación se detallan:
Criterios de inclusión
Luego de otorgar el consentimiento informado, se consideran candidatos para esta terapia a los pacientes que cumplan con las siguientes condiciones:
Pacientes con adenocarcinoma de próstata histológicamente confirmado, metastásico, hormonoresistente y en progresión.
Ausencia de otras opciones terapéuticas disponibles en el sistema de salud del paciente, que se puedan indicar en la situación clínica concreta.
Expresión comprobada en las lesiones del antígeno PSMA, documentada mediante PET/CT con 68Ga-PSMA-11 previo a la terapia.
Adecuada reserva de médula ósea: leucocitos >2.000/uL, plaquetas >75.000/uL.
Creatinina <2,0 mg/dl.
Adecuada función hepática: transaminasas (TGO o TGP) <5 veces el límite superior de normalidad.
El tratamiento debe estar separado al menos 6 meses de otros tratamientos potencialmente mielosupresores.
Índice de Karnofsky >50.
Criterios de exclusión
Pacientes con una expectativa de vida inferior a 6 meses.
Discapacidad mental.
Pacientes con captación difusa e intensa de 68Ga-PSMA-11 en PET/CT previo a la terapia.
Cualquier otra condición clínica que, a juicio del Comité de Ética, impida que el paciente ingrese al protocolo.
Serán excluidos los pacientes con patologías severas o graves que limiten su expectativa de vida o calidad de vida, más allá del tratamiento oncoespecífico.
Normas éticas
Antes de comenzar el tratamiento, todos los pacientes firmaron el consentimiento informado. La investigación fue aprobada por el Comité de Ética del Centro Uruguayo de Imagenología Molecular (CUDIM) en Montevideo, Uruguay.
Esquema terapéutico
Es un requisito imprescindible contar con un estudio PET/CT con 68Ga-PSMA-11 positivo que confirme la expresión de PSMA en las lesiones metastásicas.
La terapia con 177Lu-PSMA-617 se inició en todos los casos en un intervalo no mayor de 4 semanas desde la realización de un PET/CT.
La dosis recomendada es de 7,0 GBq (200 mCi) por vía intravenosa cada 6 semanas, durante un máximo de 6 dosis (actividad máxima acumulada por paciente de 50 GBq), o hasta la progresión de la enfermedad o la aparición de toxicidad inaceptable.
Se administraron dos ciclos terapéuticos con 177Lu-PSMA-617, separados por 6 semanas entre sí.
Aproximadamente 4 semanas después del segundo ciclo, se reestadificó al paciente mediante un nuevo PET/CT con 68Ga-PSMA-11. Teniendo en cuenta la respuesta imagenológica, la expresión del antígeno PSMA y la situación clínica del paciente, se indicaron nuevos ciclos de terapia.
Antes de cada ciclo de terapia y cada 4 semanas se realizaron estudios de laboratorio, que incluyeron: hemograma completo con lámina, creatinina, azoemia, ionograma, función hepática y enzimograma, proteína C reactiva, fosfatasa alcalina y PSA.
Administración del 177Lu-PSMA-617
La administración del radiofármaco se realizó en el Centro de Medicina Nuclear e Imagenología Molecular del Hospital de Clínicas por un médico nuclear entrenado con el apoyo del equipo de enfermería. Se controlan signos vitales (presión arterial, temperatura, frecuencia cardíaca).
Implementación de la terapia
Los pacientes recibieron hidratación intravenosa lenta mediante solución salina al 0,9% (500 mL, flujo de 333 mL/h), comenzando 30 minutos antes de la terapia.
La administración del 177Lu-PSMA-617 se realizó por vía intravenosa lenta, inyectando manualmente por un período de 30-60 segundos, a través de un filtro estéril de 0,2 μm.
Se realizó monitoreo continuo de los signos vitales.
Se realizó profilaxis de posibles reacciones inflamatorias y edema perilesional mediante prednisona vía oral, comenzando con 40 mg el día previo, luego 40 mg cada 12 horas el día del tratamiento y 20 mg cada 12 horas el día posterior a la terapia.
Se vigiló especialmente la aparición de posibles efectos secundarios: náuseas, vómitos, xerostomía, disnea y fatiga.
El paciente permaneció en el centro monitorizando a 1 m la dosimetría cada 1 hora utilizando un contador portátil Geiger. El paciente no requirió hospitalización y fue dado de alta cuando se alcanzaron valores menores a 30 mSv a 1 metro, usualmente a las 3 horas luego de la administración.
Estudios PET/CT con 68Ga-PSMA-11
Los estudios fueron adquiridos en un equipo General Electric Discovery 690 VCT, con tomógrafo de 64 cortes, con tubo de rayos X de 100 kW pico y equipo PET con detectores LYSO.
La solución de 68Ga-PSMA-11 se administró a los pacientes a través de un bolo intravenoso, con una dosis promedio de 140 Mbq para un adulto de 70 Kg (2 MBq/kg). La adquisición de las imágenes comenzó a los 30 minutos postinyección del radiotrazador.
Se realizó la tomografía computarizada de cuerpo entero sin contraste intravenoso, con el paciente en decúbito supino y brazos elevados, utilizando los siguientes parámetros: kilovoltaje de 120 kV, corriente de tubo efectiva de 30–210 mAs; 120Kv y 10 mA.
Inmediatamente después del CT, se adquirió el estudio PET en modo 3D, en dirección cráneo-caudal, desde la cabeza hasta la mitad del muslo, con tamaño de la matriz de 128 × 128 píxeles, con tiempo de adquisición de 240 segundos por cada posición de cama y superposición de corte de 11 mm, utilizando el CT para la corrección de atenuación. La duración total de la exploración fue de aproximadamente 30 minutos.
Se realizó la corrección de las imágenes PET por “tiempo de vuelo” y las imágenes fueron reconstruidas mediante el método iterativo OSEM (28 subconjuntos/2 iteraciones).
Se obtuvieron imágenes PET, CT y PET/CT fusionadas, reformadas en cortes transversales, coronales y sagitales. Se calculó el SUV máximo de cada una de las lesiones identificadas.
Controles
Todos los pacientes realizaron controles con imágenes centellográficas posteriores a la administración de la dosis con un equipo híbrido SPECT/CT Mediso AnyScan. A las 72 horas de inyectada la dosis, se adquirieron imágenes planares de cuerpo entero y, posteriormente, una tomografía por emisión de fotón único (SPECT), finalizando con una tomografía computarizada de baja dosis SPECT-CT de abdomen y pelvis.
Estadística y evaluación de la respuesta al tratamiento
En cada paciente se evaluó la respuesta al tratamiento mediante la realización de PET/CT con 68Ga-PSMA-11 antes de la tercera dosis y, posteriormente, al finalizar el esquema terapéutico.
Los cambios en los niveles séricos de PSA se utilizaron para evaluar la respuesta al tratamiento. La mejoría en el PSA se definió como cualquier descenso en comparación con el nivel basal. La progresión de PSA se definió como cualquier incremento siendo mayor o igual al 25% y mayor o igual a 2 μg/L por encima del nivel basal, de acuerdo a los criterios del Prostate Cancer Clinical Trials Working Group (PCWG2 criteria).
La falla en el tratamiento se definió como dos incrementos consecutivos del PSA, con un tiempo mínimo entre estas dos mediciones igual o mayor a 3 semanas.
Se evaluó la respuesta clínica (por alivio del dolor/uso de analgésicos), la respuesta a la terapia (por PSA y PSMA-PET, criterios de progresión) y los eventos adversos (CTCAE, versión 4.03).
Resultados
Entre octubre de 2017 y febrero de 2022, 19 pacientes con CPMHR (edad [años]: media 67,8; PSA [ng/mL]: media 287), positivos a PET/PSMA, recibieron terapia radiodirigida con 177Lu-PSMA-617.
Todos los pacientes recibieron entre 1 y 5 dosis de 177Lu-PSMA-617 (actividad media de 7,4 GBq/ciclo) cada 6 semanas (1 ciclo, n=3; 2 ciclos, n=1; 3 ciclos, n=13; 4 ciclos, n=1 y 5 ciclos, n=1). Quince pacientes (79%) completaron tres ciclos de terapia. Se administró un total de 53 dosis (Figura 1).
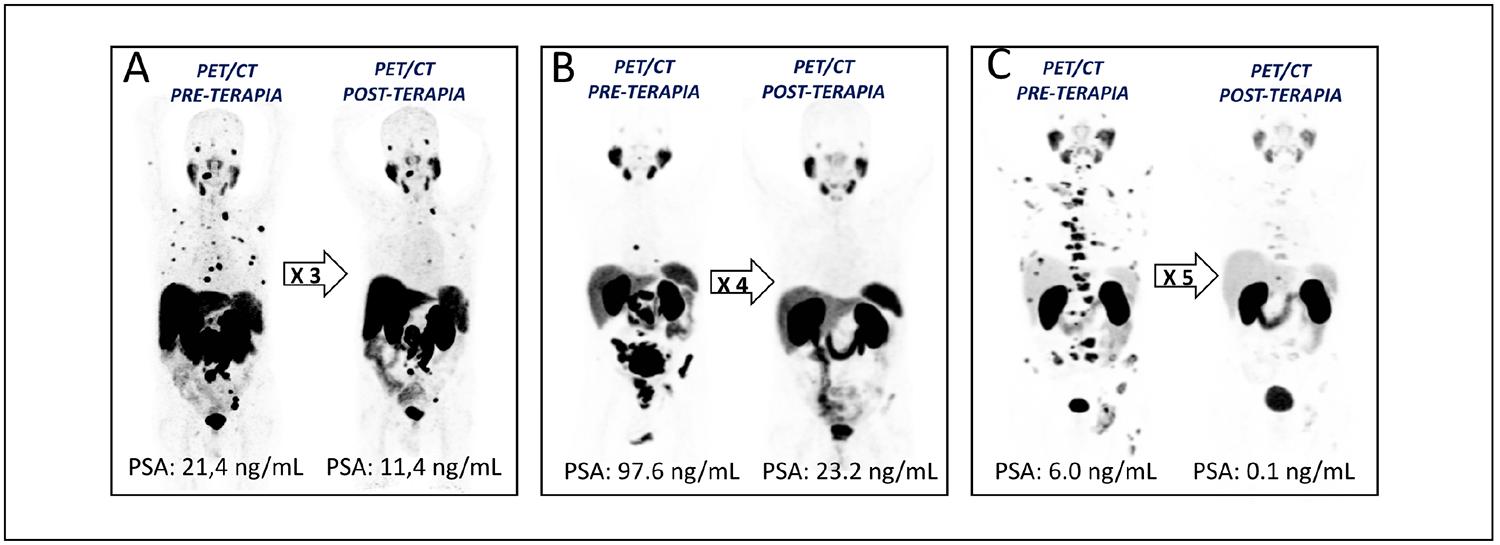
Figura 1. Estudios PET con 68Ga-PSMA-11 al inicio y al final del tratamiento. Nótese el descenso del PSA y la respuesta parcial en las imágenes PET con luego de tres (A), cuatro (B) y cinco ciclos (C), respectivamente.
Previo a la terapia, todos los pacientes presentaron lesiones metastásicas ávidas de PSMA en el PET/CT con 68Ga-PSMA-11 en los siguientes sitios: óseo (n=18), ganglios linfáticos (n=14), hígado (n=3), pulmón (n=2) y glándulas suprarrenales (n=1). En cuanto a la respuesta del PSA, 5 pacientes mostraron respuesta bioquímica, 3 pacientes enfermedad estable y 7 pacientes enfermedad progresiva. Siete de 15 pacientes (46,6%) mostraron alguna disminución de PSA. Las imágenes de PET/CT con 68Ga-PSMA-11 en los pacientes que completaron tres ciclos o más mostraron progresión de la enfermedad (n=9) y remisión parcial (n=5). Se documentó mejoría clínica como alivio del dolor y/o reducción en el uso de analgésicos (n=9), xerostomía (n=2), náuseas (n=3), fatiga (n=6) y trombocitopenia (n=2). No se demostró hepatotoxicidad ni nefrotoxicidad y se confirmó la seguridad del 177Lu-PSMA-617 para los tejidos no diana, mostrando dosis absorbidas medias (Gy) por debajo de las recomendadas en órganos críticos.
Discusión
El cáncer de próstata es el segundo tumor maligno más frecuente en el hombre y una de las enfermedades malignas más frecuentes a nivel mundial. Nuestro país presenta una de las tasas más altas de incidencia y mortalidad en el continente americano, con más de 1.500 nuevos casos diagnosticados anualmente14.
Por otra parte, el CPMHR representa un desafío clínico para el cual son necesarias nuevas herramientas terapéuticas más allá de la quimioterapia con taxanos o el tratamiento hormonal con abiraterona o enzalutamida. En efecto, en muchos casos estas terapias han demostrado una relativa ineficacia en controlar la progresión de la enfermedad. Por tal motivo, resulta urgente el desarrollo de nuevas estrategias terapéuticas capaces de controlar la evolución de la enfermedad en este estadio15.
El PSMA es una metaloenzima con función de proteasa que se encuentra en la membrana de las células prostáticas normales, pero con una marcada sobreexpresión en carcinomas de próstata pobremente diferenciados, metastásicos y hormono-refractarios. Su expresión es mínima en otros tejidos, lo que lo convierte en un blanco específico promisorio para el diagnóstico imagenológico y la terapia. Esto se debe a su localización transmembrana y a su capacidad de internalización tras la unión con el ligando.
Además, se ha demostrado que los inhibidores del PSMA basados en estructuras tipo urea (Glu-NH-CO-NH-Lys) se unen en forma específica a esta molécula. La unión de dicho farmacóforo a un quelante acíclico (HBED-CC, DOTA u otros), mediante un espaciador adecuado y su posterior marcado con 68Ga, constituye una alternativa atractiva para la obtención de un radiofármaco PET para el diagnóstico del cáncer de próstata16.
Asimismo, el PSMA puede ser marcado con 177Lu (radioisótopo emisor de electrones utilizado en radioterapia metabólica), empleando un quelante (ej., DOTA) que maximice la síntesis y la estabilidad del complejo. De esta manera, se puede lograr un procedimiento combinado con potencial para permitir un abordaje terapéutico basado en las imágenes moleculares. Esta estrategia, que emplea compuestos similares en diagnóstico y terapia capaces de reconocer el mismo blanco molecular, se denomina “theranostics” o “diagnoterapia”. La única diferencia entre el compuesto diagnóstico y el agente terapéutico radica en el radioisótopo utilizado en la marcación. La aplicación de esta estrategia en pacientes con cáncer de próstata fue descripta por primera vez por Weineisen et al., quienes trataron con 177Lu-PSMA a dos pacientes con CPMHR guiados por las imágenes PET/CT con 68Ga-PSMA-1117.
El 177Lu es un radionúclido emergente debido a sus características químicas y nucleares (E: 497 keV; E: 113 y 208 keV; período de semidesintegración T1/2: 6,7 días). Presenta un rango de penetración en tejido entre 0,5 mm y 2 mm, lo que permite la irradiación de tejidos tumorales. Al ser emisor beta y gamma simultáneamente, puede realizarse un seguimiento de su aplicación mediante SPECT. Consideramos que esta estrategia tiene el potencial de impactar positivamente en el manejo clínico de pacientes con CPMHR en nuestro país. Por este motivo, nuestro grupo se propuso valorar la eficacia de este tratamiento.
Reportamos nuestra primera experiencia clínica con 177Lu-PSMA en pacientes con CPMHR. Nuestros pacientes habían agotado todas las opciones terapéuticas convencionales disponibles. Los pacientes tratados cumplieron los criterios de inclusión y exclusión establecidos y se realizaron controles clínicos y paraclínicos para evaluar la respuesta al tratamiento, los efectos adversos y la seguridad del mismo. Un total de 19 pacientes recibieron entre 1 y 5 dosis de 177Lu-PSMA. Nuestros resultados son concordantes con las series publicadas.
Recientemente, Baum et al.7 estudiaron la toxicidad y eficacia del tratamiento con 177Lu-PSMA en 56 pacientes con CPMHR. Los autores administraron una mediana de dosis de 5,8 GBq de este radiofármaco por ciclo (1 a 5 ciclos). Se demostró una importante dosis absorbida tanto en las metástasis óseas como en las ganglionares (mediana = 3,3 mGy/MBq) con una toxicidad mínima, fundamentalmente a nivel de las glándulas salivares (2 pacientes), lo cual se puede expresar como una xerostomía leve a moderada y transitoria. Cabe destacar que no se reportaron casos de toxicidad hematológica significativos. Los autores registraron una reducción leve postratamiento del conteo de glóbulos rojos y leucocitos y ningún caso de trombocitopenia. Asimismo, la intensidad del dolor descendió en un tercio de los pacientes. En este trabajo, los niveles de PSA descendieron más del 50% en el 62% de los pacientes. Además, la TC demostró una remisión parcial en el 20% de los pacientes, mientras que el PET/CT con 68Ga-PSMA-11 demostró respuesta parcial en el 56% de los pacientes18.
Resultados similares fueron reportados por Kratochwil et al.8 quienes evaluaron retrospectivamente una serie de 30 pacientes con CPMHR sometidos a terapia con 1 a 3 ciclos de 177Lu-PSMA, con una actividad máxima administrada de 6 GBq por ciclo. Todos los pacientes presentaban lesiones detectadas mediante PET/CT con 68Ga-PSMA-11. Se obtuvo una respuesta evaluada por descenso de PSA en 70% de los pacientes, con descensos superiores al 50% en 43% de los pacientes. La toxicidad hematológica también fue leve a moderada y predecible. Fatiga, náuseas y xerostomía fueron descriptas en menos del 10% de los casos. La dosis media tumoral absorbida varió entre 6 y 22 Gy/GBq para el primer ciclo. Los estudios dosimétricos demostraron dosis de 0,75 Gy/GBq para riñones, 0,03 Gy/GBq para médula ósea y 1,4 Gy/GBq para glándulas salivales8.
Usando una metodología similar, Ahmadzadehfar et al. demostraron, en una serie de 24 pacientes, un descenso del PSA de 79% luego del primer ciclo de terapia y del 68% luego del segundo ciclo. No se registraron casos de toxicidad hematológica ni renal significativos19.
En el mismo sentido, Rahbar et al.20 publicaron un estudio retrospectivo que involucró a 28 pacientes con CPMHR tratados con esta terapia. Los autores mostraron un descenso del PSA mayor del 50% en 50% de los pacientes, luego de dos ciclos de terapia (6 GBq por ciclo). Además, los autores encontraron una mediana de sobrevida de 29,4 meses, significativamente mayor que los valores de sobrevida históricos de una cohorte de pacientes de similares características, tratados con los procedimientos estándar disponibles previos a la introducción del 177Lu-PSMA (19 semanas). Asimismo, un estudio multicéntrico realizado en Alemania y liderado por el mismo autor demostró un descenso de PSA en 64% de los pacientes (n=74), usando dosis similares. No se describieron casos de toxicidad hematológica ni renal significativos21.
Por lo tanto, todos los trabajos coinciden en que existe un bajo perfil de toxicidad, siendo los órganos críticos médula ósea, las glándulas salivales y los riñones. Fatiga, náuseas y xerostomía se observan en menos del 10% de los casos y no se reportaron casos de toxicidad hematológica, renal ni hepática significativas18.
Los beneficios esperables del tratamiento descritos en la literatura son:18
Descenso de la severidad del dolor en un tercio de los pacientes.
Descenso significativo de PSA.
Imagen: CT y PET/CT, con remisión significativa de las lesiones.
Aumento de sobrevida de la terapia con 177Lu-PSMA.
En nuestro trabajo, según la respuesta de PSA, 5 pacientes mostraron respuesta bioquímica, 3 pacientes enfermedad estable y 7 pacientes enfermedad progresiva. Siete de 15 pacientes (46,6%) presentaron alguna disminución de PSA. Estos hallazgos son consistentes con los reportes de la literatura publicada, que demuestran descensos del PSA ≥ 50%, en entre el 33% a 71% de los pacientes22.
Las imágenes de PET/CT con 68Ga-PSMA-11 en pacientes que completaron tres ciclos o más mostraron progresión de la enfermedad (n=9) y remisión parcial (n=5). Se documentaron alivio del dolor y/o reducción en uso de analgésicos (n=9), xerostomía (n=2), náuseas (n=3), fatiga (n=6) y trombocitopenia (n=2). No se evidenció hepatotoxicidad ni nefrotoxicidad, lo que concuerda con las series publicadas.
Conclusiones
La experiencia inicial en nuestro país en el uso de 177Lu-PSMA-617 como nueva opción terapéutica demostró ser factible, mejorar la calidad de vida y presentar un buen perfil de seguridad en pacientes con cáncer de próstata metastásico resistente a la castración que han agotado las opciones terapéuticas convencionales. En nuestro grupo de pacientes se observaron niveles bajos o mínimos de toxicidad.
Concluimos que la terapia con 177Lu-PSMA-617 es una opción terapéutica segura y bien tolerada para pacientes con CPMHR, contribuyendo a la mejora de la calidad de vida de los pacientes.















