Introducción
El citomegalovirus (CMV) es una de las infecciones virales más frecuentes y de mayor impacto en receptores de trasplante hepático (TH), representando una causa relevante de morbimortalidad en esta población. Su incidencia varía entre un 30% a 80%, dependiendo del riesgo inmunológico, y su espectro clínico abarca desde infección asintomática hasta enfermedad invasiva, con compromiso orgánico, siendo la hepatitis y la enterocolitis las manifestaciones más comunes1–3.
El riesgo de desarrollar infección o enfermedad por CMV está determinado por diversos factores. Los pacientes considerados de alto riesgo son los receptores seronegativos (R−) que reciben órganos de donantes seropositivos (D+), así como aquellos que reciben inmunosupresión con agentes depletores de linfocitos, como la globulina antitimocítica, en quienes la incidencia de enfermedad puede alcanzar aproximadamente el 50%3. En contraste, los receptores seropositivos (R+) que no reciben inmunosupresores depletores presentan un riesgo intermedio, con una tasa de enfermedad generalmente inferior al 10% debido a su inmunidad preexistente2–7.
Para prevenir las complicaciones por CMV, los programas de trasplante han adoptado dos estrategias principales: profilaxis universal y terapia anticipada. La profilaxis universal, generalmente administrada a pacientes de alto riesgo, consiste en administrar antivirales independientemente de la detección de replicación viral. Si bien esta estrategia ha demostrado eficacia, con reducción de la incidencia de enfermedad por CMV, presenta desventajas como toxicidad a largo plazo, costos elevados y riesgo de resistencia antiviral2.
La terapia anticipada, utilizada principalmente en pacientes de riesgo intermedio, se basa en la monitorización periódica de la carga viral mediante PCR cuantitativa en plasma o sangre, iniciando tratamiento antiviral al superar un cut-off específico, con el objetivo de prevenir la progresión a enfermedad clínica. Esta estrategia permite optimizar el uso de antivirales, evitando su administración innecesaria y reduciendo costos, pero su implementación requiere infraestructura adecuada para una monitorización virológica constante. Además, su eficacia depende de definir un punto de corte adecuado, lo que sigue siendo un desafío, ya que no existe consenso universal y las guías internacionales sugieren valores variables4–8.
A lo largo de los años, distintos cut-off han sido propuestos para guiar la terapia anticipada en receptores de TH. En 2013, Martín-Gandulet al.9 validaron un cut-off de 3.893 UI/ml (2.600 copias/ml) en receptores seropositivos sin tratamiento con globulina antitimocítica. Sin embargo, cada centro debe validar sus propios parámetros, ya que los valores pueden variar según las características de la población y la metodología utilizada para la cuantificación viral.
En el Centro Nacional de Trasplante Hepático en Montevideo, la carga viral de CMV en receptores seropositivos sin tratamiento con antitimocíticos se cuantifica mediante PCR en tiempo real, expresada en Unidades Internacionales por mililitro (UI/ml). Basado en datos locales, desde antes de 2017 se estableció un cut-off de 1.500 UI/ml para definir el inicio de la terapia anticipada. Sin embargo, este punto de corte no había sido previamente evaluado, por lo que se consideró necesario su análisis para determinar un cut-off ajustado a la población estudiada.
Materiales y métodos
Diseño del estudio:
Estudio observacional, retrospectivo, realizado en un centro único de trasplante hepático.
Población
Período de estudio:
La fase retrospectiva abarcó desde el 1 de enero de 2017 hasta el 30 de junio de 2024.
Definiciones operativas
Infección por CMV:
Identificación de replicación viral de CMV o ADN de CMV en cualquier fluido corporal o tejido al margen de que el paciente tenga síntomas o no.
Infección asintomática por CMV:
La detección de replicación del CMV en ausencia de signos o síntomas.
Enfermedad por CMV:
Presencia de infección por CMV asociada a signos y síntomas clínicos. Puede presentarse como síndrome viral o enfermedad con compromiso visceral (hepatitis, neumonitis, colitis, etc.).
Cut-off de CMV:
valor de carga viral de CMV establecido como punto de corte para iniciar tratamiento antiviral previo al inicio de síntomas. Cut-off de CMV establecido por el centro para inicio de terapia antiviral: 1.500 UI/ml.
Alto riesgo:
receptores seronegativos para CMV (R−) que reciben un injerto de un donante seropositivo (D+), y pacientes que reciben drogas inmunosupresoras depletoras de los linfocitos, como son las globulinas antitimocíticas o altas dosis de otros inmunosupresores de mantenimiento, independientemente de su estado serológico.
Profilaxis universal:
consiste en la realización de profilaxis con tratamiento antiviral en pacientes de alto riesgo (D+ R−). En nuestro centro, se utiliza Ganciclovir 5 mg/kg/día y posteriormente se rota a Valganciclovir 900 mg/día hasta completar 3 meses postrasplante, pudiendo prolongarse hasta 6 meses si se utilizan globulinas antitimocíticas. Al finalizar el tratamiento, se continúa el control con cargas virales mensuales hasta el año postrasplante.
Profilaxis selectiva:
consiste en la realización de profilaxis con tratamiento antiviral en trasplantados que reciben globulinas antitimocíticas independientemente de su estatus serológico. En este grupo, se utiliza Ganciclovir 5 mg/kg/día iv y posteriormente se rota a Valganciclovir 900 mg/día vía oral hasta completar los 3 meses postrasplante. Al finalizar el tratamiento, se continúa el control con cargas virales mensuales hasta el año.
Estrategia anticipada:
se aplica en trasplantados de riesgo intermedio. Consiste en la monitorización con carga viral de CMV de forma semanal hasta el tercer mes, quincenal desde el tercer mes al sexto mes, y mensual hasta completar el año postrasplante. Se inicia el tratamiento antiviral cuando la carga viral supera el valor de cut-off de CMV, con Valganciclovir 900 mg vía oral cada 12 horas, con un mínimo de 14 días de tratamiento y hasta obtener dos cargas virales consecutivas negativas.
Procedimientos
Las muestras de plasma fueron analizadas mediante PCR cuantitativa utilizando el estándar internacional de la OMS para la conversión de copias/ml a UI/ml. Los pacientes fueron monitoreados regularmente durante el primer año postrasplante.
Se incluyeron todos los pacientes receptores de trasplante hepático (TH) y hepatorrenal durante el período del 1 de enero de 2017 al 30 de junio de 2024 que hayan tenido al menos una determinación con carga viral de CMV detectable mediante RT-PCR antes del inicio de terapia antiviral. Cada episodio de replicación se consideró un evento. Una vez identificados todos los eventos con los valores de las cargas virales, se realizó una curva ROC para analizar el valor de corte con mayor sensibilidad y especificidad para el inicio de terapia antiviral.
En esta cohorte, los pacientes que presenten replicación viral igual o superior a 1.500 U/ml, según el protocolo de nuestro centro, iniciaron terapia antiviral. La duración del tratamiento antiviral se realizó por un mínimo de dos semanas, con control de carga viral semanal, y hasta contar con al menos dos cargas virales indetectables.
Una vez que se determinó el valor de corte de CMV, se inició la fase prospectiva del estudio para la validación del mismo.
Análisis estadístico
Para determinar el punto de corte óptimo de la carga viral para la iniciación de la terapia anticipada, se realizó un análisis de la curva ROC utilizando el software SPSS versión 23. En este análisis, se evaluaron múltiples cut-off es de carga viral, y se aplicó el índice de Youden como criterio principal para identificar el valor que optimiza el equilibrio entre la detección de verdaderos positivos y la minimización de falsos positivos. De esta forma, se seleccionó el cut-off que maximizaba dicho índice, asegurando que la estrategia de terapia anticipada ofreciera un alto poder discriminatorio en la predicción de la progresión a enfermedad por CMV.
Resultados
Se incluyeron un total de 143 pacientes sometidos a trasplante hepático, con un total de 173 episodios de viremia para CMV. En la Tabla 1 se presentan las características generales de la población estudiada, incluyendo edad promedio, sexo y tipo de trasplante realizado.
Tabla 1. Generalidades de la población receptora de trasplante hepático incluidos en el trabajo. Programa Nacional de Trasplante Hepático - Uruguay. Período 2017-2024. (n = 143 pacientes).
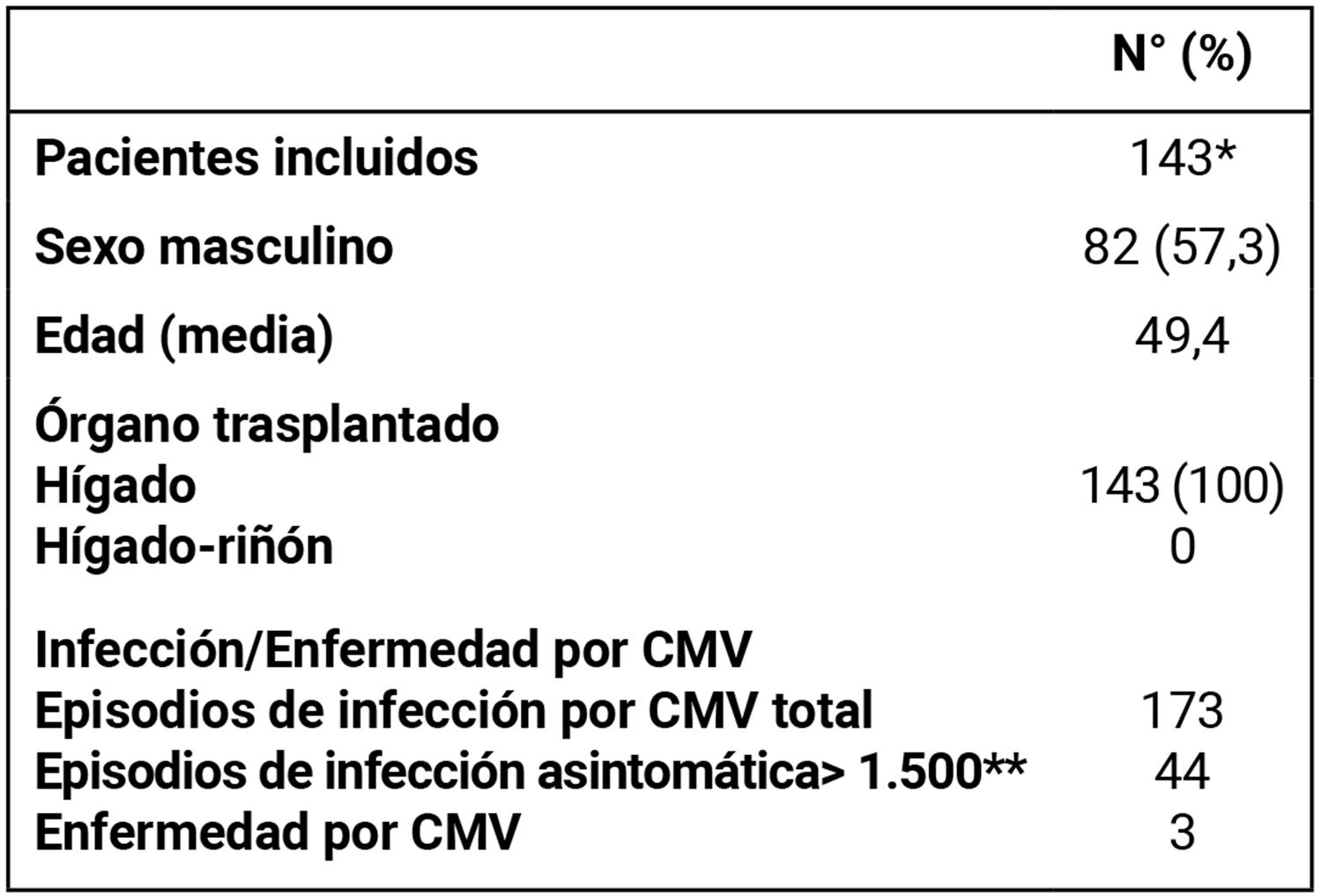
*Total de pacientes trasplantados en el periodo de estudio n= 155. Se excluyeron por ser de alto riesgo n= 12. De los cuales, 5 pacientes habían recibido timoglobulina y 7 pacientes era D+/R−.
**Estos pacientes son los que reciben antiviral preventivo, ya que superan el punto de corte establecido.
La distribución de los valores observados fue la siguiente: el 67,6% de los pacientes se ubicó en el rango <1.000, el 11,6% entre 1.000-2.000, el 16,8% entre 2.001-10.000, y el 4% presentó valores superiores a 10.000. Este dato se objetiva en la Tabla 2.
Tabla 2. Distribución de la carga viral de CMV en receptores de trasplante hepático. Programa Nacional de Trasplante Hepático - Uruguay. Período 2017-2024 (n = 173).

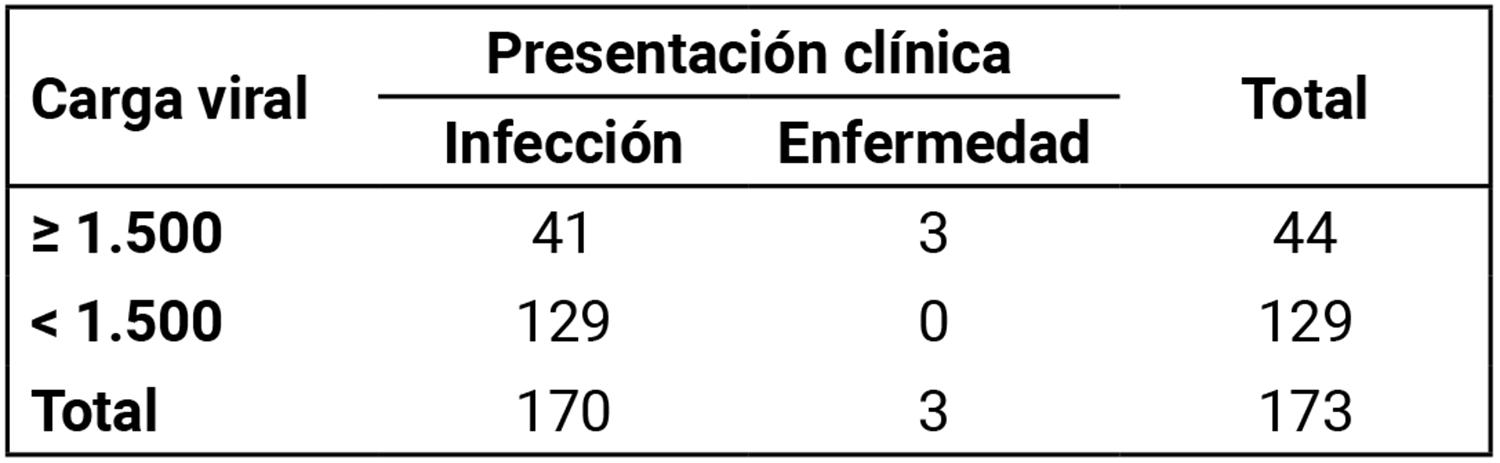
En la Tabla 3, se detalla la incidencia de enfermedad por CMV en los pacientes con viremia, reportándose un total de 3 casos (1,9%). En todos los casos de progresión a enfermedad por CMV, las cargas virales superaron los 1.500 UI/ml.
Tabla 3. Relación entre carga viral >1.500 UI/ml y presentación clínica en receptores de trasplante hepático. Programa Nacional de Trasplante Hepático - Uruguay. Período 2017-2024. (n = 173).
Las características de los episodios de viremia y su relación con los valores de carga viral también se resumen en la Figura 1, donde se estratificaron los valores de carga viral en diferentes rangos para analizar su distribución en la cohorte.
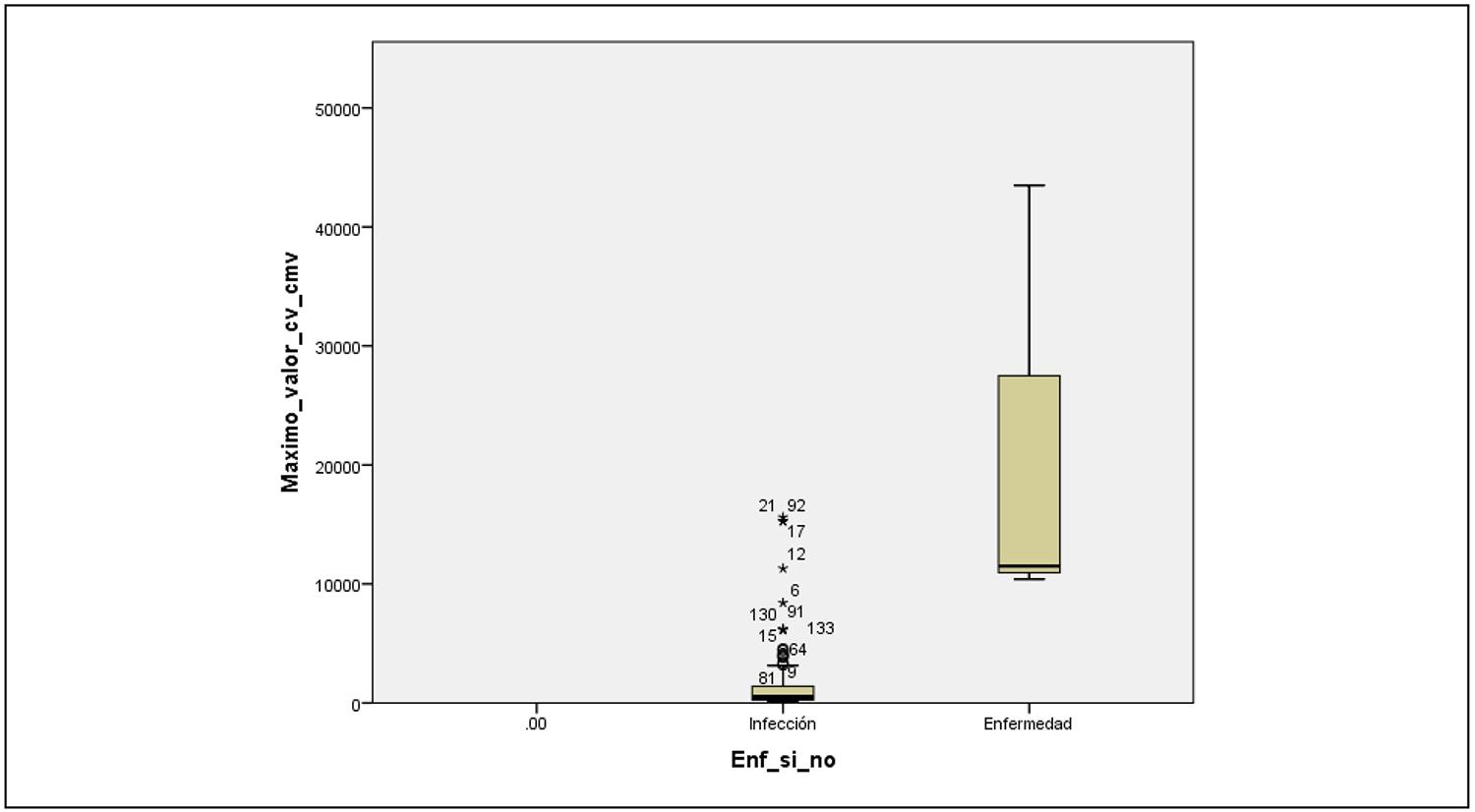
Figura 1. Distribución de valores de carga viral agrupados de acuerdo con la presentación clínica de CMV en receptores de trasplante hepático. Programa Nacional de Trasplante Hepático - Uruguay. Período 2017-2024. (n = 173 episodios de replicación viral).
La media del valor de carga viral de los pacientes con enfermedad (21.800 UI/ml) vs. aquellos que no la presentaron (1.373 UI/ml (fue estadísticamente significativa (p<0,05).
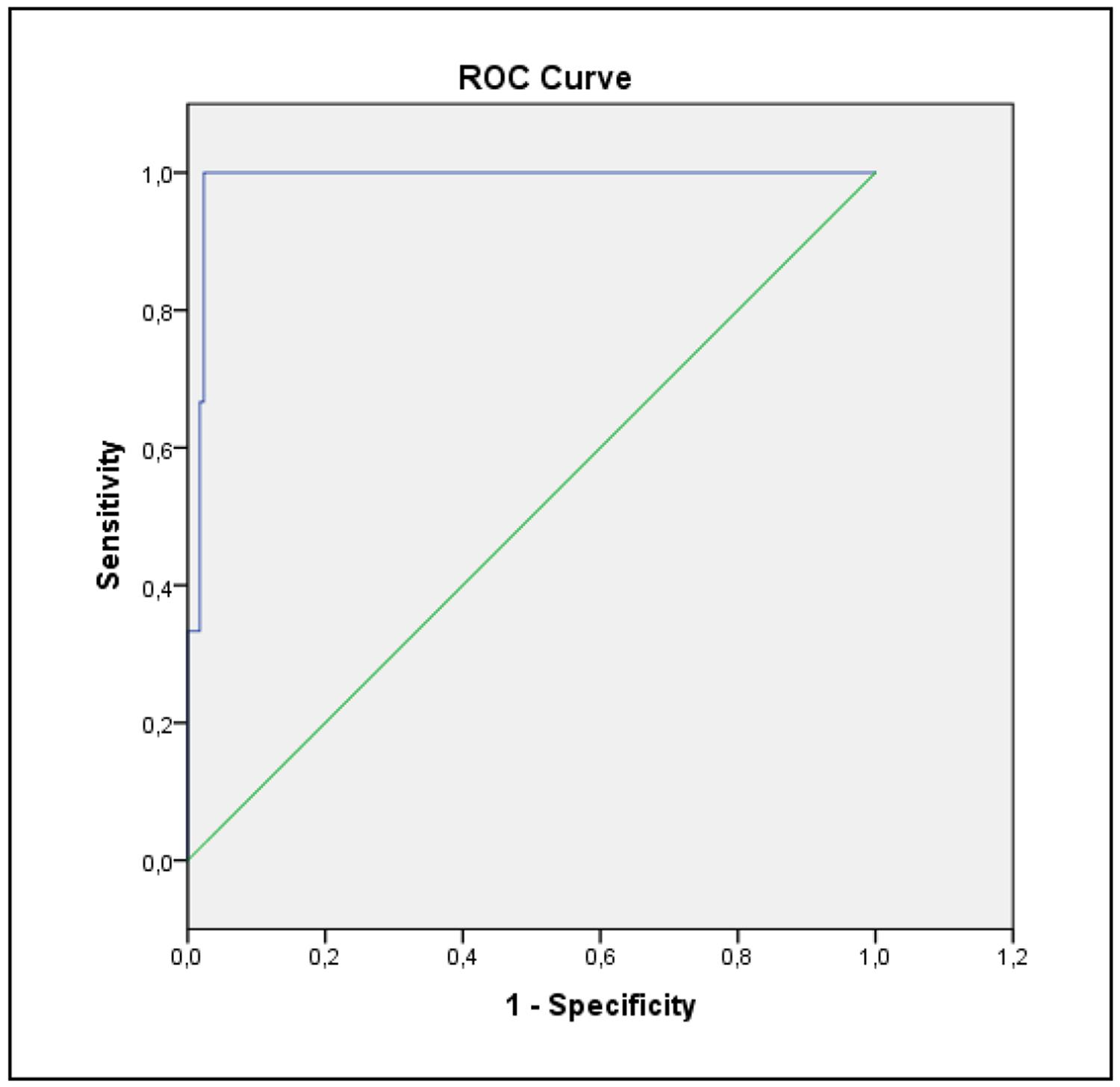
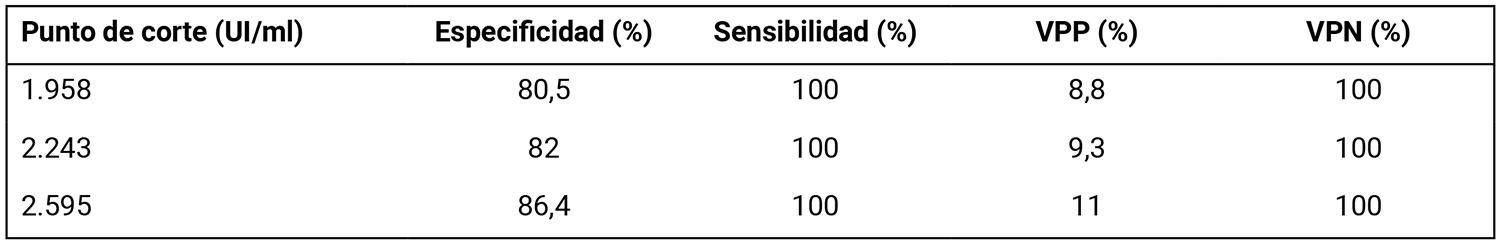
El análisis de la curva ROC se realizó para evaluar la capacidad discriminativa de la carga viral en la predicción de la progresión a enfermedad por CMV. Se analizaron varios cut-off, obteniéndose un AUC de 0,986 (IC 95%: 0,967–1,000) que respalda el desempeño del marcador. Entre los cut-off evaluados, se consideraron los valores de 1.958, 2.243 y 2.595 UI/mL. El punto de corte de 2.595 UI/mL fue seleccionado debido a que optimizaba la sensibilidad (100%) y mantenía una especificidad aceptable (86,4%), lo que garantiza la detección temprana sin incurrir en un número excesivo de falsos positivos. La Figura 2 ilustra esta comparación y en la Tabla 4 se incluyen los valores de sensibilidad, especificidad, valor predictivo positivo (VPP) y valor predictivo negativo (VPN).
Discusión
Este estudio identificó un cut-off de 2.595 UI/mL como el valor óptimo de carga viral para indicar terapia anticipada en receptores de trasplante hepático con riesgo intermedio para citomegalovirus (CMV). Este punto de corte presentó un excelente rendimiento diagnóstico, con una sensibilidad del 100%, especificidad del 86,4% y un área bajo la curva (AUC) de 0,986. Estos resultados reflejan una alta capacidad discriminativa para detectar, de forma temprana, los casos con riesgo real de progresión a enfermedad clínica, minimizando al mismo tiempo el inicio innecesario de tratamiento antiviral.
Nuestros hallazgos son consistentes con los de Martín-Gandul et al.9, quienes propusieron un cut-off de 3.893 UI/mL en una población comparable. Aunque los valores difieren ligeramente, ambos se sitúan en rangos clínicamente aceptables y expresados en Unidades Internacionales (UI/mL), lo que facilita la comparación entre centros y contribuye a la estandarización progresiva de criterios diagnósticos y terapéuticos.
La baja tasa de progresión a enfermedad (1,9%) observada en esta cohorte concuerda con datos históricos del mismo centro, 3% en 201713; así como con estudios internacionales, como el de Limaye et al.14, que reportan incidencias de hasta 4% en poblaciones de riesgo intermedio. De forma complementaria, Hakimi et al.5 demostraron que la enfermedad por CMV en receptores de órganos sólidos se asocia a un incremento del riesgo de rechazo, pérdida del injerto, mayor mortalidad hospitalaria y costos asistenciales elevados. Estos datos subrayan la importancia de estrategias preventivas efectivas y adaptadas al perfil de riesgo de cada paciente.
Asimismo, se evidenció que los pacientes que no desarrollaron enfermedad presentaron cargas virales significativamente más bajas que aquellos que sí la desarrollaron (media: 1.373 vs. 21.800 UI/mL; p < 0,05), hallazgo que coincide con reportes previos tanto de nuestro grupo como de autores como Chen Ju et al.15, y refuerza el valor pronóstico de la cuantificación virológica.
La asociación entre viremias elevadas y peores desenlaces clínicos ha sido ampliamente documentada16,17. En este sentido, McBride et al.18 reportaron que los receptores D+/R− con cargas virales altas presentaron una mayor incidencia de enfermedad severa (32% en trasplante renal y 54% en hepático), así como una mayor mortalidad asociada (10% y 26%, respectivamente), con un AUC de hasta 0,824 para la predicción de muerte. Estos hallazgos subrayan la necesidad de establecer puntos de corte que permitan intervenciones capaces de equilibrar dos objetivos fundamentales: prevenir la progresión de la enfermedad y evitar tratamientos innecesarios.
En nuestra cohorte, el cut-off previamente utilizado de 1.500 UI/mL condujo al inicio de terapia antiviral en el 24% de los casos, sin que estos pacientes desarrollaran enfermedad, lo que sugiere un sobre tratamiento evitable. El nuevo punto de corte propuesto surge, por tanto, como una herramienta más precisa, ajustada al contexto clínico y epidemiológico de nuestra población, y capaz de reducir la exposición innecesaria a valganciclovir y sus efectos adversos, como la toxicidad hematológica, la selección de cepas resistentes y el aumento de los costos institucionales19.
Actualmente, se encuentra en marcha una fase prospectiva destinada a validar este cut-off. Su eventual incorporación a los protocolos institucionales permitirá afinar las decisiones terapéuticas, armonizar estrategias entre centros y contribuir al desarrollo de criterios homogéneos y basados en evidencia para el manejo del CMV en el trasplante hepático.
Las principales limitaciones del presente estudio incluyen su diseño retrospectivo, la heterogeneidad de los esquemas inmunosupresores empleados y la no aplicabilidad de los resultados a poblaciones de alto riesgo, como los receptores seronegativos o aquellos que recibieron inmunosupresión con globulina antitimocítica. Sin embargo, la homogeneidad del grupo analizado, la sistematización del monitoreo virológico y el tamaño de la cohorte fortalecen la validez de los hallazgos.
La publicación de estos resultados aporta evidencia local relevante, que contribuirá a mejorar la optimización del manejo del CMV en trasplante hepático y facilitará el proceso de estandarización clínica de los cut-off utilizados en la práctica asistencial.
Conclusión
El valor de corte de 2.595 UI/ml mostró un excelente desempeño para guiar la terapia anticipada en receptores de TH con riesgo intermedio, permitiendo optimizar el uso de antivirales y evitar sobretratamientos. Una fase prospectiva está en curso para validar su aplicabilidad clínica e integrar este cut-off en los protocolos institucionales.